文档内容
湖北省黄冈中学 2025 届高三第三次模拟考试
化学试卷
命题教师:黄志鹏 谢俊 审题教师:陈晓峰 宋倩雯
考试时间:2025年5月25日下午14:30-17:05 试卷满分:100分
可能用到的相对原子质量:H 1 C 12 N 14 O 16
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是
符合题目要求的。
1.春节是中华民族的传统节日,在进行节日庆祝时用到了许多物品都与化学知识相关,下列
有关说法错误的是
物品或活动 涉及的化学知识或原理
A. 用糯米制作年糕 糯米中富含支链淀粉,支链淀粉在糊化时能形成凝胶
B. 燃放烟花 金属元素原子的电子从激发态跃迁回基态并释放能量
C. 用瓷器盛放食物 用高岭土烧制陶器的温度一般要高于瓷器
D. 书写春联 鞣酸铁墨水中铁含量越多,被氧气氧化后的墨水颜色越深
2.安全用水意识至关重要。下列水循环处理的相关说法不正确的是
A.原水处理:絮凝剂“阳离子聚丙烯酰胺”适用于处理电镀厂的污水
B.软化处理:使用离子交换树脂去除水中的硬度离子,防止设备结垢
C.杀菌消毒:利用臭氧杀死水中的细菌和病毒,确保水质安全
D.循环利用:用电泵将处理达标后的水输送到用水设备,主要涉及电能转化为机械能
3.关于物质的分析和测定,下列说法错误的是
A.经红外光谱和核磁共振谱分析确定青蒿素含有酯基和甲基等结构
B.质谱法是测定某种壳聚糖相对分子质量最精确而快速的方法
C.石蕊、碳酸钠、氧化铜均不能用于区分乙酸和过氧乙酸
D.通过X射线衍射可精准测定抗氧化剂丁基羟基茴香醚的分子结构
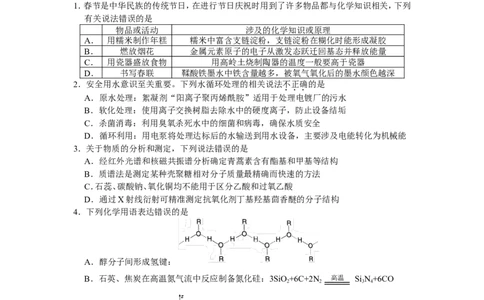
4.下列化学用语表达错误的是
A.醇分子间形成氢键:
B.石英、焦炭在高温氮气流中反应制备氮化硅:3SiO+6C+2N 高温 Si N+6CO
2 2 3 4
C.2p 电子云:
y
D.硅氧四面体的结构示意图:
湖北省黄冈中学2025届高三第三次模拟考试 化学试卷 第1页(共8页)5.下列有关理论的叙述错误的是
A.氧化还原反应中,增大氧化剂浓度或减小还原产物浓度均能增大氧化剂的氧化性
B.对于同一反应的正、逆反应,活化能大的反应的反应速率受温度影响更为显著
C.构造原理呈现的能级交错源于光谱学事实经验,不是任何理论推导的结果
D.参与成键的原子的电负性差值越大,共价键的极性越大,则分子的极性越大
6.烟酰胺(如图)属于B族维生素,具有一定的抗衰老的功效。下列叙述不正确的是
A.能与盐酸、氢氧化钠反应 B.1mol烟酰胺可与4 mol H 发生加成反应
2
C.可溶于水、甘油,不溶于醚类 D.分子中存在类似苯环的
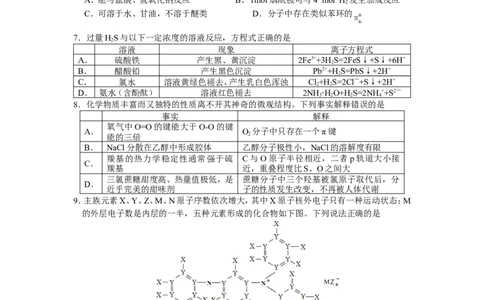
7.过量HS与以下一定浓度的溶液反应,方程式正确的是
2
溶液 现象 离子方程式
A. 硫酸铁 产生黑、黄沉淀 2Fe3++3H S=2FeS↓+S↓+6H+
2
B. 醋酸铅 产生黑色沉淀 Pb2++H S=PbS↓+2H+
2
C. 氯水 溶液黄绿色褪去,产生乳白色浑浊 Cl+H S=2Cl—+S↓+2H+
2 2
D. 氨水(含酚酞) 溶液红色褪去 2NH ·HO+HS=2NH ++S2—
3 2 2 4
8.化学物质丰富而又独特的性质离不开其神奇的微观结构。下列事实解释错误的是
事实 解释
氧气中O=O的键能大于O-O的键
A. O 分子中只存在一个π键
能的三倍 2
B. NaCl分散在乙醇中形成胶体 乙醇分子极性小,NaCl的溶解度有限
羰基的热力学稳定性通常强于硫 C与O原子半径相近,二者p轨道大小接
C.
羰基 近,重叠程度比S、O之间大
三氯蔗糖甜度高、热量值极低,是 蔗糖分子中三个羟基被氯原子取代后,分
D.
近乎完美的甜味剂 子的性质发生改变,不再被人体代谢
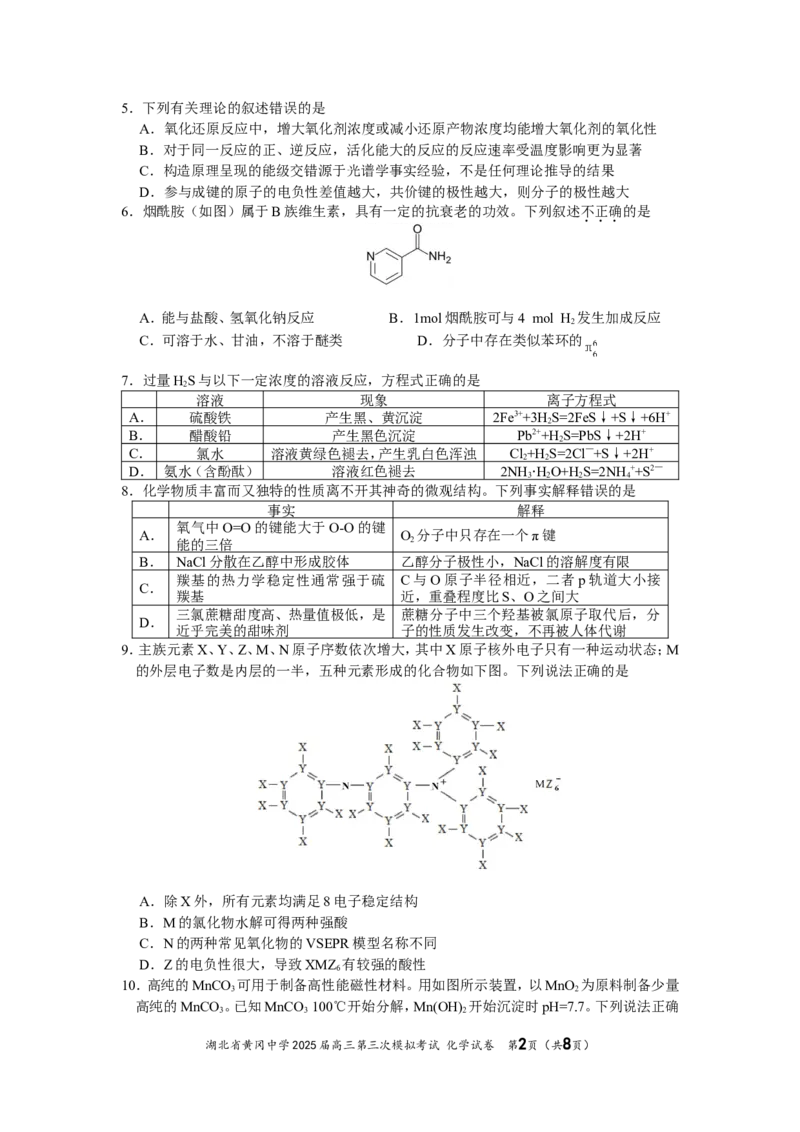
9.主族元素X、Y、Z、M、N原子序数依次增大,其中X原子核外电子只有一种运动状态;M
的外层电子数是内层的一半,五种元素形成的化合物如下图。下列说法正确的是
A.除X外,所有元素均满足8电子稳定结构
B.M的氯化物水解可得两种强酸
C.N的两种常见氧化物的VSEPR模型名称不同
D.Z的电负性很大,导致XMZ 有较强的酸性
6
10.高纯的MnCO 可用于制备高性能磁性材料。用如图所示装置,以MnO 为原料制备少量
3 2
高纯的MnCO 。已知MnCO 100℃开始分解,Mn(OH) 开始沉淀时pH=7.7。下列说法正确
3 3 2
湖北省黄冈中学2025届高三第三次模拟考试 化学试卷 第2页(共8页)的是
A.提高SO 转化率的措施可以是缓慢通入混合气体、大幅度提高水浴温度
2
B.向MnSO 溶液中加入NaHCO 时宜分批次加入,边加边搅拌,并监测溶液pH值
4 3
C.为确保MnCO 的纯度,MnCO 沉淀还需要水洗、醇洗、高温快速烘干
3 3
D.石灰乳的作用是处理尾气,其发生的主要反应是:Ca2++2OH—+SO = CaSO↓+H O
2 3 2
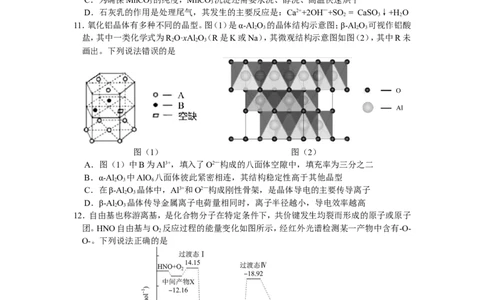
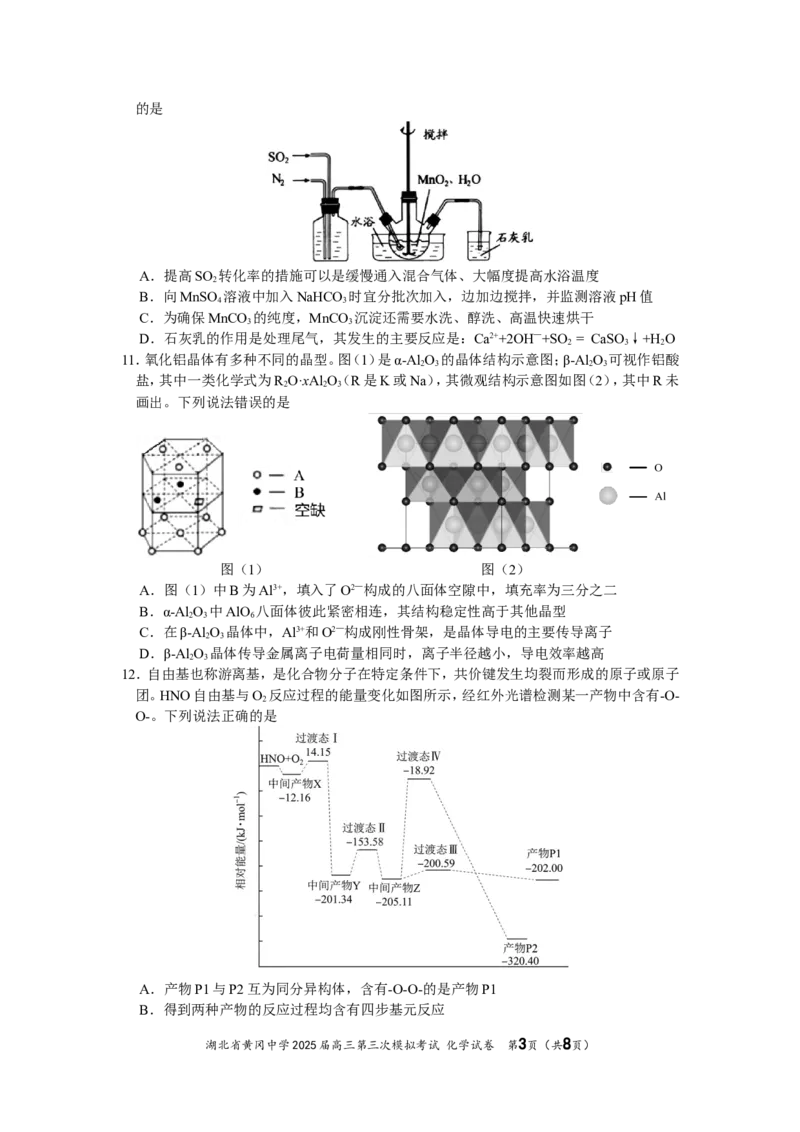
11.氧化铝晶体有多种不同的晶型。图(1)是α-AlO 的晶体结构示意图;β-Al O 可视作铝酸
2 3 2 3
盐,其中一类化学式为R O·xAl O(R是K或Na),其微观结构示意图如图(2),其中R未
2 2 3
画出。下列说法错误的是
图(1) 图(2)
A.图(1)中B为Al3+,填入了O2—构成的八面体空隙中,填充率为三分之二
B.α-AlO 中AlO 八面体彼此紧密相连,其结构稳定性高于其他晶型
2 3 6
C.在β-Al O 晶体中,Al3+和O2—构成刚性骨架,是晶体导电的主要传导离子
2 3
D.β-Al O 晶体传导金属离子电荷量相同时,离子半径越小,导电效率越高
2 3
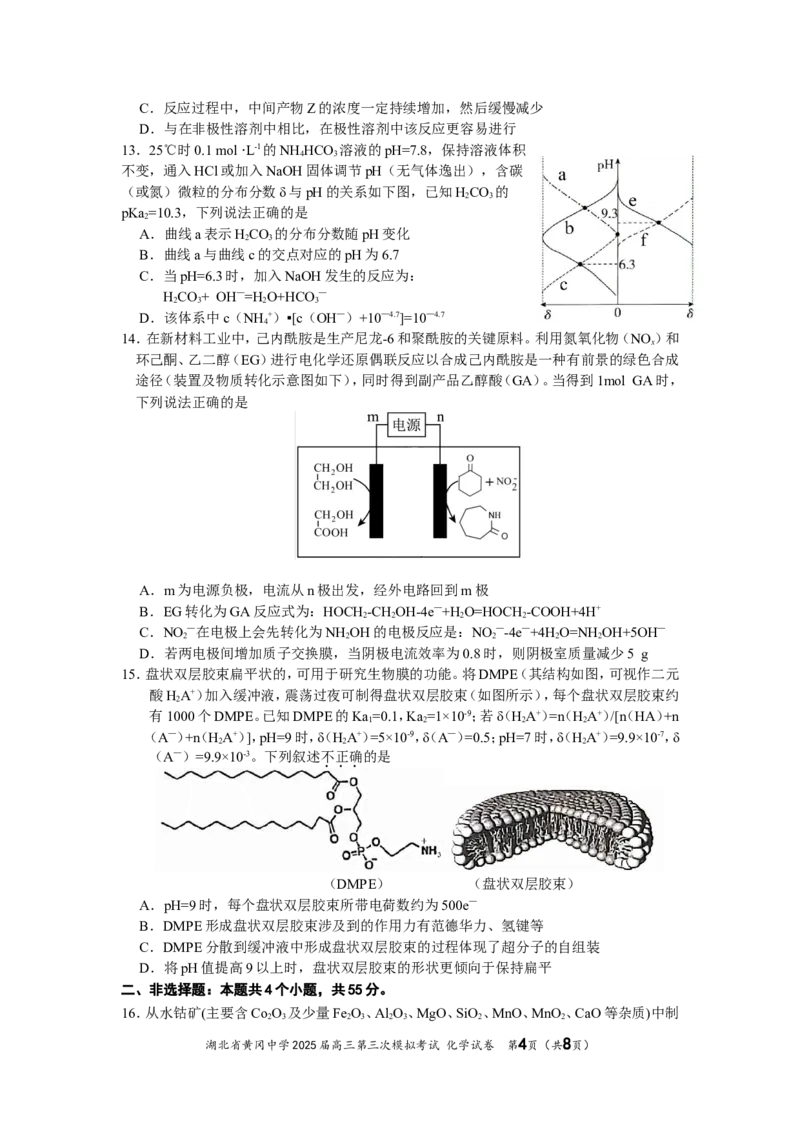
12.自由基也称游离基,是化合物分子在特定条件下,共价键发生均裂而形成的原子或原子
团。HNO自由基与O 反应过程的能量变化如图所示,经红外光谱检测某一产物中含有-O-
2
O-。下列说法正确的是
A.产物P1与P2互为同分异构体,含有-O-O-的是产物P1
B.得到两种产物的反应过程均含有四步基元反应
湖北省黄冈中学2025届高三第三次模拟考试 化学试卷 第3页(共8页)C.反应过程中,中间产物Z的浓度一定持续增加,然后缓慢减少
D.与在非极性溶剂中相比,在极性溶剂中该反应更容易进行
13.25℃时0.1 mol ·L-1的NH HCO 溶液的pH=7.8,保持溶液体积
4 3
不变,通入HCl或加入NaOH固体调节pH(无气体逸出),含碳
(或氮)微粒的分布分数δ与pH的关系如下图,已知HCO 的
2 3
pKa=10.3,下列说法正确的是
2
A.曲线a表示HCO 的分布分数随pH变化
2 3
B.曲线a与曲线c的交点对应的pH为6.7
C.当pH=6.3时,加入NaOH发生的反应为:
HCO+ OH—=H O+HCO—
2 3 2 3
D.该体系中c(NH +)▪[c(OH—)+10—4.7]=10—4.7
4
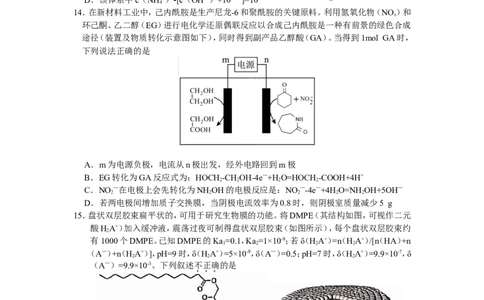
14.在新材料工业中,己内酰胺是生产尼龙-6和聚酰胺的关键原料。利用氮氧化物(NO)和
x
环己酮、乙二醇(EG)进行电化学还原偶联反应以合成己内酰胺是一种有前景的绿色合成
途径(装置及物质转化示意图如下),同时得到副产品乙醇酸(GA)。当得到1mol GA时,
下列说法正确的是
A.m为电源负极,电流从n极出发,经外电路回到m极
B.EG转化为GA反应式为:HOCH-CHOH-4e—+H O=HOCH-COOH+4H+
2 2 2 2
C.NO —在电极上会先转化为NH OH的电极反应是:NO —-4e—+4H O=NHOH+5OH—
2 2 2 2 2
D.若两电极间增加质子交换膜,当阴极电流效率为0.8时,则阴极室质量减少5 g
15.盘状双层胶束扁平状的,可用于研究生物膜的功能。将DMPE(其结构如图,可视作二元
酸HA+)加入缓冲液,震荡过夜可制得盘状双层胶束(如图所示),每个盘状双层胶束约
2
有1000个DMPE。已知DMPE的Ka=0.1,Ka=1×10-9;若δ(HA+)=n(HA+)/[n(HA)+n
1 2 2 2
(A—)+n(HA+)],pH=9时,δ(HA+)=5×10-9,δ(A—)=0.5;pH=7时,δ(HA+)=9.9×10-7,δ
2 2 2
(A—)=9.9×10-3。下列叙述不正确的是
(DMPE) (盘状双层胶束)
A.pH=9时,每个盘状双层胶束所带电荷数约为500e—
B.DMPE形成盘状双层胶束涉及到的作用力有范德华力、氢键等
C.DMPE分散到缓冲液中形成盘状双层胶束的过程体现了超分子的自组装
D.将pH值提高9以上时,盘状双层胶束的形状更倾向于保持扁平
二、非选择题:本题共4个小题,共55分。
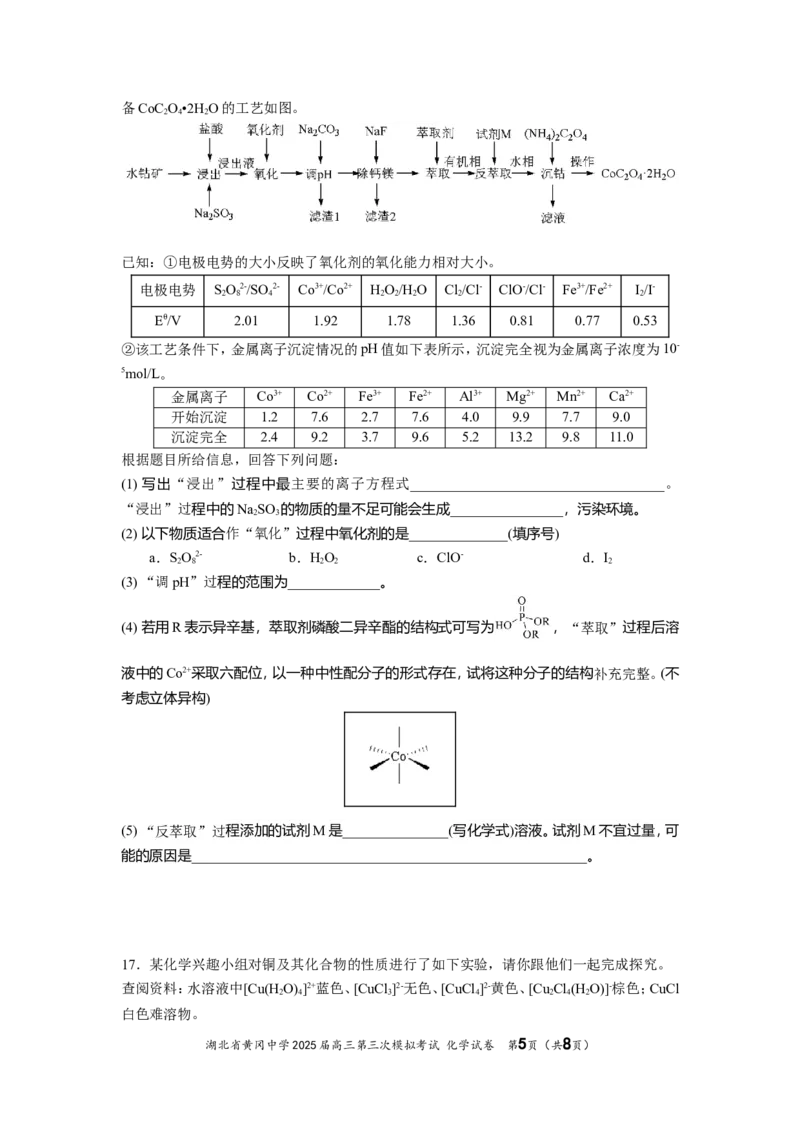
16.从水钴矿(主要含Co O 及少量Fe O、Al O、MgO、SiO、MnO、MnO 、CaO等杂质)中制
2 3 2 3 2 3 2 2
湖北省黄冈中学2025届高三第三次模拟考试 化学试卷 第4页(共8页)备CoC O•2H O的工艺如图。
2 4 2
已知:①电极电势的大小反映了氧化剂的氧化能力相对大小。
电极电势 SO2-/SO2- Co3+/Co2+ HO/H O Cl/Cl- ClO-/Cl- Fe3+/Fe2+ I/I-
2 8 4 2 2 2 2 2
Eθ/V 2.01 1.92 1.78 1.36 0.81 0.77 0.53
②该工艺条件下,金属离子沉淀情况的pH值如下表所示,沉淀完全视为金属离子浓度为10-
5mol/L。
金属离子 Co3+ Co2+ Fe3+ Fe2+ Al3+ Mg2+ Mn2+ Ca2+
开始沉淀 1.2 7.6 2.7 7.6 4.0 9.9 7.7 9.0
沉淀完全 2.4 9.2 3.7 9.6 5.2 13.2 9.8 11.0
根据题目所给信息,回答下列问题:
(1) 写出“浸出”过程中最主要的离子方程式____________________________________。
“浸出”过程中的NaSO 的物质的量不足可能会生成________________,污染环境。
2 3
(2) 以下物质适合作“氧化”过程中氧化剂的是______________(填序号)
a.SO2- b.HO c.ClO- d.I
2 8 2 2 2
(3) “调pH”过程的范围为_____________。
(4) 若用R表示异辛基,萃取剂磷酸二异辛酯的结构式可写为 ,“萃取”过程后溶
液中的Co2+采取六配位,以一种中性配分子的形式存在,试将这种分子的结构补充完整。(不
考虑立体异构)
(5) “反萃取”过程添加的试剂M是_______________(写化学式)溶液。试剂M不宜过量,可
能的原因是________________________________________________________。
17.某化学兴趣小组对铜及其化合物的性质进行了如下实验,请你跟他们一起完成探究。
查阅资料:水溶液中[Cu(H O) ]2+蓝色、[CuCl ]2-无色、[CuCl ]2-黄色、[Cu Cl(H O)]-棕色;CuCl
2 4 3 4 2 4 2
白色难溶物。
湖北省黄冈中学2025届高三第三次模拟考试 化学试卷 第5页(共8页)甲同学将等体积的溶液a分别加到等量铜粉中,实验记录如下:
编号 溶液a 实验现象
I CuCl 溶液(1mol·L-1) 产生白色沉淀,溶液蓝色变浅,5h时铜粉有剩余
2
产生细小无色气泡,溶液无色;继而溶液变为黄色;较
II 浓盐酸(10mol·L-1)
长时间后溶液变为棕色,5h时铜粉有剩余
CuCl 溶液(1mol·L-1) 溶液由黄绿色变为棕色,无气泡;随着反应进行,溶液
III 2
和浓盐酸(10mol·L-1) 颜色变浅,后接近于无色,5h时铜粉无剩余
(1)Cu2+的价层电子排布式为________。
(2)实验I中产生白色沉淀的化学方程式为__________________________________。
(3)①乙同学对实验II产生的无色气泡进行了收集并点燃,观察到了尖锐的爆鸣声。产生该
无色气泡的原因可能是________________________________。
②无色溶液变为黄色时的离子方程式为_______________________________________。
(4)为了探明实验III中无白色沉淀产生的原因,取了适量实验I中的白色沉淀,向其中加入
了饱和氯化钠溶液,发现沉淀溶解。丙同学得出结论:Cl-的大量存在,发生了反应 CuCl+2Cl-
=[CuCl ]2-,导致无白色沉淀产生。但丁同学认为丙同学的实验不够严谨,应补做对照实验:
3
______________________________________________。
(5) [Cu Cl(H O)]-中 Cu 元素的化合价为__________。若实验 III 溶液中 Cu 元素主要以
2 4 2
[CuCl ]2-和[Cu(H O) ]2+存在,试写出黄绿色变为棕色时发生反应的离子方程式
4 2 4
________________________________。
(6)戊同学拟测定某CuCl样品的纯度,完成了如下实验:准确称取样品1.200 g,将其置于足
量FeCl 溶液中,待其完全溶解后加入适量稀硫酸,用0.1000 mol·L-1 KMnO 标准溶液滴定
3 4
至终点,四次实验分别消耗测得标准液15.03 mL、14.98 mL、13.70 mL、14.99 mL。则该样
品纯度为____________。[M(CuCl)=99.0 g·mol-1,精确到0.1%]
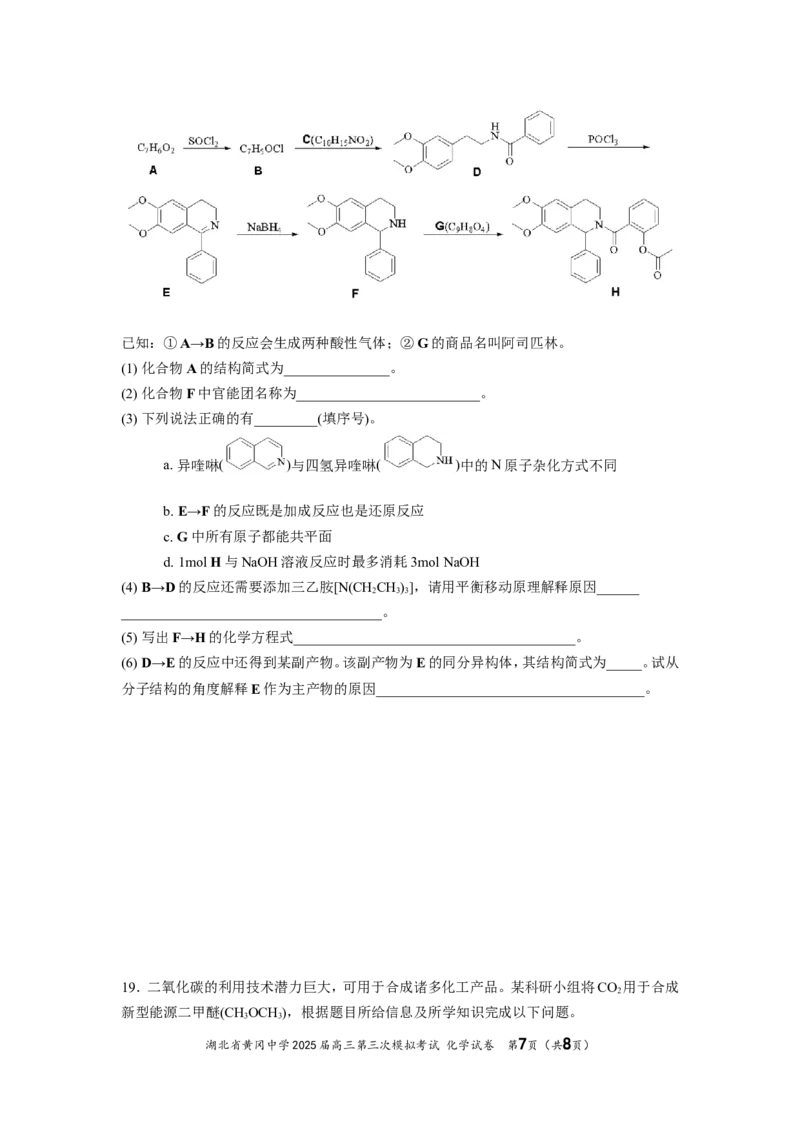
18.中医是中华民族传承千年的智慧结晶,木兰科、罂粟科等植物中的四氢异喹啉类生物碱
已证实具有抗肿瘤活性。下图是某四氢异喹啉类衍生物(H)在实验室中的合成路线,请根据
题目所给信息及现有知识完成下列问题。
湖北省黄冈中学2025届高三第三次模拟考试 化学试卷 第6页(共8页)已知:①A→B的反应会生成两种酸性气体;②G的商品名叫阿司匹林。
(1) 化合物A的结构简式为_______________。
(2) 化合物F中官能团名称为__________________________。
(3) 下列说法正确的有_________(填序号)。
a. 异喹啉( )与四氢异喹啉( )中的N原子杂化方式不同
b.E→F的反应既是加成反应也是还原反应
c.G中所有原子都能共平面
d.1mol H与NaOH溶液反应时最多消耗3mol NaOH
(4)B→D的反应还需要添加三乙胺[N(CH CH)],请用平衡移动原理解释原因______
2 3 3
_____________________________________。
(5) 写出F→H的化学方程式________________________________________。
(6)D→E的反应中还得到某副产物。该副产物为E的同分异构体,其结构简式为_____。试从
分子结构的角度解释E作为主产物的原因______________________________________。
19.二氧化碳的利用技术潜力巨大,可用于合成诸多化工产品。某科研小组将CO 用于合成
2
新型能源二甲醚(CHOCH ),根据题目所给信息及所学知识完成以下问题。
3 3
湖北省黄冈中学2025届高三第三次模拟考试 化学试卷 第7页(共8页)(1) 已知一定条件下,由元素的最稳定的单质生成1mol纯物质的热效应称为该物质的摩
尔生成焓,符号为△fHm。根据下表数据,计算出反应2CO2(g)+6H2(g) CH3OCH3(g)
+ 3H2O(g)的反应热△H为_____________kJ·mol-1。
物质 CO(g) HO(g) CHOCH (g)
2 2 3 3
△H /kJ·mol-1 -393.5 -241.8 -185
f m
(2) 上述过程主要包含以下三个反应:
反应1:CO(g)+3H(g) CHOH(g)+H O(g) △H<0
2 2 3 2 1
反应2:2CHOH(g) CHOCH (g)+HO(g) △H<0
3 3 3 2 2
反应3:CO(g)+H(g) CO(g)+HO(g) △H>0
2 2 2 3
有关上述反应体系的下列说法中正确的有___________。
A.反应1和反应2低温自发,反应3高温自发,因此应采取低温环境进行生产
B.若生产过程中移去部分CHOH(g),反应3的平衡向右移动
3
C.增大压强既能加快反应速率,也能提升CHOCH 的产率
3 3
D.加入反应1的催化剂,可提高CO 的转化率
2
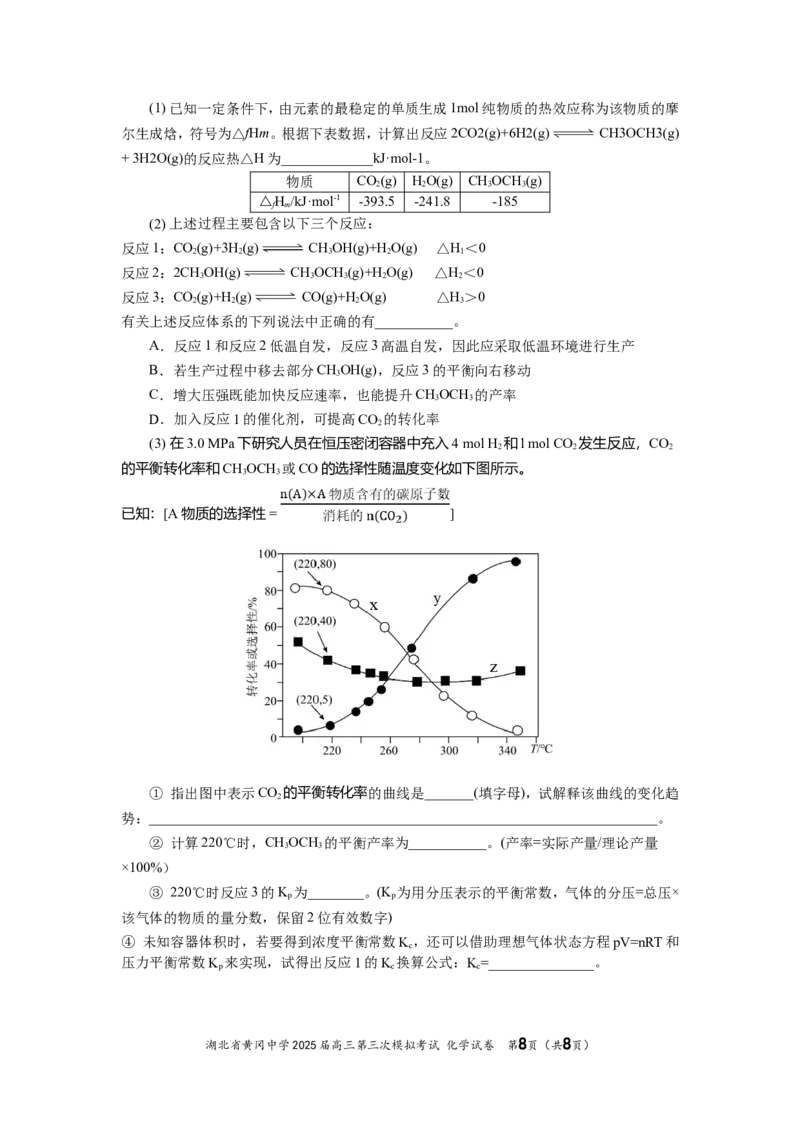
(3)在3.0 MPa下研究人员在恒压密闭容器中充入4 mol H 和l mol CO 发生反应,CO
2 2 2
的平衡转化率和CHOCH 或CO的选择性随温度变化如下图所示。
3 3
已知:[A物质的选择性 = ]
① 指出图中表示CO 的平衡转化率的曲线是_______(填字母),试解释该曲线的变化趋
2
势:________________________________________________________________________。
② 计算220℃时,CHOCH 的平衡产率为___________。(产率=实际产量/理论产量
3 3
×100%)
③ 220℃时反应3的K 为________。(K 为用分压表示的平衡常数,气体的分压=总压×
p p
该气体的物质的量分数,保留2位有效数字)
④ 未知容器体积时,若要得到浓度平衡常数K,还可以借助理想气体状态方程pV=nRT和
c
压力平衡常数K 来实现,试得出反应1的K 换算公式:K=_______________。
p c c
湖北省黄冈中学2025届高三第三次模拟考试 化学试卷 第8页(共8页)