文档内容
专题41 反应热计算——键能
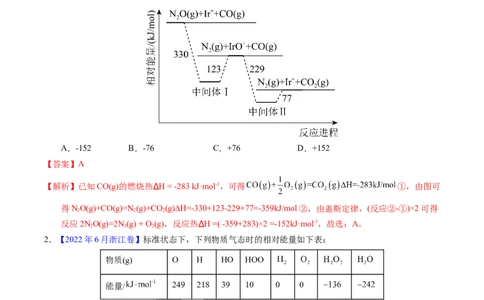
1.【2021年重庆卷】“天朗气清,惠风和畅。”研究表明,利用Ir+可催化消除大气污染物NO和CO,
2
简化中间反应进程后,相对能量变化如图所示。已知CO(g)的燃烧热 H = -283 kJ·mol-1,则
2NO(g)=2N (g) + O(g)的反应热 H (kJ·mol-1)为
2 2 2 ∆
∆
A.-152 B.-76 C.+76 D.+152
【答案】A
【解析】已知CO(g)的燃烧热∆H = -283 kJ·mol-1,可得 ①,由图可
得NO(g)+CO(g)=N (g)+CO (g)∆H=-330+123-229+77=-359kJ/mol②,由盖斯定律,(反应②-①)×2可得
2 2 2
反应2NO(g)=2N (g) + O(g),反应热∆H =( -359+283)×2 =-152kJ·mol-1,故选:A。
2 2 2
2.【2022年6月浙江卷】标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO
能量/ 249 218 39 10 0 0
可根据 计算出 中氧氧单键的键能为 。下列说法不正确的是
A. 的键能为
B. 的键能大于 中氧氧单键的键能的两倍
C.解离氧氧单键所需能量:
D.
【答案】C
【解析】A.根据表格中的数据可知, 的键能为218×2=436 ,A正确;B.由表格中的数据可知的键能为:249×2=498 ,由题中信息可知 中氧氧单键的键能为 ,则 的
键能大于 中氧氧单键的键能的两倍,B正确;C.由表格中的数据可知HOO=HO+O,解离其中
氧氧单键需要的能量为249+39-10=278 , 中氧氧单键的键能为 ,C错误;
D.由表中的数据可知 的 ,D正确;故选C。
3.(2021.1·浙江真题)已知共价键的键能与热化学方程式信息如下表:
共价键 H- H H-O
键能/(kJ·mol-1) 436 463
热化学方程式 2H(g) + O (g)=2HO(g) ΔH= -482kJ·mol-1
2 2 2
则2O(g)=O (g)的ΔH为
2
A.428 kJ·mol-1 B.-428 kJ·mol-1 C.498 kJ·mol-1 D.-498 kJ·mol-1
【答案】D
【解析】根据ΔH=反应物的键能总和-生成物的键能总和计算。反应的ΔH=2(H-H)+(O-O)-4(H-
O);-482kJ/mol=2×436kJ/mol+(O-O)-4×463kJ/mol,解得O-O键的键能为498kJ/mol,2个氧原子结合生成氧
气的过程需要释放能量,因此2O(g)=O (g)的ΔH=-498kJ/mol。
2
4.(2010·湖南高考真题)己知: 与 反应的 ; 与
反应的 。则 在水溶液中电离的 等于
A. B.
C. D.
【答案】C
【解析】HCN(aq)、HCl(aq)分别与NaOH(aq)反应△H的差值即为HCN在溶液中电离的能量,HCN属于弱
电解质,其电离过程要吸收,即△H>0,综合以上分析,可知△H =+43.5kJ·mol-1,答案为C。
5.(2016·海南高考真题)油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:C H O(s)
57 104 6
+80O (g)=57CO(g)+52HO(l)。已知燃烧1kg该化合物释放出热量3.8×104kJ。油酸甘油酯的燃烧热
2 2 2
△H为
A.3.8×104kJ·mol-1 B.-3.8×104kJ·mol-1
C.3.4×104kJ·mol-1 D.-3.4×104kJ·mol-1
【答案】D
【解析】燃烧热指的是燃烧1mol可燃物生成稳定的氧化物所放出的热量。燃烧1kg油酸甘油酯释放出热量
3.8×104kJ,1kg该化合物的物质的量为 ,则油酸甘油酯的燃烧热△H=-
≈-3.4×104kJ•mol-1,故选D。
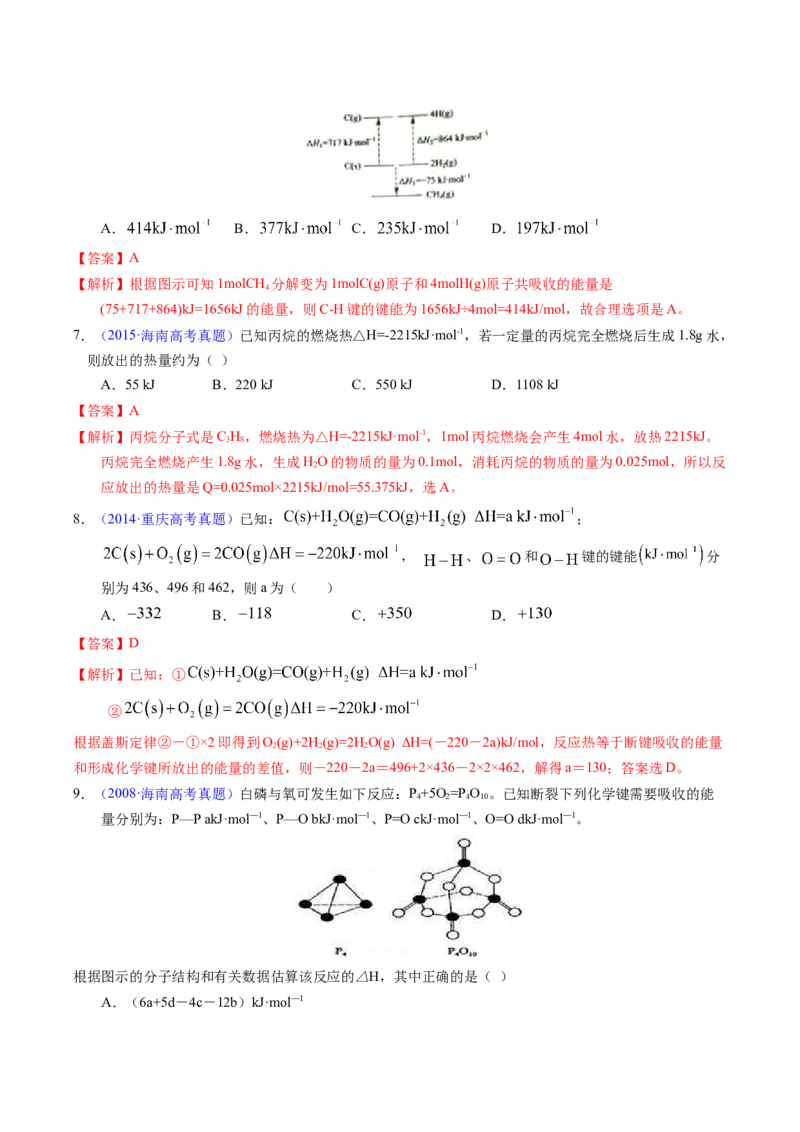
6.(2019·海南高考真题)根据图中的能量关系,可求得 的键能为( )A. B. C. D.
【答案】A
【解析】根据图示可知1molCH 分解变为1molC(g)原子和4molH(g)原子共吸收的能量是
4
(75+717+864)kJ=1656kJ的能量,则C-H键的键能为1656kJ÷4mol=414kJ/mol,故合理选项是A。
7.(2015·海南高考真题)已知丙烷的燃烧热△H=-2215kJ·mol-1,若一定量的丙烷完全燃烧后生成1.8g水,
则放出的热量约为( )
A.55 kJ B.220 kJ C.550 kJ D.1108 kJ
【答案】A
【解析】丙烷分子式是C H,燃烧热为△H=-2215kJ·mol-1,1mol丙烷燃烧会产生4mol水,放热2215kJ。
3 8
丙烷完全燃烧产生1.8g水,生成HO的物质的量为0.1mol,消耗丙烷的物质的量为0.025mol,所以反
2
应放出的热量是Q=0.025mol×2215kJ/mol=55.375kJ,选A。
8.(2014·重庆高考真题)已知: ;
, 、 和 键的键能 分
别为436、496和462,则a为( )
A. B. C. D.
【答案】D
【解析】已知:①
②
根据盖斯定律②-①×2即得到O(g)+2H(g)=2HO(g) ∆H=(-220-2a)kJ/mol,反应热等于断键吸收的能量
2 2 2
和形成化学键所放出的能量的差值,则-220-2a=496+2×436-2×2×462,解得a=130;答案选D。
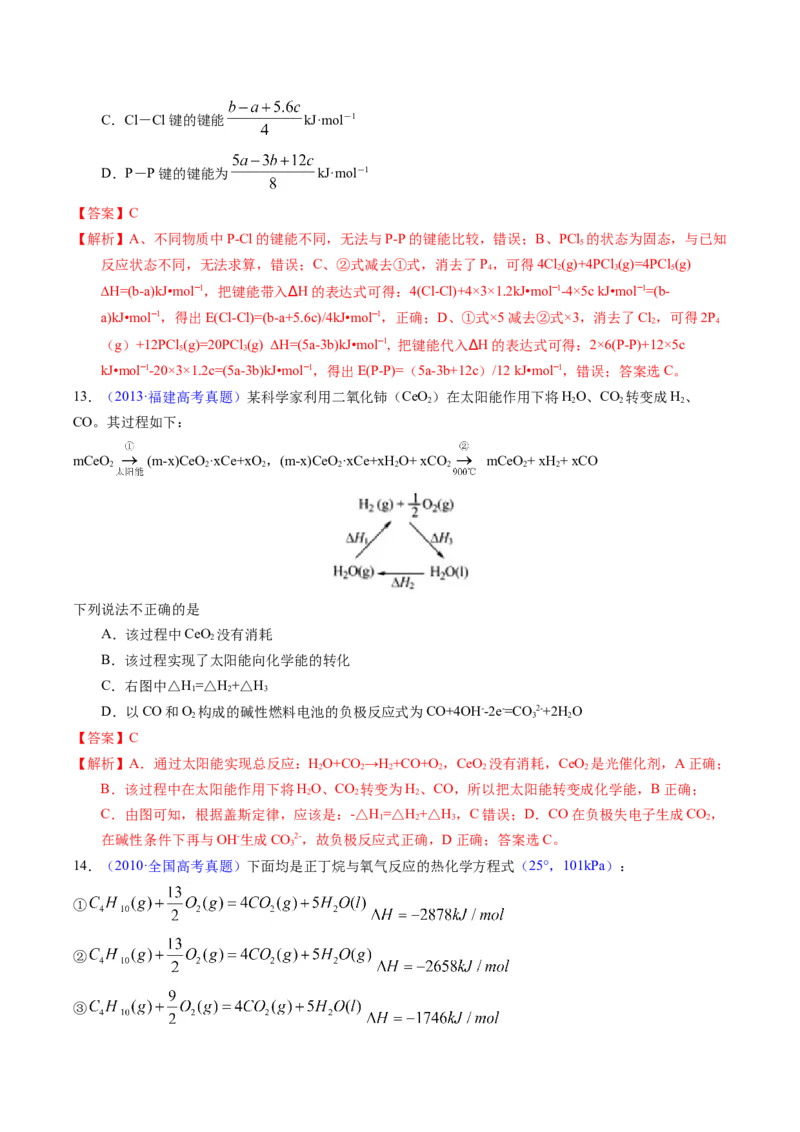
9.(2008·海南高考真题)白磷与氧可发生如下反应:P+5O =P O 。已知断裂下列化学键需要吸收的能
4 2 4 10
量分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P=O ckJ·mol—1、O=O dkJ·mol—1。
根据图示的分子结构和有关数据估算该反应的△H,其中正确的是( )
A.(6a+5d-4c-12b)kJ·mol—1B.(4c+12b-6a-5d)kJ·mol—1
C.(4c+12b-4a-5d)kJ·mol—1
D.(4a+5d-4c-12b)kJ·mol—1
【答案】A
【解析】反应热等于断键吸收的总能量与形成化学键所放出的能量的差值,由图可以看出:P 中有6mol的
4
P-P,5mol的O 中含有5molO=O,1mol的PO 中含有4mol的P=O,12mol的P-O,所以根据方
2 4 10
程式可知反应热△H=(6a+5d-4c-12b)kJ·mol-1。答案选A。
10.(2009·全国高考真题)已知:2H(g)+ O (g)=2HO(l) ΔH=-571.6kJ· mol-1
2 2 2
CH(g)+ 2O (g)=CO(g)+2HO(l) ΔH=-890kJ· mol-1
4 2 2 2
现有H 与CH 的混合气体112L(标准状况),使其完全燃烧生成CO 和HO(l),若实验测得反应放热
2 4 2 2
3695kJ,则原混合气体中H 与CH 的物质的量之比是( )
2 4
A.1∶1 B.1∶3 C.1∶4 D.2∶3
【答案】B
【解析】H 与CH 的混合气体112L(标准状况),其物质的量为n(混)=112L÷22.4L/mol=5mol,设原混合
2 4
气体中H 与CH 的物质的量分别是x mol和y mol,则有x+y=5,285.5x+890y=3695,解得x︰y=1
2 4
︰3,答案选B。
11.(2009·海南高考真题)已知: (1)Fe O(s)+ C(s)= CO(g)+2Fe(s),ΔH=+234.1kJ•mol-1
2 3 2
则 的ΔH是( )
A.-824.4 kJ•mol-1 B.-627.6kJ•mol-1 C.-744.7kJ•mol-1 D.-169.4kJ•mol-1
【答案】A
【解析】已知:(1)2Fe(s)+ CO(g)=Fe O(s)+ C(s)△H=-234.1kJ•mol-1(2)C(s)
2 2 3
+O (g)=CO (g)△H=-393.5kJ•mol-1,由盖斯定律(2)× +(1),得:2Fe(s)+
2 2
O(g)=Fe O(s)△H=(-393.5kJ•mol-1)× +(-234.1kJ•mol-1)=-824.4kJ•mol-1,可知:2Fe(s)+
2 2 3
O(g)=Fe O(s)△H=-824.4kJ•mol-1,故答案为A。
2 2 3
12.(2013·重庆高考真题)已知:P(s)+6Cl(g)=4PCl (g) ΔH=akJ·mol-1
4 2 3
P(s)+10Cl(g)=4PCl (g) ΔH= bkJ·mol-1
4 2 5
P 具有正四面体结构,PCl 中P-Cl键的键能为ckJ·mol-1,PCl 中P-Cl键的键能为1.2ckJ·mol-1
4 5 3
下列叙述正确的是( )
A.P-P键的键能大于P-Cl键的键能
B.可求Cl(g)+PCl (g)=PCl (s)的反应热ΔH
2 3 5C.Cl-Cl键的键能 kJ·mol-1
D.P-P键的键能为 kJ·mol-1
【答案】C
【解析】A、不同物质中P-Cl的键能不同,无法与P-P的键能比较,错误;B、PCl 的状态为固态,与已知
5
反应状态不同,无法求算,错误;C、②式减去①式,消去了P,可得4Cl(g)+4PCl (g)=4PCl (g)
4 2 3 5
∆H=(b-a)kJ•mol‾1,把键能带入∆H的表达式可得:4(Cl-Cl)+4×3×1.2kJ•mol‾1-4×5c kJ•mol‾1=(b-
a)kJ•mol‾1,得出E(Cl-Cl)=(b-a+5.6c)/4kJ•mol‾1,正确;D、①式×5减去②式×3,消去了Cl,可得2P
2 4
(g)+12PCl (g)=20PCl (g) ∆H=(5a-3b)kJ•mol‾1, 把键能代入∆H的表达式可得:2×6(P-P)+12×5c
5 3
kJ•mol‾1-20×3×1.2c=(5a-3b)kJ•mol‾1,得出E(P-P)=(5a-3b+12c)/12 kJ•mol‾1,错误;答案选C。
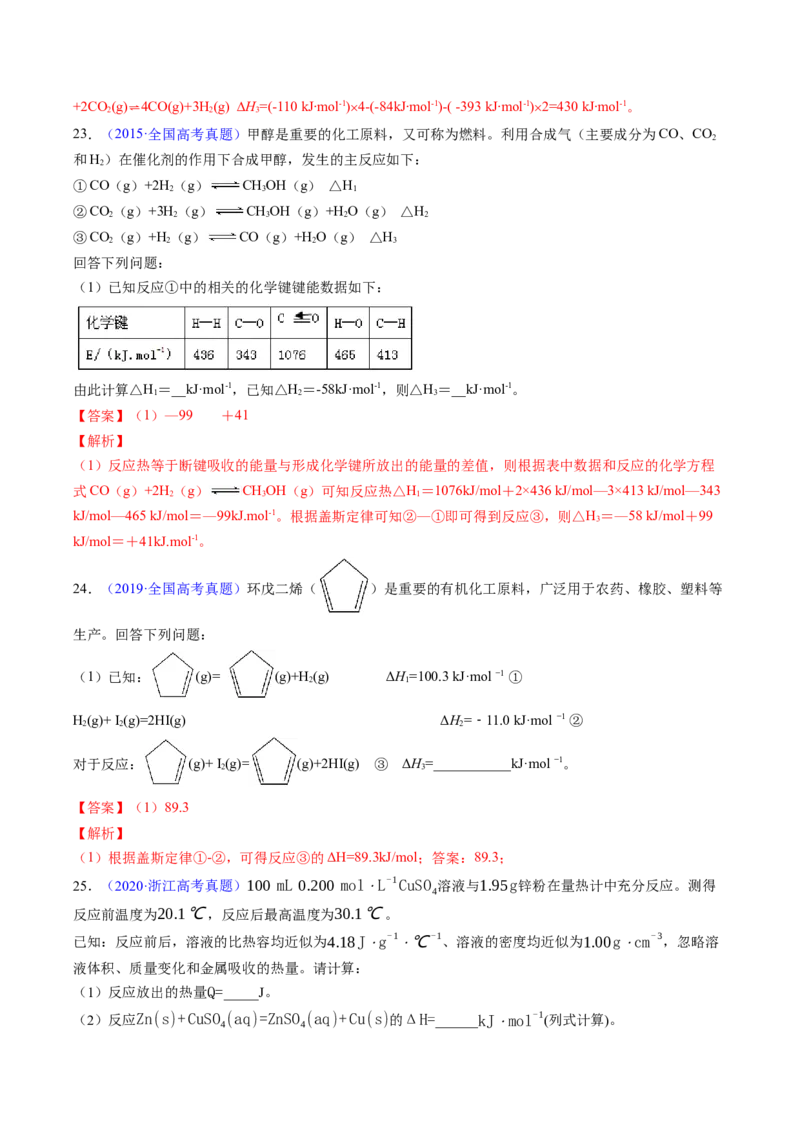
13.(2013·福建高考真题)某科学家利用二氧化铈(CeO)在太阳能作用下将HO、CO 转变成H、
2 2 2 2
CO。其过程如下:
mCeO (m-x)CeO ·xCe+xO ,(m-x)CeO ·xCe+xH O+ xCO mCeO + xH + xCO
2 2 2 2 2 2 2 2
下列说法不正确的是
A.该过程中CeO 没有消耗
2
B.该过程实现了太阳能向化学能的转化
C.右图中△H=△H+△H
1 2 3
D.以CO和O 构成的碱性燃料电池的负极反应式为CO+4OH--2e-=CO 2-+2H O
2 3 2
【答案】C
【解析】A.通过太阳能实现总反应:HO+CO→H+CO+O ,CeO 没有消耗,CeO 是光催化剂,A正确;
2 2 2 2 2 2
B.该过程中在太阳能作用下将HO、CO 转变为H、CO,所以把太阳能转变成化学能,B正确;
2 2 2
C.由图可知,根据盖斯定律,应该是:-△H=△H+△H,C错误;D.CO在负极失电子生成CO,
1 2 3 2
在碱性条件下再与OH-生成CO2-,故负极反应式正确,D正确;答案选C。
3
14.(2010·全国高考真题)下面均是正丁烷与氧气反应的热化学方程式(25°,101kPa):
①
②
③④
由此判断,正丁烷的燃烧热是
A.-2878kJ/mol B.-2658kJ/mol C.-1746kJ/mol D.-1526kJ/mol
【答案】A
【解析】燃烧热指1mol可燃物完全燃烧生成稳定的化合物时所放出的热量,反应物中C→CO(气),
2
H→H O(液),S→SO (气)等。正丁烷的燃烧热是1mol正丁烷完全燃烧生成CO(气),HO
2 2 2 2
(液)放出的热量,故热化学方程式(1)C H (g)+O (g)═4CO(g)+5H O(l)
4 10 2 2 2
△H=-2878kJ/mol,符合燃烧热的概念,所以正丁烷的燃烧热为-2878 kJ/mol。故选A。
15.(2007·重庆高考真题)已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O=O键
完全断裂时吸收热量496 kJ,水蒸气中1mol H-O键形成时放出热量463 kJ,则氢气中1mol H-H键断
裂时吸收热量为
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
【答案】C
【解析】已知1 g即0.5mol氢气完全燃烧生成水蒸气时放出热量121 kJ ,则该反应的热化学反应方程式为:
H(g)+ O(g)===HO(g)△H=-242 kJ/mol,焓变=反应物键能总和-生成物键能总和,设1mol H-H键断
2 2 2
裂时吸收热量为xkJ,则有x kJ/mol+ ×496kJ/mol-2×463 kJ/mol=-242 kJ/mol,解得x=436 kJ/mol,即
1mol H-H键断裂时吸收热量为436kJ,故答案为 C。
16.【2023年全国新课标卷】氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列
问题:
(1)根据图1数据计算反应 的 。
【答案】(1)
【解析】(1)在化学反应中,断开化学键要消耗能量,形成化学键要释放能量,反应的焓变等于反应物
的键能总和与生成物的键能总和的差,因此,由图1数据可知,反应 的。
17.(2021·海南真题)碳及其化合物间的转化广泛存在于自然界及人类的生产和生活中。已知25℃,
时:
① 葡萄糖 完全燃烧生成 和 ,放出 热量。
② 。
回答问题:
(1)25℃时, 与 经光合作用生成葡萄糖 和 的热化学方程式为
___________。
(2)25℃, 时,气态分子断开 化学键的焓变称为键焓。已知 、 键的键焓分别为
、 , 分子中碳氧键的键焓为___________ 。
【答案】
(1)
(2)664.75
【解析】
(1)由题意可知,反应①为1mol葡萄糖在氧气中完全燃烧生成二氧化碳和液态水放出2804kJ的热量,反
应的热化学方程式为 = ,二氧化碳和液态水经
光合作用生成葡萄糖和氧气的反应为葡萄糖燃烧的逆反应,生成1mol葡萄糖会吸收2804kJ的热量,
反应的热化学方程式为 = ,故答案为:
= ;
(2)由反应热的焓变为反应物的键焓之和与生成物的键焓之和的差值可得:反应②的焓变
=—283kJ/mol,解得E(C=O)=
=664.75kJ/mol,故答案为:664.75;
18.(2021·湖北真题)丙烯是一种重要的化工原料,可以在催化剂作用下,由丙烷直接脱氢或氧化脱氢制
备。
反应Ⅰ(直接脱氢):C H(g)=C H(g)+H(g)△H=+125kJ·mol-1
3 8 3 6 2 1
反应Ⅱ(氧化脱氢):C H(g)+ O(g)=C H(g)+HO(g)△H=-118kJ·mol-1
3 8 2 3 6 2 2
(1)已知键能:E(C—H)=416kJ·mol-1,E(H—H)=436kJ·mol-1,由此计算生成1mol碳碳π键放出的能量为
___kJ。
【答案】
(1)271
【解析】(1)由C H(g)=C H(g)+H(g)△H=+125kJ·mol-1可知反应需要中断裂2mol C—H键、形成1mol碳碳π键
3 8 3 6 2 1
和1mol H—H键,436kJ·mol-1×2- E (碳碳π键) = +125kJ.mol-1,解得:E(碳碳π键)= 271kJ. mol-1,所以
形成1mol碳碳π键放出的能量为271kJ;
19.【2022年海南卷】某空间站的生命保障系统功能之一是实现氧循环,其中涉及反应:
回答问题:
(1)已知:电解液态水制备 ,电解反应的 。由此计算 的燃烧热(焓)
_______ 。
【答案】(1)-286
【解析】
(1)电解液态水制备 ,电解反应的 ,由此可以判断,2mol 完全燃烧消
耗 ,生成液态水的同时放出的热量为572kJ ,故1mol 完全燃烧生成液态水放出的热量为
286kJ,因此, 的燃烧热(焓) -286 。
20.(2021·湖南真题)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两
种方法由氨气得到氢气。
方法I:氨热分解法制氢气
相关化学键的键能数据
化学键
键能 946 436.0 390.8
一定温度下,利用催化剂将 分解为 和 。回答下列问题:
(1)反应 _______ ;
【答案】
(1)+90.8
【解析】
(1) 根据反应热=反应物的总键能-生成物的总键能,2NH (g) N(g)+3H(g), H=390.8kJ mol-1 -
3 2 2
(946 kJ mol-1+436.0kJ mol-1 )= +90.8kJ mol-1,故答案为:+90.8;
21.(2021·广东真题)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重整是CO
4 2 2
利用的研究热点之一。该重整反应体系主要涉及以下反应:
a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
b)CO(g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
c)CH(g) C(s)+2H(g) ∆H
4 2 3
d)2CO(g) CO(g)+C(s) ∆H
2 4e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
(1)根据盖斯定律,反应a的∆H=_______(写出一个代数式即可)。
1
【答案】(1)∆H+∆H-∆H 或∆H-∆H
2 3 5 3 4
【解析】根据盖斯定律计算未知反应的反应热;根据影响化学反应速率和化学平衡的因素判断反应速率的
变化及转化率的变化;根据图像及曲线高低判断反应进程和活化能的相对大小;根据平衡时反应物的分压
计算平衡转化率;根据CO 的物理性质推测CO 的用途。
2 2
(1)根据题目所给出的反应方程式关系可知,a=b+c-e=c-d,根据盖斯定律则有∆H=∆H+∆H-∆H=∆H-
1 2 3 5 3
∆H;
4
22.(2020·浙江高考真题)研究 氧化 制 对资源综合利用有重要意义。相关的主要化学反
应有:
Ⅰ
Ⅱ
Ⅲ
Ⅳ
已知: 时,相关物质的相对能量(如图1)。
可根据相关物质的相对能量计算反应或变化的 ( 随温度变化可忽略)。例如:
。
请回答:
(1)①根据相关物质的相对能量计算 _____ 。
【答案】(1)430
【解析】
(1)①由图1的数据可知,C H(g)、CO(g)、CO(g)、H(g)的相对能量分别为-84kJ∙mol-1、-393 kJ∙mol-1、-
2 6 2 2
110 kJ∙mol-1、0 kJ∙mol-1。由题中信息可知,∆H=生成物的相对能量-反应物的相对能量,因此,C H(g)
2 6+2CO
2
(g)⇌4CO(g)+3H
2
(g) ∆H
3
=(-110 kJ∙mol-1)4-(-84kJ∙mol-1)-( -393 kJ∙mol-1)2=430 kJ∙mol-1。
23.(2015·全国高考真题)甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO
2
和H)在催化剂的作用下合成甲醇,发生的主反应如下:
2
①CO(g)+2H (g) CHOH(g) △H
2 3 1
②CO(g)+3H (g) CHOH(g)+H O(g) △H
2 2 3 2 2
③CO(g)+H (g) CO(g)+H O(g) △H
2 2 2 3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
由此计算△H=__kJ·mol-1,已知△H=-58kJ·mol-1,则△H=__kJ·mol-1。
1 2 3
【答案】(1)—99 +41
【解析】
(1)反应热等于断键吸收的能量与形成化学键所放出的能量的差值,则根据表中数据和反应的化学方程
式CO(g)+2H (g) CHOH(g)可知反应热△H=1076kJ/mol+2×436 kJ/mol—3×413 kJ/mol—343
2 3 1
kJ/mol—465 kJ/mol=—99kJ.mol-1。根据盖斯定律可知②—①即可得到反应③,则△H=—58 kJ/mol+99
3
kJ/mol=+41kJ.mol-1。
24.(2019·全国高考真题)环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等
生产。回答下列问题:
(1)已知: (g)= (g)+H(g) ΔH=100.3 kJ·mol −1 ①
2 1
H(g)+ I (g)=2HI(g) ΔH=﹣11.0 kJ·mol −1 ②
2 2 2
对于反应: (g)+ I (g)= (g)+2HI(g) ③ ΔH=___________kJ·mol −1。
2 3
【答案】(1)89.3
【解析】
(1)根据盖斯定律①-②,可得反应③的ΔH=89.3kJ/mol;答案:89.3;
25.(2020·浙江高考真题)100 mL 0.200 mol⋅L-1CuSO 溶液与1.95g锌粉在量热计中充分反应。测得
4
反应前温度为20.1℃,反应后最高温度为30.1℃。
已知:反应前后,溶液的比热容均近似为4.18J⋅g-1
⋅℃
-1、溶液的密度均近似为1.00g⋅cm-3,忽略溶
液体积、质量变化和金属吸收的热量。请计算:
(1)反应放出的热量Q=_____J。
(2)反应Zn(s)+CuSO (aq)=ZnSO (aq)+Cu(s)的ΔH=______kJ⋅mol-1(列式计算)。
4 44.18×103/1000
【答案】4.18×103 - =-209
0.100×0.200
【解析】
(1)100mL 0.200mol/L CuSO 溶液与1.95g锌粉发生反应的化学方程式为:CuSO +Zn=ZnSO+Cu,忽略
4 4 4
溶液体积、质量变化可知,溶液的质量m=ρV=1.00g/cm3×100mL(cm3)=100g,忽略金属吸收的热量可知,
反应放出的热量Q=cmΔt=4.18J⋅g-1 ⋅°C-1×100g×(30.1-20.1)°C= 4.18×103J,故答案为:4.18×103;
(2)上述反应中硫酸铜的物质的量n(CuSO )= 0.200mol/L×0.100L=0.020mol,锌粉的物质的量n(Zn)=
4
m 1.95g
= =0.030mol,由此可知,锌粉过量。根据题干与第(1)问可知,转化0.020mol硫酸铜所放
M 65g/mol
出的热量为4.18×103J,又因为该反应中焓变ΔH代表反应1mol硫酸铜参加反应放出的热量,单位为kJ/
4.18×103J÷1000J/kJ 4.18×103/1000
mol,则可列出计算式为:ΔH=- =- =-209 kJ/mol,故答
0.100L×0.200mol/L 0.100×0.200
4.18×103/1000
案为:- =-209(答案符合要求且合理即可)。
0.100×0.200