文档内容
纳溪中学校高 2023 级高三年级上期第二次月考化学试题卷
命题人:曾军 审题人:关兵
可能用到的相对原子质量:H—1 C—12 O—16 Se—79 Zn—65
Cu—64
一、选择题:本题共15小题,每小题3分,共45分。
1.“航空报国 追求卓越”,航空航天的发展与化学密切相关。下列有关说法错误的是
A. 隐形战机采用的碳纤维属于无机高分子材料
B. 大型液化天然气运输船成功建造:天然气液化过程中形成了新的化学键
C. 回收返回舱的降落伞的伞绳是超高分子聚乙烯,其单体为乙烯
D. 神舟飞船太阳能电池材料的砷化镓能将太阳能转化为电能
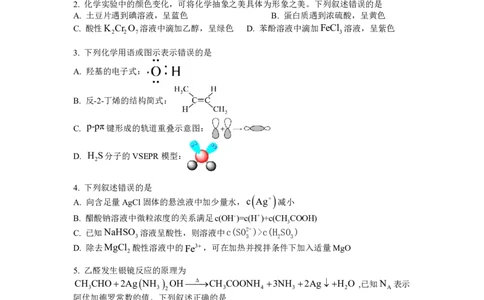
2. 化学实验中的颜色变化,可将化学抽象之美具体为形象之美。下列叙述错误的是
A. 土豆片遇到碘溶液,呈蓝色 B. 蛋白质遇到浓硫酸,呈黄色
C. 酸性K Cr O 溶液中滴加乙醇,呈绿色 D. 苯酚溶液中滴加FeCl 溶液,呈紫色
2 2 7 3
3. 下列化学用语或图示表示错误的是
A. 羟基的电子式:
B. 反-2-丁烯的结构简式:
C.
p-pπ键形成的轨道重叠示意图:
D. H S分子的VSEPR模型:
2
4. 下列叙述错误的是
A. 向含足量AgCl固体的悬浊液中加少量水,c Ag+ 减小
B. 醋酸钠溶液中微粒浓度的关系满足c(OH-)=c(H+)+c(CH COOH)
3
C. 已知NaHSO 溶液呈酸性,则溶液中c(SO2-)>c(H SO )
3 3 2 3
D. 除去MgCl 酸性溶液中的Fe3,可在加热并搅拌条件下加入适量MgO
2
5. 乙醛发生银镜反应的原理为
CH CHO2Ag NH OHCH COONH 3NH 2AgH O ,已知N 表示
3 3 2 3 4 3 2 A
阿伏加德罗常数的值.下列叙述正确的是
A. 标准状况下,22gCH CHO含有的σ键数目为2.5N
3 A
B. 常温下,1LpH 9的氨水溶液中由水电离产生的OH数目为109N
A
C. 理论上,当有标准状况下2.24LNH 生成时,转移电子的数目为0.3N
3 A
D. 500mL0.2molL1Ag NH OH溶液中Ag的数目为0.1N
3 2 A
6. 下列反应方程式书写正确的是
A. 乙烯与溴的加成:CH CH Br CH CHBr
2 2 2 3 2
B. 乙醛的氧化:2CH CHOO 一定条件2CH COOH2H O
3 2 3 2
第 1 页 共 6 页
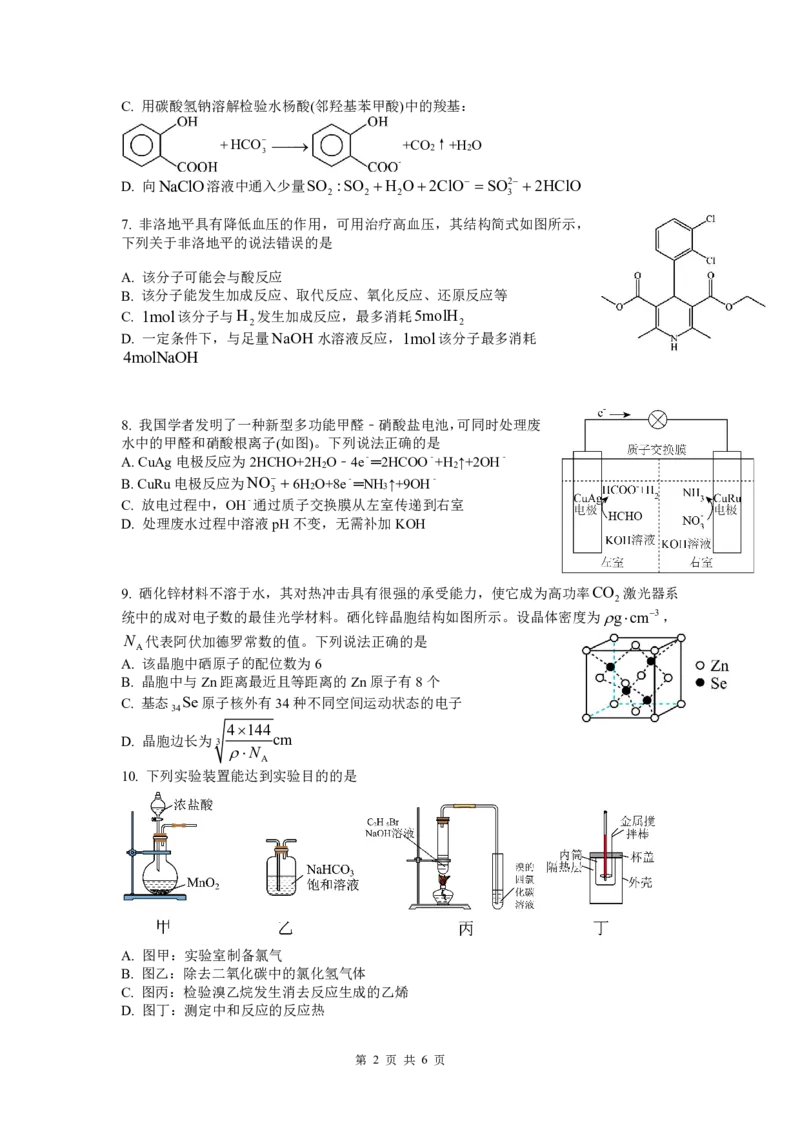
{#{QQABbYAUogigAIJAABhCUQEgCEEQkBGCAQoOhBAYsAAAyBFABAA=}#}C. 用碳酸氢钠溶解检验水杨酸(邻羟基苯甲酸)中的羧基:
+HCO +CO ↑+H O
3 2 2
D. 向NaClO溶液中通入少量SO :SO H O2ClO SO2 2HClO
2 2 2 3
7. 非洛地平具有降低血压的作用,可用治疗高血压,其结构简式如图所示,
下列关于非洛地平的说法错误的是
A. 该分子可能会与酸反应
B. 该分子能发生加成反应、取代反应、氧化反应、还原反应等
C. 1mol该分子与H 发生加成反应,最多消耗5molH
2 2
D. 一定条件下,与足量NaOH水溶液反应,1mol该分子最多消耗
4molNaOH
8. 我国学者发明了一种新型多功能甲醛﹣硝酸盐电池,可同时处理废
水中的甲醛和硝酸根离子(如图)。下列说法正确的是
A.CuAg电极反应为2HCHO+2H O﹣4e﹣═2HCOO﹣+H ↑+2OH﹣
2 2
B.CuRu电极反应为NO 6H O+8e﹣═NH ↑+9OH﹣
3 2 3
C. 放电过程中,OH﹣通过质子交换膜从左室传递到右室
D. 处理废水过程中溶液pH不变,无需补加KOH
9. 硒化锌材料不溶于水,其对热冲击具有很强的承受能力,使它成为高功率CO 激光器系
2
统中的成对电子数的最佳光学材料。硒化锌晶胞结构如图所示。设晶体密度为gcm3,
N 代表阿伏加德罗常数的值。下列说法正确的是
A
A. 该晶胞中硒原子的配位数为6
B. 晶胞中与Zn距离最近且等距离的Zn原子有8个
C. 基态 Se原子核外有34种不同空间运动状态的电子
34
4144
D. 晶胞边长为 3 cm
N
A
10. 下列实验装置能达到实验目的的是
A. 图甲:实验室制备氯气
B. 图乙:除去二氧化碳中的氯化氢气体
C. 图丙:检验溴乙烷发生消去反应生成的乙烯
D. 图丁:测定中和反应的反应热
第 2 页 共 6 页
{#{QQABbYAUogigAIJAABhCUQEgCEEQkBGCAQoOhBAYsAAAyBFABAA=}#}11. 短周期主族元素W、X、Y、Z的原子序数依次增大,其中W、X和Y的原子序数之和
为22,基态X原子核外未成对电子数为3,Y元素无正化合价,Z单质遇冷的浓硫酸会发
生钝化。下列说法错误的是
A.Y、Z形成的二元化合物为共价化合物
B. 离子半径:X>Y>Z
C.W单质和Y单质的晶体类型可能相同
D. 第一电离能:Y>X>W
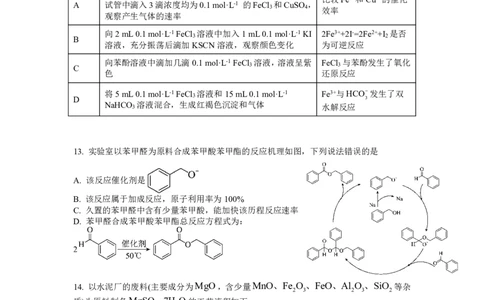
12. 室温下,探究0.1mol·L-1FeCl 溶液的性质,下列实验方案能达到探究目的的是
3
选项 探究方案 探究目的
向两支试管中分别加入5mL5%的H O 溶液,再向两支
2 2 比较Fe3+和Cu2+的催化
A 试管中滴入3滴浓度均为0.1mol·L-1 的FeCl 和CuSO ,
3 4 效率
观察产生气体的速率
向2mL0.1mol·L-1FeCl 溶液中加入1mL0.1mol·L-1KI 2Fe3++2I-=2Fe2++I 是否
3 2
B
溶液,充分振荡后滴加KSCN溶液,观察颜色变化 为可逆反应
向苯酚溶液中滴加几滴0.1mol·L-1FeCl 溶液,溶液呈紫 FeCl 与苯酚发生了氧化
3 3
C
色 还原反应
将5mL0.1mol·L-1FeCl 溶液和15mL0.1mol·L-1 Fe3+与HCO发生了双
D 3 3
NaHCO 3 溶液混合,生成红褐色沉淀和气体 水解反应
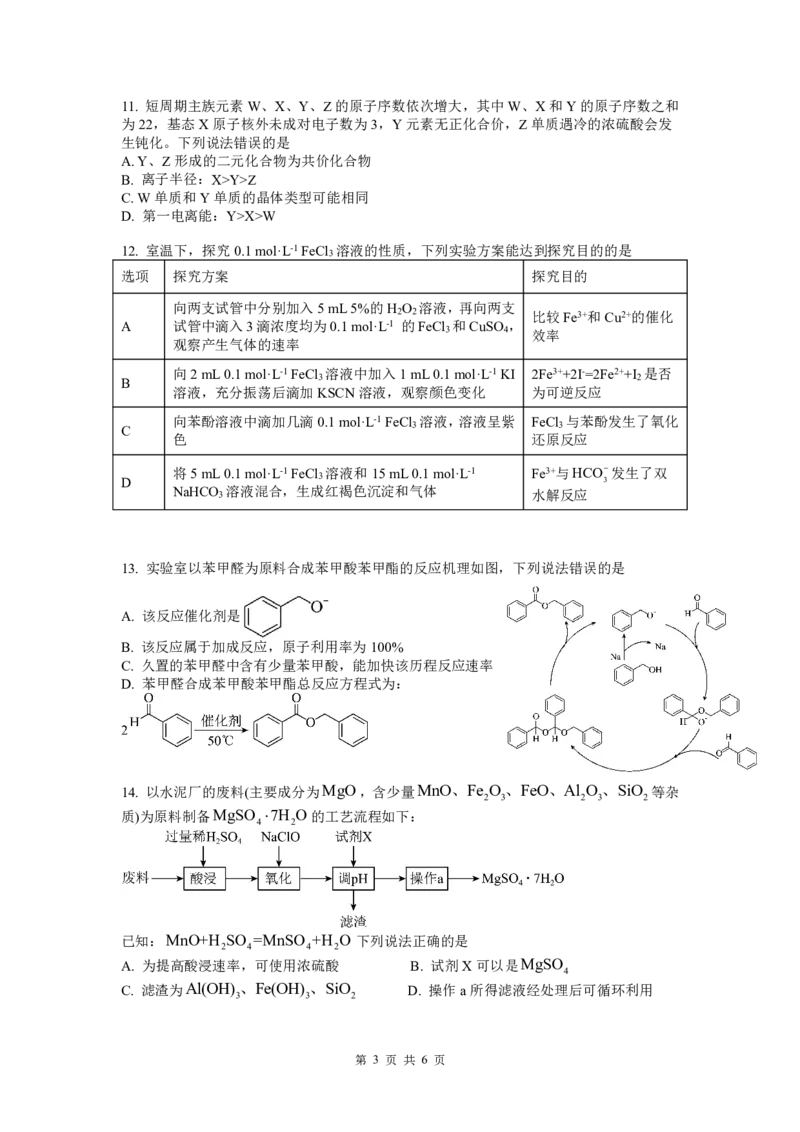
13. 实验室以苯甲醛为原料合成苯甲酸苯甲酯的反应机理如图,下列说法错误的是
A. 该反应催化剂是
B. 该反应属于加成反应,原子利用率为100%
C. 久置的苯甲醛中含有少量苯甲酸,能加快该历程反应速率
D. 苯甲醛合成苯甲酸苯甲酯总反应方程式为:
14. 以水泥厂的废料(主要成分为MgO,含少量MnO、Fe O、FeO、Al O、SiO 等杂
2 3 2 3 2
质)为原料制备MgSO 7H O的工艺流程如下:
4 2
已知:MnO+H SO =MnSO +H O 下列说法正确的是
2 4 4 2
A. 为提高酸浸速率,可使用浓硫酸 B. 试剂X可以是MgSO
4
C. 滤渣为Al(OH)、Fe(OH)、SiO D. 操作a所得滤液经处理后可循环利用
3 3 2
第 3 页 共 6 页
{#{QQABbYAUogigAIJAABhCUQEgCEEQkBGCAQoOhBAYsAAAyBFABAA=}#}15. 25C , K CH COOH K NH H O 。向 20mL 浓度均为 0.01molL1 的
2 3 b 3 2
NaOH和NH H O混合溶液中逐滴加入mmolL1的醋酸溶液,溶液电导率、pOH随醋
3 2
酸体积增加的变化趋势如图所示。已知pOHlgc
OH
,下列说法正确的是
A.a点,pOH2 B.b点,c
Na
c
NH
c
CH
COO
4 3
C. 若d点V
CH COOH
40mL,则m0.01
D. 水的电离程度:a bcd
3
二、非选择题:本题共 4小题,共 55分。
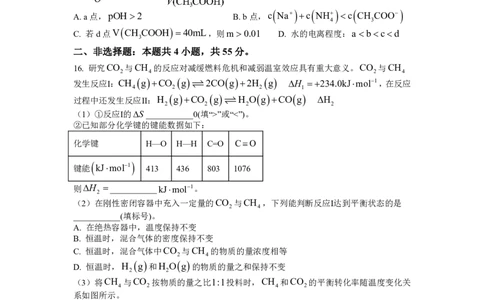
16. 研究CO 与CH 的反应对减缓燃料危机和减弱温室效应具有重大意义。CO 与CH
2 4 2 4
发生反应Ⅰ:CH g CO g 2CO g 2H g H 234.0kJmol1,在反应
4 2 2 1
过程中还发生反应Ⅱ:H
g
CO
g
H O
g
CO
g
ΔH
2 2 2 2
(1)①反应Ⅰ的S ___________0(填“>”或“<”)。
②已知部分化学键的键能数据如下:
化学键 H—O H—H C=O CO
键能 kJmol1 413 436 803 1076
则H ___________kJmol1。
2
(2)在刚性密闭容器中充入一定量的CO 与CH ,下列能判断反应Ⅰ达到平衡状态的是
2 4
___________(填标号)。
A. 在绝热容器中,温度保持不变
B. 恒温时,混合气体的密度保持不变
C. 恒温时,混合气体中CO 与CH 的物质的量浓度相等
2 4
D. 恒温时,H g 和H O g 的物质的量之和保持不变
2 2
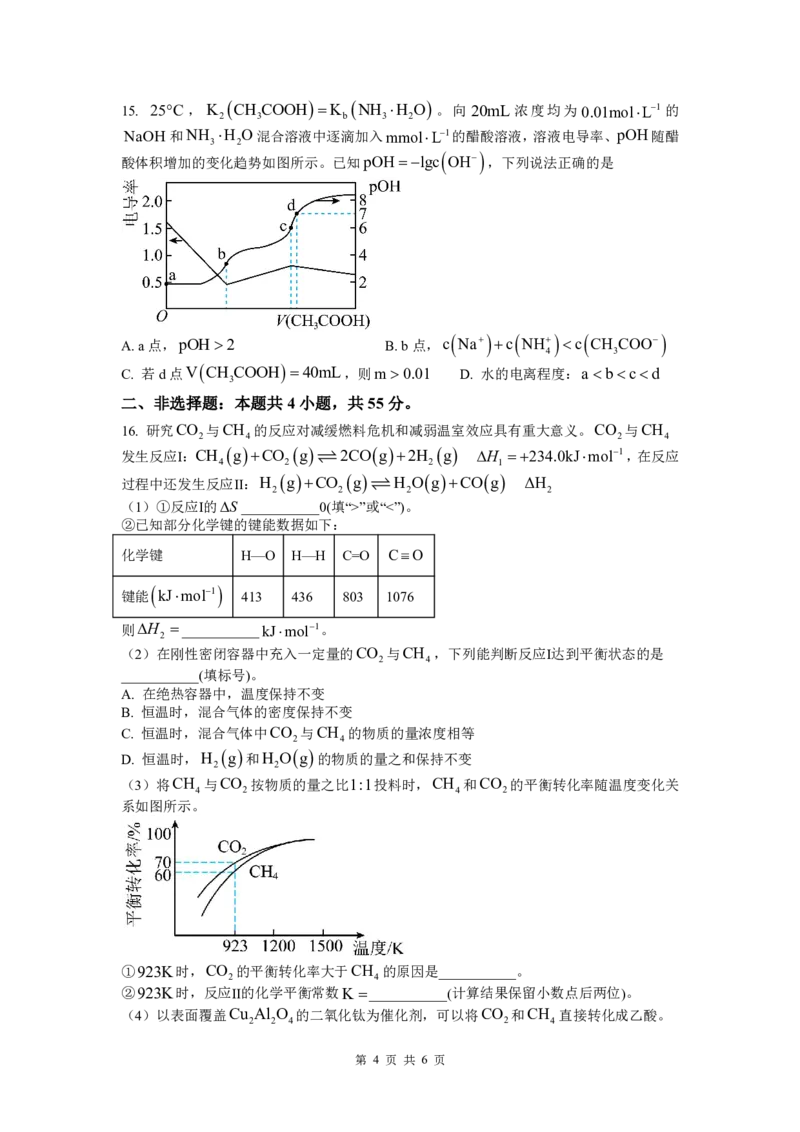
(3)将CH 与CO 按物质的量之比1:1投料时,CH 和CO 的平衡转化率随温度变化关
4 2 4 2
系如图所示。
①923K时,CO 的平衡转化率大于CH 的原因是___________。
2 4
②923K时,反应Ⅱ的化学平衡常数K___________(计算结果保留小数点后两位)。
(4)以表面覆盖Cu Al O 的二氧化钛为催化剂,可以将CO 和CH 直接转化成乙酸。
2 2 4 2 4
第 4 页 共 6 页
{#{QQABbYAUogigAIJAABhCUQEgCEEQkBGCAQoOhBAYsAAAyBFABAA=}#}①为了提高该反应中CH 的平衡转化率,可以采取的措施是___________(任写一种)。
4
②催化剂在该反应中的作用是___________(填标号)。
A.降低反应的活化能 B.降低反应的焓变
C.改变反应的历程 D.增大反应的平衡常数
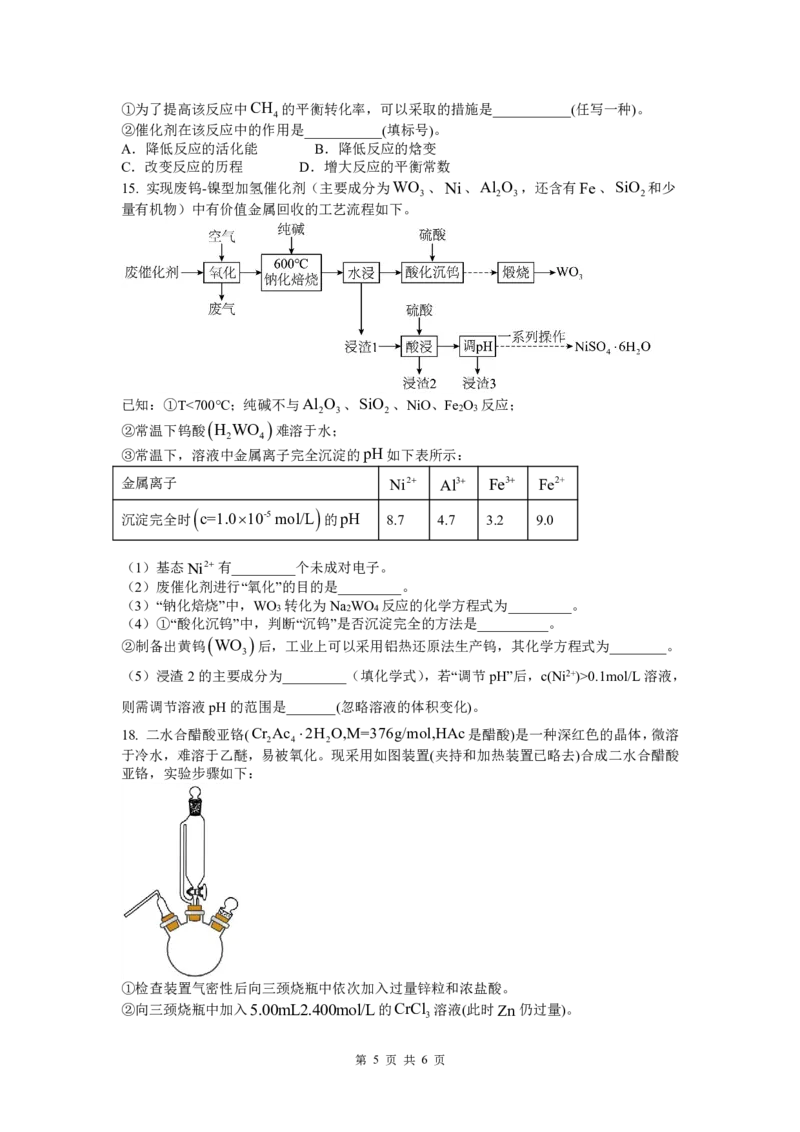
15. 实现废钨-镍型加氢催化剂(主要成分为WO 、Ni、Al O ,还含有Fe、SiO 和少
3 2 3 2
量有机物)中有价值金属回收的工艺流程如下。
已知:①T<700℃;纯碱不与Al O 、SiO 、NiO、Fe O 反应;
2 3 2 2 3
②常温下钨酸 H WO 难溶于水;
2 4
③常温下,溶液中金属离子完全沉淀的pH如下表所示:
金属离子 Ni2 Al3 Fe3 Fe2+
沉淀完全时 c=1.010-5mol/L 的pH 8.7 4.7 3.2 9.0
(1)基态Ni2有_________个未成对电子。
(2)废催化剂进行“氧化”的目的是_________。
(3)“钠化焙烧”中,WO 转化为Na WO 反应的化学方程式为_________。
3 2 4
(4)①“酸化沉钨”中,判断“沉钨”是否沉淀完全的方法是__________。
②制备出黄钨 WO 后,工业上可以采用铝热还原法生产钨,其化学方程式为________。
3
(5)浸渣2的主要成分为_________(填化学式),若“调节pH”后,c(Ni2+)>0.1mol/L溶液,
则需调节溶液pH的范围是_______(忽略溶液的体积变化)。
18. 二水合醋酸亚铬(Cr Ac 2H O,M=376g/mol,HAc是醋酸)是一种深红色的晶体,微溶
2 4 2
于冷水,难溶于乙醚,易被氧化。现采用如图装置(夹持和加热装置已略去)合成二水合醋酸
亚铬,实验步骤如下:
①检查装置气密性后向三颈烧瓶中依次加入过量锌粒和浓盐酸。
②向三颈烧瓶中加入5.00mL2.400mol/L的CrCl 溶液(此时Zn仍过量)。
3
第 5 页 共 6 页
{#{QQABbYAUogigAIJAABhCUQEgCEEQkBGCAQoOhBAYsAAAyBFABAA=}#}③待溶液中由深绿色变为蓝色时,表明得到Cr(Ⅱ)溶液,再向三颈烧瓶中加入过量的NaAc
溶液,并进行加热。
④待不再出现晶体时,停止加热,随后将装置置于冰水浴中冷却。
⑤将沉淀过滤后分别用冷水和无水乙醚洗涤两次,在密闭容器中减压抽干,称量得到产物
1.880g。
根据以上信息,回答以下问题:
(1)实验中使用的恒压滴液漏斗相对于普通的分液漏斗的优点是___________。
(2)步骤①的目的是___________,另配制本实验中所用到的溶液时,需要对蒸馏水进行
___________操作。
(3)写出步骤②发生的离子方程式:___________。
(4)为了减少晶体中的Cr元素被氧化,我们应该尽可能让得到的晶体体积更大,解释其原
因___________。
(5)步骤⑤用乙醚洗涤的目的是___________。
(6)计算最终产率为___________(保留2位有效数字)。
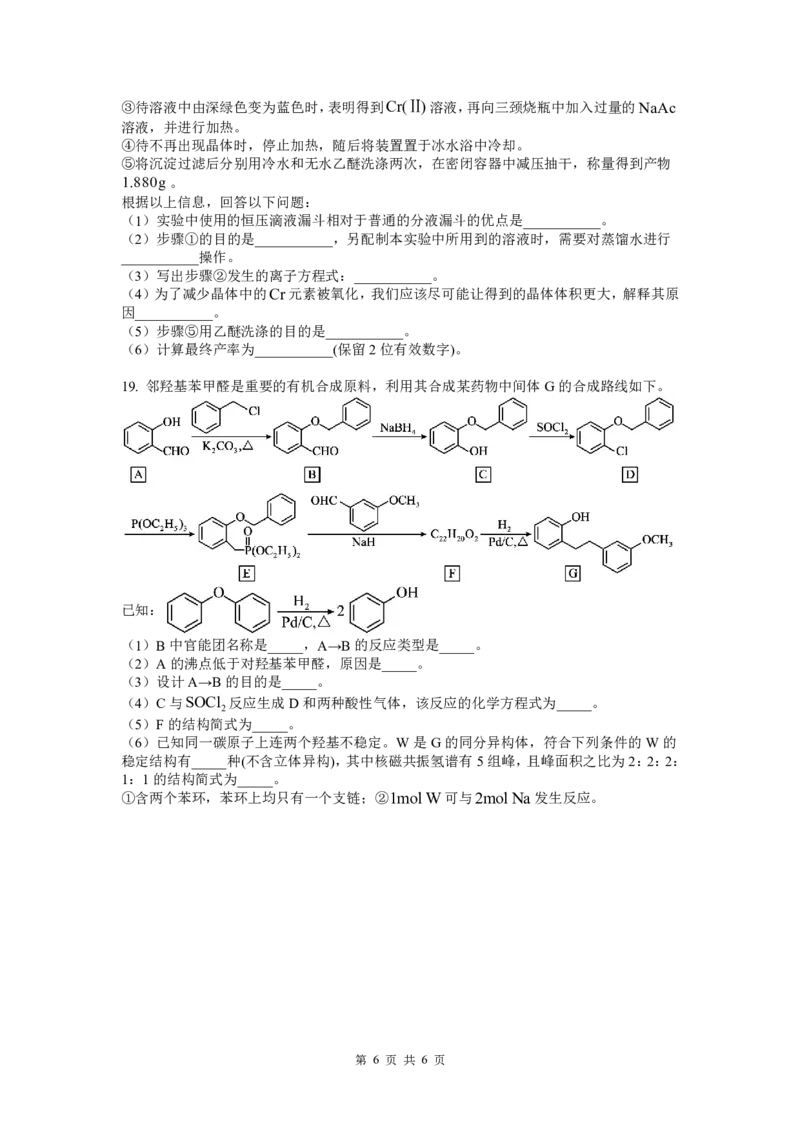
19. 邻羟基苯甲醛是重要的有机合成原料,利用其合成某药物中间体G的合成路线如下。
已知:
(1)B中官能团名称是_____,A→B的反应类型是_____。
(2)A的沸点低于对羟基苯甲醛,原因是_____。
(3)设计A→B的目的是_____。
(4)C与SOCl 反应生成D和两种酸性气体,该反应的化学方程式为_____。
2
(5)F的结构简式为_____。
(6)已知同一碳原子上连两个羟基不稳定。W是G的同分异构体,符合下列条件的W的
稳定结构有_____种(不含立体异构),其中核磁共振氢谱有5组峰,且峰面积之比为2:2:2:
1:1的结构简式为_____。
①含两个苯环,苯环上均只有一个支链;②1mol W可与2mol Na发生反应。
第 6 页 共 6 页
{#{QQABbYAUogigAIJAABhCUQEgCEEQkBGCAQoOhBAYsAAAyBFABAA=}#}纳溪中学高 2023 级高三年级上期第二次月考化学参考答案
一、选择题答案
1-5.BBCAB
6-10.CDBDB
11-15.ADDDC
二、填空题
16、(1) > +140
(2)AD
(3)反应Ⅰ中CH 和CO 的转化率相同,CO 又发生反应Ⅱ,转化率增大 0.39
4 2 2
(4) 增大CO 浓度、增大压强等 AC
2
17、(1) 2
(2)除去有机物,氧化Fe和Ni
高温
(3)WO Na CO Na WO CO
3 2 3 2 4 2
(4)①将沉淀后的悬浊液静置分层,向上层清液中继续滴加硫酸,若无明显现象,
则沉淀完全;若上层清液变浑浊,则沉淀不完全
高温
②. WO 2Al WAl O
3 2 3
SiO
(5) 2 4.7≤pH<7.3
18. (1)平衡气压,利于液体顺利滴下
(2) ①. 产生H ,排尽装置内空气,防止Cr2+被氧化 ②. 煮沸
2
(3)减小晶体与空气的接触面积,减缓晶体被氧化的速度
(4)洗掉晶体表面残留的水,同时减少产品溶解损耗
(5)83%
19. (1)醛基、醚键 取代反应
(2)A形成分子内氢键,对羟基苯甲醛形成分子间氢键
(3)保护酚羟基不被氧化
(4)
(5)
(6) 9
{#{QQABbYAUogigAIJAABhCUQEgCEEQkBGCAQoOhBAYsAAAyBFABAA=}#}