文档内容
专题47 电解应用
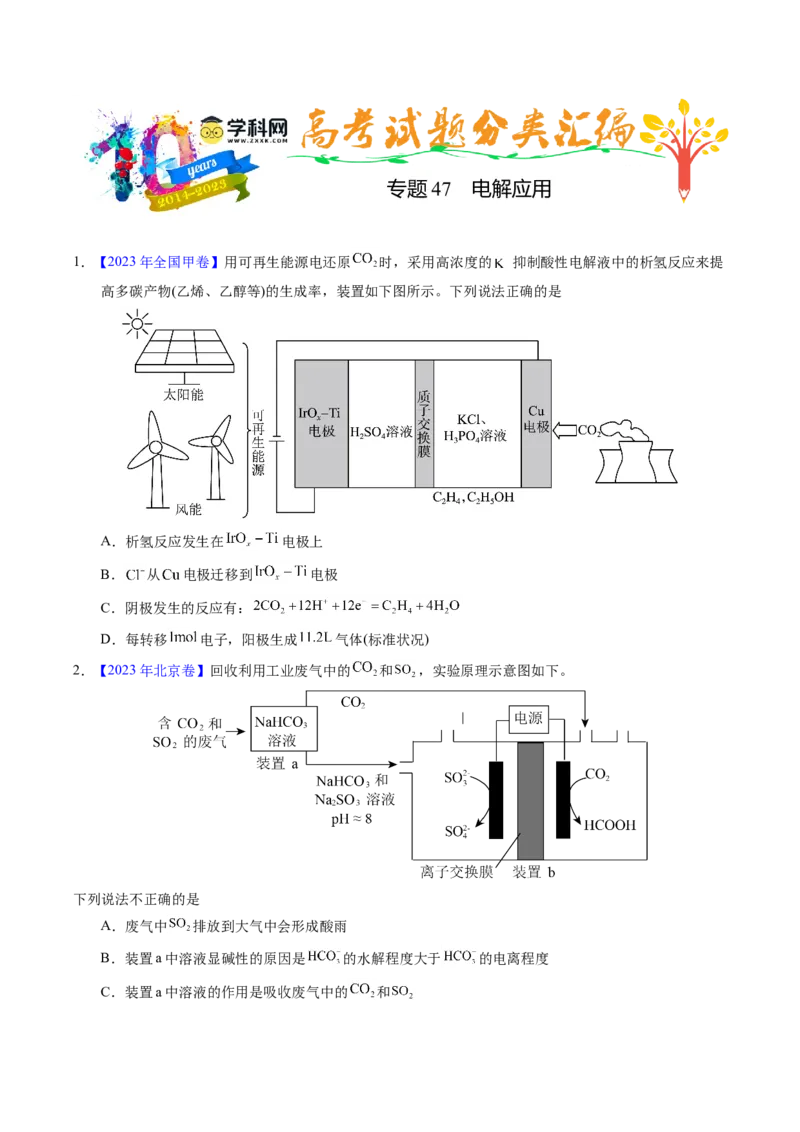
1.【2023年全国甲卷】用可再生能源电还原 时,采用高浓度的 抑制酸性电解液中的析氢反应来提
高多碳产物(乙烯、乙醇等)的生成率,装置如下图所示。下列说法正确的是
A.析氢反应发生在 电极上
B. 从 电极迁移到 电极
C.阴极发生的反应有:
D.每转移 电子,阳极生成 气体(标准状况)
2.【2023年北京卷】回收利用工业废气中的 和 ,实验原理示意图如下。
下列说法不正确的是
A.废气中 排放到大气中会形成酸雨
B.装置a中溶液显碱性的原因是 的水解程度大于 的电离程度
C.装置a中溶液的作用是吸收废气中的 和D.装置 中的总反应为
3.(2021·湖北真题)NaCr O 的酸性水溶液随着H+浓度的增大会转化为CrO。电解法制备CrO 的原理
2 2 7 3 3
如图所示。下列说法错误的是
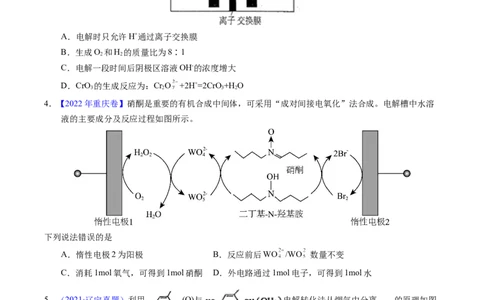
A.电解时只允许H+通过离子交换膜
B.生成O 和H 的质量比为8∶1
2 2
C.电解一段时间后阴极区溶液OH-的浓度增大
D.CrO 的生成反应为:Cr O +2H+=2CrO +H O
3 2 3 2
4.【2022年重庆卷】硝酮是重要的有机合成中间体,可采用“成对间接电氧化”法合成。电解槽中水溶
液的主要成分及反应过程如图所示。
下列说法错误的是
A.惰性电极2为阳极 B.反应前后WO /WO 数量不变
C.消耗1mol氧气,可得到1mol硝酮 D.外电路通过1mol电子,可得到1mol水
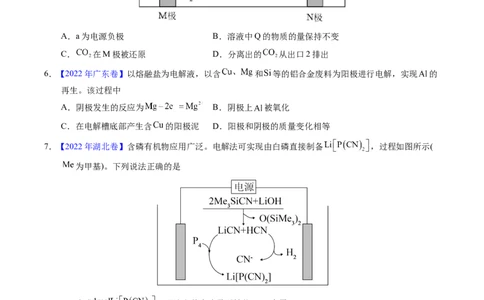
5.(2021·辽宁真题)利用 (Q)与 电解转化法从烟气中分离 的原理如图。
已知气体可选择性通过膜电极,溶液不能通过。下列说法错误的是A.a为电源负极 B.溶液中Q的物质的量保持不变
C. 在M极被还原 D.分离出的 从出口2排出
6.【2022年广东卷】以熔融盐为电解液,以含 和 等的铝合金废料为阳极进行电解,实现 的
再生。该过程中
A.阴极发生的反应为 B.阴极上 被氧化
C.在电解槽底部产生含 的阳极泥 D.阳极和阴极的质量变化相等
7.【2022年湖北卷】含磷有机物应用广泛。电解法可实现由白磷直接制备 ,过程如图所示(
为甲基)。下列说法正确的是
A.生成 ,理论上外电路需要转移 电子
B.阴极上的电极反应为:
C.在电解过程中 向铂电极移动
D.电解产生的 中的氢元素来自于
8.(2020·浙江高考真题)电解高浓度RCOONa(羧酸钠)的NaOH溶液,在阳极RCOO-放电可得到R-R(烷烃)。
下列说法不正确的是( )通电
A.电解总反应方程式:2RCOONa+2H O ¿R-R+2CO ↑+H ↑+2NaOH
2 2 2
¿
B.RCOO-在阳极放电,发生氧化反应
C.阴极的电极反应:2H O+2e-=2OH-+H ↑
2 2
D.电解CH COONa、CH CH COONa和NaOH混合溶液可得到乙烷、丙烷和丁烷
3 3 2
9.(2017·全国高考真题)用电解氧化法可以在铝制品表面形成致密、耐腐蚀的氧化膜,电解质溶液一般
为 混合溶液。下列叙述错误的是
A.待加工铝质工件为阳极
B.可选用不锈钢网作为阴极
C.阴极的电极反应式为:
D.硫酸根离子在电解过程中向阳极移动
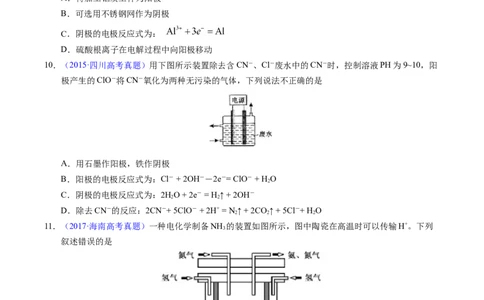
10.(2015·四川高考真题)用下图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳
极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是
A.用石墨作阳极,铁作阴极
B.阳极的电极反应式为:Cl- + 2OH--2e-= ClO- + H O
2
C.阴极的电极反应式为:2HO + 2e- = H ↑ + 2OH-
2 2
D.除去CN-的反应:2CN-+ 5ClO- + 2H+ = N ↑ + 2CO ↑ + 5Cl-+ H O
2 2 2
11.(2017·海南高考真题)一种电化学制备NH 的装置如图所示,图中陶瓷在高温时可以传输H+。下列
3
叙述错误的是
A.Pd电极b为阴极
B.阴极的反应式为:N+6H++6e− 2NH
2 3
C.H+由阳极向阴极迁移
D.陶瓷可以隔离N 和H
2 212.(2012·浙江高考真题)以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:
下列说法不正确的是
A.在阴极式,发生的电极反应为:2HO+2e- 2OH―+H↑
2 2
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2 +2H+
+HO向右移动
2
C.该制备过程总反应的化学方程式为:4KCrO+4HO 2KCr O+4KOH+2H↑+2O↑
2 4 2 2 2 7 2 2
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比为d,则此时铬酸钾的转化率为α=
13.(2013·海南高考真题)下列叙述正确的是
A.合成氨的“造气”阶段会产生废气
B.电镀的酸性废液用碱中和后就可以排放
C.电解制铝的过程中,作为阳极材料的无烟煤不会消耗
D.使用煤炭转化的管道煤气比直接燃煤可减少环境污染
14.(2013·全国高考真题)电解法处理酸性含铬废水(主要含有Cr O2-)时,以铁板作阴、阳极,处理过
2 7
程中存在反应Cr O2-+6Fe2++14H+=2Cr3++6Fe3++7HO,最后Cr3+以Cr(OH) 形式除去,下列说法
2 7 2 3
不正确的是
A.阳极反应为Fe-2e-=Fe2+
B.电解过程中溶液pH不会变化
C.过程中有Fe(OH) 沉淀生成
3
D.电路中每转移12 mol电子,最多有1 mol Cr O2-被还原
2 7
15.(2013·北京高考真题)用石墨电极电解CuCl 溶液(见右图)。下列分析正确的是
2
A.a端是直流电源的负极B.通电使CuCl 发生电离
2
C.阳极上发生的反应:Cu2++2e-=Cu
D.通电一段时间后,在阴极附近观察到黄绿色气体
16.(2010·海南高考真题)利用电解法可将含有Fe、Zn、Ag、Au等杂质的粗铜提纯,下列叙述正确的是
A.电解时以纯铜作阳极
B.电解时阴极发生氧化反应
C.粗铜连接电源负极,电极反应是Cu -2e-=Cu2+
D.电解结束,电解槽底部会形成含少量Ag、Au等阳极泥
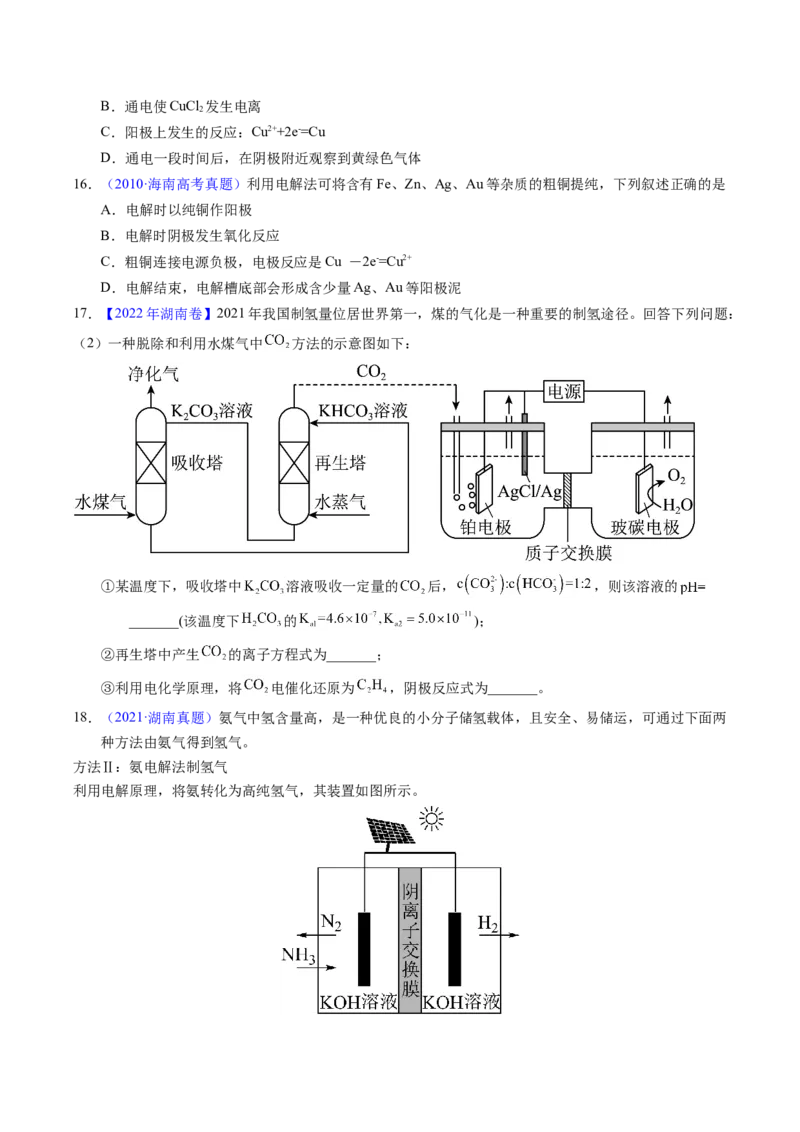
17.【2022年湖南卷】2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回答下列问题:
(2)一种脱除和利用水煤气中 方法的示意图如下:
①某温度下,吸收塔中 溶液吸收一定量的 后, ,则该溶液的
_______(该温度下 的 );
②再生塔中产生 的离子方程式为_______;
③利用电化学原理,将 电催化还原为 ,阴极反应式为_______。
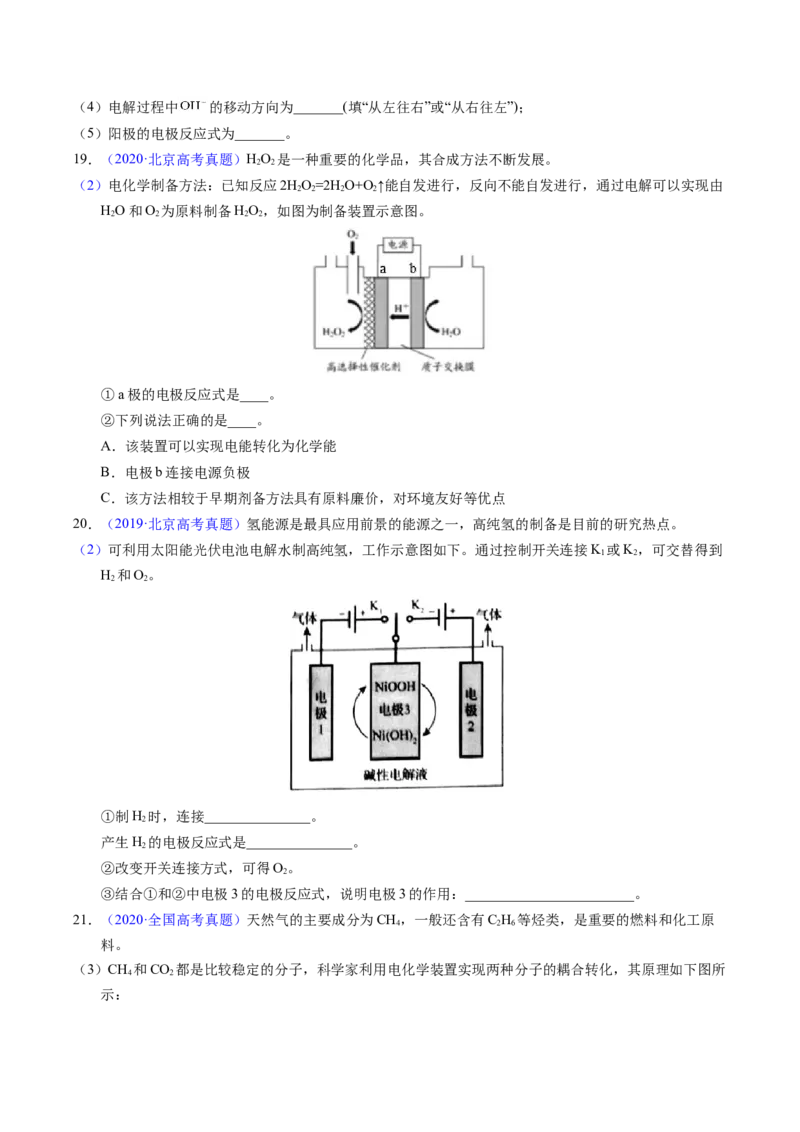
18.(2021·湖南真题)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两
种方法由氨气得到氢气。
方法Ⅱ:氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。(4)电解过程中 的移动方向为_______(填“从左往右”或“从右往左”);
(5)阳极的电极反应式为_______。
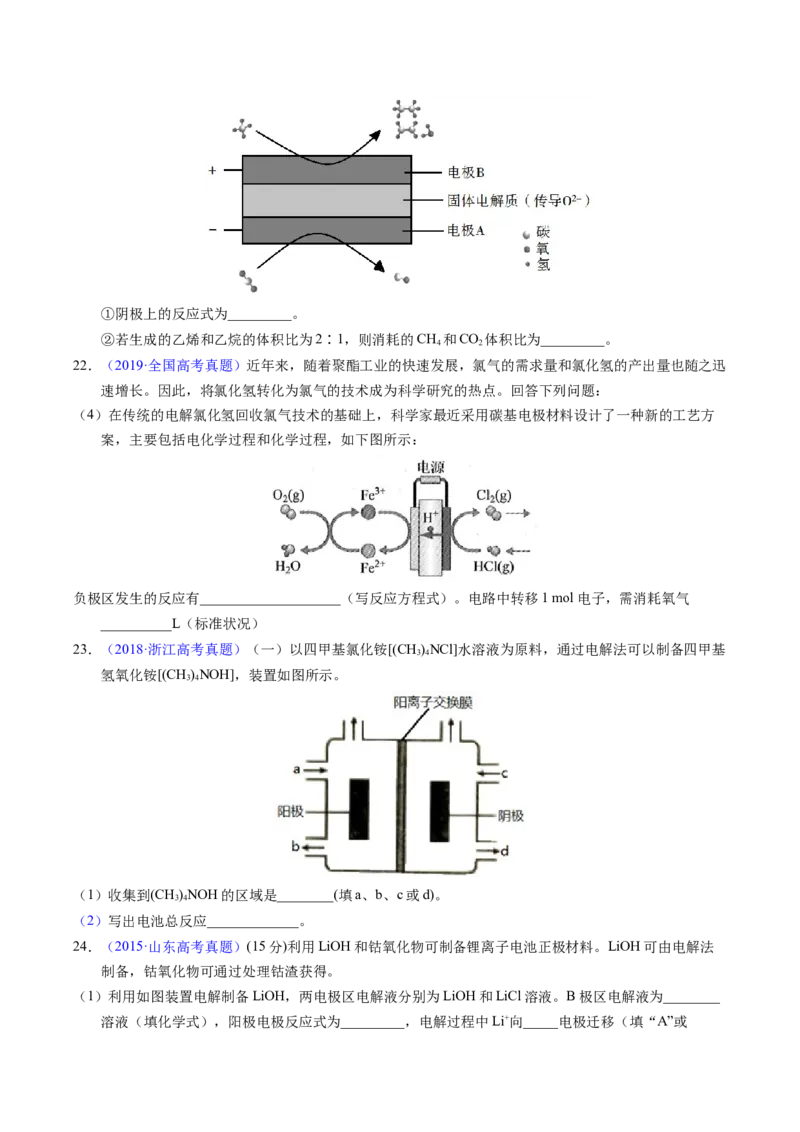
19.(2020·北京高考真题)HO 是一种重要的化学品,其合成方法不断发展。
2 2
(2)电化学制备方法:已知反应2HO=2H O+O↑能自发进行,反向不能自发进行,通过电解可以实现由
2 2 2 2
HO和O 为原料制备HO,如图为制备装置示意图。
2 2 2 2
①a极的电极反应式是____。
②下列说法正确的是____。
A.该装置可以实现电能转化为化学能
B.电极b连接电源负极
C.该方法相较于早期剂备方法具有原料廉价,对环境友好等优点
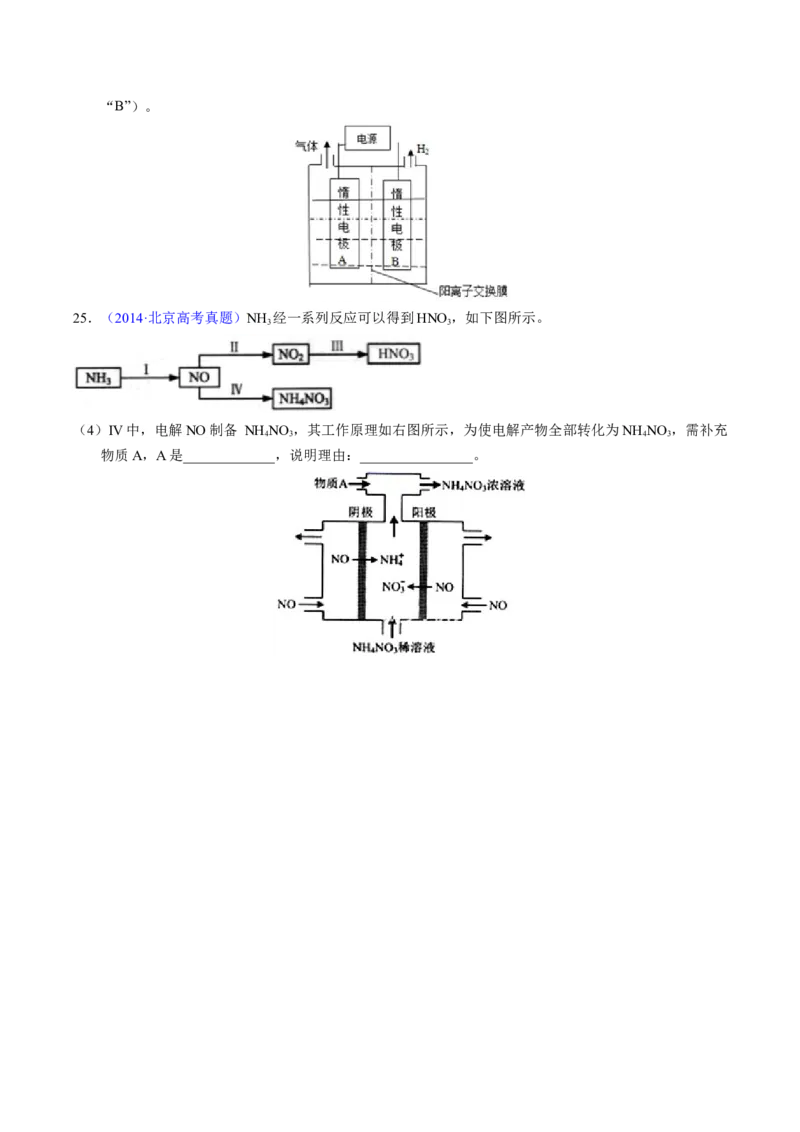
20.(2019·北京高考真题)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
(2)可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K 或K,可交替得到
1 2
H 和O。
2 2
①制H 时,连接_______________。
2
产生H 的电极反应式是_______________。
2
②改变开关连接方式,可得O。
2
③结合①和②中电极3的电极反应式,说明电极3的作用:________________________。
21.(2020·全国高考真题)天然气的主要成分为CH,一般还含有C H 等烃类,是重要的燃料和化工原
4 2 6
料。
(3)CH 和CO 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所
4 2
示:①阴极上的反应式为_________。
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH 和CO 体积比为_________。
4 2
22.(2019·全国高考真题)近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅
速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
(4)在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方
案,主要包括电化学过程和化学过程,如下图所示:
负极区发生的反应有____________________(写反应方程式)。电路中转移1 mol电子,需消耗氧气
__________L(标准状况)
23.(2018·浙江高考真题)(一)以四甲基氯化铵[(CH )NCl]水溶液为原料,通过电解法可以制备四甲基
3 4
氢氧化铵[(CH )NOH],装置如图所示。
3 4
(1)收集到(CH)NOH的区域是________(填a、b、c或d)。
3 4
(2)写出电池总反应_____________。
24.(2015·山东高考真题)(15分)利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法
制备,钴氧化物可通过处理钴渣获得。
(1)利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为________
溶液(填化学式),阳极电极反应式为_________,电解过程中Li+向_____电极迁移(填“A”或“B”)。
25.(2014·北京高考真题)NH 经一系列反应可以得到HNO,如下图所示。
3 3
(4)IV中,电解NO制备 NH NO ,其工作原理如右图所示,为使电解产物全部转化为NH NO ,需补充
4 3 4 3
物质A,A是_____________,说明理由:________________。