文档内容
专题52 化学反应速率
1.【2023年山东卷】一定条件下,化合物E和TFAA合成H的反应路径如下:
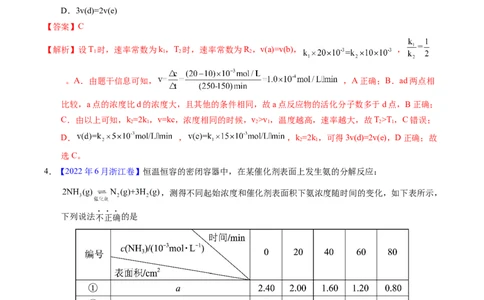
已知反应初始E的浓度为0.10mol∙L-1,TFAA的浓度为0.08mol∙L-1,部分物种的浓度随时间的变化关系如
图所示,忽略反应过程中的体积变化。下列说法正确的是
A.t 时刻,体系中有E存在
1
B.t 时刻,体系中无F存在
2
C.E和TFAA反应生成F的活化能很小
D.反应达平衡后,TFAA的浓度为0.08mol∙L-1
【答案】AC
【解析】一定条件下,化合物E和TFAA合成H的反应路径中,共发生三个反应:
①E+TFAA F ②F G ③G H+TFAA
t 之后的某时刻,H为0.02 mol∙L-1,此时TFAA的浓度仍为0,则表明0.10mol∙L-1E、起始时的
1
0.08mol∙L-1TFAA、G分解生成的0.02 mol∙L-1 TFAA全部参加反应,生成0.10mol∙L-1F;在t 时刻,H
2
为0.08mol∙L-1,TFAA为0.06mol∙L-1,G为0.01 mol∙L-1,则F为0.01 mol∙L-1。A.由图可知,反应0时
刻后,TFAA的浓度由0.08mol/L降为0,说明E与TFAA反应极快,根据合成路线可知,E与TFAA以
1:1进行反应,E的起始浓度为0.1 mol/L,则反应后E的浓度降为0.02 mol/L,故t 时刻体系中有E存
1
在,A正确;B.由分析可知,t 时刻,H为0.08mol∙L-1,TFAA为0.06mol∙L-1,G为0.01 mol∙L-1,则F
2
为0.01 mol∙L-1,所以体系中有F存在,B不正确;C.t 之后的某时刻,H为0.02 mol∙L-1,此时TFAA
1
的浓度仍为0,表明此时E和TFAA完全反应生成F,所以E和TFAA生成F的反应速率快,反应的活化能很小,C正确;D.在t 时刻,H为0.08mol∙L-1,TFAA为0.06mol∙L-1,G为0.01 mol∙L-1,F为
2
0.01 mol∙L-1,只有F、G全部转化为H和TFAA时,TFAA的浓度才能为0.08mol∙L-1,而G
H+TFAA为可逆反应,所以反应达平衡后,TFAA的浓度一定小于0.08mol∙L-1,D不正确;故选AC。
2.【2022年北京卷】CO 捕获和转化可减少CO 排放并实现资源利用,原理如图1所示。反应①完成之后,
2 2
以N 为载气,以恒定组成的N、CH 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物
2 2 4
质的量随反应时间变化如图2所示。反应过程中始终未检测到CO,在催化剂上有积碳。
2
下列说法不正确的是
A.反应①为CaO+CO =CaCO ;反应②为CaCO +CH CaO+2CO+2H
2 3 3 4 2
B.t~t,n(H )比n(CO)多,且生成H 速率不变,可能有副反应CH C+2H
1 3 2 2 4 2
C.t 时刻,副反应生成H 的速率大于反应②生成H 速率
2 2 2
D.t 之后,生成CO的速率为0,是因为反应②不再发生
3
【答案】C
【解析】A.由题干图1所示信息可知,反应①为CaO+CO =CaCO ,结合氧化还原反应配平可得反应②为
2 3
,A正确;B.由题干图2信息可知,t~t,n(H )比n(CO)多,且生
1 3 2
成H 速率不变,且反应过程中始终未检测到CO,在催化剂上有积碳,故可能有副反应
2 2
,反应②和副反应中CH 和H 的系数比均为1:2,B正确;C.由题干反应②方程
4 2
式可知,H 和CO的反应速率相等,而t 时刻信息可知,H 的反应速率未变,仍然为2mmol/min,而
2 2 2
CO变为1~2mmol/min之间,故能够说明副反应生成H 的速率小于反应②生成H 速率,C错误;D.
2 2
由题干图2信息可知,t 之后,CO的速率为0,CH 的速率逐渐增大,最终恢复到1,说明生成CO的
3 4
速率为0,是因为反应②不再发生,而后副反应逐渐停止反应,D正确;答案选C。
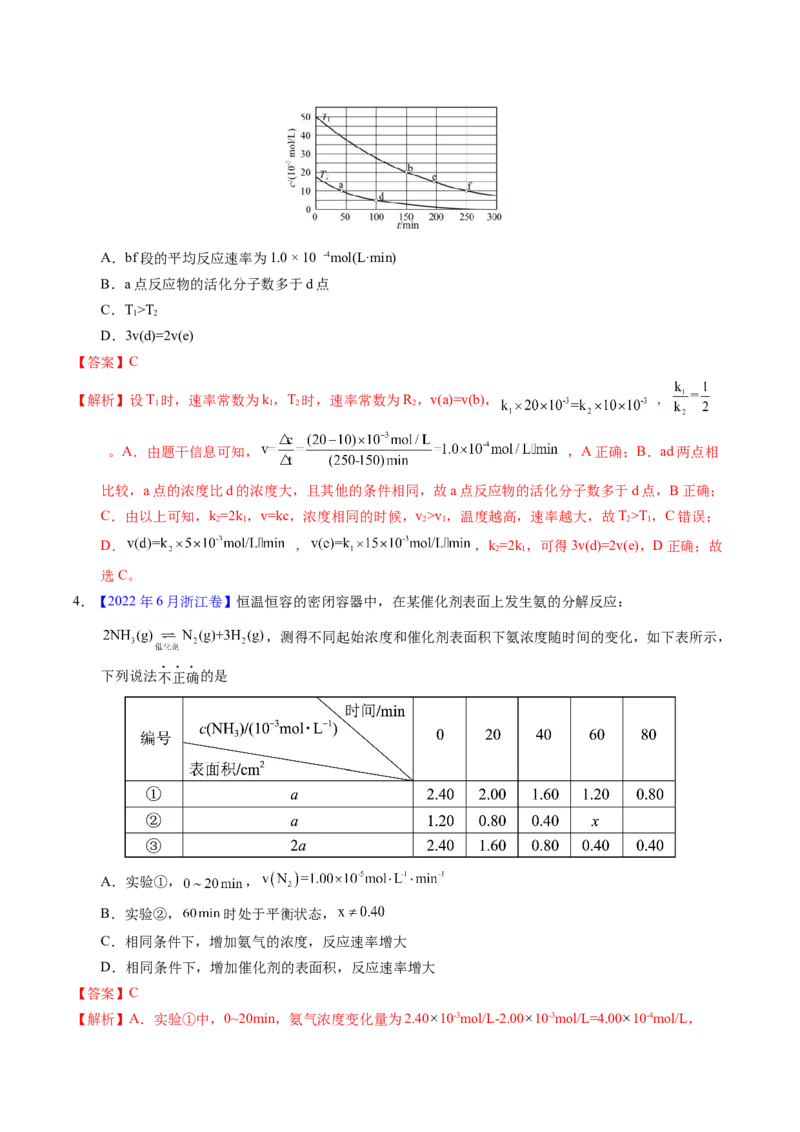
3.【2021年重庆卷】甲异腈(CHNC)在恒容密闭容器中发生异构化反应: CHNC(g) →CHCN(g),反应过
3 3
程中甲异腈浓度c随时间t的变化曲线如图所示(图中T为温度)。该反应的反应速率v与c的关系为
v=kc,k为速率常数(常温下为常数),a点和b点反应速率相等,即v(a)=v(b)。下列说法错误的是A.bf段的平均反应速率为1.0 × 10 -4mol(L·min)
B.a点反应物的活化分子数多于d点
C.T>T
1 2
D.3v(d)=2v(e)
【答案】C
【解析】设T 时,速率常数为k,T 时,速率常数为R ,v(a)=v(b), ,
1 1 2 2
。A.由题干信息可知, ,A正确;B.ad两点相
比较,a点的浓度比d的浓度大,且其他的条件相同,故a点反应物的活化分子数多于d点,B正确;
C.由以上可知,k=2k,v=kc,浓度相同的时候,v>v,温度越高,速率越大,故T>T,C错误;
2 1 2 1 2 1
D. , ,k=2k,可得3v(d)=2v(e),D正确;故
2 1
选C。
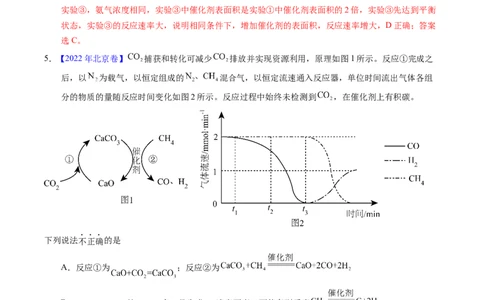
4.【2022年6月浙江卷】恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解反应:
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,
下列说法不正确的是
A.实验①, ,
B.实验②, 时处于平衡状态,
C.相同条件下,增加氨气的浓度,反应速率增大
D.相同条件下,增加催化剂的表面积,反应速率增大
【答案】C
【解析】A.实验①中,0~20min,氨气浓度变化量为2.40 10-3mol/L-2.00 10-3mol/L=4.00 10-4mol/L,v(NH )= =2.00 10-5mol/(L·min),反应速率之比等于化学计量数之比,v(N )=
3 2
v(NH )=1.00 10-5mol/(L·min),A正确;B.催化剂表面积大小只影响反应速率,不影响平衡,实验③
3
中氨气初始浓度与实验①中一样,实验③达到平衡时氨气浓度为4.00 10-4mol/L,则实验①达平衡时
氨气浓度也为4.00 10-4mol/L,而恒温恒容条件下,实验②相对于实验①为减小压强,平衡正向移动,
因此实验②60min时处于平衡状态,x<0.4,即x≠0.4,B正确;C.实验①、实验②中0~20min、
20min~40min氨气浓度变化量都是4.00 10-4mol/L,实验②中60min时反应达到平衡状态,实验①和实
验②催化剂表面积相同,实验①中氨气初始浓度是实验②中氨气初始浓度的两倍,实验①60min时反
应未达到平衡状态,相同条件下,增加氨气浓度,反应速率并没有增大,C错误;D.对比实验①和
实验③,氨气浓度相同,实验③中催化剂表面积是实验①中催化剂表面积的2倍,实验③先达到平衡
状态,实验③的反应速率大,说明相同条件下,增加催化剂的表面积,反应速率增大,D正确;答案
选C。
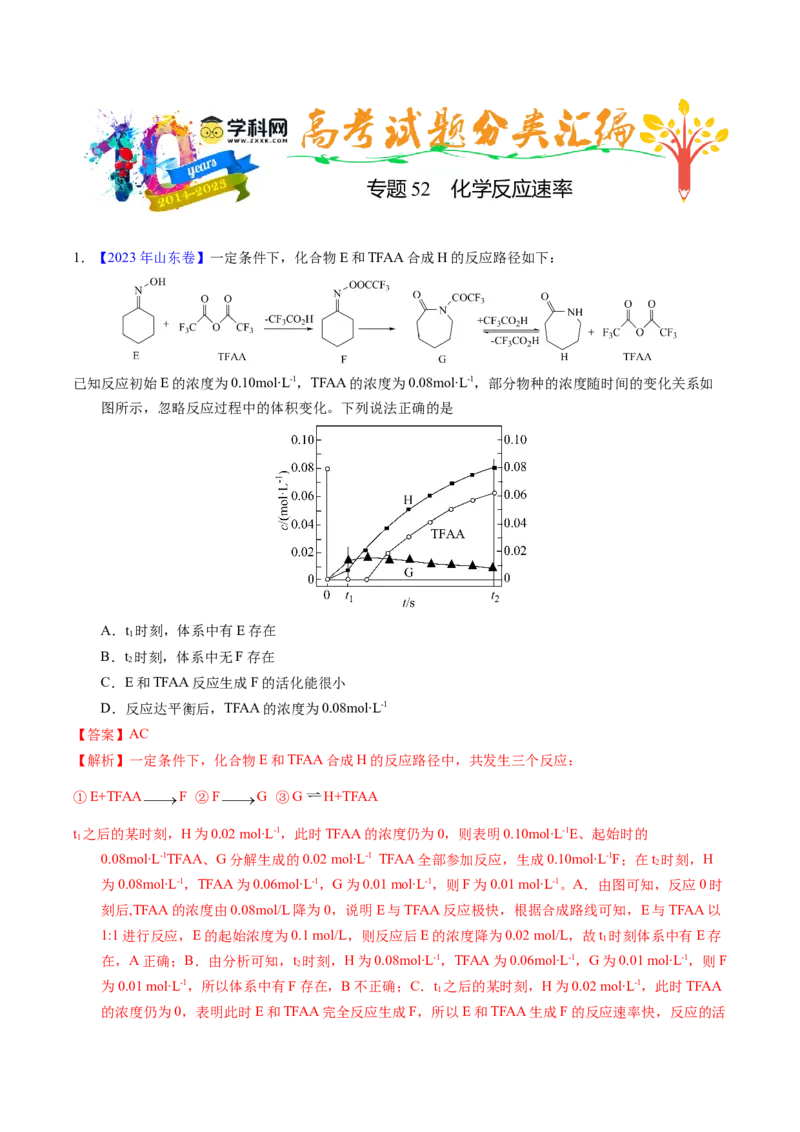
5.【2022年北京卷】 捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应①完成之
后,以 为载气,以恒定组成的 混合气,以恒定流速通入反应器,单位时间流出气体各组
分的物质的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上有积碳。
下列说法不正确的是
A.反应①为 ;反应②为
B. , 比 多,且生成 速率不变,可能有副反应
C. 时刻,副反应生成 的速率大于反应②生成 速率
D. 之后,生成 的速率为0,是因为反应②不再发生
【答案】C
【解析】A.由题干图1所示信息可知,反应①为 ,结合氧化还原反应配平可得反应②
为 ,A正确;B.由题干图2信息可知, , 比 多,且生成 速率不变,且反应过程中始终未检测到 ,在催化剂上有积碳,故可能有副反应
,反应②和副反应中CH 和H 的系数比均为1:2,B正确;C.由题干反应②方程
4 2
式可知,H 和CO的反应速率相等,而 时刻信息可知,H 的反应速率未变,仍然为2mmol/min,而
2 2
CO变为1~2mmol/min之间,故能够说明副反应生成 的速率小于反应②生成 速率,C错误;D.
由题干图2信息可知, 之后,CO的速率为0,CH 的速率逐渐增大,最终恢复到1,说明生成 的
4
速率为0,是因为反应②不再发生,而后副反应逐渐停止反应,D正确;故答案为:C。
6.(2021.6·浙江真题)一定温度下:在 的四氯化碳溶液( )中发生分解反应:
。在不同时刻测量放出的 体积,换算成 浓度如下表:
222
0 600 1200 1710 2820 x
1.40 0.96 0.66 0.48 0.35 0.24 0.12
下列说法正确的是
A. ,生成 的平均速率为
B.反应 时,放出的 体积为 (标准状况)
C.反应达到平衡时,
D.推测上表中的x为3930
【答案】D
【解析】A. , 的变化量为(0.96-0.66) ==0.3 ,在此时间段内 的变化量
为其2倍,即0.6 ,因此,生成 的平均速率为 ,A说法不
正确;B.由表中数据可知,反应 时, 的变化量为(1.40-0.35) ==1.05 ,其物
质的量的变化量为1.05 0.1L=0.105mol, 的变化量是其 ,即0.0525mol,因此,放出的
在标准状况下的体积为0.0525mol 22.4L/mol= ,B说法不正确;C.反应达到平衡时,正反
应速率等于逆反应速率,用不同物质表示该反应的速率时,其数值之比等于化学计量数之比,
,C说法不正确;D.分析表中数据可知,该反应经过1110s(600-1710,1710-
2820)后 的浓度会变为原来的 ,因此, 的浓度由0.24 变为0.12 时,可以
推测上表中的x为(2820+1110)=3930,D说法正确。综上所述,本题选D。
7.(2021.1·浙江真题)取50 mL过氧化氢水溶液,在少量I- 存在下分解:2HO=2H O+O↑。在一定温度
2 2 2 2
下,测得O 的放出量,转换成HO 浓度(c)如下表:
2 2 2t/min 0 20 40 60 80
c/(mol·L-1) 0.80 0.40 0.20 0.10 0.050
下列说法不正确的是
A.反应20min时,测得O 体积为224mL(标准状况)
2
B.20~40min,消耗HO 的平均速率为0.010mol·L-1·min-1
2 2
C.第30min时的瞬时速率小于第50min时的瞬时速率
D.HO 分解酶或Fe O 代替I-也可以催化HO 分解
2 2 2 3 2 2
【答案】C
【解析】A.反应20min时,过氧化氢的浓度变为0.4mol/L,说明分解的过氧化氢的物质的量
n(H O)=(0.80-0.40)mol/L×0.05L=0.02mol,过氧化氢分解生成的氧气的物质的量n(O )=0.01mol,标况
2 2 2
下的体积V=n·V =0.01mol×22.4L/mol=0.224L=224mL,A正确;B.20~40min,消耗过氧化氢的浓度
m
为(0.40-0.20)mol/L=0.20mol/L,则这段时间内的平均速率v= = =0.010mol/(L·min),B正
确;C.随着反应的不断进行,过氧化氢的浓度不断减小,某一时刻分解的过氧化氢的量也不断减小,
故第30min时的瞬时速率大于第50min时的瞬时速率,C错误;D.I-在反应中起到催化的作用,故也
可以利用过氧化氢分解酶或Fe O 代替,D正确;故答案选C。
2 3
8.(2019·浙江高考真题)高温高压液态水具有接近常温下弱酸的c(H+)或弱碱的c(OH−),油脂在其中能以
较快的反应速率水解。与常温常压水相比,下列说法不正确的是
A.高温高压液态水中,体系温度升高,油脂水解反应速率加快
B.高温高压液态水中,油脂与水的互溶能力增强,油脂水解反应速率加快
C.高温高压液态水中,c(H+)增大,可催化油脂水解反应,且产生的酸进一步催化水解
D.高温高压液态水中的油脂水解,相当于常温下在体系中加入了相同c(H+)的酸或相同c(OH−)的碱的
水解
【答案】D
【解析】A.对于任何化学反应,体系温度升高,均可加快反应速率,正确;B.由于高温高压液态水中,
c(H+)和c(OH−)增大,油脂水解向右移动的倾向变大,因而油脂与水的互溶能力增强,反应速率加快,
正确;C.油脂在酸性条件下水解,以H+做催化剂,加快水解速率,因而高温高压液态水中,c(H+)增
大,可催化油脂水解反应,且产生的酸进一步催化水解,正确;D.高温高压液态水中的油脂水解,
其水环境仍呈中性,因而不能理解成相当于常温下在体系中加入了相同c(H+)的酸或相同c(OH−)的碱
的水解,而是以体系升温、增加水和油脂的互溶以及提高水中H+浓度的方式,促进油脂的水解,不正
确。故答案选D。
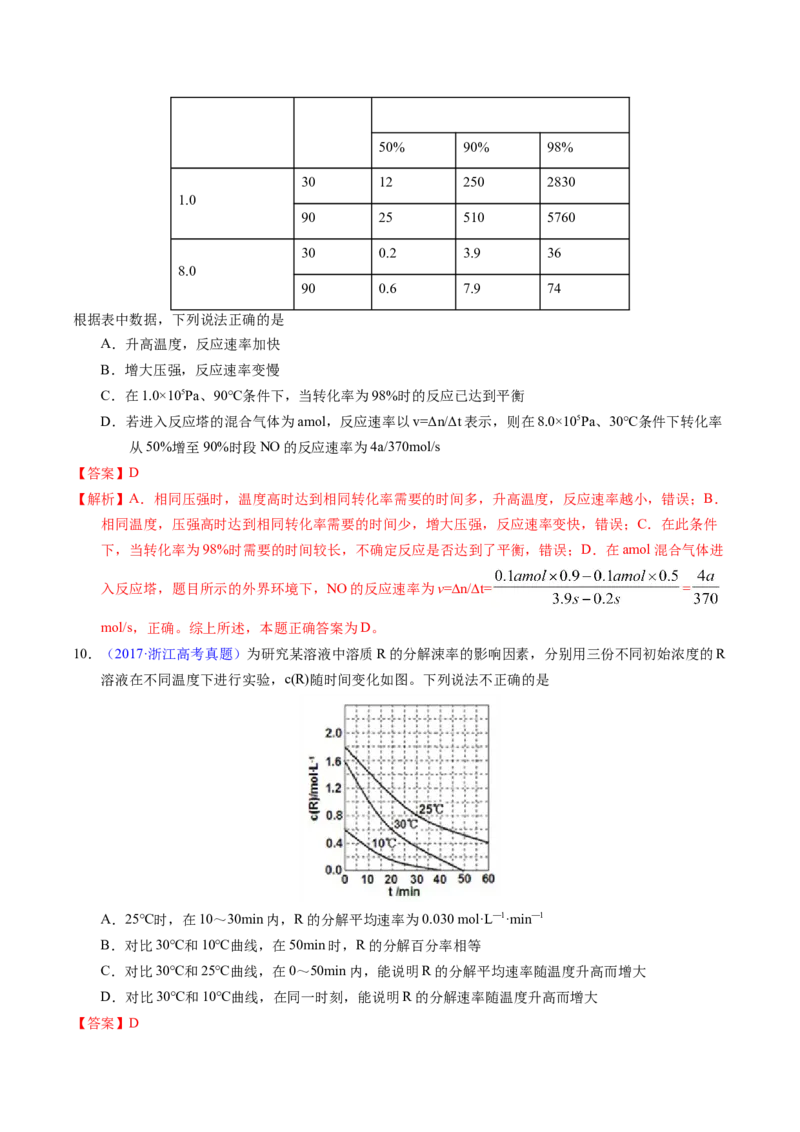
9.(2018·浙江高考真题)某工业流程中,进入反应塔的混合气体中NO和O 的物质的量分数分别为0.10
2
和0.06,发生化学反应 ,在其他条件相同时,测得实验数据如下
表:
压强/(×105Pa) 温度/℃ NO达到所列转化率需要时间/s50% 90% 98%
30 12 250 2830
1.0
90 25 510 5760
30 0.2 3.9 36
8.0
90 0.6 7.9 74
根据表中数据,下列说法正确的是
A.升高温度,反应速率加快
B.增大压强,反应速率变慢
C.在1.0×105Pa、90℃条件下,当转化率为98%时的反应已达到平衡
D.若进入反应塔的混合气体为amol,反应速率以v=Δn/Δt表示,则在8.0×105Pa、30℃条件下转化率
从50%增至90%时段NO的反应速率为4a/370mol/s
【答案】D
【解析】A.相同压强时,温度高时达到相同转化率需要的时间多,升高温度,反应速率越小,错误;B.
相同温度,压强高时达到相同转化率需要的时间少,增大压强,反应速率变快,错误;C.在此条件
下,当转化率为98%时需要的时间较长,不确定反应是否达到了平衡,错误;D.在amol混合气体进
入反应塔,题目所示的外界环境下,NO的反应速率为v=∆n/∆t= =
mol/s,正确。综上所述,本题正确答案为D。
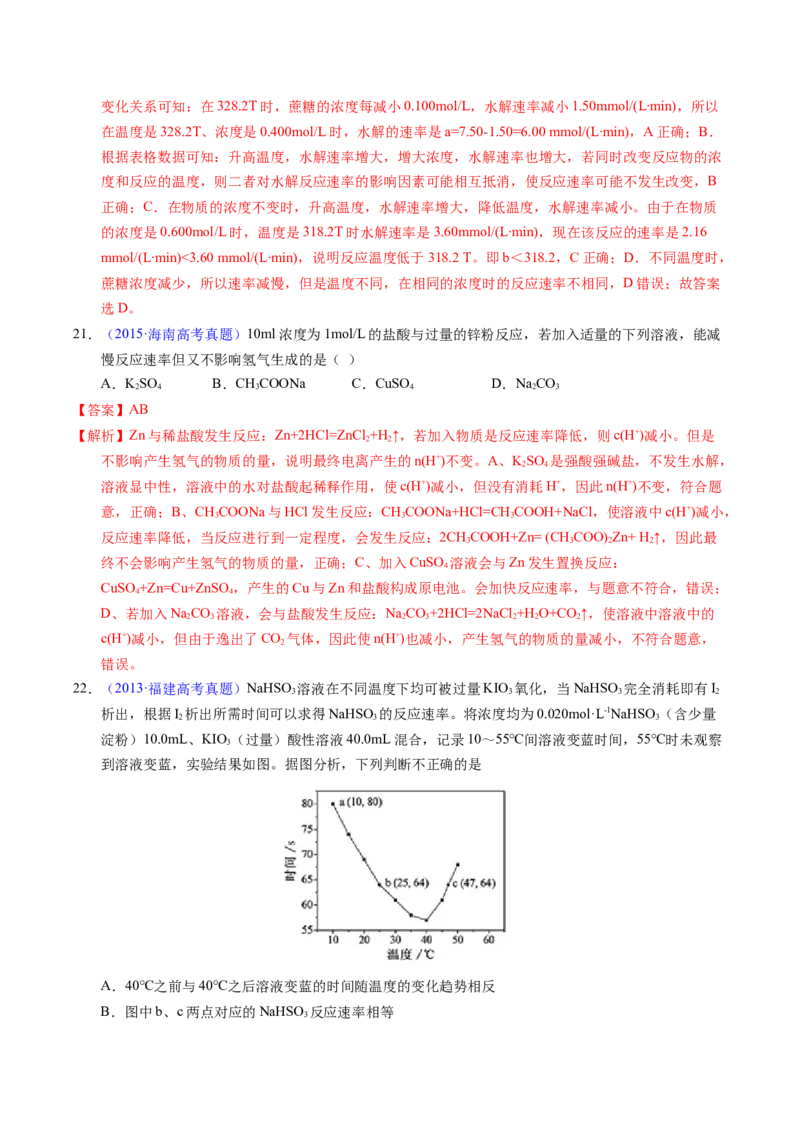
10.(2017·浙江高考真题)为研究某溶液中溶质R的分解涑率的影响因素,分别用三份不同初始浓度的R
溶液在不同温度下进行实验,c(R)随时间变化如图。下列说法不正确的是
A.25℃时,在10~30min内,R的分解平均速率为0.030 mol·L—1·min—1
B.对比30℃和10℃曲线,在50min时,R的分解百分率相等
C.对比30℃和25℃曲线,在0~50min内,能说明R的分解平均速率随温度升高而增大
D.对比30℃和10℃曲线,在同一时刻,能说明R的分解速率随温度升高而增大
【答案】D【解析】A.25 ℃时,在0~30 min内,R的分解平均速度为[(1.8-0.8)/30]mol·L-1·min-1=0.033 mol·L-
1·min-1,正确;B.对比30 ℃和10 ℃曲线,在50 min时,R的分解百分率相等,正确;C.对比30
℃和25 ℃曲线,在0~50 min内,能说明R的分解平均速度随温度升高而增大,正确;D.对比30
℃和10 ℃曲线,在同一时刻,两曲线R的浓度不同,不能说明R的分解速率随温度升高而增大,不
正确。故选D。
11.(2017·江苏高考真题)HO 分解速率受多种因素影响。实验测得70℃时不同条件下HO 浓度随时间
2 2 2 2
的变化如图所示。下列说法不正确的是
A.图甲表明,其他条件相同时,HO 浓度越小,其分解速率越慢
2 2
B.图乙表明,其他条件相同时,溶液碱性越弱,HO 分解速率越慢
2 2
C.图丙表明,少量Mn2+存在时,溶液碱性越强,HO 分解速率越快
2 2
D.图丙和图丁表明,碱性溶液中,c(Mn2+)对HO 分解速率的影响大
2 2
【答案】C
【解析】A、由甲图可知,双氧水浓度越小,分解越慢,正确;B、由图乙可知,溶液的碱性越弱,双氧水
分解越慢,正确;C、根据变量控制法,3个实验必须加入等量的Mn2+才能比较溶液的碱性对双氧水
分解的影响。由图丙可知,3个实验中由于仅在其中一个加入了Mn2+,不正确;D、由图丙和图丁可
知,溶液的碱性越强、Mn2+浓度越大,双氧水分解越快,正确。答案选C。
12.(2016·浙江高考真题)X(g)+3Y(g) 2Z(g) ΔH=-akJ·mol-1。一定条件下,将1 molX和3
molY通入2L的恒容密闭容器,反应10 min,测得Y的物质的量为2.4 mol。下列说法正确的是( )
A.10 min内,Y的平均反应速率为0.03 mol·L-1·s-1
B.10 min内,消耗0.2 molX,生成0.4 molZ
C.第10 min时,X的反应速率为0.01 mol·L-1·min-1
D.10 min内,X和Y反应放出的热量为a kJ
【答案】B
【解析】A.用Y表示平均反应速率为
,错误;B.根据化学反应
方程式可知,10min内,消耗0.2molX,生成0.4molZ,正确;C.化学反应速率表示的是平均速率,
不是瞬时速率,故第10 min时,无法计算其速率,错误;D.10min内,Y的转化率为,则放出热量为 ,错误;答案选B。
13.(2017·浙江高考真题)对水样中溶质M的分解速率影响因素进行研究。在相同温度下,M的物质的
量浓度(mol·L-1)随时间(min)变化的有关实验数据见下表。
时间
0 5 10 15 20 25
水样
I (pH=2) 0.40 0.28 0.19 0.13 0.10 0.09
II(pH=4) 0.40 0.31 0.24 0.20 0.18 0.16
Ⅲ(pH=4) 0.20 0.15 0.12 0.09 0.07 0.05
IV(pH=4,含Cu2+) 0.20 0.09 0.05 0.03 0.01 0
下列说法不正确的是( )
A.在0~20 min内,I中M的平均分解速率为0.015mol·L-1·min-1
B.其它条件相同时,水样酸性越强,M的分解速率越快
C.在0~25 min内,Ⅲ中M的分解百分率比II大
D.由于Cu2+存在,IV 中M的分解速率比I快
【答案】D
【解析】A、根据化学反应速率数学表达式,v(M)= =0.015mol/(L·min),正确;B、对
比I和II,在相同的时间内,I中消耗M的量大于II中,说明其他条件下不变,酸性越强,M的分解
速率越快,正确;C、在0~25 min内,III中M的分解百分率= ×100%=75%,
II中M的分解百分率= ×100%=60%,因此III中M的分解百分率大于II,正确;
D、I和IV中pH不同,因此不能说明Cu2+存在,IV中M的分解速率大于I,错误。故选D。
14.(2014·北京高考真题)在一定温度下,10mL0.40mol/L HO 发生催化分解。不同时刻测定生成O 的
2 2 2
体积(已折算为标准状况)如下表。
t/min 0 2 4 6 8 10
V(O )/mL 0.0 9.9 17.2 22.4 26.5 29.9
2
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~6min的平均反应速率:v(HO) mol/(L·min)
2 2
B.6~10min的平均反应速率:v(HO)< mol/(L·min)
2 2C.反应至6min时,c(HO)=0.3mol/L
2 2
D.反应至6min时,HO 分解了50%
2 2
【答案】C
【解析】A.0~6min时间内,△c(HO)=0.002mol÷0.01L=0.2mol/L,所以v(HO)=0.2mol/L÷6min
2 2 2 2
mol/(L·min), A正确;B.随着反应的进行,HO 的浓度逐渐减小,反应速率减慢,B正确;
2 2
C.6min时,c(HO)=0.002mol÷0.01L=0.2mol/L, C错误;D.6min时,HO 分解率为:
2 2 2 2
=50%, D正确。答案选C。
15.(2014·全国高考真题)已知分解1mol HO 放出热量98kJ,在含少量I-的溶液中,HO 的分解机理为:
2 2 2 2
HO+I-→HO+IO- 慢,HO+IO-→HO+O+I- 快;下列有关反应的说法正确的是( )
2 2 2 2 2 2 2
A.反应的速率与I-的浓度有关 B.IO-也是该反应的催化剂
C.反应活化能等于98kJ·mol-1 D.v(H O)=v(HO)=v(O )
2 2 2 2
【答案】A
【解析】A、根据反应机理可知I-是HO 分解的催化剂,碘离子浓度大,产生的IO-就多反应速率就快,A
2 2
正确;B、IO-不是该反应的催化剂,B错误;C、反应的活化能是反应物的总能量与生成物的总能量
的差值。这与反应的物质得到多少,错误;D、 HO 分解的总方程式是2HO=2H O+ O ↑;由于水是
2 2 2 2 2 2
纯液体,不能用来表示反应速率,而且HO 和O 的系数不同,表示的化学反应速率也不同,D错误;
2 2 2
故合理选项为A。
16.(2016·北京高考真题)下列食品添加剂中,其使用目的与反应速率有关的是( )
A.抗氧化剂 B.调味剂
C.着色剂 D.增稠剂
【答案】A
【解析】A.抗氧化剂减少食品与氧气的接触,延缓氧化的反应速率,正确;B. 调味剂是为了增加食品
的味道,与速率无关,错误;C. 着色剂是为了给食品添加某种颜色,与速率无关,错误;D. 增稠
剂是改变物质的浓度,与速率无关,错误。故选:A。
17.(2008·广东高考真题)对于反应2SO (g)+O(g) 2SO (g),能增大正反应速率的措施是( )
2 2 3
A.通入大量O B.增大容器容积
2
C.移去部分SO D.降低体系温度
3
【答案】A
【解析】A.通入大量O,增大了反应物的浓度,化学反应速率增大;B.增大容器的容积,各组分的浓
2
度减小,化学反应速率减小;C.移去部分SO ,减小了生成物的浓度,化学反应速率减小;D.降低
3
体系温度,化学反应速率减小。综上所述,能增大正反应速率的措施是A。
18.(2009·广东高考真题)已知汽车尾气无害化处理反应为
。
下列说法不正确的是 ( )
A.升高温度可使该反应的逆反应速率降低B.使用高效催化剂可有效提高正反应速率
C.反应达到平衡后,N0的反应速率保持恒定
D.单位时间内消耗CO和CO 的物质的量相等时,反应达到平衡
2
【答案】A
【解析】A.升高温度,正、逆反应速率都增大,错误;B.使用高效催化剂,能够降低活化能,从而提高
反应速率,正、逆反应速率都提高,正确;C.反应达到平衡后,体系各组分的反应速率都保持恒定,
正确;D.消耗1mol 一氧化碳能生成1mol 二氧化碳,而同时又消耗1mol 二氧化碳,可知正逆反应
速率相同,反应达到平衡状态,正确。答案选A。
19.(2015·上海高考真题)对于合成氨反应,达到平衡后,以下分析正确的是( )。
A.升高温度,对正反应的反应速率影响更大
B.增大压强,对正反应的反应速率影响更大
C.减小反应物浓度,对逆反应的反应速率影响更大
D.加入催化剂,对逆反应的反应速率影响更大
【答案】B
【解析】A.合成氨反应的正反应是放热反应,升高温度,正反应、逆反应的反应速率都增大,但是温度
对吸热反应的速率影响更大,所以对该反应来说,对逆速率影响更大,错误;B.合成氨的正反应是
气体体积减小的反应,增大压强,对正反应的反应速率影响更大,正反应速率大于逆反应速率,所以
平衡正向移动,正确;C.减小反应物浓度,使正反应的速率减小,由于生成物的浓度没有变化,所
以逆反应速率不变,逆反应速率大于正反应速率,所以化学平衡逆向移动,错误;D.加入催化剂,
使正反应、逆反应速率改变的倍数相同,正反应、逆反应速率相同,化学平衡不发生移动,错误。本
题选B。
20.(2015·福建高考真题)在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表。下列
判断不正确的是
A.a=6.00
B.同时改变反应温度和蔗糖的浓度,v可能不变
C.b<318.2
D.不同温度时,蔗糖浓度减少一半所需的时间相同
【答案】D
【解析】A.根据表格的数据可知:温度不变时,蔗糖的浓度越大,水解的速率越快。根据浓度与速率的变化关系可知:在328.2T时,蔗糖的浓度每减小0.100mol/L,水解速率减小1.50mmol/(L∙min),所以
在温度是328.2T、浓度是0.400mol/L时,水解的速率是a=7.50-1.50=6.00 mmol/(L∙min),A正确;B.
根据表格数据可知:升高温度,水解速率增大,增大浓度,水解速率也增大,若同时改变反应物的浓
度和反应的温度,则二者对水解反应速率的影响因素可能相互抵消,使反应速率可能不发生改变,B
正确;C.在物质的浓度不变时,升高温度,水解速率增大,降低温度,水解速率减小。由于在物质
的浓度是0.600mol/L时,温度是318.2T时水解速率是3.60mmol/(L∙min),现在该反应的速率是2.16
mmol/(L∙min)<3.60 mmol/(L∙min),说明反应温度低于318.2 T。即b<318.2,C正确;D.不同温度时,
蔗糖浓度减少,所以速率减慢,但是温度不同,在相同的浓度时的反应速率不相同,D错误;故答案
选D。
21.(2015·海南高考真题)10ml浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减
慢反应速率但又不影响氢气生成的是( )
A.KSO B.CHCOONa C.CuSO D.NaCO
2 4 3 4 2 3
【答案】AB
【解析】Zn与稀盐酸发生反应:Zn+2HCl=ZnCl +H ↑,若加入物质是反应速率降低,则c(H+)减小。但是
2 2
不影响产生氢气的物质的量,说明最终电离产生的n(H+)不变。A、KSO 是强酸强碱盐,不发生水解,
2 4
溶液显中性,溶液中的水对盐酸起稀释作用,使c(H+)减小,但没有消耗H+,因此n(H+)不变,符合题
意,正确;B、CHCOONa与HCl发生反应:CHCOONa+HCl=CH COOH+NaCl,使溶液中c(H+)减小,
3 3 3
反应速率降低,当反应进行到一定程度,会发生反应:2CHCOOH+Zn= (CH COO) Zn+ H↑,因此最
3 3 2 2
终不会影响产生氢气的物质的量,正确;C、加入CuSO 溶液会与Zn发生置换反应:
4
CuSO +Zn=Cu+ZnSO ,产生的Cu与Zn和盐酸构成原电池。会加快反应速率,与题意不符合,错误;
4 4
D、若加入NaCO 溶液,会与盐酸发生反应:NaCO+2HCl=2NaCl +H O+CO↑,使溶液中溶液中的
2 3 2 3 2 2 2
c(H+)减小,但由于逸出了CO 气体,因此使n(H+)也减小,产生氢气的物质的量减小,不符合题意,
2
错误。
22.(2013·福建高考真题)NaHSO 溶液在不同温度下均可被过量KIO 氧化,当NaHSO 完全消耗即有I
3 3 3 2
析出,根据I 析出所需时间可以求得NaHSO 的反应速率。将浓度均为0.020mol·L-1NaHSO(含少量
2 3 3
淀粉)10.0mL、KIO (过量)酸性溶液40.0mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察
3
到溶液变蓝,实验结果如图。据图分析,下列判断不正确的是
A.40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反
B.图中b、c两点对应的NaHSO 反应速率相等
3C.图中a点对应的NaHSO 反应速率为5.0 ×10-5mol·L-1·s-1
3
D.温度高于40℃时,淀粉不宜用作该实验的指示剂
【答案】B
【解析】A、从图像中可以看出,40℃以前,温度越高,反应速度越快,40℃后温度越高,变色时间越长,
反应越慢,而55℃,未变蓝,说明没有生成I,A正确;B、b、c点对应的反应原理不一样,发生不
2
同的反应,无法比较反应速率,B错误;C、速率为 =5.0×10-5mol·L-1·s-1,C正确;
D、55℃时,没有出现蓝色,故淀粉已不能作为该反应的指示剂,D正确。答案选B。
23.(2008·上海高考真题)等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产
生气体体积V的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实验组别可能是( )
A.4-3-2-1 B.1-2-3-4 C.3-4-2-1 D.1-2-4-3
【答案】AC
【解析】溶液温度越高、盐酸浓度越大、反应物接触面积越大,反应速率越快,生成相同体积的气体所需
时间越短,且温度影响远远大于浓度和反应物接触面积的影响,温度高低顺序是3>4=2>1,且2、
3、4中盐酸浓度相等,但4中反应物接触面积大于2和3,所以反应速率大小顺序是3>4>2>1或4
>3>2>1,结合图象知,曲线a、b、c、d所对应的实验组别可能 3-4-2-1或4>3>2>1,故选AC。