文档内容
专题61 盐类水解及应用
1.【2023年北京卷】下列过程与水解反应无关的是
A.热的纯碱溶液去除油脂
B.重油在高温、高压和催化剂作用下转化为小分子烃
C.蛋白质在酶的作用下转化为氨基酸
D.向沸水中滴入饱和 溶液制备 胶体
【答案】B
【解析】A.热的纯碱溶液因碳酸根离子水解显碱性,油脂在碱性条件下能水解生成易溶于水的高级脂肪
酸盐和甘油,故可用热的纯碱溶液去除油脂,A不符合题意;B.重油在高温、高压和催化剂作用下
发生裂化或裂解反应生成小分子烃,与水解反应无关,B符合题意;C.蛋白质在酶的作用下可以发
生水解反应生成氨基酸,C不符合题意;D. Fe3+能发生水解反应生成 Fe(OH) ,加热能增大Fe3+ 的
3
水解程度,D不符合题意;故选B。
2.【2023年6月浙江卷】草酸( )是二元弱酸。某小组做如下两组实验:
实验I:往 溶液中滴加 溶液。
实验Ⅱ:往 溶液中滴加 溶液。
[已知: 的电离常数 ,溶液混合后体积变化忽略不
计],下列说法正确的是
A.实验I可选用甲基橙作指示剂,指示反应终点
B.实验I中 时,存在
C.实验Ⅱ中发生反应
D.实验Ⅱ中 时,溶液中
【答案】D
【解析】A. 溶液被氢氧化钠溶液滴定到终点时生成显碱性的草酸钠溶液,为了减小实验误差要
选用变色范围在碱性范围的指示剂,因此,实验I可选用酚酞作指示剂,指示反应终点,故A错误;
B.实验I中 时,溶质是 、 且两者物质的量浓度相等,
,,则草酸氢根的电离程度大于草酸根的水解程度,因此存在
,故B错误;C.实验Ⅱ中,由于开始滴加的氯化钙量较少而 过量,因此该反应在初始阶段发生的是 ,该反应的平衡常数为
,因为平衡常数很大,说明反应能够完全进行,
当 完全消耗后, 再和 发生反应,故C错误;D.实验Ⅱ中 时,
溶液中的钙离子浓度为 ,溶液中
,故D正确。综上所述,答案为D。
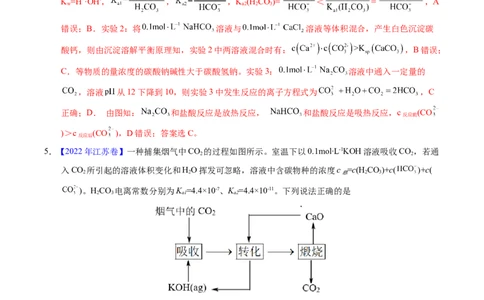
3.(2021·北京真题)下列实验中,均产生白色沉淀。
下列分析不正确的是
A.NaCO 与NaHCO 溶液中所含微粒种类相同
2 3 3
B.CaCl 能促进NaCO、NaHCO 水解
2 2 3 3
C.Al (SO ) 能促进NaCO、NaHCO 水解
2 4 3 2 3 3
D.4个实验中,溶液滴入后,试管中溶液pH均降低
【答案】B
【解析】A.NaCO 溶液、NaHCO 溶液均存在Na+、 、 、HCO、H+、OH-、HO,故含有的
2 3 3 2 3 2
微粒种类相同,A正确;B. H++ ,加入Ca2+后,Ca2+和 反应生成沉淀,促进
的电离,B错误;C.Al3+与 、 都能发生互相促进的水解反应,C正确;D.由题干
信息可知形成沉淀时会消耗碳酸根和碳酸氢根,则它们浓度减小,水解产生的氢氧根的浓度会减小,
pH减小,D正确;故选B。
4.【2021年江苏卷】室温下,通过下列实验探究NaHCO 、NaCO 溶液的性质。
3 2 3
实验1:用pH试纸测量0.1mol·L-1NaHCO 溶液的pH,测得pH约为8
3
实验2:将0.1mol·L-1NaHCO 溶液与0.1mol·L-1CaCl 溶液等体积混合,产生白色沉淀
3 2
实验3:向0.1mol·L-1NaCO 溶液中通入CO,溶液pH从12下降到约为9
2 3 2
实验4:向0.1mol·L-1NaCO 溶液中滴加新制饱和氯水,氯水颜色褪去
2 3
下列说法正确的是
A.由实验1可得出:K (H CO)>
a2 2 3B.实验2中两溶液混合时有:c(Ca2+)·c(CO )[CH COO-]>[H+]>[OH-]
3 3
B.①②等体积混合后,醋酸根离子浓度小于③的二分之一
C.①③等体积混合以后,溶液呈酸性,则(Na+)>(CH COO-)>(H+)
3
D.①②等体积混合以后,水的电离程度比①③等体积混合的电离程度小
【答案】B
【解析】A.CHCOOH溶液中的H+来自醋酸分子的电离和水的电离,所以
3
[CHCOOH]>[H+]>[CH COO-]>[OH-],错误;B.①②等体积混合后恰好反应生成CHCOONa,体积大
3 3 3
约为原来的2倍,如果CHCOO-不水解,浓度约为原来的1/2,CHCOONa为弱酸强碱盐,越稀越水
3 3
解,CHCOO- +H O CHCOOH+OH-,水解平衡向正向移动,因此CHCOO-浓度小于原来的1/2,
3 2 3 3
正确;C.①③等体积混合以后,溶液呈酸性,说明CHCOOH的电离程度大于CHCOO- 的水解程度,
3 3
因此(CHCOO-)>(Na+)>(H+),错误;D.①②等体积混合以后恰好反应生成CHCOONa,CHCOO- 的
3 3 3
水解促进水的电离,①③等体积混合,CHCOOH电离产生的H+抑制水的电离,因此总体上看①②等
3
体积混合后水的电离程度比①③等体积混和后水的电离程度大,错误;答案选B。
9.(2019·浙江高考真题)聚合硫酸铁[Fe(OH)SO ] 能用作净水剂(絮凝剂),可由绿矾(FeSO ·7H O)和
4 n 4 2
KClO 在水溶液中反应得到。下列说法不正确的是
3
A.KClO 作氧化剂,每生成1 mol [Fe(OH)SO ] 消耗6/n mol KClO
3 4 n 3
B.生成聚合硫酸铁后,水溶液的pH增大
C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水
D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强
【答案】A
【解析】A.根据题干中信息,可利用氧化还原配平法写出化学方程式:
6nFeSO +nKClO +3nH O=6[Fe(OH)SO ]n+nKCl,可知KClO 做氧化剂,同时根据计量数关系亦知每生
4 3 2 4 3
成1 mol [Fe(OH)SO ] 消耗n/6 mol KClO ,错误;B.绿矾溶于水后,亚铁离子水解使溶液呈酸性,当
4 n 3
其转系为聚合硫酸铁后,亚铁离子的浓度减小,因而水溶液的pH增大,正确;C.聚合硫酸铁可在水
中形成氢氧化铁胶体,胶体粒子吸附杂质微粒引起聚沉,因而净水,正确;D.多元弱碱的阳离子的
水解是分步进行的。[Fe(OH)]2+的水解相当于Fe3+的二级水解,由于其所带的正电荷比Fe3+少,因而在
相同条件下,其结合水电离产生的OH-的能力较弱,故其水解能力不如Fe3+,即在相同条件下,一级
水解的程度大于二级水解,正确。故答案选A。
10.(2019·浙江高考真题)下列溶液呈碱性的是
A.NH NO B.(NH )SO C.KCl D.KCO
4 3 4 2 4 2 3
【答案】D
【解析】盐类水解是指弱酸阴离子或弱碱阳离子发生水解,导致溶液的酸碱性发生变化,本题四个选项均
涉及盐类水解。A.该盐属于强酸弱碱盐,NH
4
++H
2
O⇌NH
3
·H
2
O+H+,溶液显酸性,A不合题意;B.
同A,NH +发生水解,使得溶液显酸性,B不合题意;C.该盐属于强酸强碱盐,不发生水解,溶液
4
显中性,C不合题意;D.该盐属于强碱弱酸盐,CO
3
2-+H
2
O⇌HCO
3
-+OH-,HCO
3
-
+H
2
O⇌H
2
CO
3
+OH-,溶液显碱性,符合题意。故答案选D。11.(2018·浙江高考真题)下列物质因发生水解而使溶液呈酸性的是
A.HNO B.CuCl C.KCO D.NaCl
3 2 2 3
【答案】B
【解析】A、HNO 不是盐,不能水解,故不是因水解而使溶液显酸性,选项A错误;B、CuCl 为强酸弱
3 2
碱盐,在溶液中水解显酸性,选项B正确;C、碳酸钾是强碱弱酸盐,水解显碱性,选项C错误;
D、氯化钠是强酸强碱盐,不水解,选项D错误。答案选B。
12.(2017·浙江高考真题)下列物质的水溶液因水解而呈酸性的是( )
A.NaOH B.(NH )SO C.NaCO D.NaCl
4 2 4 2 3
【答案】B
【解析】A.NaOH是强碱,水溶液显碱性,A错误;B.(NH )SO 是强酸弱碱盐,铵根离子水解显酸性,
4 2 4
B正确;C.NaCO 是强碱弱酸盐,碳酸根离子水解显碱性,C错误;D.NaCl溶液显中性,D错误。
2 3
答案选B。
13.(2017·上海高考真题)下列物质的水溶液呈酸性,并且使水的电离平衡向正方向移动的是:
A.NaCO B.NH Cl C.HSO D.NaHCO
2 3 4 2 4 3
【答案】B
【解析】A.NaCO 是强碱弱酸盐,碳酸根离子水解导致溶液呈碱性,促进水电离,错误;B.氯化铵是
2 3
强酸弱碱盐,铵根离子水解,溶液显酸性,促进水的电离,正确;C.硫酸完全电离生成氢离子而导
致溶液中c(H+)增大,溶液显酸性,抑制水的电离,错误;D.碳酸氢钠是强碱弱酸酸式盐,碳酸氢根
离子水解程度大于电离程度,溶液显碱性,促进水的电离,错误;故选B。
14.(2015·天津高考真题)室温下,将0.05 mol Na CO 固体溶于水配成100 mL溶液,向溶液中加入下列
2 3
物质,有关结论正确的是( )
加入物质 结论
A 50 mL 1 mol·L-1HSO 反应结束后,c(Na+)=c(SO )
2 4
B 0.05 mol CaO 溶液中 增大
C 50 mL H O 由水电离出的c(H+)·c(OH-)不变
2
D 0.1 mol NaHSO 固体 反应完全后,溶液pH减小,c(Na+)不变
4
【答案】B
【解析】室温下,将0.05 mol Na CO 固体溶于水配成100mL溶液,溶液中存在CO2-+H O HCO-
2 3 3 2 3
+OH-溶液呈碱性,据此分析解答。A.加入50mL 1 mol·L-1HSO ,HSO 与NaCO 恰好反应,则反
2 4 2 4 2 3
应后的溶液溶质为NaSO ,故根据物料守恒反应结束后c(Na+)=2c(SO2-),A错误;B.向溶液中加入
2 4 4
0.05molCaO,则CaO+ H O=Ca(OH) ,则c(OH-)增大,且Ca2++CO 2-=CaCO ↓,使CO2-+H O
2 2 3 3 3 2HCO -+OH-平衡左移,c(HCO -)减小,故 增大,B正确;C.加入50mL HO,溶液体积变
3 3 2
大,CO2-+H O HCO-+OH-平衡右移,但c(OH-)减小,NaCO 溶液中H+、OH-均由水电离,故由
3 2 3 2 3
水电离出的c(H+)·c(OH-)减小,C错误;D.加入0.1molNaHSO 固体,NaHSO 为强酸酸式盐电离出
4 4
H+与CO2-反应,则反应后溶液为NaSO 溶液,溶液呈中性,故溶液pH减小,引入了Na+,(Na+)增大,
3 2 4
D错误;答案选B。
15.(2007·北京高考真题)有① NaCO 溶液 ② CHCOONa溶液 ③ NaOH溶液各25mL,物质的量浓
2 3 3
度均为0.1mol·L-1,下列说法正确的是
A.3种溶液pH的大小顺序是③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是②
C.若分别加入25mL0.1mol·L-1盐酸后,pH最大的是①
D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>②
【答案】C
【解析】A.酸越弱,相应的钠盐越容易水解,醋酸的酸性强于碳酸的,所以碳酸钠的碱性强于醋酸钠的,
A不正确;B.稀释促进水解,所以pH变化最大的是氢氧化钠,B不正确;C.醋酸钠和氢氧化钠都
恰好与盐酸反应,但碳酸钠生成碳酸氢钠,溶液显碱性,pH最大,C正确;D.氢氧化钠是强碱,所
以选项D中应该是②>①>③,D不正确;答案选C。
16.(2014·广东高考真题)常温下,0.2mol/L一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液
中部分微粒组分及浓度如图所示,下列说法正确的是
A.HA是强酸
B.该混合液pH=7
C.图中x表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y)=c(Na+)
【答案】D
【解析】A、0.2mol/L一元酸HA与等浓度的NaOH溶液等体积混合后,得到的溶液为0.1mol/L的NaA溶
液,若HA为强酸,则溶液为中性,且c(A-)=0.1mol/L,与图不符,所以HA为弱酸,A错误;B、根
据A的分析,可知该溶液的pH>7,B错误;C、A-水解使溶液显碱性,所以溶液中的粒子浓度的大
小关系是c(Na+)>c(A-)>c(OH-)>c(HA)>c(H+),所以X是OH-,Y是HA,Z表示H+,C错误;
D、根据元素守恒,有c(A-)+c(HA)=c(Na+),D正确;答案选D。
17.(2008·重庆高考真题)向三份0.1mol/L CH COONa溶液中分别加入少量NH NO 、NaSO 、FeCl 固
3 4 3 2 3 2体(忽略溶液体积变化),则CHCOO-浓度的变化依次为( )
3
A.减小、增大、减小 B.增大、减小、减小
C.减小、增大、增大 D.增大、减小、增大
【答案】A
【解析】CHCOONa为强碱弱酸盐水解后溶液呈碱性,NH NO 和FeCl 为强酸弱碱盐水解后溶液呈酸性,
3 4 3 2
因此,这两种盐能促进CHCOONa的水解,溶液中的CHCOO-减小;NaSO 为强碱弱酸盐,水解后
3 3 2 3
溶液呈碱性,抑制CHCOONa的水解,溶液中的CHCOO-浓度增大。答案选A。
3 3
18.(2012·上海高考真题)常温下a mol/L CH COOH稀溶液和b mol/L KOH稀溶液等体积混合,下列判
3
断一定错误的是
A.若c(OH-)>c(H+),a=b B.若c(K+)>c(CHCOO-),a>b
3
C.若c(OH-)=c(H+),a>b D.若c(K+)<c(CHCOO-),a<b
3
【答案】D
【解析】A.若c(OH−)>c(H+),溶液为醋酸钾溶液或醋酸钾和KOH的混合液,则a b,不符合题意;B.
若c(K+)>c(CHCOO−),由电荷守恒c(CHCOO−)+ c(OH−)= c(H+)+ c(K+)可知,c(OH−)>c(H+),则
3 3 ⩽
a b,若当a>b,也就是弱酸强碱中和时,弱酸过量,溶液可能呈酸性、中性或碱性,醋酸过量的极
少,所以过量的醋酸电离出的H+小于醋酸根水解产生的OH−,有可能成立,不符合题意;C.若
⩽
c(OH−)=c(H+),溶液显中性,一定为醋酸和醋酸钾的混合液,则a>b,不符合题意;D.若c(K+)<
c(CHCOO−),由电荷守恒可知c(CHCOO−)+ c(OH−)= c(H+)+ c(K+),c(OH−)<c(H+),则a>b,符合题意;
3 3
答案选D。
19.(2012·天津高考真题)下列有关电解质溶液的叙述正确的是
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7
B.在含有BaSO 沉淀的溶液中加入NaSO 固体,c(Ba2+)增大
4 2 4
C.含1 mol KOH的溶液与1 mol CO 完全反应后,溶液中c(K+)=c(HCO -)
2 3
D.在CHCOONa溶液中加入适量CHCOOH,可使c(Na+)=c(CHCOO-)
3 3 3
【答案】D
【解析】A、同浓度、同体积的强酸与强碱溶液混合后,溶液的pH不一定等于7,如同浓度、同体积的氢
氧化钠和硫酸混合后,PH<7,A错误;B、加入NaSO 固体,硫酸根离子浓度增大,由于溶度积常数
2 4
不变,故钡离子浓度减小,B错误;C、含1 mol KOH的溶液与1 mol CO 完全反应后,生成
2
KHCO ,但HCO -发生水解,则c(K+)> c(HCO -),C错误;D、CHCOONa溶液呈碱性,加入适量
3 3 3 3
CHCOOH,使溶液呈中性时,根据电荷守恒可使c(Na+)= c(CHCOO-),D正确。答案选D。
3 3
20.(2016·浙江高考真题)下列物质的水溶液因水解呈酸性的是
A.NaOH B.NaCO C.NH Cl D.HCl
2 3 4
【答案】C
【解析】A.氢氧化钠是强碱,电离显碱性,不水解,错误;B.碳酸钠是强碱弱酸盐,水解显碱性,错误;
C.氯化铵为强酸弱碱盐,在溶液中水解显酸性,正确;D.HCl不是盐,不能水解,是电离使溶液显
酸性,错误;故选C。21.(2016·全国高考真题)下列有关电解质溶液的说法正确的是
A.向0.1 mol·L-1 CH COOH溶液中加入少量水,溶液中 减小
3
B.将CHCOONa溶液从20℃升温至30℃,溶液中 增大
3
C.向盐酸中加入氨水至中性,溶液中 >1
D.向AgCl、AgBr的饱和溶液中加入少量AgNO,溶液中 不变
3
【答案】D
【解析】A.溶液中 =K(CHCOOH)/K ,因为K(CHCOOH)、K 仅受温度影响,
a 3 w a 3 w
当温度不变时,它们的值不会随着浓度的变化而变化,故向0.1 mol·L-1 CH COOH溶液中加入少量水,
3
溶液中 不变,A错误;B.CHCOO-+H O CHCOOH+OH-,
3 2 3
,温度升高促进CHCOO-水解,水解平衡常数增大,
3
=1/K ,故将CHCOONa溶液从20℃升温至30℃,溶液中
h 3
减小,B错误; C.由电荷守恒可知c(NH +)+c(H+)=c(Cl-)+c(OH-),因为溶液
4
呈中性,c(H+)=c(OH-),所以c(NH +)=c(Cl-),c(NH +)/c(Cl-)=1,C错误;D.向AgCl、AgBr的饱和溶
4 4
液中加入少量AgNO,溶液中 =K (AgCl)/Ksp(AgI),故溶液中 不变,D正确;答案选
3 sp
D。
22.(2012·上海高考真题)将l00ml 1mol/L 的NaHCO 溶液等分为两份,其中一份加入少许冰醋酸,另外
3
一份加入少许Ba(OH) 固体,忽略溶液体积变化。两份溶液中c(CO2-)的变化分别是
2 3
A.减小、减小 B.减小、增大 C.增大、增大 D.增大、减小
【答案】B
【解析】将l00ml 1mol/L 的NaHCO 溶液等分为两份,一份加入少许冰醋酸,发生HAc+HCO -
3 3
=H O+CO↑+Ac-,则溶液中c(CO2-)减小;另外一份加入少许Ba(OH) 固体,发生Ba2++2OH-+2HCO-
2 2 3 2 3
=2H O+BaCO ↓+CO 2-,则溶液中c(CO2-)增大,故答案选B。
2 3 3 3
23.(2015·海南高考真题)化学与生活密切相关。下列应用中利用了物质氧化性的是( )A.明矾净化水 B.纯碱去油污
C.食醋除水垢 D.漂白粉漂白织物
【答案】D
【解析】A、明矾净水是利用Al3+水解产生的Al(OH) 胶体吸附水中悬浮的杂质而沉降下来,与物质的氧化
3
性无关,错误;B、纯碱去油污是利用纯碱溶于水电离产生的碳酸根离子水解显碱性,油脂在碱性条
件下发生较彻底的水解反应产生可溶性的物质高级脂肪酸钠和甘油,与物质的氧化性无关,错误;
C、食醋除水垢,是利用醋酸与水垢的主要成分碳酸钙和氢氧化镁发生复分解反应生成可溶性物质,
与物质的氧化性无关,错误;D、漂白粉漂白织物是利用次氯酸钙生成的次氯酸的强氧化性漂白,正
确;答案选D。
24.(2009·全国高考真题)现有等浓度的下列溶液:①醋酸,②苯酚,③苯酚钠,④碳酸,⑤碳酸钠,⑥
碳酸氢钠。按溶液pH由小到大排列正确的是
A.④①②⑤⑥③B.④①②⑥⑤③ C.①④②⑥③⑤ D.①④②③⑥⑤
【答案】C
【解析】①醋酸、②苯酚、④碳酸是酸,等浓度的三种溶液,醋酸的酸性大于碳酸,碳酸的酸性大于苯酚,
所以pH由小到大的顺序是:①醋酸<④碳酸<②苯酚; ③苯酚钠、⑤碳酸钠、⑥碳酸氢钠是盐,碳
酸的酸性大于苯酚,碳酸的第一步电离程度大于第二步电离程度,碳酸根离子对应的酸是碳酸氢根离
子,所以等浓度的三种盐,苯酚钠的水解程度小于碳酸钠,碳酸氢钠的水解程度小于苯酚钠,所以
pH由小到大的顺序是:⑥碳酸氢钠<③苯酚钠<⑤碳酸钠,则这六种溶液pH由小到大排列正确的是
①④②⑥③⑤,故选C。
25.(2013·天津高考真题)下列有关电解质溶液的说法正确的是( )
A.在蒸馏水中滴加浓HSO ,K 不变
2 4 W
B.CaCO 难溶于稀硫酸,也难溶于醋酸
3
C.在NaS稀溶液中,c(H+)=c(OH-)-2c(H S)-c(HS-)
2 2
D.NaCl溶液和CHCOONH 溶液均显中性,两溶液中水的电离程度相同
3 4
【答案】C
【解析】A.在蒸馏水中滴加浓HSO ,温度升高,K 变大,错误;B.CaCO 与稀硫酸反应生成微溶物
2 4 W 3
CaSO 阻碍了反应的进行,所以CaCO 难溶于稀硫酸,但是和醋酸反应生成醋酸钙是溶于水的,反应
4 3
可以继续进行, aCO 可溶于醋酸,错误;C.在NaS稀溶液中,c(H+)=c(OH-)-2c(HS)-c(HS-)这是质
3 2 2
子守恒,正确;D.NaCl溶液不发生水解,CHCOONH 溶液中CHCOO- 和 NH +的水解促进了水的
3 4 3 4
电离,但程度相当,溶液显中性,所以两溶液中水的电离程度不同,错误。答案选C。
26.(2009·北京高考真题)有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合面成:①CHCOONa
3
与HCl ②CHCOONa与NaOH ③CHCOONa与NaCl ④CHCOONa与NaHCO 下列各项排序正确的
3 3 3 3
是( )
A.pH:②>③>④>① B.c(CHCOO-):②>④>③>①
3
C.溶液中c(H+):①>③>②>④ D.c(CHCOOH):①>④>③>②
3
【答案】B
【解析】①:CHCOONa与HCl反应后生成CHCOOH和NaCl,其溶液呈酸性;②:CHCOONa与NaOH
3 3 3溶液,OH―阻止CHCOO―水解,溶液呈强碱性;③:CHCOONNa与NaCl,CHCOONa水解溶液呈
3 3 3
碱性;④:CHCOONa与NaHCO 溶液,NaHCO 水解呈碱性,HCO ―水解能力大于CHCOO―的水解
3 3 3 3 3
能力,HCO ―水解对CHCOONa水解有一定抑制作用;A.HCO ―水解能力大于CHCOO―的水解能
3 3 3 3
力,④中的pH>③中pH,错误;B.②中由于OH―对CHCOO―水解抑制作用强,其c(CHCOO―)最
3 3
大,④中HCO ―水解对CHCOONa水解有一定抑制作用,c(CHCOO―)较大,①中生成了
3 3 3
CHCOOH,c(CHCOO―)最小,c(CHCOO-)从大到小的排序②④③①,正确;C.②中含有NaOH,
3 3 3
水中H+浓度最小;①中含有CHCOOH,会电离出H+,其c(H+)最大;④中含有NaHCO ,由于
3 3
HCO ―水解能力大于CHCOO―的水解能力碱性④强于③,则③中c(H+)大于④,从大到小的准确排序
3 3
为①③④②;错误;D.④中含有的NaHCO 水解呈碱性,HCO ―水解对CHCOONa水解有一定抑制
3 3 3
作用,CHCOO-水解生成CHCOOH较少,则③中c(CHCOOH)>④中c(CHCOOH),错误;本题答
3 3 3 3
案选B。
27.(2014·山东高考真题)已知某温度下CHCOOH和NH ·H O的电离常数相等,现向10mL浓度为
3 3 2
0.1mol·L-1的CHCOOH溶液中滴加相同浓度的氨水,在滴加过程中( )
3
A.水的电离程度始终增大
B. 先增大再减小
C.c(CHCOOH)与c(CHCOO-)之和始终保持不变
3 3
D.当加入氨水的体积为10mL时,c(NH +)=c(CHCOO-)
4 3
【答案】D
【解析】A.酸溶液、碱溶液抑制了水的电离,溶液显示中性前,随着氨水的加入,溶液中氢离子浓度逐
渐减小,水的电离程度逐渐增大;当氨水过量后,随着溶液中氢氧根离子浓度逐渐增大,水的电离程
度逐渐减小,所以滴加过程中,水的电离程度先增大后减小,错误;B.由CHCOONH 的水解常数
3 4
K= ,随着氨水的加入,c(H+)逐渐减小,K 不变,则 始终减小,
h h
错误;C.n(CHCOOH)与n(CHCOO-)之和为0.001mol,始终保持不变,由于溶液体积逐渐增大,
3 3
所以c(CHCOOH)与c(CHCOO-)之和逐渐减小,错误;D.当加入氨水的体积为10mL时,醋酸
3 3
和一水合氨的物质的量相等,由于二者的电离常数相等,所以溶液显示中性,c(H+)=c(OH-),根
据电荷守恒可知:c(NH +)=c(CHCOO-),正确;故答案为D。
4 3
28.(2013·广东高考真题)下列各溶液中,离子的物质的量浓度关系正确的是
A.pH=4的醋酸中:c(H+)= 0.4mol·L-1
B.饱和碳酸氢钠溶液中(已知碳酸氢钠溶液呈碱性):c(Na+)= c(HCO -)
3
C.饱和食盐水中:c(Na+)+ c(H+)= c(Cl-)+c(OH-)
D.pH=12的纯碱溶液中:c(OH-)=1.0×10-12mol·L-1
【答案】C
【解析】A.pH=4的醋酸中c(H+)= mol·L-1,A不正确;B.饱和碳酸氢钠溶液中(已知碳酸氢钠溶液呈碱性),因为碳酸氢根既能水解又能电离(以水解为主,所以溶液显碱性),导致c(Na+)>c
(HCO -),所以B不正确;C.饱和食盐水呈电中性,存在电荷守恒:c(Na+)+ c(H+)= c(Cl-)+c
3
(OH-),所以C正确;D.纯碱溶液中,因碳酸根离子水解而使溶液呈碱性,所以c(OH-)> c
(H+),常温下pH=12的纯碱溶液中,c(H+)=1.0×10-12mol·L-1,根据水的离子积可以求出c(OH-)
= 1.0×10-2mol·L-1,所以D不正确。本题选C。
29.(2009·天津高考真题)25 ℃时,浓度均为0.2 mol/L的NaHCO 和NaCO 溶液中,下列判断不正确的
3 2 3
是
A.均存在电离平衡和水解平衡
B.存在的粒子种类相同
C.c(OH-)前者大于后者
D.分别加入NaOH固体,恢复到原温度,c(CO2-)均增大
3
【答案】C
【解析】A.NaCO 溶液中存在CO2-的水解平衡和水的电离平衡,NaHCO 溶液中既存在HCO -的电离平
2 3 3 3 3
衡又存在HCO -的水解平衡,同时存在水的电离平衡,正确;B.NaCO 和NaHCO 溶液中存在的粒
3 2 3 3
子种类相同,都有Na+、H+、OH-、HCO -、CO2-、HCO 和HO,正确;C.由于碳酸的一级电离远
3 3 2 3 2
大于二级电离,所以HCO -的水解能力弱于CO2-,0.2mol/LNaHCO 溶液中c(OH-)<0.2mol/LNa CO
3 3 3 2 3
溶液中c(OH-),错误;D.NaHCO 溶液中加入NaOH,HCO -转化成CO2-,c(CO2-)增大,
3 3 3 3
NaCO 溶液中加入NaOH,抑制CO2-的水解,c(CO2-)增大,正确;答案选C。
2 3 3 3
30.(2008·海南高考真题)下列离子方程式中,属于水解反应的是( )
A.HCOOH+H O HCOO-+ H O+
2 3
B.CO+H O HCO -+ H+
2 2 3
C.CO2-+ H O HCO -+ OH-
3 2 3
D.HS-+ H O S2-+ H O+
2 3
【答案】C
【解析】弱离子水解反应的实质是:弱离子和水电离出的氢离子或氢氧根离子结合生成弱电解质的过程,
水解方程式用可逆号。A、是甲酸的电离方程式,错误;B、是碳酸的一级电离方程式,错误;C、是
碳酸根的水解方程式,正确;D、是硫氢根离子的电离方程式,错误。