文档内容
黑龙江省大庆市2026届高三第一次教学质量检测化学试题
2025.09
注意事项:
1.答题前,考生先将自己的姓名、班级、考场号/座位号填写在答题卡上,认真核对条形码上的姓
名、准考证号,并将条形码粘贴在答题卡的指定位置上。
2.选择题答案使用2B铅笔填涂,如需改动,用橡皮擦干净后,再选涂其它答案的标号;非选择题
答案使用0.5毫米黑色中性(签字)笔或碳素笔书写,字体工整,笔迹清楚。
3.请按照题号在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效。
4.保持卷面及答题卡清洁,不折叠,不破损,不准使用涂改液、修正带、刮纸刀。
可能用到的相对原子质量: H-1 C-12 N-14 O-16 K-39 Cr—52 Co-59
一、选择题(本题共15小题,每小题3分,共45分,在每小题给出的四个选项中,只有一项符合题目
要求。)
1.传统文化中的化学知识很早就被人们巧妙运用。下列说法错误的是
A.战国时期的青铜器“曾侯乙编钟”的主要材质为铜合金
B.古代壁画中常用的红色颜料主要成分是铁红(FeyO )、朱砂(HgS)等
C.元代瓷器“青花麒麟纹梅瓶”的主要成分中含有硅酸盐
₄
D.南宋《蚕织图》描绘了种桑、养蚕的场景,蚕丝的主要成分是蛋白质
2.下列化学用语或图示正确的是
A.二氧化硅的分子式:SiO
B. NH 的电子式: ₂
C. C H 的球棍模型:
₃
D.基态 ₂ C₂ 原子的价电子轨道表示式:
3.设NA为阿伏加德罗常数的值,下列说法正确的是
A. 32gO 含有的氧原子数为2NA
B. 1mol⋅L−1KCl溶液中含有的 K 数为NA
₂
C. 标准状况下, 11.2LH O 含有的水分子数为0.5NA
⁺
D.1mol苯( )中含有的碳碳双键数目为3NA
₂
4.下列图示实验中,操作规范且能达到实验目的的是
A.灼烧海带 B.萃取碘水中的碘 C.稀释浓硫酸 D.测定醋酸溶液的pH
5.钠及其化合物有很多性质和用途,下列化学方程式或离子方程式书写正确的是
A.用金属钠除去甲苯中的微量水: 2Na+2H O2NaOH+H ↑
2 2
B.小苏打治疗胃酸过多: CO2−+2H+CO ↑+H O
3 2 2
C.向次氯酸钠溶液中加入浓盐酸: ClO−+H+HClO❑
D.溴乙烷与氢氧化钠的乙醇溶液共热: CH CH Br+NaOH→CH CH OH+NaBr
3 2 3 2
❑
6.化学在食品生产中有重要应用,下列生产项目与化学知识的描述均正确且有关联的是
选项 生产项目 化学知识
A 用福尔马林浸泡食材 福尔马林有防腐作用
B
在水果罐头中添加维生素C 维生素C有还原性
向葡萄酒中添加适量: SO₂ SO₂有漂白性
C
D 用粮食酿酒 淀粉水解生成乙醇
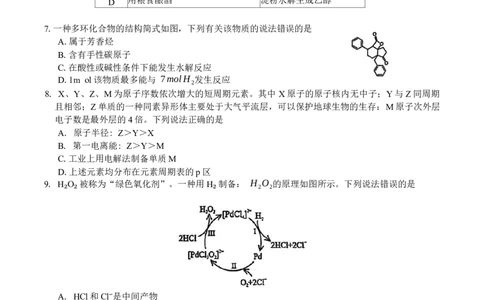
7.一种多环化合物的结构简式如图,下列有关该物质的说法错误的是
A.属于芳香烃
B.含有手性碳原子
C.在酸性或碱性条件下能发生水解反应
D.1m ol该物质最多能与 7molH 发生反应
2
8. X、Y、Z、M为原子序数依次增大的短周期元素。其中 X原子的原子核内无中子;Y与Z同周期
且相邻;Z单质的一种同素异形体主要处于大气平流层,可以保护地球生物的生存:M原子次外层
电子数是最外层的4倍。下列说法正确的是
A. 原子半径: Z>Y>X
B. 第一电离能: Z>Y>M
C.工业上用电解法制备单质M
D.上述元素均分布在元素周期表的p区
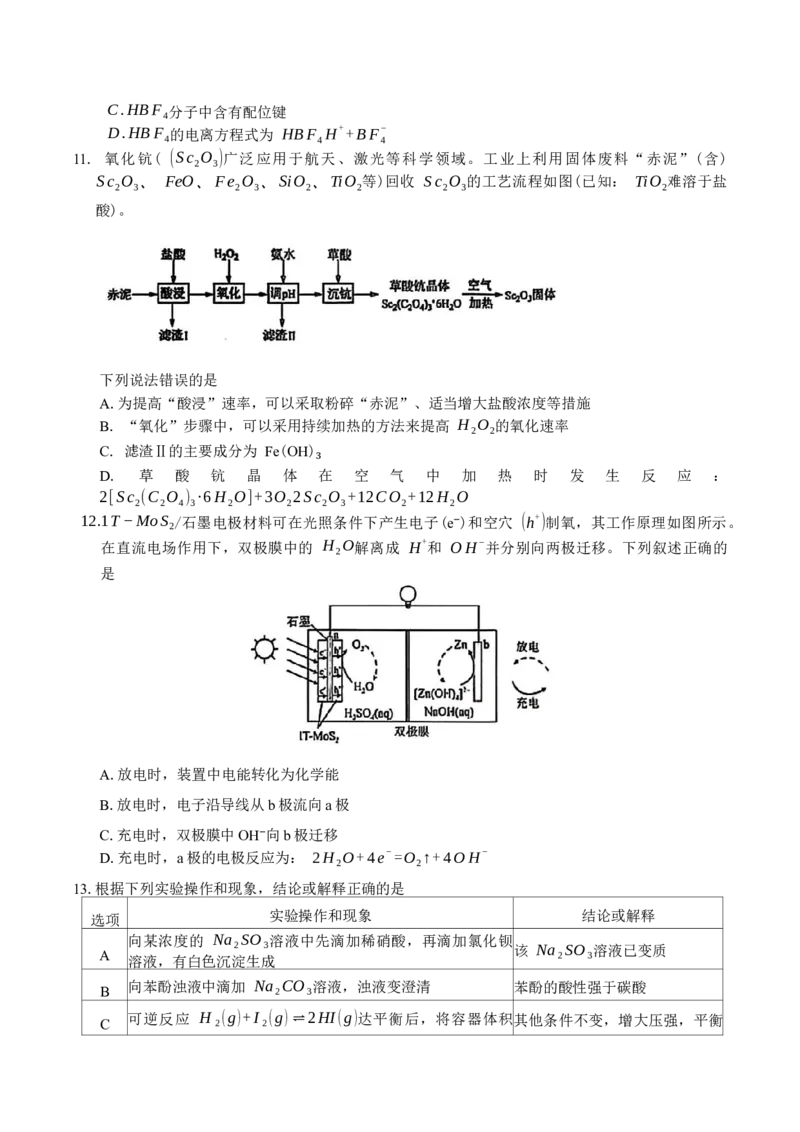
9. H O 被称为“绿色氧化剂”。一种用H 制备: H O 的原理如图所示。下列说法错误的是
2 2
₂ ₂ ₂
A. HCl和Cl⁻是中间产物
B.反应Ⅰ涉及非极性键的断裂和极性键的形成
C.整个过程总反应的原子利用率是 100%
D.使用催化剂可以改变反应历程,从而改变总反应的反应热
10.氟硼酸(HBF )是一种强酸,用它代替硫酸作铅蓄电池的电解质溶液,可使电池在低温下工作时的
性能更优良。 HBF 可由如下反应制备: HF+BF =HBF 。下列说法错误的是
₄ 4 3 4
A. HF 的沸点比 HCl的沸点高
B.BF 中B原子的杂化方式是 sp2杂化
3C.HBF 分子中含有配位键
4
D.HBF 的电离方程式为 HBF H++BF−
4 4 4
11. 氧化钪( (Sc O )广泛应用于航天、激光等科学领域。工业上利用固体废料“赤泥”(含)
2 3
Sc O 、 FeO、Fe O 、SiO 、TiO 等)回收 Sc O 的工艺流程如图(已知: TiO 难溶于盐
2 3 2 3 2 2 2 3 2
酸)。
下列说法错误的是
A.为提高“酸浸”速率,可以采取粉碎“赤泥”、适当增大盐酸浓度等措施
B. “氧化”步骤中,可以采用持续加热的方法来提高 H O 的氧化速率
2 2
C. 滤渣Ⅱ的主要成分为 Fe(OH)
D. 草 酸 钪 晶 体 在 空 气 中 加 热 时 发 生 反 应 :
₃
2[Sc (C O ) ·6H O]+3O 2Sc O +12CO +12H O
2 2 4 3 2 2 2 3 2 2
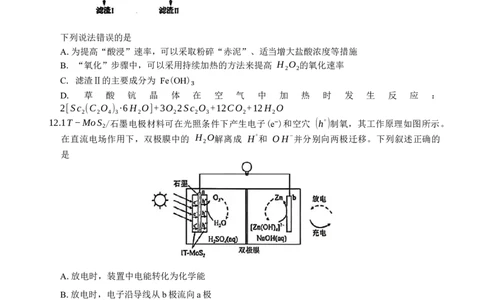
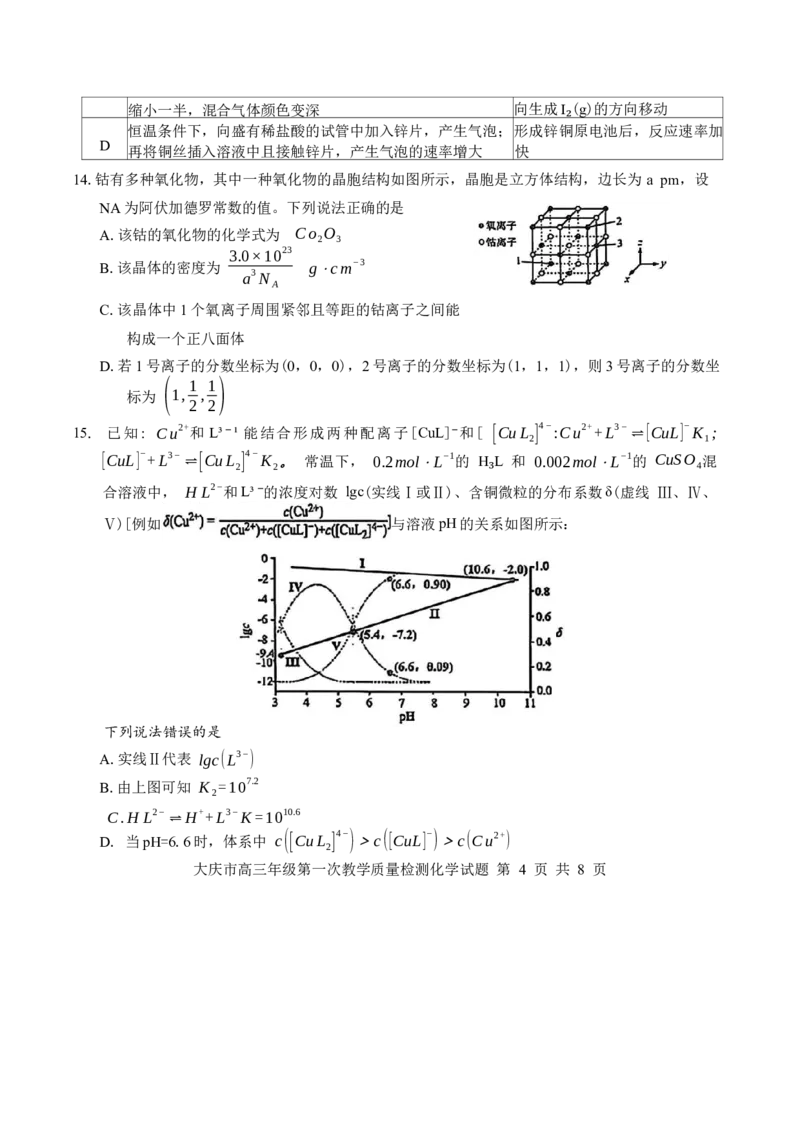
12.1T−MoS /石墨电极材料可在光照条件下产生电子(e⁻)和空穴 (h+)制氧,其工作原理如图所示。
2
在直流电场作用下,双极膜中的 H O解离成 H+和 OH−并分别向两极迁移。下列叙述正确的
2
是
A.放电时,装置中电能转化为化学能
B.放电时,电子沿导线从b极流向a极
C.充电时,双极膜中OH⁻向b极迁移
D.充电时,a极的电极反应为: 2H O+4e−=O ↑+4OH−
2 2
13.根据下列实验操作和现象,结论或解释正确的是
实验操作和现象 结论或解释
选项
向某浓度的 Na₂SO₃溶液中先滴加稀硝酸,再滴加氯化钡
该 Na₂SO₃溶液已变质
A
溶液,有白色沉淀生成
向苯酚浊液中滴加 Na₂CO₃溶液,浊液变澄清 苯酚的酸性强于碳酸
B
C
可逆反应 H₂(g)+I₂(g)⇌2HI(g)达平衡后,将容器体积其他条件不变,增大压强,平衡缩小一半,混合气体颜色变深 向生成I (g)的方向移动
恒温条件下,向盛有稀盐酸的试管中加入锌片,产生气泡;形成锌铜原电池后,反应速率加
D ₂
再将铜丝插入溶液中且接触锌片,产生气泡的速率增大 快
14.钴有多种氧化物,其中一种氧化物的晶胞结构如图所示,晶胞是立方体结构,边长为 a pm,设
NA为阿伏加德罗常数的值。下列说法正确的是
A.该钴的氧化物的化学式为 Co O
2 3
3.0×1023
B.该晶体的密度为 g⋅cm−3
a3N
A
C.该晶体中1个氧离子周围紧邻且等距的钴离子之间能
构成一个正八面体
D.若1号离子的分数坐标为(0,0,0),2号离子的分数坐标为(1,1,1),则3号离子的分数坐
( 1 1)
标为 1, ,
2 2
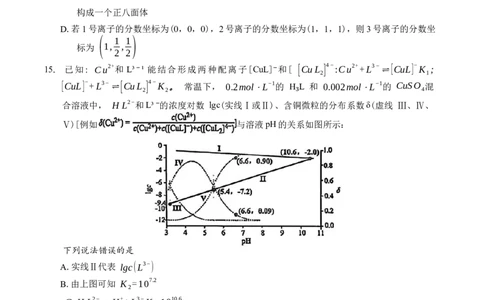
15. 已知: Cu2+和 L³⁻¹能结合形成两种配离子[CuL]⁻和[ [CuL ] 4− :Cu2++L3− ⇌[CuL] − K ;
2 1
[CuL] −+L3− ⇌[CuL
2
] 4− K
2
。 常温下, 0.2mol⋅L−1的 H L 和 0.002mol⋅L−1的 CuSO
4
混
合溶液中, H L2−和L³⁻的浓度对数 lgc(实线Ⅰ或Ⅱ)、含铜₃微粒的分布系数δ(虚线 Ⅲ、Ⅳ、
Ⅴ)[例如 与溶液pH的关系如图所示:
下列说法错误的是
A.实线Ⅱ代表 lgc(L3−)
B.由上图可知 K =107.2
2
C.H L2− ⇌H++L3−K=1010.6
D. 当pH=6.6时,体系中 c([CuL ] 4−)>c([CuL] −)>c(Cu2+)
2
大庆市高三年级第一次教学质量检测化学试题 第 4 页 共 8 页二、非选择题(本题共4小题,共55分)
16. (14分) As O 可用于治疗白血病和肝癌,镓(Ga)是一种稀散金属,有“电子工业脊梁”的美誉。
2 3
由废料(主要成分为 AS S 、GaAs、Fe O )提取回收 As O 和 Ga的部分工艺流程如下:
2 3 2 3 2 3
已知: Ga与 Al同族, Na[Ga(OH) ]是可溶性盐, Na[Ga(OH) ]与少量的酸反应会生成
4 4
Ga(OH) ,Ga(OH) 难溶于水,但能溶于酸和碱。
3 3
(1)已知砷(As)是33号元素,它位于元素周期表中的第 周期 族。
(2) “焙烧”操作中, GaAs转化为 Ga O 和 As O ,As S 转化为 As O 和气体X,则气
2 3 2 3 2 3 2 3
体X是 (填化学式)。
(3) “碱浸氧化”时会生成产物 Na[Ga(OH) ]和 Na AsO ,,写出此步骤生成 Na AsO
3 4 3 4
的化学方程式 ₄ 。
(4) 流 程 中 “ 调 pH” 的 目 的 是
(请用离子方程式和适当文字说明)。
(5)“还原”过程中,氧化剂与还原剂的物质的量之比为 。
(6)“旋流电积”是一种先进的电解技术。流程中“旋流电积”所得“尾液”中可循环利用的物
质是 (填化学名称)。
(7)已知GaAs晶体结构与金刚石相似,如图所示,1m ol GaAs晶体中含有 mol共价键。
17. (13分)重铬酸钾( (K Cr O )是一种重要的氧化剂,广泛应用于实验室和工业中。某实验小组通
2 2 7
过铬铁矿粉(主要成分为 FeO⋅Cr O ,还含有硅、铝等杂质)为原料制备 K Cr O 晶体,实验步骤
2 3 2 2 7
如下:
①氧化:将6.08g铬铁矿粉与 NaNO 混匀,分几次加入到NaOH与 Na CO 的熔融混合物中,
3 2 3
并不断搅拌,加热0.5h后自然冷却。
②浸取:用水多次浸取熔块,过滤除去含铁不溶物。③除杂:加冰醋酸调节滤液 pH至7-8,过滤除去杂质,再向滤液中滴加冰醋酸调至 pH≈S,溶
液由黄色转化为橙红色。
④提纯:向制得的重铬酸钠溶液中加入KCl 固体,经过一系列操作后得到重铬酸钾粗品,提纯后
最终得到 3.5gK Cr O 晶体。
2 2 7
已知:铬铁矿在碱性介质中易被氧化,生成可溶性铬酸盐
2[FeO⋅Cr O ]+4Na CO +7NaNO =4Na CrO +Fe O +7NaNO +4CO l
2 3 2 3 3 2 4 2 3 2 2
回答下列问题:
(1)“氧化”过程加热融化 NaOH与 Na CO 混合物选用的仪器是 。
2 3
A.蒸发皿 B.瓷坩埚 C.铁坩埚 D.石英坩埚
(2)把矿粉与 NaNO 的混合物分几次加入并不断搅拌的原因是 。
3
(3)“除杂”时加冰醋酸调节滤液pH至7-8的目的是 ,再向滤
液中滴加冰醋酸调至 pH≈5过程中发生反应的离子方程式 。
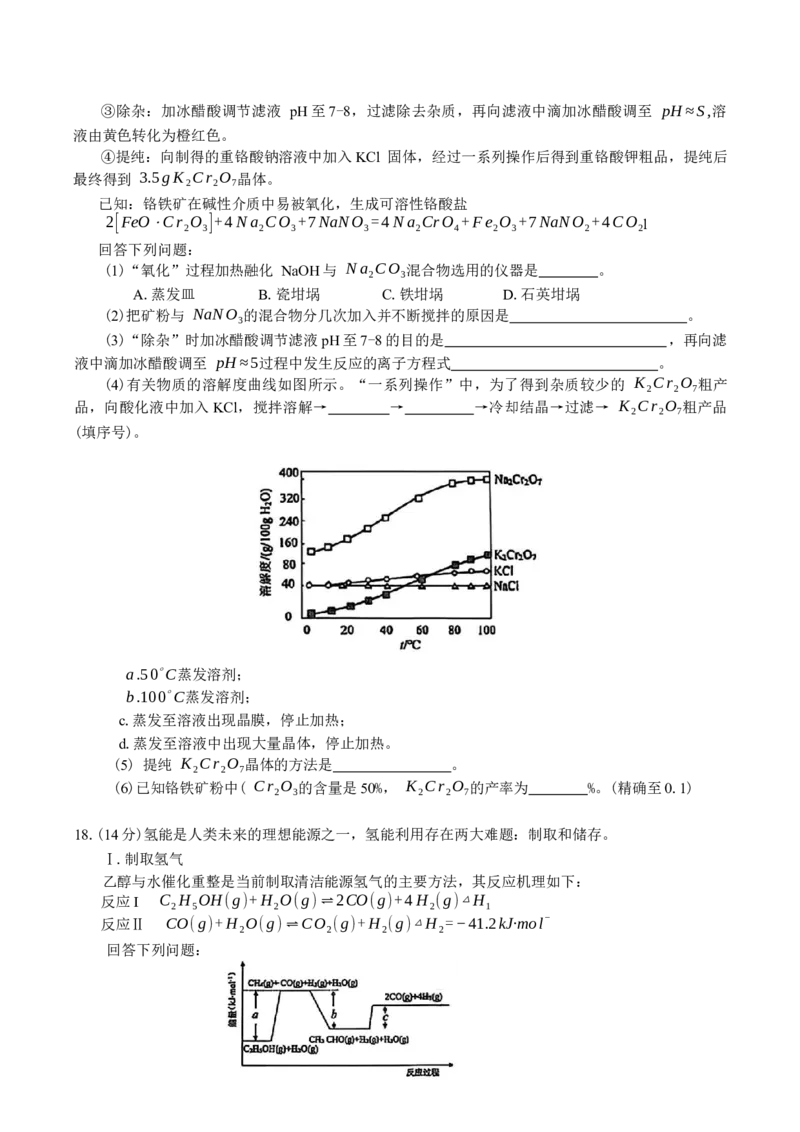
(4)有关物质的溶解度曲线如图所示。“一系列操作”中,为了得到杂质较少的 K Cr O 粗产
2 2 7
品,向酸化液中加入KCl,搅拌溶解→ → →冷却结晶→过滤→ K Cr O 粗产品
2 2 7
(填序号)。
a.50∘C蒸发溶剂;
b.100∘C蒸发溶剂;
c.蒸发至溶液出现晶膜,停止加热;
d.蒸发至溶液中出现大量晶体,停止加热。
(5) 提纯 K Cr O 晶体的方法是 。
2 2 7
(6)已知铬铁矿粉中( Cr O 的含量是50%, K Cr O 的产率为 %。(精确至0.1)
2 3 2 2 7
18.(14分)氢能是人类未来的理想能源之一,氢能利用存在两大难题:制取和储存。
Ⅰ.制取氢气
乙醇与水催化重整是当前制取清洁能源氢气的主要方法,其反应机理如下:
反应I C H OH(g)+H O(g)⇌2CO(g)+4H (g)△H
2 5 2 2 1
反应Ⅱ CO(g)+H O(g)⇌CO (g)+H (g)△H =−41.2kJ·mol−
2 2 2 2
回答下列问题:(1)在催化剂作用下,反应I可通过如图所示的反应历程实现催化重整,则
△H
1
=k J·mol−1
⏟
(用含字母a、b、c的代数式表示),该反应在 (填“高温”“低温”或“任意温度”)
下能自发进行。
(2)下列措施中一定能提高H 平衡产率的是 。
A.选择合适的催化剂 B.降低温度
₂
C.增大水蒸气浓度 D.恒温恒容下通入气体 Ar
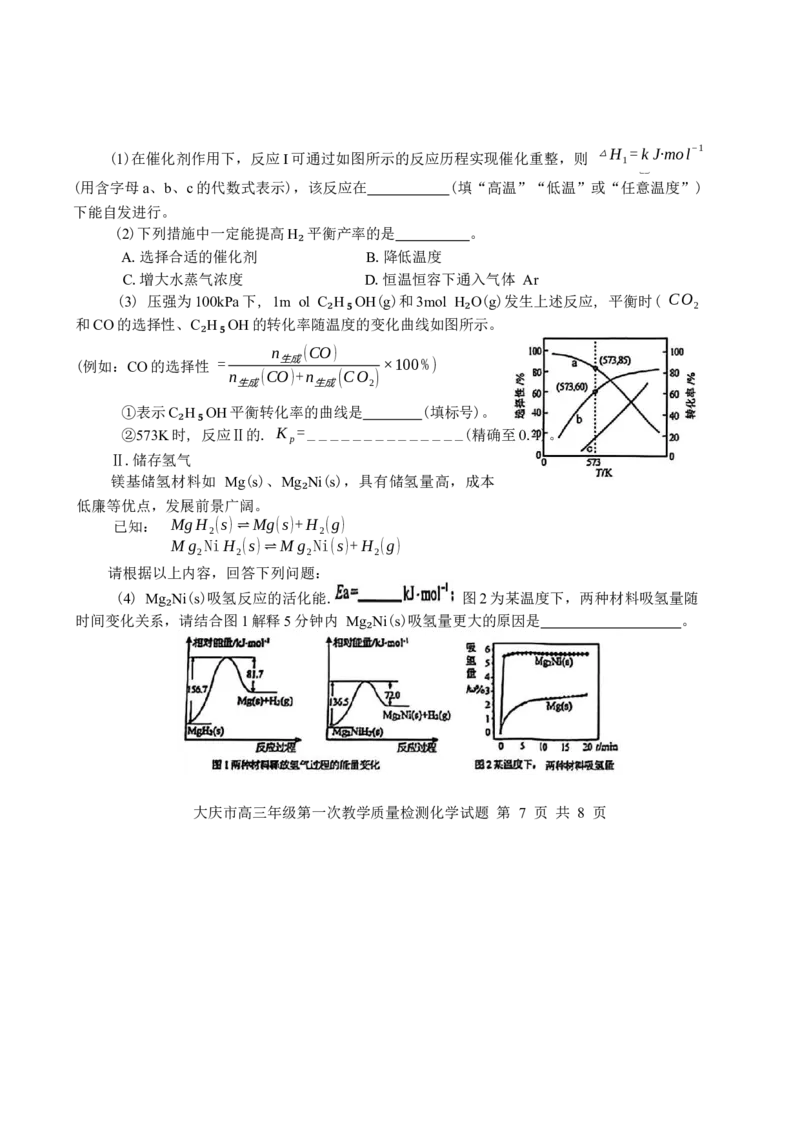
(3) 压强为100kPa下, 1m ol C H₅OH(g)和3mol H O(g)发生上述反应, 平衡时( CO
2
和CO的选择性、C H₅OH的转化率随温度的变化曲线如图所示。
₂ ₂
n (CO)
(例如:CO的选择性 ₂ = 生成 ×100%)
n (CO)+n (CO )
生成 生成 2
①表示C H₅OH平衡转化率的曲线是 (填标号)。
②573K时, 反应Ⅱ的. K =______________(精确至0.1)。
p
₂
Ⅱ.储存氢气
镁基储氢材料如 Mg(s)、Mg Ni(s),具有储氢量高,成本
低廉等优点,发展前景广阔。
₂
已知: MgH (s)⇌Mg(s)+H (g)
2 2
M g NiH (s)⇌M g Ni(s)+H (g)
2 2 2 2
请根据以上内容,回答下列问题:
(4) Mg Ni(s)吸氢反应的活化能. 图2为某温度下,两种材料吸氢量随
时间变化关系,请结合图1解释5分钟内 Mg Ni(s)吸氢量更大的原因是 。
₂
₂
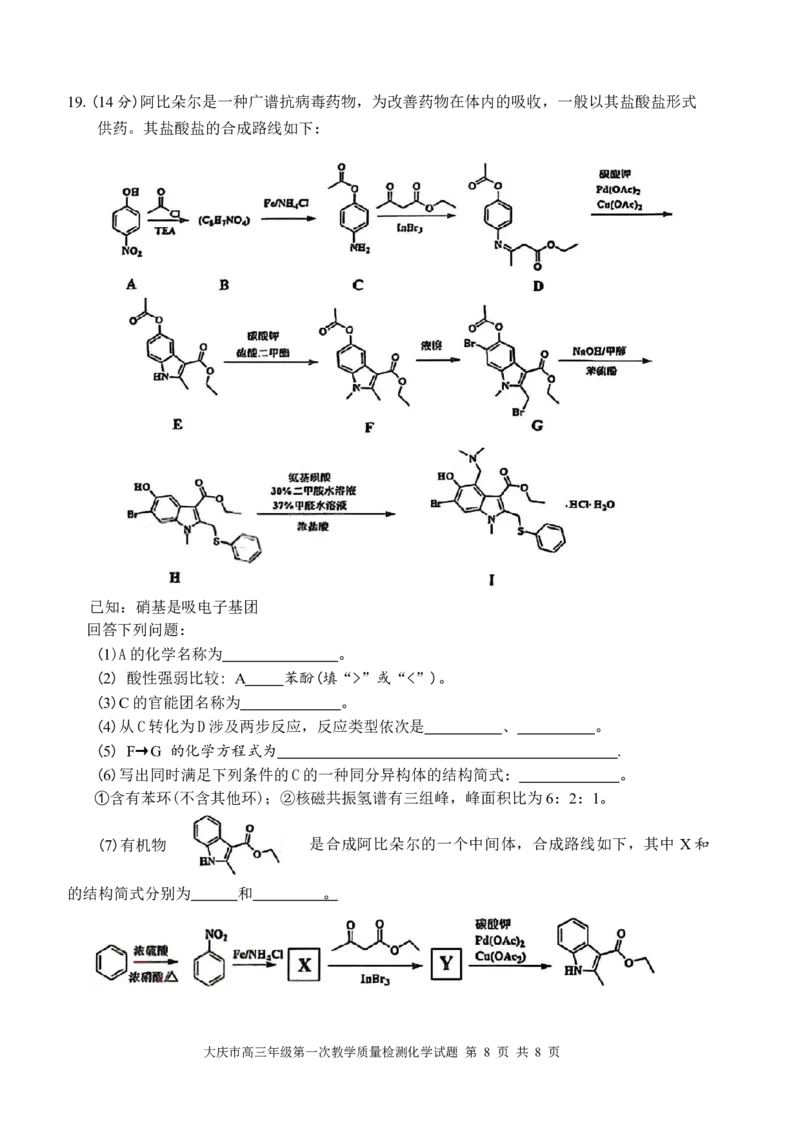
大庆市高三年级第一次教学质量检测化学试题 第 7 页 共 8 页19.(14分)阿比朵尔是一种广谱抗病毒药物,为改善药物在体内的吸收,一般以其盐酸盐形式
供药。其盐酸盐的合成路线如下:
碳酸钾
Pd(OAc)₂
Fe/NH₄Cl Cu(OAc)₂
A B C D
人。
。人。
6.
碳酸钾
浓镍
硫酸、二甲 NnOH/甲醇
酯 米圆圈
Br
E F G
N
氨基磺酸
HO、 o. 30%二甲胺水溶液
1 o 37%甲醛水溶液 . HCl·H₂O
Br
浓盐酸
◯
s
已知:硝基是吸电子基团
回答下列问题:
(1)A的化学名称为 。
(2) 酸性强弱比较: A 苯酚(填“>”或“<”)。
(3)C的官能团名称为 。
(4)从C转化为D涉及两步反应,反应类型依次是 、 。
(5) F→G 的化学方程式为 .
(6)写出同时满足下列条件的C的一种同分异构体的结构简式: 。
①含有苯环(不含其他环);②核磁共振氢谱有三组峰,峰面积比为6:2:1。
(7)有机物 是合成阿比朵尔的一个中间体,合成路线如下,其中 X和
Y
的结构简式分别为 和 。
碳酸钾
出生 2024
Pd(OAc)₂
C核酸配合
Cu(OAc₂)
X Y
InBr₃
大庆市高三年级第一次教学质量检测化学试题 第 8 页 共 8 页大庆市2026届高三年级化学第一次质量检测参考答案
(2025.09)
一、选择题(每题3分,共计45分)
1 2 3 4 5
B D A C A
6 7 8 9 10
B A C D D
11 12 13 14 15
B B D C C
二、非选择题(共55分)
16. (14分)
(1)四(或4) VA (各1分)
(2) SO (2分)
(3)As O +6NaOH+2H O =2Na AsO +5H O(2 分)(配平错误、系数不是最简的均不给
₂2 3 2 2 3 4 2
分)
(4) Na[Ga(OH) ]与少量的稀硫酸发生反应: [Ga(OH) ] − +H+=Ga(OH) ↓+H O, 调至合适的
4 3 2
pH保证Ga(OH) 沉₄淀完全, 便于将 Ga(OH) 和Na AsO 分离干净 (2分) (离子方程式写对的给1
分, 写出“便于分₃ 离”意思的再给1分) ₃ ₃ ₄
(5)1:1(2分)
(6)硫酸 (2分)(写分子式不给分)
(7)4(2分)
17.(13分)
(1) C (1分)
(2)使反应物充分接触、防止熔融物喷溅(或防止反应过于剧烈)(2分)(答对一条给1分)
(3) 生成 Al(OH) 、H SiO 沉淀, 过滤除杂 (2分);
2CrO2
4
−+2
₃
CH
3₂
COO
₃
H⇌Cr
2
O
7
2−+H
2
O+2CH
3
COO−(2分)
(4)a c(2分)
(5)重结晶(2分)
(6)59.5(2分)18.(14分)
(1) a-b+c (2分) 高温(2分)
(2)C (2分)
(3)①b (2分)
②14.0(2分)
(4) 72.0 (2分)
Mg Ni 吸氢反应活化能小,反应速率快。(2分)
₂
19.(14分)
(1)对硝基苯酚或4-硝基苯酚(1分)
(2)>(1分)
(3)酯基、氨基(2分)
(4)加成反应、消去反应(2分)