文档内容
专题46 电解原理
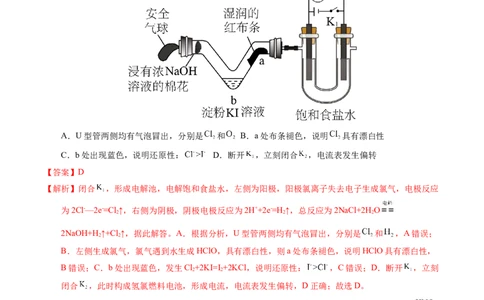
1.【2023年广东卷】利用活性石墨电极电解饱和食盐水,进行如图所示实验。闭合 ,一段时间后
A.U型管两侧均有气泡冒出,分别是 和 B.a处布条褪色,说明 具有漂白性
C.b处出现蓝色,说明还原性: D.断开 ,立刻闭合 ,电流表发生偏转
【答案】D
【解析】闭合 ,形成电解池,电解饱和食盐水,左侧为阳极,阳极氯离子失去电子生成氯气,电极反应
为2Cl-—2e-=Cl↑,右侧为阴极,阴极电极反应为2H++2e-=H ↑,总反应为2NaCl+2H O
2 2 2
2NaOH+H ↑+Cl↑,据此解答。A.根据分析,U型管两侧均有气泡冒出,分别是 和 ,A错误;
2 2
B.左侧生成氯气,氯气遇到水生成HClO,具有漂白性,则a处布条褪色,说明HClO具有漂白性,
B错误;C.b处出现蓝色,发生Cl+2KI=I +2KCl,说明还原性: ,C错误;D.断开 ,立刻
2 2
闭合 ,此时构成氢氯燃料电池,形成电流,电流表发生偏转,D正确;故选D。
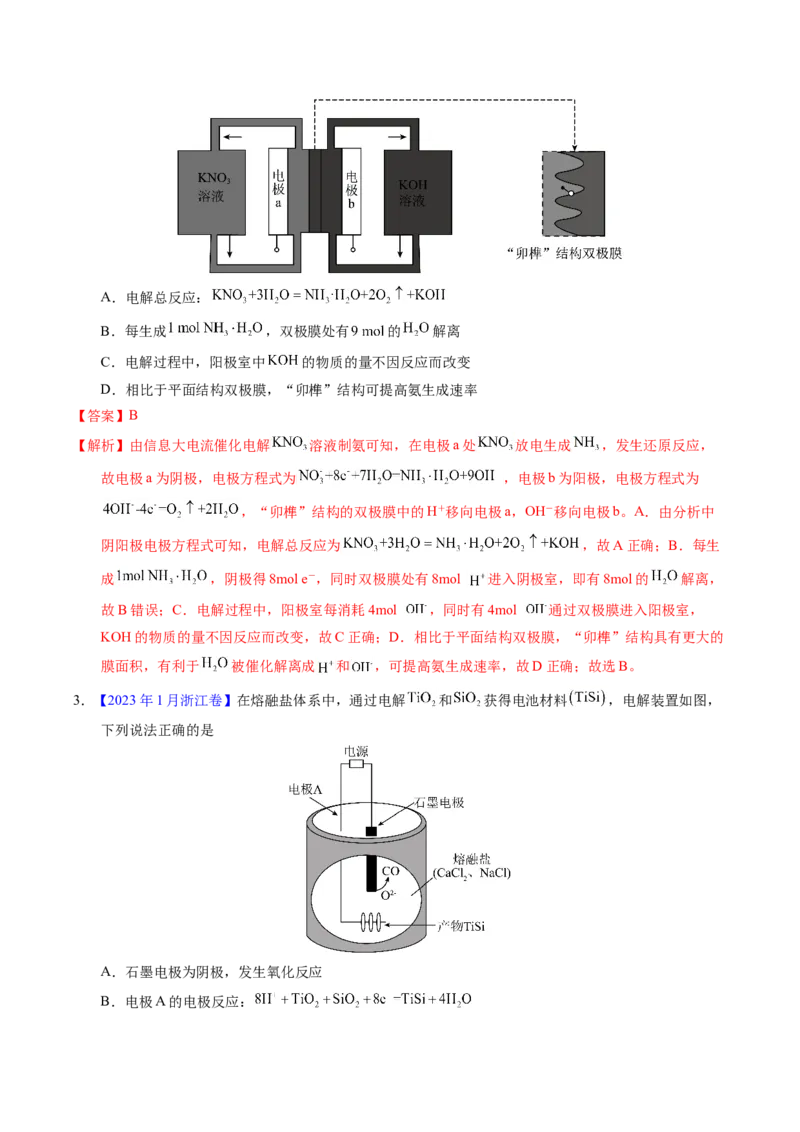
2.【2023年广东卷】用一种具有“卯榫”结构的双极膜组装电解池(下图),可实现大电流催化电解
溶液制氨。工作时, 在双极膜界面处被催化解离成 和 ,有利于电解反应顺利进行。下列说
法不正确的是A.电解总反应:
B.每生成 ,双极膜处有 的 解离
C.电解过程中,阳极室中 的物质的量不因反应而改变
D.相比于平面结构双极膜,“卯榫”结构可提高氨生成速率
【答案】B
【解析】由信息大电流催化电解 溶液制氨可知,在电极a处 放电生成 ,发生还原反应,
故电极a为阴极,电极方程式为 ,电极b为阳极,电极方程式为
,“卯榫”结构的双极膜中的H+移向电极a,OH-移向电极b。A.由分析中
阴阳极电极方程式可知,电解总反应为 ,故A正确;B.每生
成 ,阴极得8mol e-,同时双极膜处有8mol 进入阴极室,即有8mol的 解离,
故B错误;C.电解过程中,阳极室每消耗4mol ,同时有4mol 通过双极膜进入阳极室,
KOH的物质的量不因反应而改变,故C正确;D.相比于平面结构双极膜,“卯榫”结构具有更大的
膜面积,有利于 被催化解离成 和 ,可提高氨生成速率,故D正确;故选B。
3.【2023年1月浙江卷】在熔融盐体系中,通过电解 和 获得电池材料 ,电解装置如图,
下列说法正确的是
A.石墨电极为阴极,发生氧化反应
B.电极A的电极反应:C.该体系中,石墨优先于 参与反应
D.电解时,阳离子向石墨电极移动
【答案】C
【解析】由图可知,在外加电源下石墨电极上C转化为CO,失电子发生氧化反应,为阳极,与电源正极
相连,则电极A作阴极, 和 获得电子产生电池材料 ,电极反应为
。A.在外加电源下石墨电极上C转化为CO,失电子发生氧化反应,为
阳极,选项A错误;B.电极A的电极反应为 ,选项B错误;C.根据图
中信息可知,该体系中,石墨优先于 参与反应,选项C正确;D.电解池中石墨电极为阳极,阳离
子向阴极电极A移动,选项D错误;答案选C。
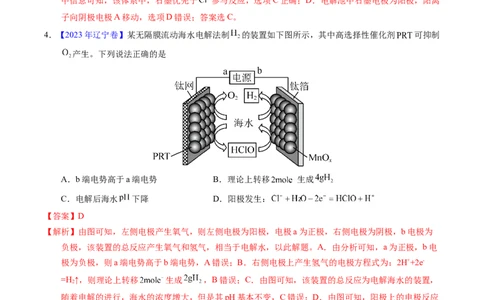
4.【2023年辽宁卷】某无隔膜流动海水电解法制 的装置如下图所示,其中高选择性催化剂 可抑制
产生。下列说法正确的是
A.b端电势高于a端电势 B.理论上转移 生成
C.电解后海水 下降 D.阳极发生:
【答案】D
【解析】由图可知,左侧电极产生氧气,则左侧电极为阳极,电极a为正极,右侧电极为阴极,b电极为
负极,该装置的总反应产生氧气和氢气,相当于电解水,以此解题。A.由分析可知,a为正极,b电
极为负极,则a端电势高于b端电势,A错误;B.右侧电极上产生氢气的电极方程式为:2H++2e-
=H ↑,则理论上转移 生成 ,B错误;C.由图可知,该装置的总反应为电解海水的装置,
2
随着电解的进行,海水的浓度增大,但是其pH基本不变,C错误;D.由图可知,阳极上的电极反应
为: ,D正确;故选D。
5.【2022年北京卷】利用下图装置进行铁上电镀铜的实验探究。
装置示意图 序号 电解质溶液 实验现象
0.1mol/LCuSO 阴极表面有无色气体,一段时间后阴极表面有红色固体,
4
①
+少量HSO 气体减少。经检验电解液中有
2 4
② 0.1mol/LCuSO 4 阴极表面未观察到气体,一段时间后阴极表面有致密红色+过量氨水 固体。经检验电解液中无 元素
下列说法不正确的是
A.①中气体减少,推测是由于溶液中 减少,且 覆盖铁电极,阻碍 与铁接触
B.①中检测到 ,推测可能发生反应:
C.随阴极析出 ,推测②中溶液 减少, 平衡逆移
D.②中 生成 ,使得 比①中溶液的小, 缓慢析出,镀层更致密
【答案】C
【解析】由实验现象可知,实验①时,铁做电镀池的阴极,铁会先与溶液中的氢离子、铜离子反应生成亚
铁离子、氢气和铜,一段时间后,铜离子在阴极得到电子发生还原反应生成铜;实验②中铜离子与过
量氨水反应生成四氨合铜离子,使得溶液中铜离子浓度比①中要小,电解速率减慢,铜离子在阴极得
到电子缓慢发生还原反应生成铜,在铁表面得到比实验①更致密的镀层。A.由分析可知,实验①时,
铁会先与溶液中的氢离子、铜离子反应,当溶液中氢离子浓度减小,反应和放电生成的铜覆盖铁电极,
阻碍氢离子与铁接触,导致产生的气体减少,故A正确;B.由分析可知,实验①时,铁做电镀池的
阴极,铁会先与溶液中的氢离子、铜离子反应生成亚铁离子、氢气和铜,可能发生的反应为
,故B正确;C.由分析可知,铜离子在阴极得到电子发生还原
反应,在阴极析出铜,但阳极发生Cu-2e-=Cu2+的反应,铜离子浓度不变,
平衡不移动,故C错误;D.由分析可知,实验②中铜离子与过量氨
水反应生成四氨合铜离子,使得溶液中铜离子浓度比①中要小,电解速率减慢,铜离子在阴极得到电
子缓慢发生还原反应生成铜,在铁表面得到比实验①更致密的镀层,故D正确;故选C。
6.【2022年天津卷】实验装置如图所示。接通电源后,用碳棒( 、 )作笔,在浸有饱和NaCl溶液和石
蕊溶液的湿润试纸上同时写字, 端的字迹呈白色。下列结论正确的是
A.a为负极
B. 端的字迹呈蓝色
C.电子流向为:D.如果将 、 换成铜棒,与碳棒作电极时的现象相同
【答案】B
【解析】A.根据实验现象,a'端呈白色,即生成了氯气,即氯离子失去电子,为阳极,即a为正极,A错
误;B.b'端为阴极,水得到电子放电的同时,生成氢氧根离子,遇石蕊变蓝,B正确;C.电子从电
源的负极出来,即从a极出来,而不是b极,C错误;D. 如果换成铜棒,铜做阳极放电,现象与碳
作电极时不相同,D错误;故选B。
7.(2021·海南真题)液氨中存在平衡: 。如图所示为电解池装置,以 的液氨溶
液为电解液,电解过程中a、b两个惰性电极上都有气泡产生。下列有关说法正确的是
A.b电极连接的是电源的负极 B.a电极的反应为
C.电解过程中,阴极附近K+浓度减小 D.理论上两极产生的气体物质的量之比为1:1
【答案】B
【解析】A.根据图示可知:在b电极上产生N,N元素化合价升高,失去电子,发生氧化反应,所以b
2
电极为阳极,连接电源的正极,A错误;B.电极a上产生H,H元素化合价降低得到电子,发生还
2
原反应,所以a电极为阴极,电极反应式为: ,B正确;C.电解过程中,阴极
附近产生 ,使附近溶液中阴离子浓度增大,为维持溶液电中性,阳离子K+会向阴极区定向移动,
最终导致阴极附近K+浓度增大,C错误;D.每反应产生1 mol H ,转移2 mol电子,每反应产生1
2
mol N,转移6 mol电子,故阴极产生H 与阳极产生的N 的物质的量的比是3:1,D错误;选B。
2 2 2
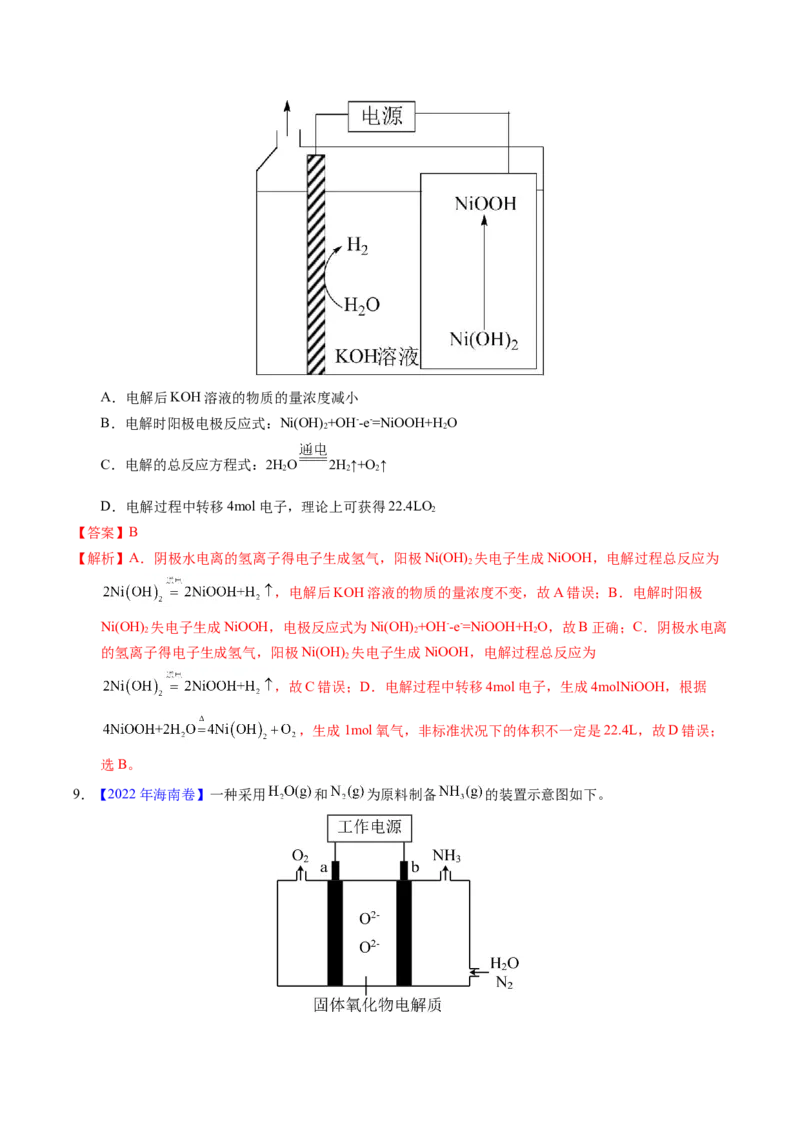
8.【2021年江苏卷】通过下列方法可分别获得H 和O:①通过电解获得NiOOH和H(如图);②在90℃
2 2 2
将NiOOH与HO反应生成Ni(OH) 并获得O。下列说法正确的是
2 2 2A.电解后KOH溶液的物质的量浓度减小
B.电解时阳极电极反应式:Ni(OH) +OH--e-=NiOOH+H O
2 2
C.电解的总反应方程式:2HO 2H↑+O ↑
2 2 2
D.电解过程中转移4mol电子,理论上可获得22.4LO
2
【答案】B
【解析】A.阴极水电离的氢离子得电子生成氢气,阳极Ni(OH) 失电子生成NiOOH,电解过程总反应为
2
,电解后KOH溶液的物质的量浓度不变,故A错误;B.电解时阳极
Ni(OH) 失电子生成NiOOH,电极反应式为Ni(OH) +OH--e-=NiOOH+H O,故B正确;C.阴极水电离
2 2 2
的氢离子得电子生成氢气,阳极Ni(OH) 失电子生成NiOOH,电解过程总反应为
2
,故C错误;D.电解过程中转移4mol电子,生成4molNiOOH,根据
,生成1mol氧气,非标准状况下的体积不一定是22.4L,故D错误;
选B。
9.【2022年海南卷】一种采用 和 为原料制备 的装置示意图如下。下列有关说法正确的是
A.在b电极上, 被还原
B.金属Ag可作为a电极的材料
C.改变工作电源电压,反应速率不变
D.电解过程中,固体氧化物电解质中 不断减少
【答案】A
【解析】由装置可知,b电极的N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,因此b为
2 3
阴极,电极反应式为N+3H O+6e-=2NH+3O2-,a为阳极,电极反应式为2O2-+4e-=O ,据此分析解答;
2 2 3 2
A.由分析可得,b电极上N 转化为NH ,N元素的化合价降低,得到电子发生还原反应,即N 被还
2 3 2
原,A正确;B.a为阳极,若金属Ag作a的电极材料,则金属Ag优先失去电子,B错误;C.改变
工作电源的电压,电流强度发生改变,反应速率也会改变,C错误;D.电解过程中,阴极电极反应
式为N+3H O+6e-=2NH+3O2-,阳极电极反应式为2O2-+4e-=O ,因此固体氧化物电解质中O2-不会改变,
2 2 3 2
D错误;答案选A。
10.【2022年6月浙江卷】通过电解废旧锂电池中的 可获得难溶性的 和 ,电解示意
图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。
下列说法不正确的是
A.电极A为阴极,发生还原反应
B.电极B的电极发应:
C.电解一段时间后溶液中 浓度保持不变
D.电解结束,可通过调节 除去 ,再加入 溶液以获得
【答案】C
【解析】A.由电解示意图可知,电极B上Mn2+转化为了MnO ,锰元素化合价升高,失电子,则电极B
2
为阳极,电极A为阴极,得电子,发生还原反应,A正确;B.由电解示意图可知,电极B上Mn2+失
电子转化为了MnO ,电极反应式为:2HO+Mn2+-2e-=MnO+4H+,B正确;C.电极A为阴极,
2 2 2
LiMn O 得电子,电极反应式为:2LiMn O+6e-+16H+=2Li++4Mn2++8H O,依据得失电子守恒,电解池
2 4 2 4 2
总反应为:2LiMn O+4H+=2Li++Mn2++3MnO+2H O,反应生成了Mn2+,Mn2+浓度增大,C错误;D.
2 4 2 2电解池总反应为:2LiMn O+4H+=2Li++Mn2++3MnO+2H O,电解结束后,可通过调节溶液pH将锰离
2 4 2 2
子转化为沉淀除去,然后再加入碳酸钠溶液,从而获得碳酸锂,D正确;答案选C。
11.(2020·山东高考真题)采用惰性电极,以去离子水和氧气为原料通过电解法制备双氧水的装置如下图
所示。忽略温度变化的影响,下列说法错误的是
A.阳极反应为
B.电解一段时间后,阳极室的pH未变
C.电解过程中,H+由a极区向b极区迁移
D.电解一段时间后,a极生成的O 与b极反应的O 等量
2 2
【答案】D
【解析】a极析出氧气,氧元素的化合价升高,做电解池的阳极,b极通入氧气,生成过氧化氢,氧元素的
化合价降低,被还原,做电解池的阴极。A.依据分析a极是阳极,属于放氧生酸性型的电解,所以
阳极的反应式是2HO-4e-=4H++O ↑,正确;B.电解时阳极产生氢离子,氢离子是阳离子,通过质子
2 2
交换膜移向阴极,所以电解一段时间后,阳极室的pH值不变,正确;C.有B的分析可知,C正确;
D.电解时,阳极的反应为:2HO-4e-=4H++O ↑,阴极的反应为:O+2e-+2H+=H O,总反应为:
2 2 2 2 2
O+2H O=2HO,要消耗氧气,即是a极生成的氧气小于b极消耗的氧气,错误;故选:D。
2 2 2 2
12.(2020·全国高考真题)电致变色器件可智能调控太阳光透过率,从而实现节能。下图是某电致变色器
件的示意图。当通电时,Ag+注入到无色WO 薄膜中,生成AgWO,器件呈现蓝色,对于该变化过
3 x 3
程,下列叙述错误的是
A.Ag为阳极 B.Ag+由银电极向变色层迁移
C.W元素的化合价升高 D.总反应为:WO+xAg=AgWO
3 x 3
【答案】C
【解析】从题干可知,当通电时,Ag+注入到无色WO 薄膜中,生成Ag WO 器件呈现蓝色,说明通电时,
3 x 3
Ag电极有Ag+生成然后经固体电解质进入电致变色层,说明Ag电极为阳极,透明导电层时阴极,g
电极上发生氧化反应,电致变色层发生还原反应。A.通电时,Ag电极有Ag+生成,g电极为阳极,正确;B.通电时电致变色层变蓝色,说明有Ag+从Ag电极经固体电解质进入电致变色层,正确;
C.过程中,W由WO 的+6价降低到Ag WO 中的+(6-x)价,错误;D.该电解池中阳极即Ag电极上
3 x 3
发生的电极反应为:xAg-xe-= xAg+,而另一极阴极上发生的电极反应为:WO+xAg++xe- = AgxWO,
3 3
故发生的总反应式为:xAg + WO =Ag WO,正确;答案选C。
3 x 3
13.(2013·天津高考真题)为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电
解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下: 电池: Pb(s) + PbO (s) + 2H SO (aq)
2 2 4
=2PbSO(s) + 2H O(l);
4 2
电解池:2Al+3O Al O+3H ↑电解过程中,以下判断正确的是( )
2 2 3 2
电池 电解池
A H+移向Pb电极 H+移向Pb电极
B 每消耗3molPb 生成2molAl O
2 3
C 正极:PbO +4H++2e—=Pb2++2H O 阳极:2Al+3H O-6e—=AlO+6H+
2 2 2 2 3
D
【答案】D
【解析】A.原电池中,溶液中氢离子向正极二氧化铅电极移动,错误;B.根据电子守恒分析,每消耗
3molPb,转移6mol电子,根据电子守恒生成lmolAl O,错误;C.原电池正极上二氧化铅得电子生
2 3
成硫酸铅,错误;D.原电池中铅作负极,负极上铅失电子和硫酸根离子反应生成难溶性的硫酸铅,
所以质量增加,在电解池中,Pb阴极,阴极上氢离子得电子生成氢气,所以铅电极质量不变,正确;
故选D。
14.(2007·全国高考真题)以惰性电极电解足量的CuSO 溶液。若阳极上产生气体的物质的量为0.0100
4
mol,则阴极上析出铜的质量为( )
A.0.64 g B.1.28 g C.2.56 g D.5.12 g
【答案】B
【解析】惰性电极电解CuSO 溶液时,阳极产生的是氧气,则转移电子是0.04mol,因此根据电子得失守
4
恒可知,析出铜是 =0.02mol,质量是0.02mol×64g/mol=1.28g;答案选B。
15.(2014·上海高考真题)如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中,下列分析正
确的是A.K 闭合,铁棒上发生的反应为2H++2e-=H ↑
1 2
B.K 闭合,石墨棒周围溶液pH逐渐升高
1
C.K 闭合,铁棒不会被腐蚀,属于牺牲阳极的阴极保护法
2
D.K 闭合,电路中通过0.002N 个电子时,两极共产生0.001 mol气体
2 A
【答案】B
【解析】A、K 闭合构成原电池,铁是活泼的金属,铁棒是负极,铁失去电子,铁棒上发生的反应为Fe-2e
1
-=Fe2+,A不正确;B、K 闭合构成原电池,铁棒是负极,铁失去电子,石墨棒是正极,溶液中的氧
1
气得到电子转化为OH-,电极反应式为O+4e-+2HO=4OH-,石墨棒周围溶液pH逐渐升高,B正
2 2
确;C、K 闭合构成电解池,铁棒与电源的负极相连,作阴极,溶液中的氢离子放电产生氢气,铁不
2
会被腐蚀,属于外加电流的阴极保护法,C不正确;D、K 闭合构成电解池,铁棒与电源的负极相连,
2
作阴极,溶液中的氢离子放电生成氢气。石墨棒是阳极,溶液中的氯离子放电生成氯气,电极反应式
分别为2H++2e-=H↑、2Cl--2e-=Cl↑,电路中通过0.002N 个电子时,两极均产生0.001mol气体,
2 2 A
共计是0.002mol气体,D不正确;答案选B。
16.(2012·安徽高考真题)某兴趣小组设计如下微型实验装置。实验时,现断开K,闭合K,两极均有
2 1
气泡产生;一段时间后,断开K,闭合K,发现电流表指针偏转,下列有关描述正确的是
1 2
A.断开K,闭合K 时,总反应的离子方程式为:2H++2Cl— Cl↑+H ↑
2 1 2 2
B.断开K,闭合K 时,石墨电极附近溶液变红
2 1
C.断开K,闭合K 时,铜电极上的电极反应为:Cl+2e—=2Cl—
1 2 2
D.断开K,闭合K 时,石墨电极作正极
1 2
【答案】D
【解析】A、断开K、闭合K 时,装置为电解池,两极均有气泡产生,则总反应为2Cl-+2H O
2 1 2H↑+2OH-+Cl↑,石墨为阳极,铜为阴极,因此石墨电极处产生Cl,在铜电极处产生H,铜电极附近
2 2 2 2
产生OH-,溶液变红,A错误;B、根据A中分析可知B错误;C、断开K、闭合K 时,装置为原电
1 2
池,铜电极上的电极反应为H-2e-+2OH-=2H O,其为负极,而石墨上的电极反应为Cl+2e-=2Cl-,其
2 2 2
为正极,C错误;D、根据C中分析可知D正确,答案选D。
17.(2007·上海高考真题)某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的
混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,
下列叙述正确的是
A.铅笔端作阳极,发生还原反应
B.铂片端作阴极,发生氧化反应
C.铅笔端有少量的氯气产生
D.a点是负极,b点是正极
【答案】D
【解析】出现红色字迹,说明溶液中有OH-生成,所以铅笔端作阴极,氢离子放电,发生还原反应,因此
a是电源的负极,b是正极。A.铅笔端作阴极,发生还原反应,错误;B.铂片端作阳极,发生氧化
反应,错误;C.铅笔端作阴极,溶液中的阳离子在铅笔端放电,所以不会生成氯气,错误;D.铅笔
端作阴极,则a是电源的负极,b是正极,正确;答案选D。
18.(2012·上海高考真题)右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H↑,下列说法错误的
2
是
A.a、b不可能是同种材料的电极
B.该装置可能是电解池,电解质溶液为稀盐酸
C.该装置可能是原电池,电解质溶液为稀盐酸
D.该装置可看作是铜-锌原电池,电解质溶液是稀硫酸
【答案】A
【解析】A、如果此装置是电解池装置,阴阳两极可以都为锌,电解质溶液是硫酸溶液,错误;B、如果是
电解池,阳极是锌,电极反应式:Zn-2e-=Zn2+,阴极:2H++2e-=H ↑,正确;B、如果是原电池,
2
负极为Zn,反应式为Zn-2e-=Zn2+,正极反应式:2H++2e-=H ↑,正确;D、锌比铜活泼,锌作负
2
极,负极为Zn,反应式为Zn-2e-=Zn2+,铜作正极,正极反应式:2H++2e-=H ↑,正确。
2
19.(2012·海南高考真题)下列各组中,每种电解质溶液电解时(惰性电极)只生成氢气和氧气的是
A.HCl、CuCl 、Ba(OH) B.NaOH、CuSO 、HSO
2 2 4 2 4C.NaOH、HSO 、Ba(OH) D.NaBr、HSO 、Ba(OH)
2 4 2 2 4 2
【答案】C
【解析】A、根据我们所学的电解原理,惰性电极电解CuCl 时阳极析出氯气,阴极析出铜,A错误;B、
2
惰性电极电解CuSO 时阴极析出铜,阳极产生氧气,B错误;C、惰性电极电解NaOH、HSO 、
4 2 4
Ba(OH) 实质上均是电解水,只生成氢气和氧气,C正确;D、惰性电极电解NaBr时,阳极析出溴单
2
质,阴极产生氢气,D错误。答案选C
20.(2012·福建高考真题)将下图所示实验装置的 K 闭合,下列判断正确的是
A.Cu 电极上发生还原反应
B.电子沿 Zn→a→b→Cu 路径流动
C.片刻后甲池中c(SO 2-)增大
4
D.片刻后可观察到滤纸b点变红色
【答案】A
【解析】关闭K后,甲、乙装置能自发的进行氧化还原反应,所以是原电池,锌易失电子作负极,铜作正
极,则含有硫酸钠溶液的滤纸是电解池,a是阴极,b是阳极。A、铜电极上铜离子得电子发生还原反
应生成铜,正确;B、电子从Zn→a,b→Cu路径流动,电子不能进入电解质溶液,错误;C、锌作负
极,负极上锌失电子发生氧化反应生成锌离子进入溶液,硫酸根离子不参加反应,所以硫酸根离子浓
度不变,错误;D、电解池中,a电极上氢离子放电生成氢气,同时a电极附近生成氢氧根离子,导致
溶液碱性增强,所以a点变红色,错误;答案选A。
21.(2014·江苏高考真题)硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有
多种方法。
(1)将烧碱吸收HS后的溶液加入到如题图—1所示的电解池的阳极区进行电解。电解过程中阳极区发生
2
如下反应:S2-—2e-=S(n—1)S+ S2-=S2-。
n
①写出电解时阴极的电极反应式:__________________。
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成_____________。【答案】(1)2HO+2e-=H ↑+2OH- S 2-+2H+=(n-1)S↓+H S↑
2 2 n 2
【解析】
(1)①阳极上硫离子放电,电极反应式为S2--2e-=S,阴极上氢离子放电生成氢气,电极反应式为
2HO+2e-=H ↑+2OH-,故答案为2HO+2e-=H ↑+2OH-;
2 2 2 2
②电解后阳极区离子为S2-,酸性条件下,S2-和氢离子反应生成S单质,S元素失电子发生氧化反应生成S
n n
单质,同时S元素得电子生成HS,反应方程式为S2-+2H+=(n-1)S↓+HS↑,故答案为S2-+2H+=
2 n 2 n
(n-1)S↓+HS↑;
2
22.(2019·江苏高考真题)CO 的资源化利用能有效减少CO 排放,充分利用碳资源。
2 2
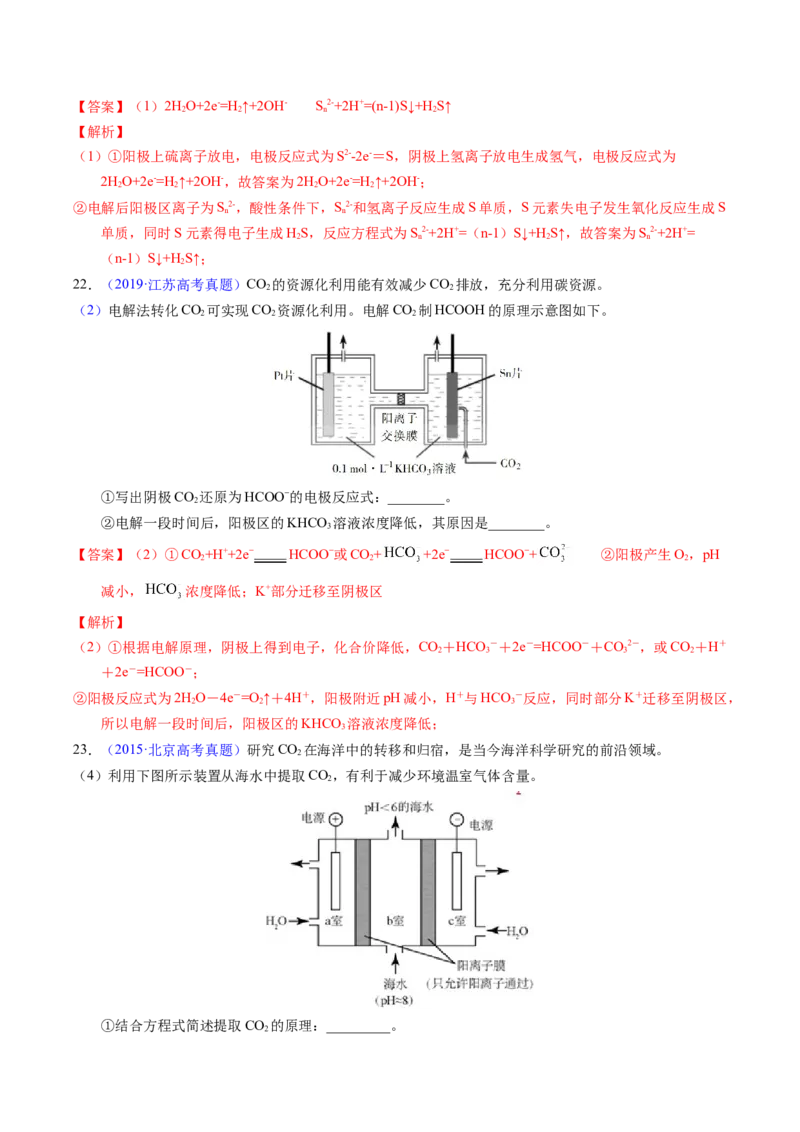
(2)电解法转化CO 可实现CO 资源化利用。电解CO 制HCOOH的原理示意图如下。
2 2 2
①写出阴极CO 还原为HCOO−的电极反应式:________。
2
②电解一段时间后,阳极区的KHCO 溶液浓度降低,其原因是________。
3
【答案】(2)①CO+H++2e− HCOO−或CO+ +2e− HCOO−+ ②阳极产生O,pH
2 2 2
减小, 浓度降低;K+部分迁移至阴极区
【解析】
(2)①根据电解原理,阴极上得到电子,化合价降低,CO+HCO -+2e-=HCOO-+CO2-,或CO+H+
2 3 3 2
+2e-=HCOO-;
②阳极反应式为2HO-4e-=O ↑+4H+,阳极附近pH减小,H+与HCO -反应,同时部分K+迁移至阴极区,
2 2 3
所以电解一段时间后,阳极区的KHCO 溶液浓度降低;
3
23.(2015·北京高考真题)研究CO 在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。
2
(4)利用下图所示装置从海水中提取CO,有利于减少环境温室气体含量。
2
①结合方程式简述提取CO 的原理:_________。
2②用该装置产生的物质处理b室排出的海水,合格后排回大海。处理至合格的方法是_______。
【答案】(4)①a室:2HO-4e-= O ↑+4H+,H+通过阳离子膜进入b室,发生反应:HCO -+H+=
2 2 3
CO↑+H O ② c室的反应:2HO+2e-=2OH-+H ↑,用c室排出的碱液将从b室排出的酸性海水调节
2 2 2 2
至接近装置入口海水的pH
【解析】
(4)①海水pH>8,显碱性,需要H+中和降低海水的碱性,a室发生阳极反应:2HO-4e-= O ↑+4H+,c
2 2
(OH-)下降,HO OH-+H+平衡右移,c(H+)增大,H+从a室进入b室,发生反应:HCO -
2 3
+H+= CO+H O。
2 2
②c室的反应:2HO+2e-=2OH-+H ↑,用c室排出的碱液将从b室排出的酸性海水调节至接近装置入口海水
2 2
的pH 。
24.(2012·全国高考真题)由黄铜矿(主要成分是CuFeS)炼制精铜的工艺流程示意图如下:
2
(3)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极 (填图中的字母);在电极d
上发生的电极反应式为_______;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为
______。
【答案】(3) c Cu2++2e-= Cu Au、Ag以单质的形式沉积在c(阳极)下方,Fe以Fe2+的形式进入电
解质溶液中
【解析】
(3)①在粗铜的电解过程中,粗铜板作阳极,应是图中电极c;
②在电极d为阴极,发生的电极反应式为Cu2++2e-=Cu;
③若粗铜中还含有Au、Ag、Fe,Au、Ag的活泼性弱于铜,所以Au、Ag以单质形式沉积在阳极下方,铁
比铜活泼,会失电子生成Fe2+,Fe2+氧化性弱于Cu2+,所以Fe以Fe2+形式进入电解液中。
25.(2014·重庆高考真题)氢能是重要的新能源。储氢作为氢能利用的关键技术,是当前关注的热点之一。
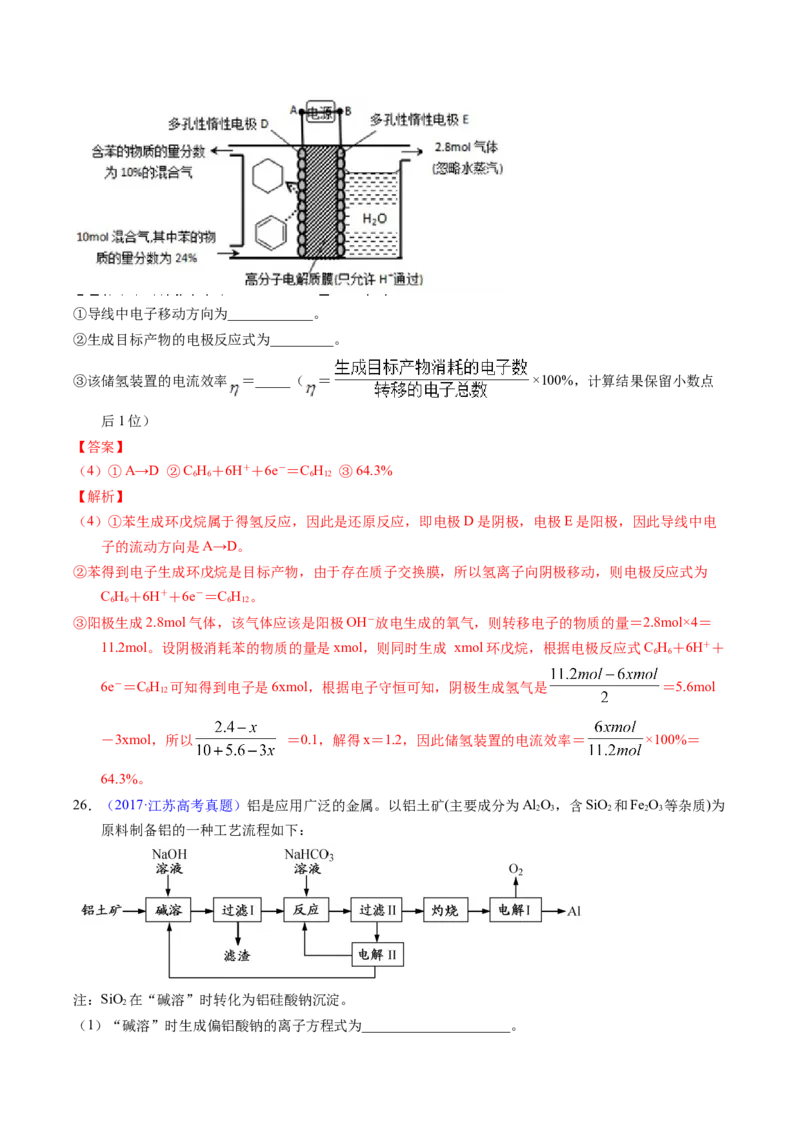
(4)一定条件下,题11图示装置可实现有机物的电化学储氢(忽略其它有机物)。①导线中电子移动方向为____________。
②生成目标产物的电极反应式为_________。
③该储氢装置的电流效率 =_____( = ×100%,计算结果保留小数点
后1位)
【答案】
(4)①A→D ②C H+6H++6e-=C H ③64.3%
6 6 6 12
【解析】
(4)①苯生成环戊烷属于得氢反应,因此是还原反应,即电极D是阴极,电极E是阳极,因此导线中电
子的流动方向是A→D。
②苯得到电子生成环戊烷是目标产物,由于存在质子交换膜,所以氢离子向阴极移动,则电极反应式为
C H+6H++6e-=C H 。
6 6 6 12
③阳极生成2.8mol气体,该气体应该是阳极OH-放电生成的氧气,则转移电子的物质的量=2.8mol×4=
11.2mol。设阴极消耗苯的物质的量是xmol,则同时生成 xmol环戊烷,根据电极反应式C H+6H++
6 6
6e-=C H 可知得到电子是6xmol,根据电子守恒可知,阴极生成氢气是 =5.6mol
6 12
-3xmol,所以 =0.1,解得x=1.2,因此储氢装置的电流效率= ×100%=
64.3%。
26.(2017·江苏高考真题)铝是应用广泛的金属。以铝土矿(主要成分为Al O,含SiO 和Fe O 等杂质)为
2 3 2 2 3
原料制备铝的一种工艺流程如下:
注:SiO 在“碱溶”时转化为铝硅酸钠沉淀。
2
(1)“碱溶”时生成偏铝酸钠的离子方程式为_____________________。(2)向“过滤Ⅰ”所得滤液中加入NaHCO 溶液,溶液的pH_________ (填“增大”、“不变”或“减
3
小”)。
(3)“电解Ⅰ”是电解熔融Al O,电解过程中作阳极的石墨易消耗,原因是___________。
2 3
(4)“电解Ⅱ”是电解NaCO 溶液,原理如图所示。阳极的电极反应式为_____________________,阴
2 3
极产生的物质A的化学式为____________。
【答案】(1)Al O+2OH−=2 +H O (2)减小 (3) 石墨电极被阳极上产生的O 氧化
2 3 2 2
(4)4 +2H O−4e−=4 +O ↑ H
2 2 2
【解析】以铝土矿(主要成分为Al O,含SiO 和Fe O 等杂质)为原料制备铝,由流程可知,加NaOH溶
2 3 2 2 3
解时Fe O 不反应,由信息可知SiO 在“碱溶”时转化为铝硅酸钠沉淀,过滤得到的滤渣为Fe O、铝
2 3 2 2 3
硅酸钠,碳酸氢钠与偏铝酸钠反应生成Al(OH),过滤II得到Al(OH),灼烧生成氧化铝,电解
3 3
I为电解氧化铝生成Al和氧气,电解II为电解NaCO 溶液,结合图可知,阳极上碳酸根离子失去电
2 3
子生成碳酸氢根离子和氧气,阴极上氢离子得到电子生成氢气。
(1)“碱溶”时生成偏铝酸钠的离子方程式为:Al O+2OH-==2AlO -+H O;(2)向“过滤I”所得滤液中
2 3 2 2
加入NaHCO 溶液,与NaAlO 反应生成氢氧化铝沉淀和碳酸钠,碱性为OH->AlO->CO2-,可知
3 2 2 3
溶液的pH减小,NaHCO 中存在化学键有:离子键和共价键;(3)“电解I”是电解熔融Al O,电解
3 2 3
过程中作阳极的石墨易消耗,原因是石墨电极被阳极上产生的O 氧化。(4)由图可知,阳极反应为
2
4CO2-+2H O-4e-═4HCO -+O ↑,阴极上氢离子得到电子生成氢气,则阴极产生的物质A的化学式为
3 2 3 2
H。
2
27.(2011·天津高考真题)工业废水中常含有一定量的 ,它们会对人类及生态系统产生
很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法
该法的工艺流程为
其中第①步存在平衡:
方法2:电解法
该法用Fe做电极电解含Cr O 的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH) 沉
淀。(5)用Fe做电极的原因为 。
(6)在阴极附近溶液pH升高的原因是(用电极反应解释) 。
溶液中同时生成的沉淀还有 。
【答案】
(5)阳极极反应:Fe-2e-=Fe2+,提供还原剂Fe2+
(6)2H++2e-=H ↑,氢氧化铁或Fe(OH)
2 3
【解析】
(5)金属铁做阳极,失电子生成亚铁离子,能够把Cr O2-还原为Cr3+;
2 3
综上所述,本题正确答案:阳极极反应:Fe-2e-=Fe2+,提供还原剂Fe2+。
(6)在阴极,溶液中的氢离子得电子发生还原反应:2H++2e-=H ↑,氢离子浓度减小,阴极附近溶液pH
2
升高; 氢离子浓度减小,氢氧根离子浓度增大,被亚铁离子氧化成的铁离子与氢氧根离子反应生成
氢氧化铁沉淀,
综上所述,本题正确答案:2H++2e-=H ↑,氢氧化铁或Fe(OH) 。
2 3
28.(2010·全国高考真题)右图是一个用铂丝作电极,电解稀的MgSO 溶液的装置,电解液中加有中性
4
红指示剂,此时溶液呈红色。(指示剂的pH变色范围:6.8~8.0,酸色—红色,碱色—黄色)
回答下列问题:
(1)下列关于电解过程中电极附近溶液颜色变化的叙述正确的是________(填编号);
①A管溶液由红变黄;②B管溶液由红变黄;
③A管溶液不变色;④B管溶液不变色;
(2)写出A管中发生反应的反应式:_________________________________;
(3)写出B管中发生反应的反应式:_________________________________;
(4)检验a管中气体的方法是_______________________________________;
(5)检验b管中气体的方法是____________________________________________;
(6)电解一段时间后,切断电源,将电解液倒入烧杯内观察到的现象是_____________________。
【答案】(1)①④ (2)2H++2e-=H ↑(或2HO+2e-=2OH-+H ↑)、Mg2++2OH-=Mg(OH)↓ (3)
2 2 2 2
4OH- -4e- =O ↑+2H O (或2HO-4e- =O ↑+4H+) (4)用拇指按住管口,取出试管,靠近火焰,放
2 2 2 2
开拇指,有爆鸣声,管口有蓝色火焰 (5)用拇指按住管口,取出试管,放开拇指,将带有火星
的木条伸入试管内会复燃 (6)溶液呈红色,白色沉淀溶解(或大部分溶解)
【解析】
(1)由装置图可知A为电解池的阴极,电极反应为:4H++4e-=2H ↑;B为电解池的阳极,电极反应为:
24OH--4e-=2H O+O↑。根据放电情况可知A管由于H+放电,A管中溶液显碱性,溶液由红变黄,同时
2 2
还会发生反应Mg2++2OH-=Mg(OH) ↓;B管由于OH-放电,B管中溶液显酸性,溶液不变色;答案选
2
①④。
(2)A管中发生的反应有:2H++2e-=H ↑(或2HO+2e-=2OH-+H ↑)、Mg2++2OH-=Mg(OH)↓。
2 2 2 2
(3)B管中发生的反应有:4OH- -4e- =O ↑+2H O (或2HO-4e- =O ↑+4H+)。
2 2 2 2
(4)a管中为H,检验H 时利用其可燃性,方法是:用拇指按住管口,取出试管,靠近火焰,放开拇指,
2 2
有爆鸣声,管口有蓝色火焰。
(5)b管中为O,检验O 时利用其能使带火星的木条复燃的性质进行检验,方法是:用拇指按住管口,
2 2
取出试管,放开拇指,将带有火星的木条伸入试管内会复燃。
(6)由于该电解反应的实质是电解水,所以将电解液倒入烧杯后,整个溶液呈中性,故溶液呈红色,
Mg(OH) 沉淀会溶解。
2
29.(2014·北京高考真题)(15分)用FeCl 酸性溶液脱除HS后的废液,通过控制电压电解得以再生。
3 2
某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/LFeCl 溶液,研究废液再生机理。记
2
录如下(a、b、c代表电压值:)
序号 电压/V 阳极现象 检验阳极产物
I x≥a 电极附近出现黄色,有气泡产 有Fe3+、有Cl
2
生
II a>x≥b 电极附近出现黄色,无气泡产 有Fe3+、无Cl
2
生
III b>x>0 无明显变化 无Fe3+、无Cl
2
(1)用KSCN溶液检验出Fe3+的现象是_______。
(2)I中,Fe2+产生的原因可能是Cl-在阳极放电,生成的Cl 将Fe2+氧化。写出有关反应的方程式_____。
2
(3)由II推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有_____性。
(4)II中虽未检测出Cl,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记
2
录如下:
序号 电压/V 阳极现象 检验阳极产物
IV a>x≥c 无明显变化 有Cl
2
V c>x≥b 无明显变化 无Cl
2
①NaCl溶液的浓度是________mol/L。
②IV中检测Cl 的实验方法:____________________。
2
③与II对比,得出的结论(写出两点):___________________。
【答案】(1)溶液变为血红色(2)2Cl--2e-=Cl↑;2Fe2++Cl=2Fe3++2Cl-;
2 2
(3)还原
(4)①0.2②取少量阳极附近的溶液,滴在淀粉KI试纸上,试纸变蓝
③通过控制电压,证实了产生Fe3+的两种原因都成立;通过控制电压,验证了Fe2+先于Cl-放电
【解析】
(1)铁离子与KSCN反应生成血红色络合物,故现象为溶液变为血红色;
(2)Cl-在阳极放电,电解反应式为2Cl--2e-=Cl↑,生成的氯气氧化Fe2+为Fe3+,方程式为:2Fe2+
2
+Cl=2Fe3++2Cl-;
2
(3)因为阳极产物无Cl,又Fe2+具有还原性,故也可能是Fe2+在阳极放电,被氧化为Fe3+;
2
(4)①因为为对比实验,l-浓度应与电解FeCl 的相同,即为0.1mol/L ×2=0.2mol/L;
2
②检测氯气可以用淀粉碘化钾试纸,可取少量阳极附近的溶液,滴在淀粉KI试纸上,若试纸变蓝色,则
说明有氯气存在;
③与II对比可知,IV中电解氯化亚铁时,电压较大a>x≥c时,氯离子放电产生氯气,即说明Fe3+可能是
由氯气氧化亚铁离子得到;电压较小c>x≥b时,氯离子不放电,即还原性Fe2+>Cl-,同时也说明了铁
离子也可能是由亚铁离子直接放电得到的。故结论为:①通过控制电压,证实了产生Fe3+的两种原因
都成立;②通过控制电压,验证了Fe2+先于Cl-放电。