文档内容
2023-2024 学年春学期期初学情调研试卷
高三化学
命题人: 复核人:
注意事项:
1.本试卷分为选择题和非选择题两部分,共100分,考试时间75分钟。
2.将选择题的答案填涂在答题卡的对应位置上,非选择题的答案写在答题卡的指定栏目
内。
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Na—23 S—32
Mn—55 Fe—56 Co—59
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.2024年是中国芯片产业突围之年。下列属于芯片中常用半导体材料的是( )
A.石墨 B.聚乙烯 C.镁铝合金 D.晶体硅
2.反应 应用于石油开采。下列说法正确的是( )
A.基态N原子的轨道表示式为
B. 的结构示意图 为
C. 中N原子杂化类型为
D. 的空间填充模型 为
3. 实验室制备水合肼( )溶液的反应原理为 ,
能与 剧烈反应。下列装置和操作能达到实验目的的是( )
A. 用装置 甲制取
学科网(北京)股份有限公司B. 用装置乙制备 溶液
C. 用装置丙制备水合肼溶液
D. 用装置丁分离水合肼和 混合溶液
4. 可用于除去某些重金属离子。下列说法正确的是( )
A.电负性: B.离子半径:
C.电离能: D.热稳定性:
阅读下列材料,完成5~8题。
铁元素的常见价态有+2、+3价,实验室可用赤血盐(K [Fe(CN) ])溶液检验Fe2+,黄血盐(K [Fe(CN) ])溶
3 6 4 6
液检验Fe3+。Fe O 是重要的化工原料,Au/Fe O 可用作反应CO(g)+HO(g)===CO (g)+H(g)的催化剂。
2 3 2 3 2 2 2
硫铁矿烧渣中含有大量Fe O,工业上常用于制取绿矾(FeSO ·7H O)。
2 3 4 2
5. 下列有关铁及其化合物的说法正确的是 ( )
A. Fe元素位于周期表的第ⅥB族
B. 绿矾中Fe2+核外有6个未成对电子
C. 赤血盐是含有配位键的离子化合物
D. 若黄血盐受热分解产物之一的晶胞结构如右图所示,则其化学式为Fe C
4 3
6. 在指定条件下,下列有关铁单质的转化不能实现的是 ( )
A. Fe(s)――→FeCl (s) B. Fe(s)――→Fe O(s)
3 2 3
C. Fe(s)――→Fe(NO ) aq) D. Fe(s)――→FeSO (aq)
3 3( 4
7. 对于反应CO(g)+HO(g)===CO (g)+H(g),下列有关说法不正确的是 ( )
2 2 2
A. 加入催化剂Au/Fe O,反应的焓变ΔH不变
2 3
B. 升高温度,反应体系的活化分子百分数增多
C. 向固定容积的反应体系中充入氦气,反应速率加快
D. 其他条件相同,增大,反应的平衡常数K不变
8. 由硫铁矿烧渣(主要含Fe O、Al O、SiO)制取绿矾的流程如下:
2 3 2 3 2
下列有关说法不正确的是 ( )
A. “酸溶”时先将烧渣粉碎并不断搅拌,可提高铁元素的浸出率
学科网(北京)股份有限公司B. “反应”时发生的主要反应为2Fe3++Fe===3Fe2+
C. “检验”时可用K[Fe(CN) ]溶液检验上一步“反应”是否进行完全
4 6
D. 将第二次“过滤”所得滤液加热,经蒸发结晶可以制得绿矾
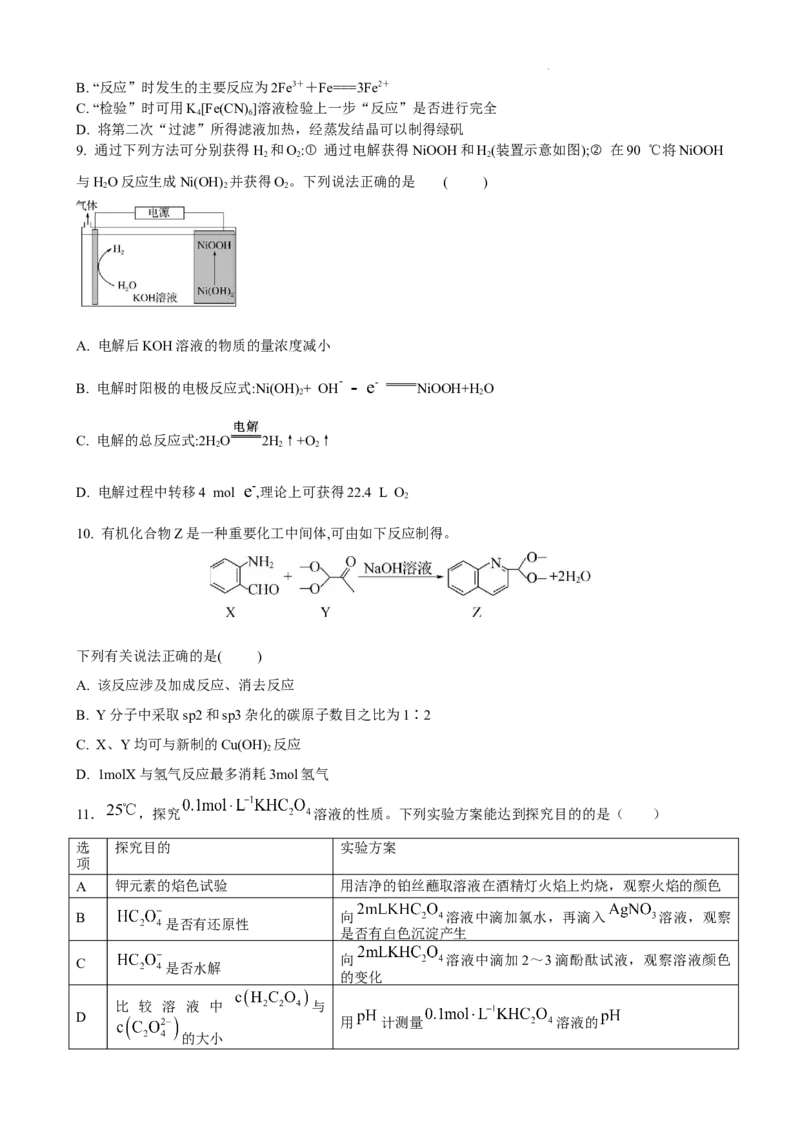
9. 通过下列方法可分别获得H 和O:① 通过电解获得NiOOH和H(装置示意如图);② 在90 ℃将NiOOH
2 2 2
与HO反应生成Ni(OH) 并获得O。下列说法正确的是 ( )
2 2 2
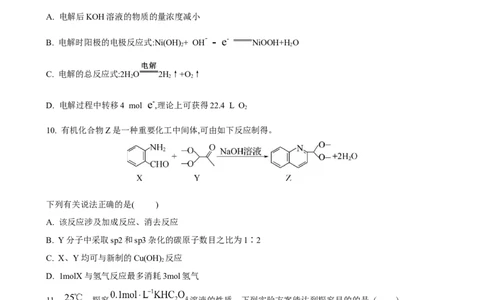
A. 电解后KOH溶液的物质的量浓度减小
B. 电解时阳极的电极反应式:Ni(OH) + OH - - e- NiOOH+H O
2 2
C. 电解的总反应式:2H O 2H↑+O ↑
2 2 2
D. 电解过程中转移4 mol e- ,理论上可获得22.4 L O
2
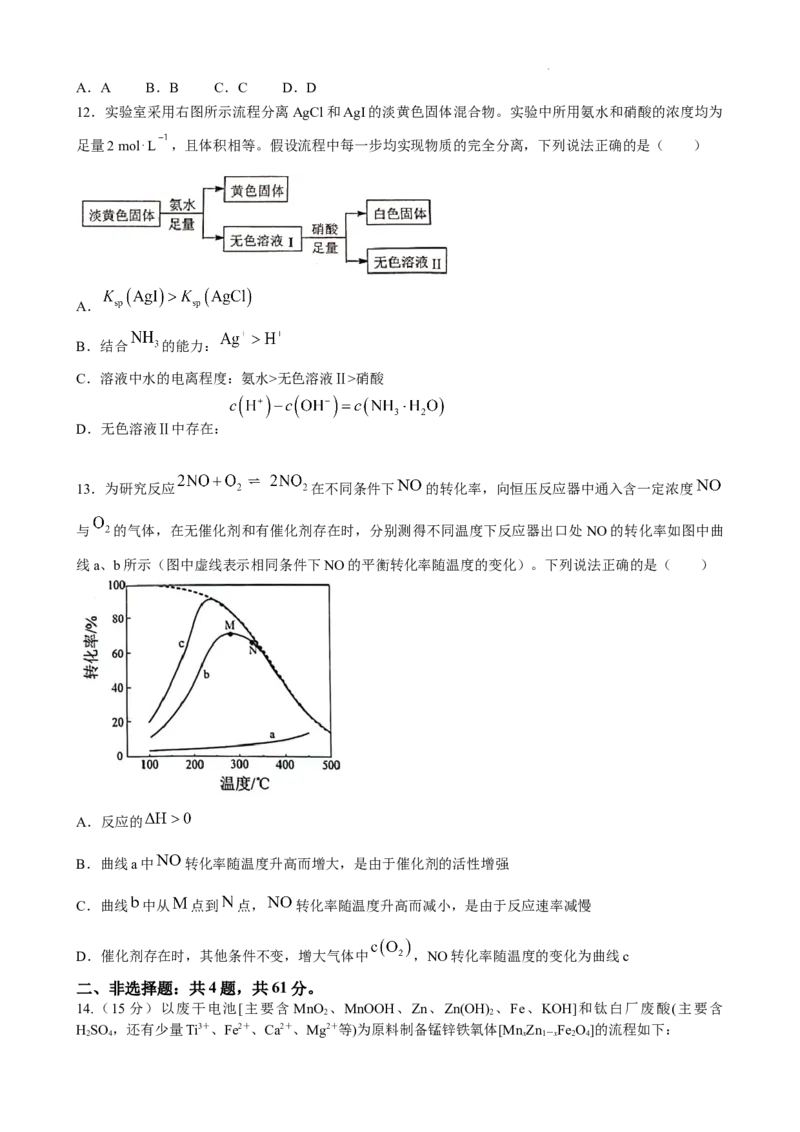
10. 有机化合物Z是一种重要化工中间体,可由如下反应制得。
下列有关说法正确的是( )
A. 该反应涉及加成反应、消去反应
B. Y分子中采取sp2和sp3杂化的碳原子数目之比为1∶2
C. X、Y均可与新制的Cu(OH) 反应
2
D. 1molX与氢气反应最多消耗3mol氢气
11. ,探究 溶液的性质。下列实验方案能达到探究目的的是( )
选 探究目的 实验方案
项
A 钾元素的焰色试验 用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色
B 向 溶液中滴加氯水,再滴入 溶液,观察
是否有还原性
是否有白色沉淀产生
C 是否水解
向 溶液中滴加2~3滴酚酞试液,观察溶液颜色
的变化
比 较 溶 液 中 与
D
用 计测量 溶液的
的大小
学科网(北京)股份有限公司A.A B.B C.C D.D
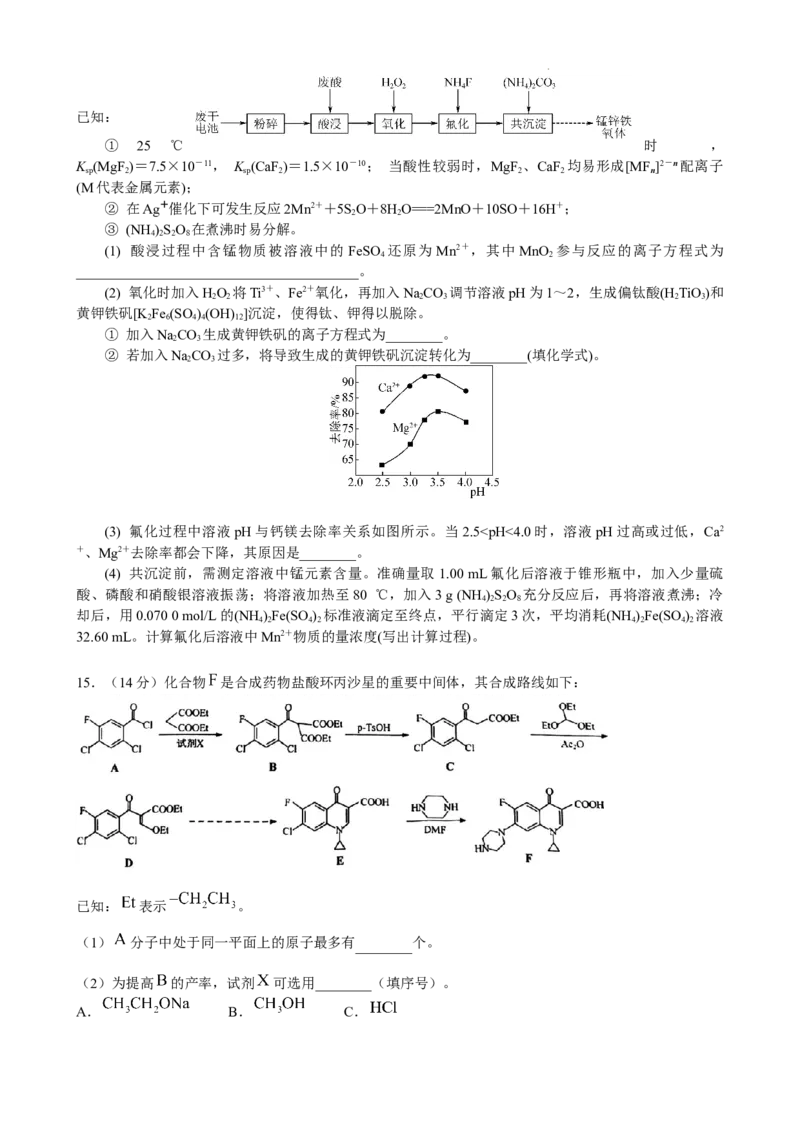
12.实验室采用右图所示流程分离AgCl和AgI的淡黄色固体混合物。实验中所用氨水和硝酸的浓度均为
足量2 mol⋅L ,且体积相等。假设流程中每一步均实现物质的完全分离,下列说法正确的是( )
A.
B.结合 的能力:
C.溶液中水的电离程度:氨水>无色溶液Ⅱ>硝酸
D.无色溶液Ⅱ中存在:
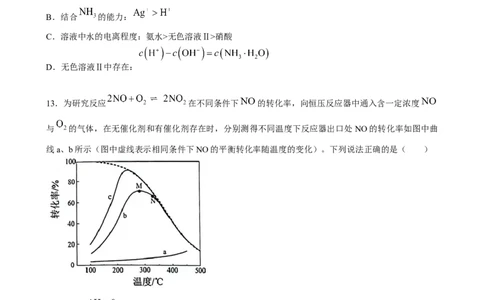
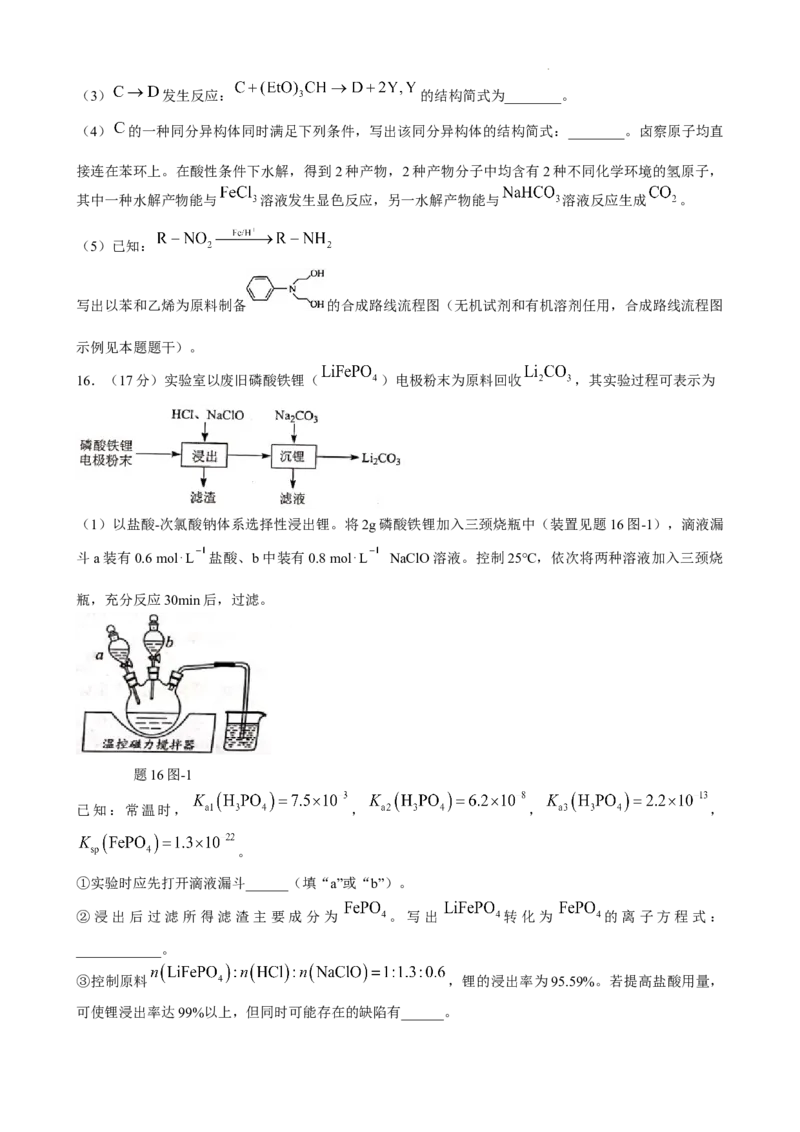
13.为研究反应 在不同条件下 的转化率,向恒压反应器中通入含一定浓度
与 的气体,在无催化剂和有催化剂存在时,分别测得不同温度下反应器出口处NO的转化率如图中曲
线a、b所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是( )
A.反应的
B.曲线a中 转化率随温度升高而增大,是由于催化剂的活性增强
C.曲线 中从 点到 点, 转化率随温度升高而减小,是由于反应速率减慢
D.催化剂存在时,其他条件不变,增大气体中 ,NO转化率随温度的变化为曲线c
二、非选择题:共4题,共61分。
14.(15 分)以废干电池[主要含 MnO 、MnOOH、Zn、Zn(OH) 、Fe、KOH]和钛白厂废酸(主要含
2 2
HSO ,还有少量Ti3+、Fe2+、Ca2+、Mg2+等)为原料制备锰锌铁氧体[MnZn Fe O]的流程如下:
2 4 x 1-x 2 4
学科网(北京)股份有限公司已知:
① 25 ℃ 时 ,
K (MgF )=7.5×10-11, K (CaF )=1.5×10-10; 当酸性较弱时,MgF 、CaF 均易形成[MF ]2-n配离子
sp 2 sp 2 2 2 n
(M代表金属元素);
② 在Ag+催化下可发生反应2Mn2++5SO+8HO===2MnO+10SO+16H+;
2 2
③ (NH )SO 在煮沸时易分解。
4 2 2 8
(1) 酸浸过程中含锰物质被溶液中的 FeSO 还原为 Mn2+,其中 MnO 参与反应的离子方程式为
4 2
________________________________________。
(2) 氧化时加入HO 将Ti3+、Fe2+氧化,再加入NaCO 调节溶液pH为1~2,生成偏钛酸(H TiO)和
2 2 2 3 2 3
黄钾铁矾[K Fe (SO )(OH) ]沉淀,使得钛、钾得以脱除。
2 6 4 4 12
① 加入NaCO 生成黄钾铁矾的离子方程式为________。
2 3
② 若加入NaCO 过多,将导致生成的黄钾铁矾沉淀转化为________(填化学式)。
2 3
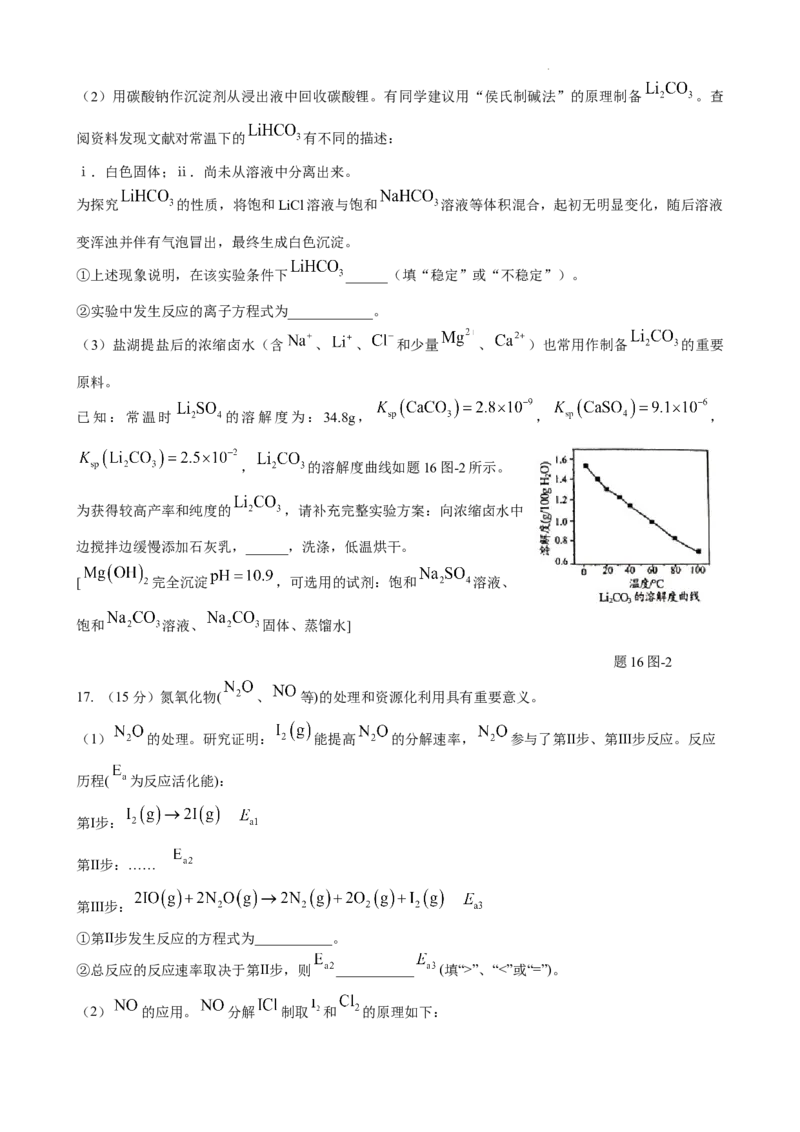
(3) 氟化过程中溶液pH与钙镁去除率关系如图所示。当 2.5”、“<”或“=”)。
(2) 的应用。 分解 制取 和 的原理如下:
学科网(北京)股份有限公司反应Ⅰ:
反应Ⅱ:
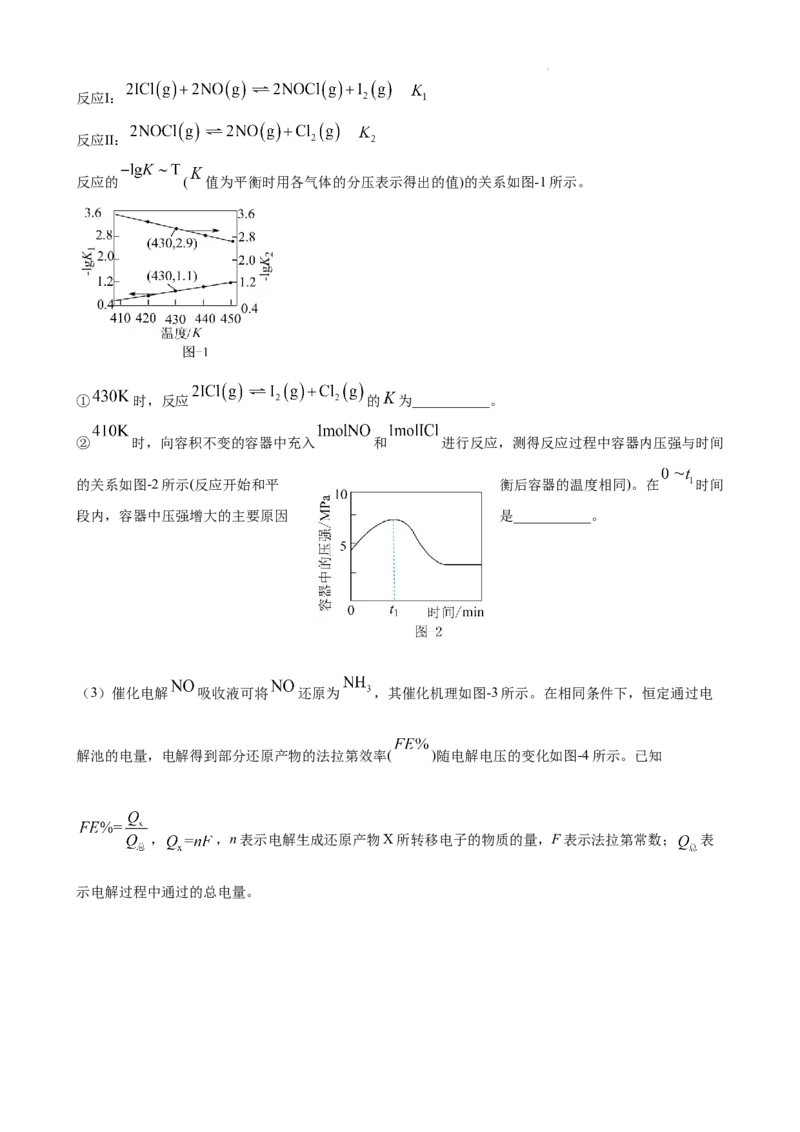
反应的 ( 值为平衡时用各气体的分压表示得出的值)的关系如图-1所示。
① 时,反应 的 为___________。
② 时,向容积不变的容器中充入 和 进行反应,测得反应过程中容器内压强与时间
的关系如图-2所示(反应开始和平 衡后容器的温度相同)。在 时间
段内,容器中压强增大的主要原因 是___________。
(3)催化电解 吸收液可将 还原为 ,其催化机理如图-3所示。在相同条件下,恒定通过电
解池的电量,电解得到部分还原产物的法拉第效率( )随电解电压的变化如图-4所示。已知
, ,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数; 表
示电解过程中通过的总电量。
学科网(北京)股份有限公司①当电解电压为 时,电解生成的 和 的物质的量之比为___________。
②当电解电压为 时,催化电解 生成 的电极反应式为___________。
③电解电压大于 后,随着电解电压的不断增大, 的法拉第效率迅速增大,可能原因是
___________(吸附在催化剂上的物种加“*”表示,如 、 等)。
学科网(北京)股份有限公司