文档内容
绝密★启用前
山东中学联盟 2024 届高三考前模拟冲刺大联考
化 学
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2.选择题的作答:选出每小题答案后,用 2B铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: H1 C12 N14 O16 Ti48 Rb85 Sr88 Rh 103 Ir 192
一、选择题:本题共10小题,每小题2分。共20分。每小题只有一个选项符合题目要求。
1.化学与生活密切相关.下列说法错误的是
A.还原铁粉用作食品脱氧剂后,转化成Fe₃O₄
B.氯乙烷具有冷冻麻醉作用,对损伤处有镇痛效果
C.在新买的汽车中可放入活性炭,可吸附甲醛
D.乙二醇可用作汽车防冻液的主要成分
2.下列实验操作或实验仪器使用错误的是
A.分液漏斗使用前需要检查两处是否漏水
B. 可用pH试纸检验NaClO溶液中 ClO-发生水解
C.灼烧海带时,不能用坩埚钳夹持坩埚直接加热
D. 托盘天平称取10.4gNaOH时, 看盘上放10g砝码并拨动游码至 0.4g处
3.下列关于物质的结构与性质描述错误的是
A.CS₂为直线形分子,在苯中溶解度大于水中的
B.基态原子的第二电离能,O高于N和F的
C.苯甲醇分子中,碳原子与氧原子间的共价键类型为sp3-pσ键
D.晶体硅的熔点、硬度均低于金刚石
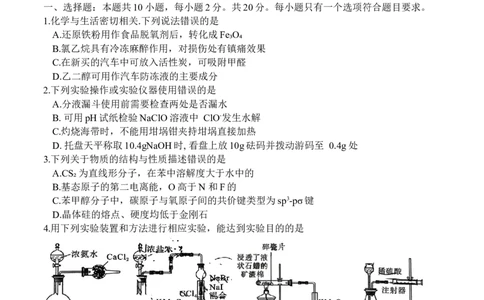
4.用下列实验装置和方法进行相应实验,能达到实验目的的是
A.用装置甲制备干燥的氨·
B.用装置乙证明氧化性; Cl₂-I₂、Br₂>I₂
C.用装置丙证明石蜡含不饱和烃
D.利用装置丁测量化学反应速率
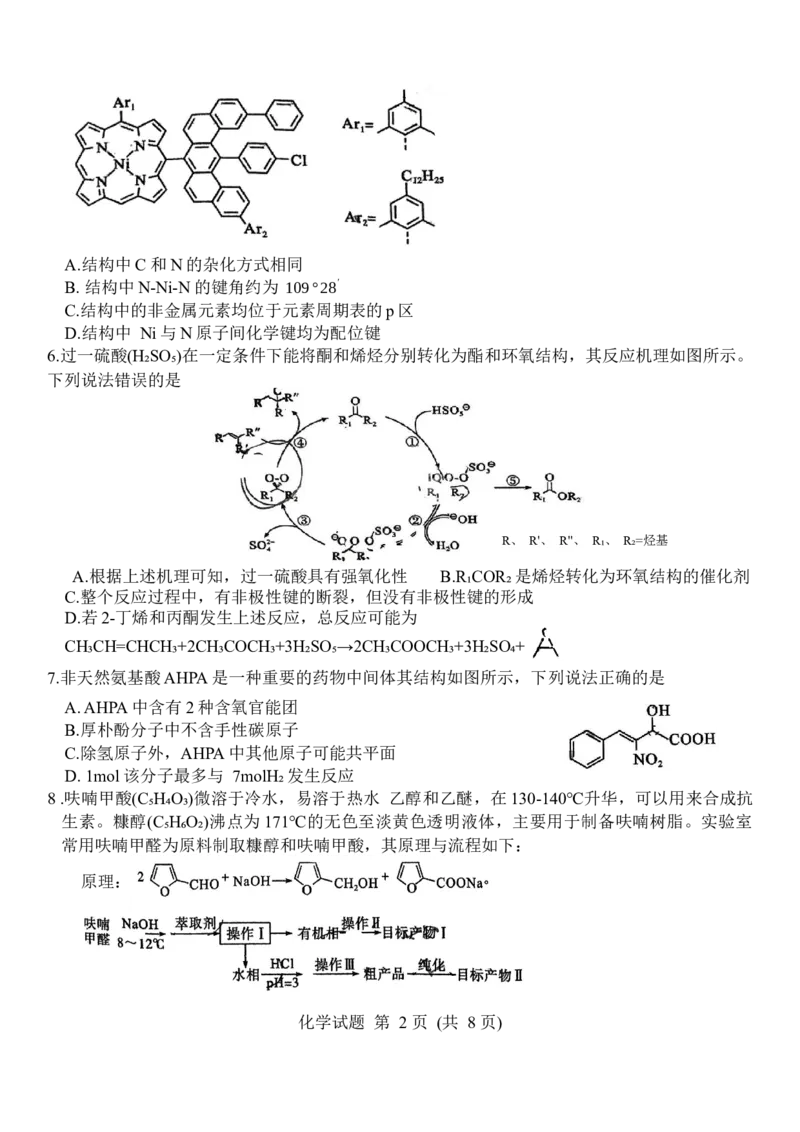
5.金属卟啉稠合石墨烯纳米带为平面带状结构,具有高电导率、高热导率和低噪声等优良性能,
有望成为微纳集成电路的互连材料。Ni的卟啉稠合石墨烯结构如图所示,下列说法正确的是
化学试题 第 1 页 (共 8 页)A.结构中C 和N的杂化方式相同
B. 结构中N-Ni-N 的键角约为 109°28'
C.结构中的非金属元素均位于元素周期表的p区
D.结构中 Ni与N原子间化学键均为配位键
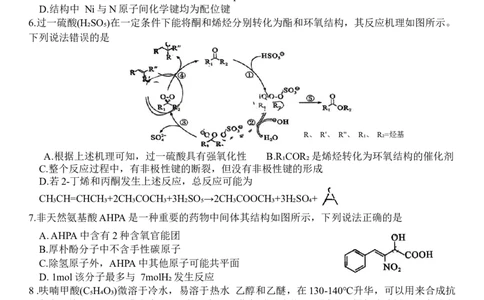
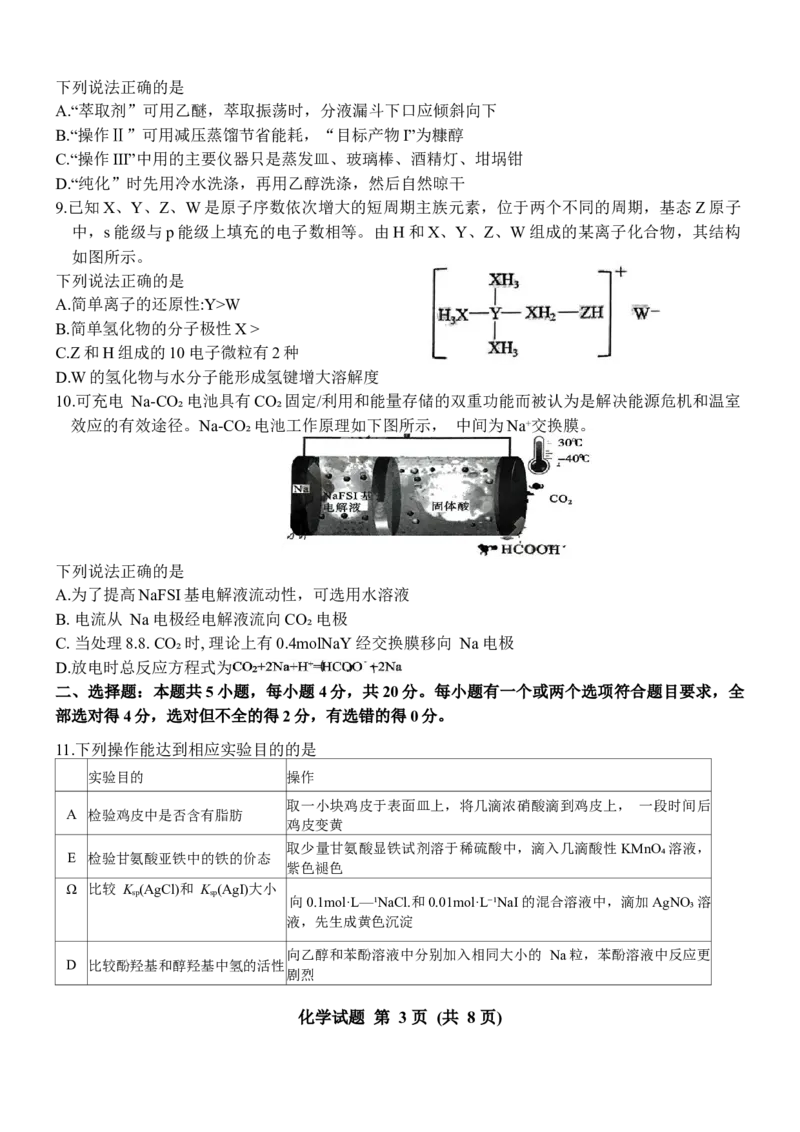
6.过一硫酸(H₂SO₅)在一定条件下能将酮和烯烃分别转化为酯和环氧结构,其反应机理如图所示。
下列说法错误的是
R、 R'、 R"、 R₁、 R₂=烃基
A.根据上述机理可知,过一硫酸具有强氧化性 B.R₁COR₂是烯烃转化为环氧结构的催化剂
C.整个反应过程中,有非极性键的断裂,但没有非极性键的形成
D.若2-丁烯和丙酮发生上述反应,总反应可能为
CH₃CH=CHCH₃+2CH₃COCH₃+3H₂SO₅→2CH₃COOCH₃+3H₂SO₄+
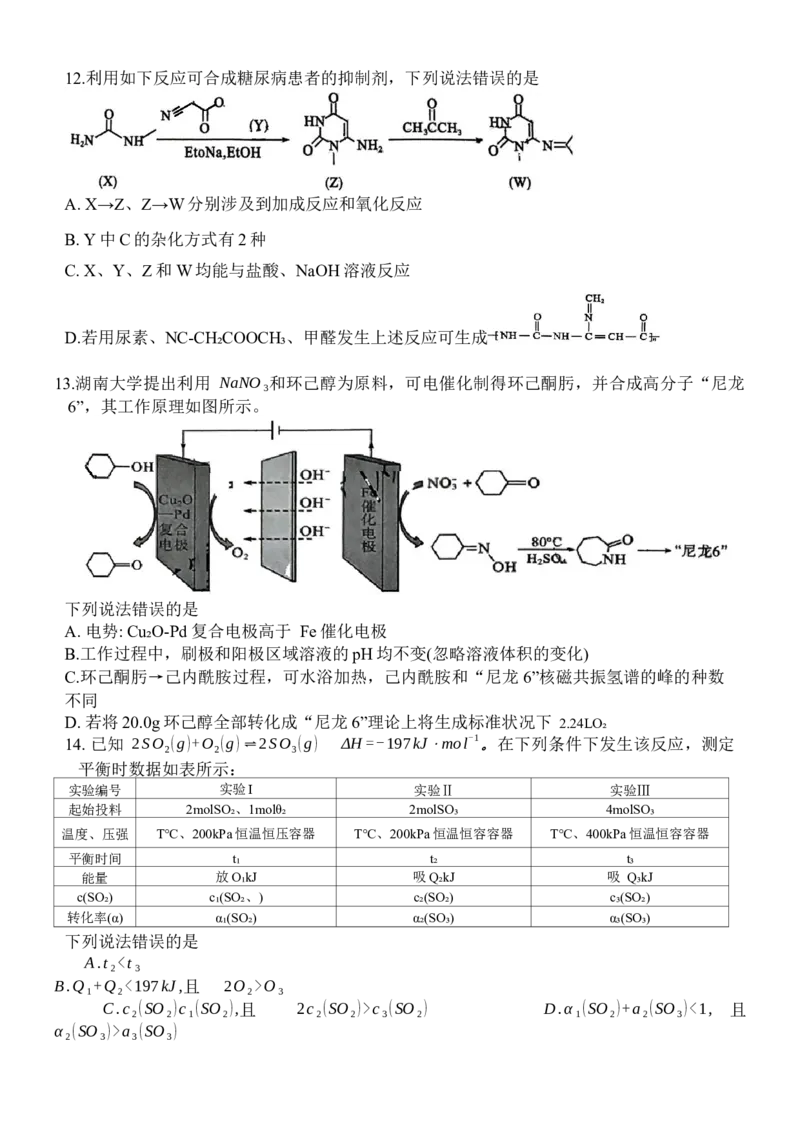
7.非天然氨基酸AHPA是一种重要的药物中间体其结构如图所示,下列说法正确的是
A. AHPA 中含有2种含氧官能团
B.厚朴酚分子中不含手性碳原子
C.除氢原子外,AHPA中其他原子可能共平面
D. 1mol该分子最多与 7molH₂发生反应
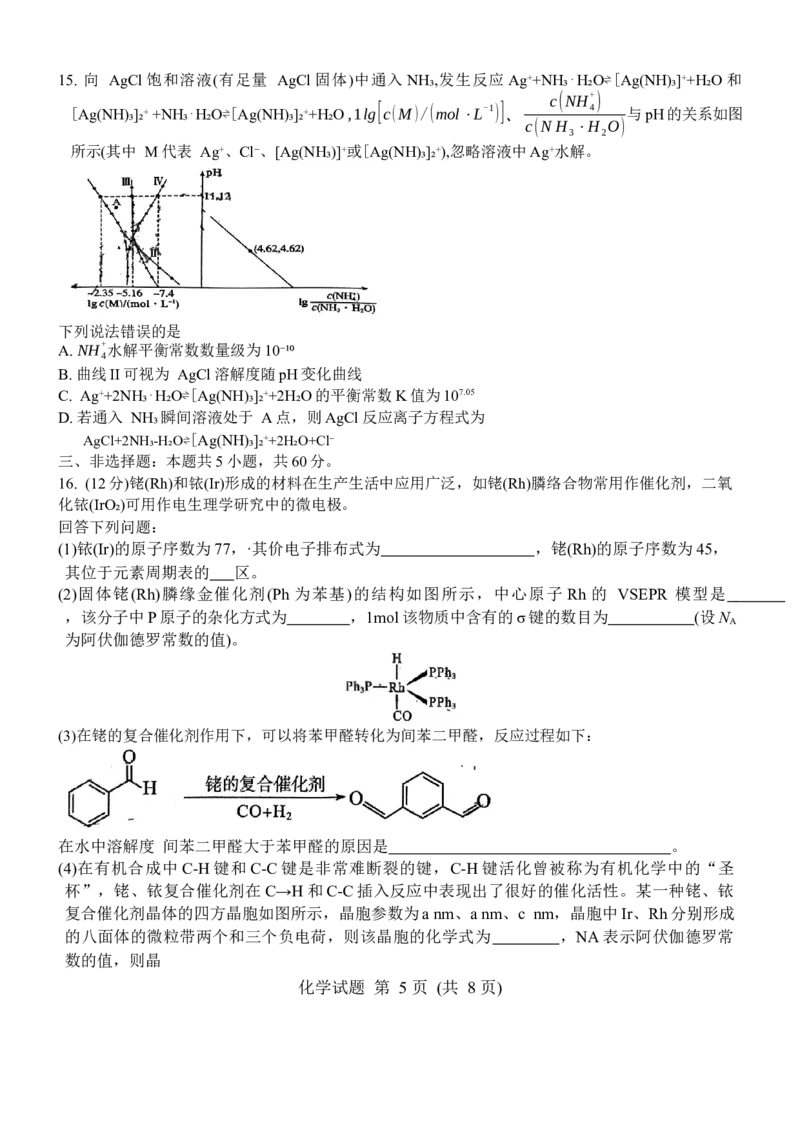
8 .呋喃甲酸(C₅H₄O₃)微溶于冷水,易溶于热水 乙醇和乙醚,在130-140℃升华,可以用来合成抗
生素。糠醇(C₅H₆O₂)沸点为171℃的无色至淡黄色透明液体,主要用于制备呋喃树脂。实验室
常用呋喃甲醛为原料制取糠醇和呋喃甲酸,其原理与流程如下:
原理:
化学试题 第 2 页 (共 8 页)下列说法正确的是
A.“萃取剂”可用乙醚,萃取振荡时,分液漏斗下口应倾斜向下
B.“操作Ⅱ”可用减压蒸馏节省能耗,“目标产物I”为糠醇
C.“操作III”中用的主要仪器只是蒸发皿、玻璃棒、酒精灯、坩埚钳
D.“纯化”时先用冷水洗涤,再用乙醇洗涤,然后自然晾干
9.已知X、Y、Z、W是原子序数依次增大的短周期主族元素,位于两个不同的周期,基态Z原子
中,s能级与p能级上填充的电子数相等。由H和X、Y、Z、W组成的某离子化合物,其结构
如图所示。
下列说法正确的是
A.简单离子的还原性:Y>W
B.简单氢化物的分子极性X >
C.Z和H组成的10电子微粒有2种
D.W的氢化物与水分子能形成氢键增大溶解度
10.可充电 Na-CO₂电池具有CO₂固定/利用和能量存储的双重功能而被认为是解决能源危机和温室
效应的有效途径。Na-CO₂电池工作原理如下图所示, 中间为Na⁺交换膜。
下列说法正确的是
A.为了提高NaFSI基电解液流动性,可选用水溶液
B. 电流从 Na电极经电解液流向CO₂电极
C. 当处理8.8. CO₂时, 理论上有0.4molNaY经交换膜移向 Na电极
D.放电时总反应方程式为
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全
部选对得4分,选对但不全的得2分,有选错的得0分。
11.下列操作能达到相应实验目的的是
实验目的 操作
取一小块鸡皮于表面皿上,将几滴浓硝酸滴到鸡皮上, 一段时间后
A 检验鸡皮中是否含有脂肪
鸡皮变黄
取少量甘氨酸显铁试剂溶于稀硫酸中,滴入几滴酸性KMnO₄溶液,
E 检验甘氨酸亚铁中的铁的价态
紫色褪色
Ω 比较 K (AgCl)和 K (AgI)大小
sp sp
向0.1mol·L—¹NaCl.和0.01mol·L⁻¹NaI的混合溶液中,滴加AgNO₃溶
液,先生成黄色沉淀
向乙醇和苯酚溶液中分别加入相同大小的 Na粒,苯酚溶液中反应更
D 比较酚羟基和醇羟基中氢的活性
剧烈
化学试题 第 3 页 (共 8 页)12.利用如下反应可合成糖尿病患者的抑制剂,下列说法错误的是
A. X→Z、Z→W分别涉及到加成反应和氧化反应
B. Y中C的杂化方式有2种
C. X、Y、Z和W均能与盐酸、NaOH溶液反应
D.若用尿素、NC-CH₂COOCH₃、甲醛发生上述反应可生成
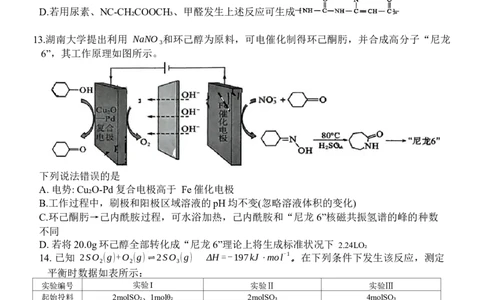
13.湖南大学提出利用 NaNO₃和环己醇为原料,可电催化制得环己酮肟,并合成高分子“尼龙
6”,其工作原理如图所示。
下列说法错误的是
A. 电势: Cu₂O-Pd复合电极高于 Fe催化电极
B.工作过程中,刷极和阳极区域溶液的pH均不变(忽略溶液体积的变化)
C.环己酮肟→己内酰胺过程,可水浴加热,己内酰胺和“尼龙 6”核磁共振氢谱的峰的种数
不同
D. 若将20.0g环己醇全部转化成“尼龙6”理论上将生成标准状况下 2.24LO₂
14. 已知 2SO (g)+O (g)⇌2SO (g) ΔH=-197kJ⋅mol-1。在下列条件下发生该反应,测定
2 2 3
平衡时数据如表所示:
实验编号 实验I 实验Ⅱ 实验Ⅲ
起始投料 2molSO₂、1molθ₂ 2molSO₃ 4molSO₃
温度、压强 T℃、200kPa恒温恒压容器 T℃、200kPa恒温恒容容器 T℃、400kPa恒温恒容容器
平衡时间 t₁ t₂ t₃
能量 放O₁kJ 吸Q₂kJ 吸 Q₃kJ
c(SO₂) c₁(SO₂、) c₂(SO₂) c₃(SO₂)
转化率(α) α₁(SO₂) α₂(SO₃) α₃(SO₃)
下列说法错误的是
A.t₂O₃
C.c₂(SO₂)c₁(SO₂),且 2c₂(SO₂)>c₃(SO₂) D.α₁(SO₂)+a₂(SO₃)<1, 且
α₂(SO₃)>a₃(SO₃)化学试题 第 4 页 (共 8 页)15. 向 AgCl 饱和溶液(有足量 AgCl 固体)中通入 NH₃,发生反应 Ag⁺+NH₃⋅H₂O⇌[Ag(NH)₃]⁺+H₂O 和
c(NH+)
[Ag(NH)₃]₂⁺ +NH₃⋅H₂O⇌[Ag(NH)₃]₂⁺+H₂O ,1lg[c(M)/(mol⋅L-1)]、 4 与pH的关系如图
c(N H ⋅H O)
3 2
所示(其中 M代表 Ag⁺、Cl⁻、[Ag(NH₃)]⁺或[Ag(NH)₃]₂⁺),忽略溶液中Ag⁺水解。
下列说法错误的是
A.
NH+水解平衡常数数量级为10⁻¹⁰
4
B. 曲线II可视为 AgCl溶解度随pH变化曲线
C. Ag⁺+2NH₃⋅H₂O⇌[Ag(NH)₃]₂⁺+2H₂O的平衡常数K值为107.05
D. 若通入 NH₃瞬间溶液处于 A点,则AgCl反应离子方程式为
AgCl+2NH₃-H₂O⇌[Ag(NH)₃]₂⁺+2H₂O+Cl⁻
三、非选择题:本题共5小题,共60分。
16. (12分)铑(Rh)和铱(Ir)形成的材料在生产生活中应用广泛,如铑(Rh)膦络合物常用作催化剂,二氧
化铱(IrO₂)可用作电生理学研究中的微电极。
回答下列问题:
(1)铱(Ir)的原子序数为77,·其价电子排布式为 ,铑(Rh)的原子序数为45,
其位于元素周期表的 区。
(2)固体铑(Rh)膦缘金催化剂(Ph 为苯基)的结构如图所示,中心原子 Rh 的 VSEPR 模型是
,该分子中P原子的杂化方式为 ,1mol该物质中含有的σ键的数目为 (设N
A
为阿伏伽德罗常数的值)。
(3)在铑的复合催化剂作用下,可以将苯甲醛转化为间苯二甲醛,反应过程如下:
在水中溶解度 间苯二甲醛大于苯甲醛的原因是 。
(4)在有机合成中C-H键和C-C键是非常难断裂的键,C-H键活化曾被称为有机化学中的“圣
杯”,铑、铱复合催化剂在C→H和C-C插入反应中表现出了很好的催化活性。某一种铑、铱
复合催化剂晶体的四方晶胞如图所示,晶胞参数为a nm、a nm、c nm,晶胞中Ir、Rh分别形成
的八面体的微粒带两个和三个负电荷,则该晶胞的化学式为 ,NA表示阿伏伽德罗常
数的值,则晶
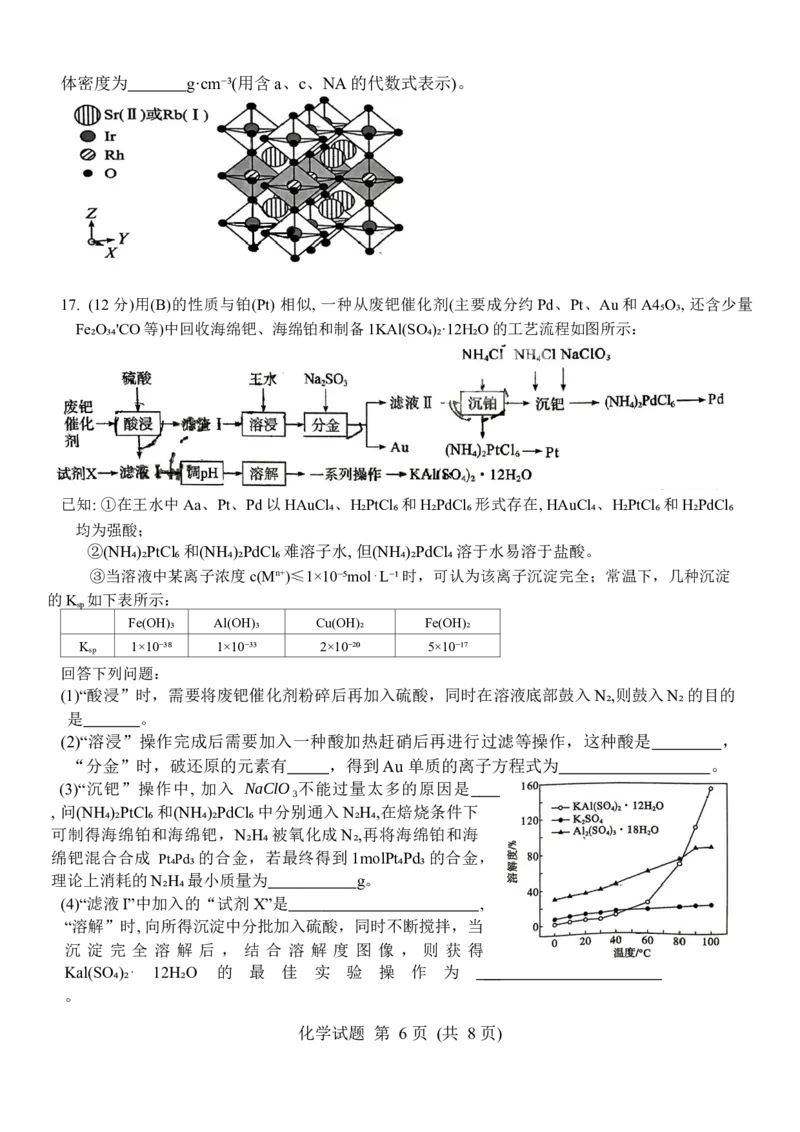
化学试题 第 5 页 (共 8 页)体密度为 g·cm⁻³(用含a、c、NA的代数式表示)。
17. (12分)用(B)的性质与铂(Pt) 相似, 一种从废钯催化剂(主要成分约Pd、Pt、Au和A4₅O₃, 还含少量
Fe₂O₃₄'CO等)中回收海绵钯、海绵铂和制备1KAl(SO₄)₂·12H₂O的工艺流程如图所示:
已知: ①在王水中Aa、Pt、Pd以HAuCl₄、H₂PtCl₆和H₂PdCl₆形式存在, HAuCl₄、H₂PtCl₆和H₂PdCl₆
均为强酸;
②(NH₄)₂PtCl₆和(NH₄)₂PdCl₆难溶子水, 但(NH₄)₂PdCl₄溶于水易溶于盐酸。
③当溶液中某离子浓度c(Mn+)≤1×10⁻⁵mol⋅L⁻¹时,可认为该离子沉淀完全;常温下,几种沉淀
的K 如下表所示:
sp
Fe(OH)₃ Al(OH)₃ Cu(OH)₂ Fe(OH)₂
K 1×10⁻³⁸ 1×10⁻³³ 2×10⁻²⁰ 5×10⁻¹⁷
sp
回答下列问题:
(1)“酸浸”时,需要将废钯催化剂粉碎后再加入硫酸,同时在溶液底部鼓入N₂,则鼓入N₂的目的
是 。
(2)“溶浸”操作完成后需要加入一种酸加热赶硝后再进行过滤等操作,这种酸是 ,
“分金”时,破还原的元素有 ,得到Au 单质的离子方程式为 。
(3)“沉钯”操作中, 加入 NaClO₃不能过量太多的原因是
, 问(NH₄)₂PtCl₆和(NH₄)₂PdCl₆中分别通入N₂H₄,在焙烧条件下
可制得海绵铂和海绵钯,N₂H₄被氧化成N₂,再将海绵铂和海
绵钯混合合成 Pt₄Pd₃的合金,若最终得到1molPt₄Pd₃的合金,
理论上消耗的N₂H₄最小质量为 g。
(4)“滤液I”中加入的“试剂X”是 ,
“溶解”时, 向所得沉淀中分批加入硫酸,同时不断搅拌,当
沉 淀 完 全 溶 解 后 , 结 合 溶 解 度 图 像 , 则 获 得
Kal(SO₄)₂⋅ 12H₂O 的 最 佳 实 验 操 作 为
。
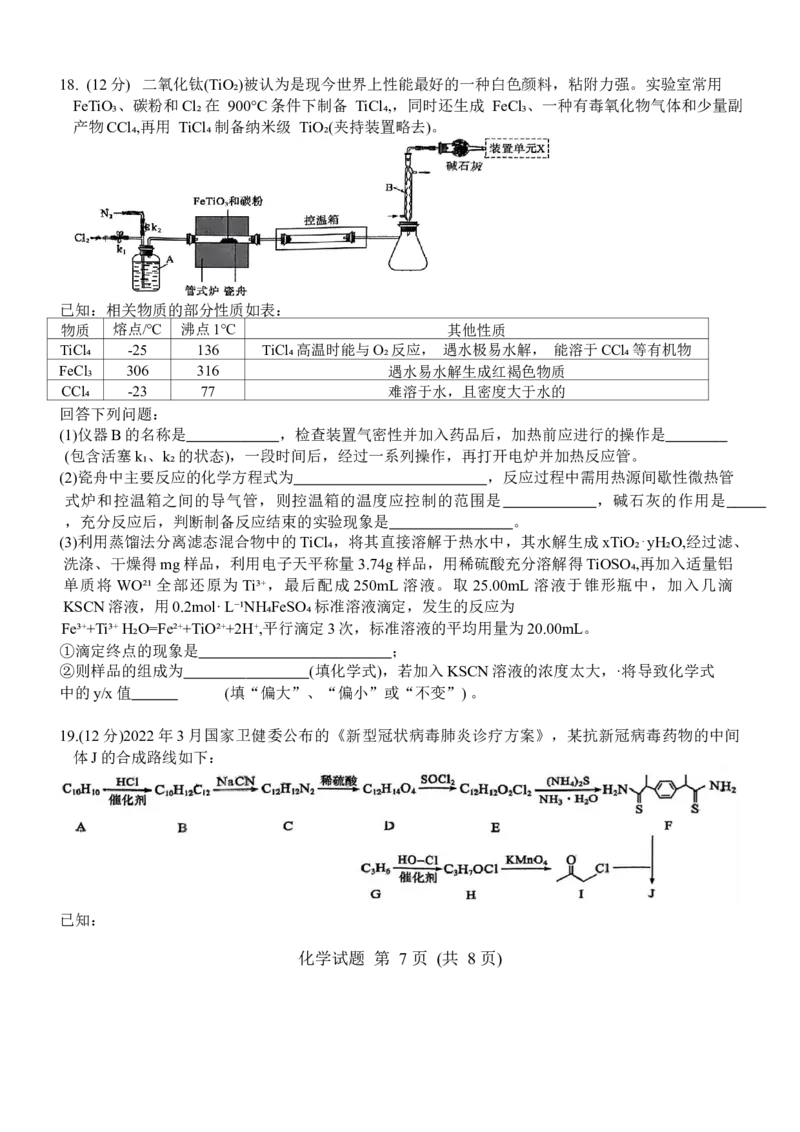
化学试题 第 6 页 (共 8 页)18. (12分) 二氧化钛(TiO₂)被认为是现今世界上性能最好的一种白色颜料,粘附力强。实验室常用
FeTiO₃、碳粉和Cl₂在 900°C条件下制备 TiCl₄,,同时还生成 FeCl₃、一种有毒氧化物气体和少量副
产物CCl₄,再用 TiCl₄制备纳米级 TiO₂(夹持装置略去)。
已知:相关物质的部分性质如表:
物质 熔点/℃ 沸点1℃ 其他性质
TiCl₄ -25 136 TiCl₄高温时能与O₂反应, 遇水极易水解, 能溶于CCl₄等有机物
FeCl₃ 306 316 遇水易水解生成红褐色物质
CCl₄ -23 77 难溶于水,且密度大于水的
回答下列问题:
(1)仪器B的名称是 ,检查装置气密性并加入药品后,加热前应进行的操作是
(包含活塞k₁、k₂的状态),一段时间后,经过一系列操作,再打开电炉并加热反应管。
(2)瓷舟中主要反应的化学方程式为 ,反应过程中需用热源间歇性微热管
式炉和控温箱之间的导气管,则控温箱的温度应控制的范围是 ,碱石灰的作用是
,充分反应后,判断制备反应结束的实验现象是 。
(3)利用蒸馏法分离滤态混合物中的TiCl₄,将其直接溶解于热水中,其水解生成xTiO₂⋅yH₂O,经过滤、
洗涤、干燥得mg样品,利用电子天平称量3.74g样品,用稀硫酸充分溶解得TiOSO₄,再加入适量铝
单质将 WO²¹ 全部还原为 Ti³⁺,最后配成 250mL 溶液。取 25.00mL 溶液于锥形瓶中,加入几滴
KSCN溶液,用0.2mol· L⁻¹NH₄FeSO₄标准溶液滴定,发生的反应为
Fe³⁺+Ti³⁺ H₂O=Fe²⁺+TiO²⁺+2H⁺,平行滴定3次,标准溶液的平均用量为20.00mL。
①滴定终点的现象是 ;
②则样品的组成为 (填化学式),若加入KSCN溶液的浓度太大,·将导致化学式
中的y/x值 (填“偏大”、“偏小”或“不变”) 。
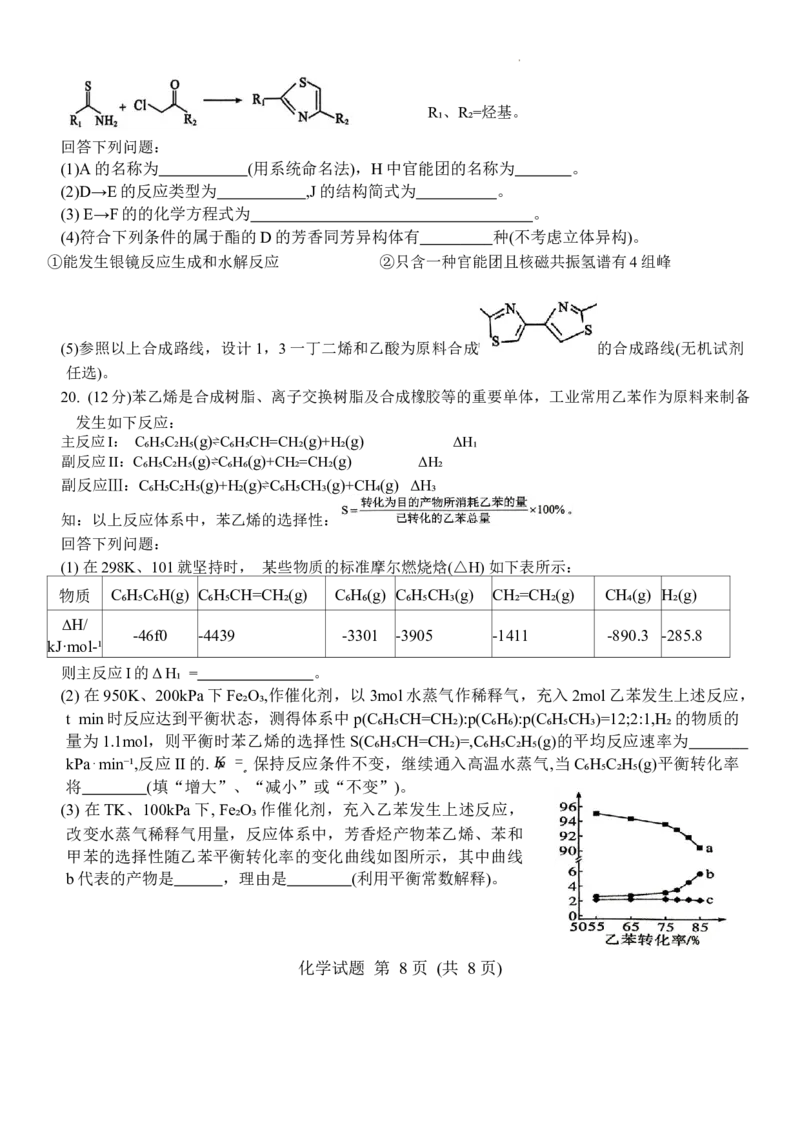
19.(12分)2022年3月国家卫健委公布的《新型冠状病毒肺炎诊疗方案》,某抗新冠病毒药物的中间
体J的合成路线如下:
已知:
化学试题 第 7 页 (共 8 页)R₁、R₂=烃基。
回答下列问题:
(1)A的名称为 (用系统命名法),H中官能团的名称为 。
(2)D→E的反应类型为 ,J的结构简式为 。
(3) E→F的的化学方程式为 。
(4)符合下列条件的属于酯的D的芳香同芳异构体有 种(不考虑立体异构)。
①能发生银镜反应生成和水解反应 ②只含一种官能团且核磁共振氢谱有4组峰
(5)参照以上合成路线,设计1,3一丁二烯和乙酸为原料合成 的合成路线(无机试剂
任选)。
20. (12分)苯乙烯是合成树脂、离子交换树脂及合成橡胶等的重要单体,工业常用乙苯作为原料来制备
发生如下反应:
主反应I: C₆H₅C₂H₅(g)⇌C₆H₅CH=CH₂(g)+H₂(g) ΔH₁
副反应II:C₆H₅C₂H₅(g)⇌C₆H₆(g)+CH₂=CH₂(g) ΔH₂
副反应Ⅲ:C₆H₅C₂H₅(g)+H₂(g)⇌C₆H₅CH₃(g)+CH₄(g) ΔH₃
知:以上反应体系中,苯乙烯的选择性:
回答下列问题:
(1) 在298K、101就坚持时, 某些物质的标准摩尔燃烧焓(△H) 如下表所示:
物质 C₆H₅C₆H(g) C₆H₅CH=CH₂(g) C₆H₆(g) C₆H₅CH₃(g) CH₂=CH₂(g) CH₄(g) H₂(g)
ΔH/
-46f0 -4439 -3301 -3905 -1411 -890.3 -285.8
kJ·mol-¹
则主反应I的Δ H₁ = 。
(2) 在950K、200kPa下Fe₂O₃,作催化剂,以3mol水蒸气作稀释气,充入2mol乙苯发生上述反应,
t min时反应达到平衡状态,测得体系中p(C₆H₅CH=CH₂):p(C₆H₆):p(C₆H₅CH₃)=12;2:1,H₂的物质的
量为1.1mol,则平衡时苯乙烯的选择性S(C₆H₅CH=CH₂)=,C₆H₅C₂H₅(g)的平均反应速率为
kPa⋅min⁻¹,反应II的. Kₚ = 保持反应条件不变,继续通入高温水蒸气,当C₆H₅C₂H₅(g)平衡转化率
。
将 (填“增大”、“减小”或“不变”)。
(3) 在TK、100kPa下, Fe₂O₃作催化剂,充入乙苯发生上述反应,
改变水蒸气稀释气用量,反应体系中,芳香烃产物苯乙烯、苯和
甲苯的选择性随乙苯平衡转化率的变化曲线如图所示,其中曲线
b代表的产物是 ,理由是 (利用平衡常数解释)。
化学试题 第 8 页 (共 8 页)
学科网(北京)股份有限公司