文档内容
2023—2024 学年度上学期 2021 级
10 月月考化学试卷
时间:75分钟 满分:100分
命题人:黄菊 审题人:李昌坤
可能用到的相对原子质量:H-1 O-16 Na-23 S-32 Fe-56
一、选择题(本题包括18个小题,每小3分,共54分,每小题只有1个选项符合题意)
1. 化学与科技、生活有密切的关系。下列叙述正确的是
A. 第三代核电“华龙一号”落户福建,核反应属于化学反应
B. 城市内的光化学烟雾污染与氮、碳及硫的氧化物都有关
C.“84”消毒液沾到皮肤上应立即用大量水清洗,并涂抹维生素C
D. 运动员“战袍”内层添加石墨烯片用于保暖,石墨烯和碳纳米管互为同位素
2. 下列有关物质的分类或归类正确的是
A. 电解质:芒硝、干冰、冰醋酸 B. 碱性氧化物:
C. 胶体:稀豆浆、墨水、碘酒 D. 混合物:漂白粉、水玻璃、铝热剂
3. 2022年3月23日,神舟十三号航天员进行第二次太空授课,王亚平将小苏打和醋酸混合,先
得到过饱和醋酸钠溶液的“液体球”,再经结晶以后得到了热的“冰球”。下列说法错误的是
A.“液体球”中存在的化学键有:离子键、共价键、氢键
B. CHCOOH分子中σ键和π键的数目之比为7∶1
3
C. 过饱和醋酸钠溶液结晶形成热的“冰球”的过程属于放热过程
D. 可用X-射线衍射实验测定“冰球”是否是晶体
4. 化学物质与生活密切相关,下列叙述错误的是
A. 可以作为食品添加剂 B. 可作织物漂白剂
C. 碳酸钡可用于胃肠X射线造影检查 D. FeS可作废水中Cu2+和 的沉淀剂
5. 用 代表阿伏加德罗常数的数值。下列说法正确的是
A. 晶体硅中含 键
B. 通常状况下, 氧气所含分子数小于
C. 中含有的中子数为
D. 电解精炼铜,阳极质量减少 时电路中通过的电子数为
1
学科网(北京)股份有限公司6. 下列反应的离子方程式书写错误的是
A. 长期放置的KI溶液出现黄色:
B. 饱和NaCO 溶液中通入过量CO:
2 3 2
C. 将少量溴水滴入过量NaSO 溶液中:
2 3
D. 向酸性KMnO 溶液中滴加HO 溶液:
4 2 2
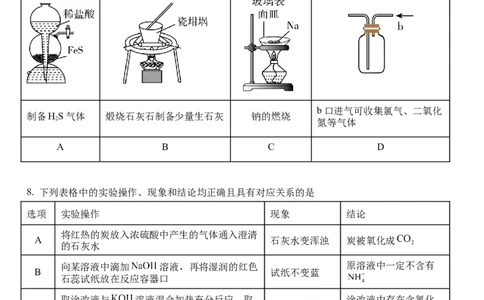
7. 下列实验能达到目的的是
b口进气可收集氯气、二氧化
制备HS气体 煅烧石灰石制备少量生石灰 钠的燃烧
2 氮等气体
A B C D
8. 下列表格中的实验操作、现象和结论均正确且具有对应关系的是
选项 实验操作 现象 结论
将红热的炭放入浓硫酸中产生的气体通入澄清
A 石灰水变浑浊 炭被氧化成
的石灰水
向某溶液中滴加 溶液,再将湿润的红色 原溶液中一定不含有
B 试纸不变蓝
石蕊试纸放在反应容器口
取涂改液与 溶液混合加热充分反应,取 涂改液中存在含氯化
C 出现白色沉淀
上层清液,先加硝酸酸化,再加入硝酸银溶液 合物
D 用玻璃棒蘸取某溶液置于酒精灯的外焰中灼烧 火焰呈黄色 该溶液中含有 元素
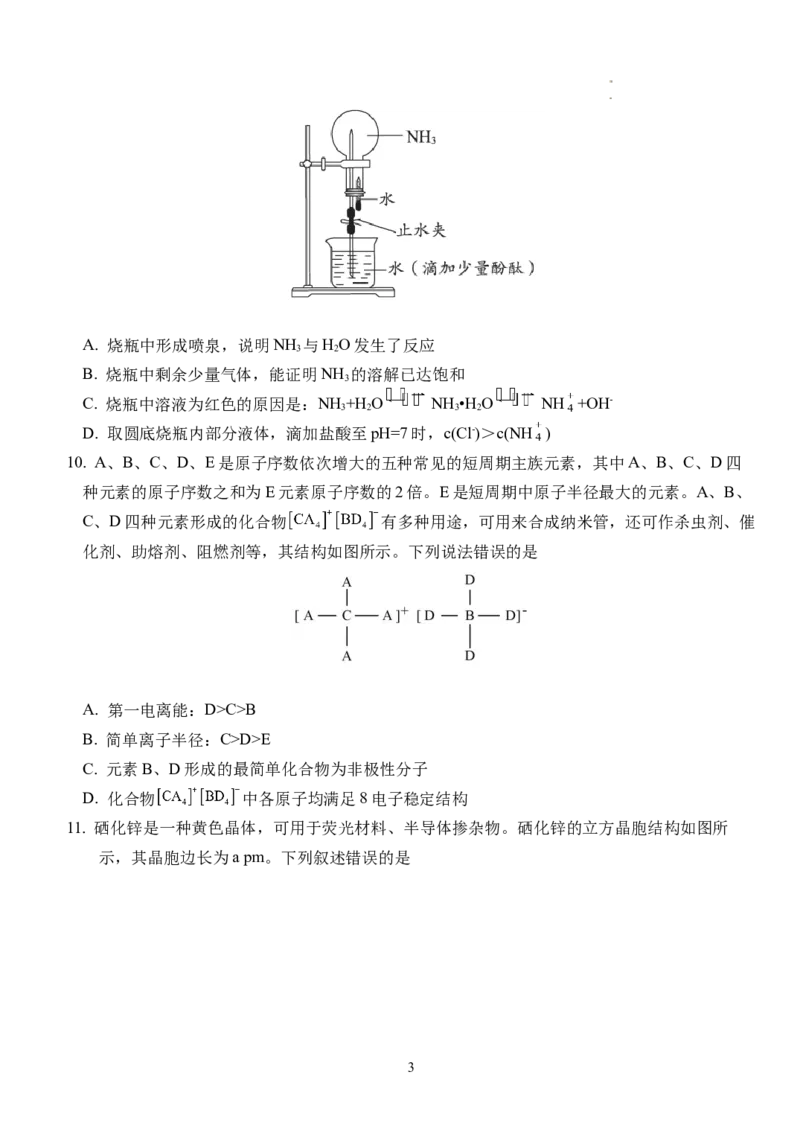
9. 用圆底烧瓶收集NH 后进行喷泉实验。对实验现象的分析正确的是
3
2
学科网(北京)股份有限公司A. 烧瓶中形成喷泉,说明NH 与HO发生了反应
3 2
B. 烧瓶中剩余少量气体,能证明NH 的溶解已达饱和
3
C. 烧瓶中溶液为红色的原因是:NH +H O NH •H O NH +OH-
3 2 3 2
D. 取圆底烧瓶内部分液体,滴加盐酸至pH=7时,c(Cl-)>c(NH )
10. A、B、C、D、E是原子序数依次增大的五种常见的短周期主族元素,其中A、B、C、D四
种元素的原子序数之和为E元素原子序数的2倍。E是短周期中原子半径最大的元素。A、B、
C、D四种元素形成的化合物 有多种用途,可用来合成纳米管,还可作杀虫剂、催
化剂、助熔剂、阻燃剂等,其结构如图所示。下列说法错误的是
A. 第一电离能:D>C>B
B. 简单离子半径:C>D>E
C. 元素B、D形成的最简单化合物为非极性分子
D. 化合物 中各原子均满足8电子稳定结构
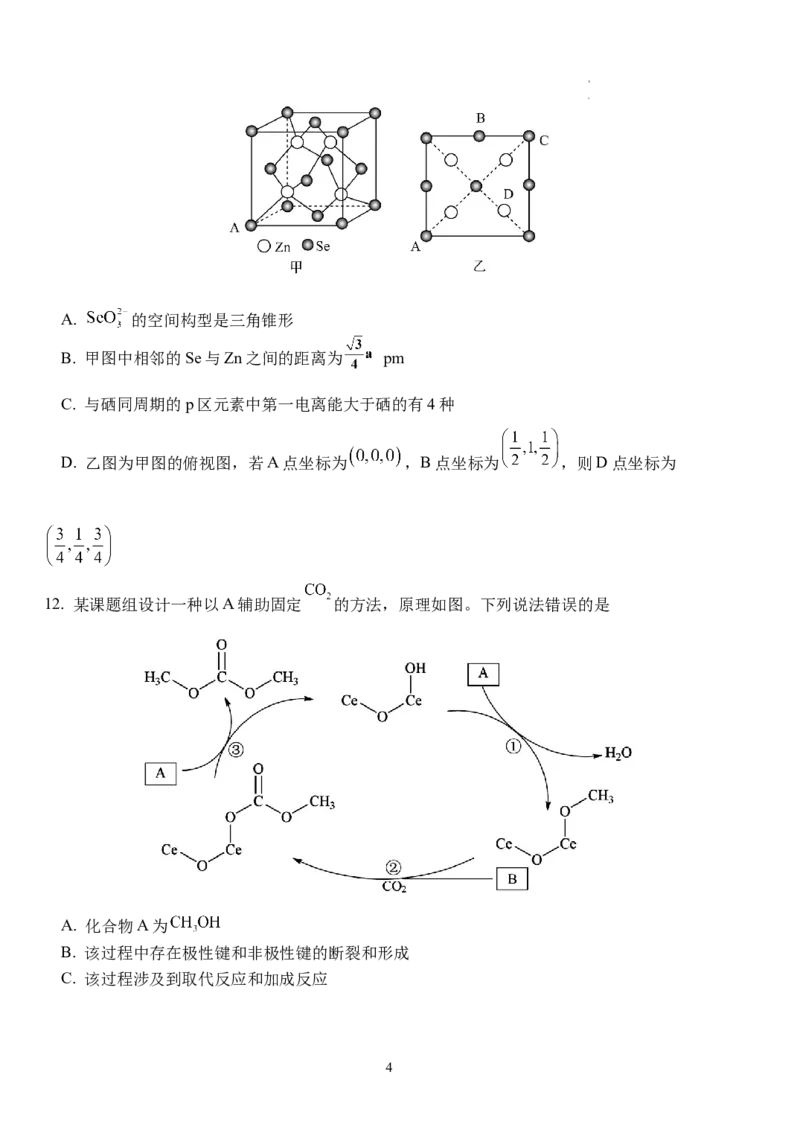
11. 硒化锌是一种黄色晶体,可用于荧光材料、半导体掺杂物。硒化锌的立方晶胞结构如图所
示,其晶胞边长为a pm。下列叙述错误的是
3
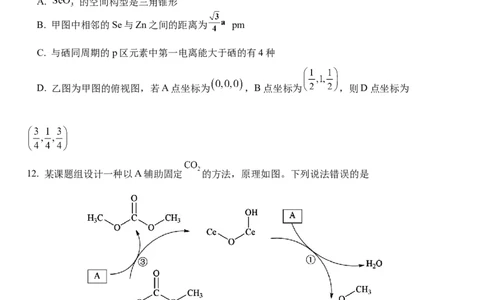
学科网(北京)股份有限公司A. 的空间构型是三角锥形
B. 甲图中相邻的Se与Zn之间的距离为 pm
C. 与硒同周期的p区元素中第一电离能大于硒的有4种
D. 乙图为甲图的俯视图,若A点坐标为 ,B点坐标为 ,则D点坐标为
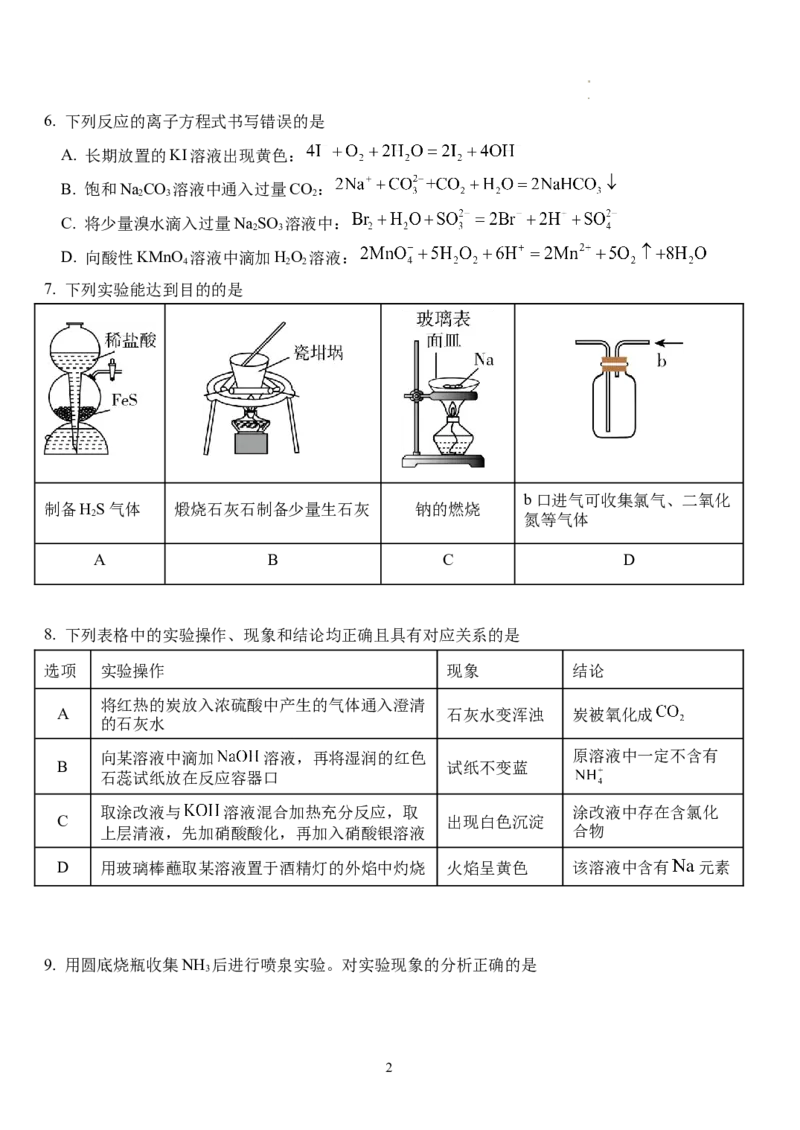
12. 某课题组设计一种以A辅助固定 的方法,原理如图。下列说法错误的是
A. 化合物A为
B. 该过程中存在极性键和非极性键的断裂和形成
C. 该过程涉及到取代反应和加成反应
4
学科网(北京)股份有限公司D. 若用 辅助固定,则产物为
13. 向 溶液中通入过量 ,过程和现象如图。
经检验,白色沉淀为 ;灰色固体中含有 。
下列说法错误的是
A. ①中生成白色沉淀的离子方程式为
B. ①中未生成 ,证明溶度积:
C. 放置一段时间②中产生灰色固体是因为过量的 将部分 还原。
D. 该实验条件下, 与 反应生成 的速率大于生成 的速率
14. 某溶液含 、 、 、 、 、 中的几种,且各离子浓度相同。为确定其组
成,进行实验:①取少量溶液,加入足量 酸化的Ba(NO )(aq),产生白色沉淀,过滤;
3 2
②向滤液中加入足量的 ,产生红褐色沉淀,进一步微热,产生刺激性气味的气
体。下列关于原溶液的说法正确的是
A. 不能确定是否有 B. 需通过焰色试验确定 是否存在
C. 、 都存在 D. 存在 、 、 、
15.足量铜溶于一定量浓硝酸,产生NO 、NO 、NO的混合气体,这些气体若与1.12 L O (标准
2 2 4 2
状况)混合后通入水中,气体被水完全吸收。若向原所得溶液中加入 2 mol·L-1 HSO 溶液
2 4
100 mL,则继续溶解的Cu的质量为
A.6.4 g B.9.6 g C.19.2 g D.24 g
二、非选择题(本题包括4个小题,共55分)
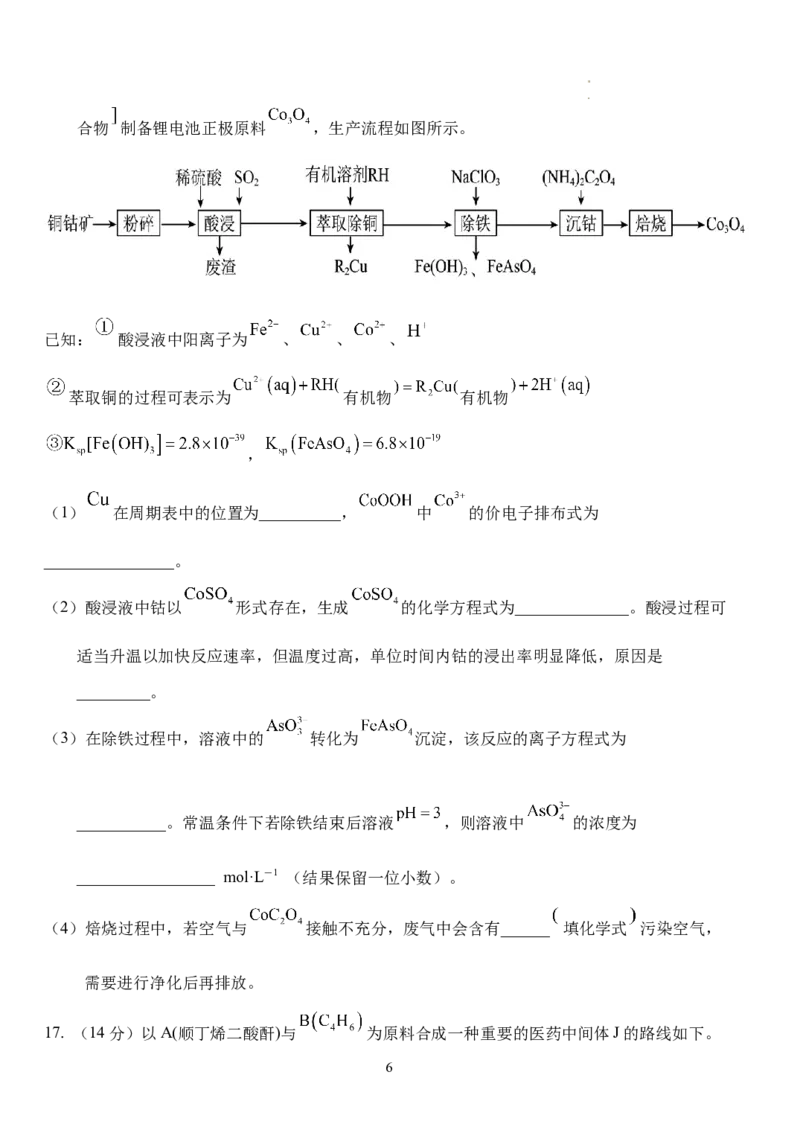
16.(14分) 以钴铜矿 主要成分为 、 、 ,另含少量 及含砷化
5
学科网(北京)股份有限公司合物 制备锂电池正极原料 ,生产流程如图所示。
已知: 酸浸液中阳离子为 、 、 、
萃取铜的过程可表示为 有机物 有机物
,
(1) 在周期表中的位置为__________, 中 的价电子排布式为
________________。
(2)酸浸液中钴以 形式存在,生成 的化学方程式为______________。酸浸过程可
适当升温以加快反应速率,但温度过高,单位时间内钴的浸出率明显降低,原因是
_________。
(3)在除铁过程中,溶液中的 转化为 沉淀,该反应的离子方程式为
___________。常温条件下若除铁结束后溶液 ,则溶液中 的浓度为
_________________ mol·L-1 (结果保留一位小数)。
(4)焙烧过程中,若空气与 接触不充分,废气中会含有______ 填化学式 污染空气,
需要进行净化后再排放。
17. (14分)以A(顺丁烯二酸酐)与 为原料合成一种重要的医药中间体J的路线如下。
6
学科网(北京)股份有限公司的
已知:①反应A+B→C 原子利用率为100%,
②图中Et代表乙基。回答下列问题:
(1)B的名称为_______;
(2)C→D的反应类型为_______;
(3)H中含氧官能团名称为_______;
(4)一分子G在碱作用下发生取代反应生成一分子H和一分子X。X的结构简式为_______;
(5)M是J的同分异构体,其中满足以下条件的有_______种(不考虑立体异构),任写出其中一
种的结构简式_______;
①只存在含有一个O原子的六元环 ②核磁共振氢谱显示3组峰,且面积之比为3∶2∶1
O
(6)预测过氧乙酸CH-C-O-OH的性质_______(答一点即可)。
3
18.(13分) 某实验小组拟探究铁的化合物 的分解产物,设计如下实验。已知几种物
质的物理性质如下表所示。
物质
熔点
沸点
7
学科网(北京)股份有限公司实验装置如图所示 加热和夹持装置省略 。
回答下列问题:
(1)点燃酒精灯之前,通入一段时间 ,其目的是______________。
(2)低温浴槽II控制的温度范围为 。
(3)甲、乙、丙三组分别进行实验,测得相关实验数据如下 不考虑损失且不考虑生成 ,
在该温度下完全反应 :
处温度
质量 低温浴槽 净增质量 低温浴槽 净增质量
甲
乙
丙
根据实验数据分析,甲组实验中 装置得到的纯净固体产物是__________ 填化学式
。
经检测,乙组实验的固体产物为纯净物,写出 中发生的化学反应方程式:
(4)为了进一步分析丙组实验得到的固体纯净物成分,他们取少量固体溶于稀硫酸中,将溶液
分成两份,进行如下实验 不考虑 的存在 :
实
操作 现象
验
在一份溶液中滴加 溶液 产生蓝色沉淀
在另一份溶液中滴加 溶液 溶液变红色
根据实验推知,丙组实验中 分解生成的固体产物、 、 的物质的量之比为
_________。
(5)为了进一步探究气体产物成分,将 仪器导出的气体通入酸化的 淀粉溶液中,一段时
8
学科网(北京)股份有限公司间后,若________________________________ 填实验现象 ,则说明有 生成。
(6)将I中产物1100 g溶于900 g 98%的浓硫酸所得产物为 ,其质量分数为
_______________
19.(14分) 回答下列问题:
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应: 。该
可逆反应达到平衡的标志是_________(填字母)。
A. 混合气体的物质的量不再随时间变化 B. 混合气体的质量不再随时间变化
C. 混合气体的颜色不再随时间变化 D. 混合气体的密度不再随时间变化
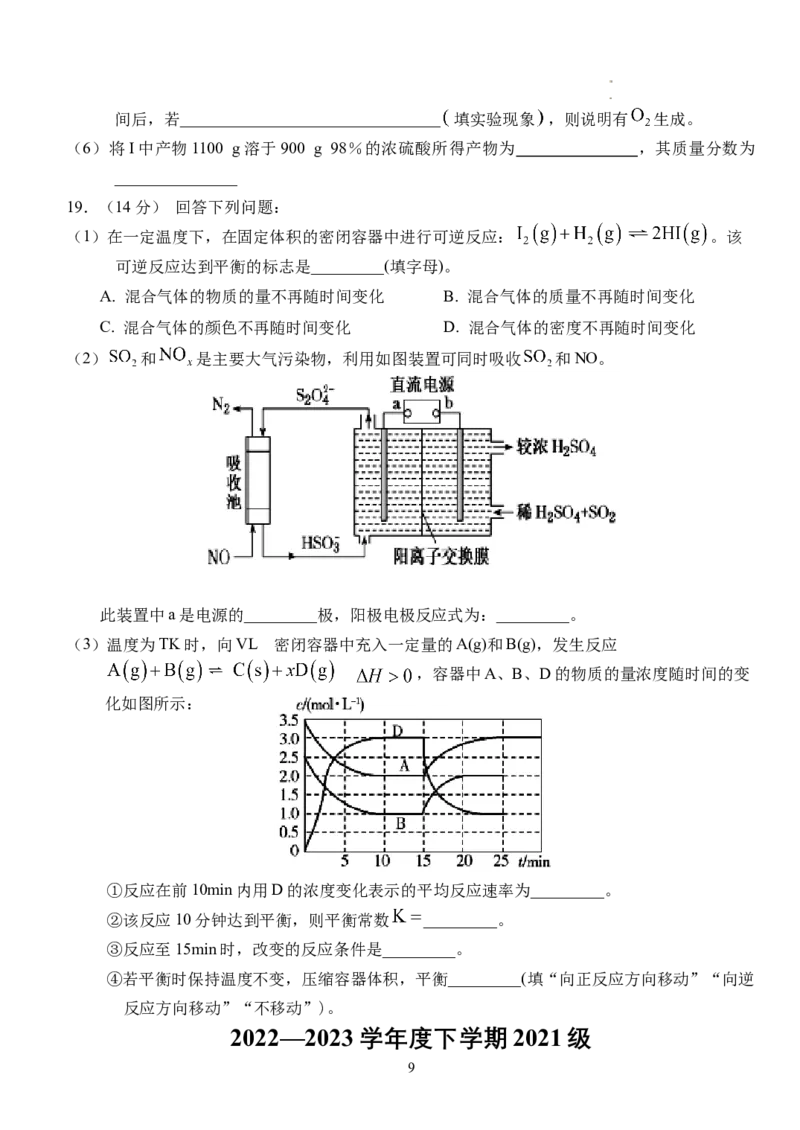
(2) 和 是主要大气污染物,利用如图装置可同时吸收 和NO。
此装置中a是电源的_________极,阳极电极反应式为:_________。
的
(3)温度为TK时,向VL 密闭容器中充入一定量的A(g)和B(g),发生反应
,容器中A、B、D的物质的量浓度随时间的变
化如图所示:
①反应在前10min内用D的浓度变化表示的平均反应速率为_________。
②该反应10分钟达到平衡,则平衡常数 _________。
③反应至15min时,改变的反应条件是_________。
④若平衡时保持温度不变,压缩容器体积,平衡_________(填“向正反应方向移动”“向逆
反应方向移动”“不移动”)。
2022—2023 学年度下学期 2021 级
9
学科网(北京)股份有限公司10 月月考化学试卷 参考答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
C D A C B C A C C D C B B D B
16.(14分,每空2分)(1) ①第四周期第Ⅰ 族 ②
(2) ①
② 温度过高,二氧化硫的溶解度降低,所以钴的浸出率降低
(3) ①
②
(4)CO
17.(14分,每空2分)(1)1,3—丁二烯
(2)还原反应
(3)酯基、酮羰基
(4)CHCHOH
3 2
(5) ① 2 ②. 或
(6)氧化性或者酸性(答一点即可)
18.(13分,除标注外每空2分)(1)排尽装置内空气,避免 、 等干扰实验
(2) (1分)
(3) ① ②
(4)1∶2∶4
(5)溶液变蓝色 (1分)
(6)发烟硫酸(1分) 51%
19(14分,每空2分)(1)C
(2) ①负 ②
10
学科网(北京)股份有限公司(3) ① ② 4.5 ③ 降低温度 ④ 不移动
11
学科网(北京)股份有限公司