文档内容
绝密★启用前
重庆市高三化学考试
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无
效。
3.考试结束后,将本试卷和答题卡一并交回。
4.可能用到的相对原子质量:H1 C12 O16 K 39 I127 Nd144.
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
1.人民对美好生活的向往,就是我们的奋斗目标。下列生活中使用的物质的主要成分不是高分子材料的是
选项 A B C D
生活中
使用的
物质
名称 防紫外线树脂眼镜 大理石玉石蓝纹背景墙 有机玻璃板 飞机上使用的芳砜纶纤维
2.下列化学用语的表述错误的是
A.C₂H₂的结构模型:
B.2-丁烯的键线式:
C.N₂分子的电子式:
D.基态O原子的轨道表示式:
3.化学与生活、社会发展息息相关,下列有关说法错误的是
A.将一氧化碳中毒的病人移至高压氧舱,救治原理与平衡移动有关
B. K₂FeO₄是一种绿色消毒剂,不仅可用于水体杀菌消毒,而且可以软化硬水
C.医用防护服的核心材料是微孔聚四氟乙烯薄膜,其单体四氟乙烯属于卤代烃
D.将香蕉和青苹果放在一起,青苹果更容易成熟,是因为香蕉释放的乙烯有催熟作用
4.下列物质的应用中,涉及氧化还原反应的是
【高三化学 第 1 页 (共 8 页)】A.热的纯碱溶液洗涤油污
B.含硫酸钙的卤水点制豆腐
C.袋装食品常用铁粉和生石灰来防止食品变质
D.食醋用于清除水壶中的少量水垢(主要成分为CaCO₃)
5.离子键的百分数是依据电负性的差值计算出来的,差值越大,离子键的百分数越大,下列几种化合物的化
学键中离子键的百分数最大的是
A. LiF B. AlCl₃ C. MgO D. SO₃
6.下列离子方程式与所给事实不相符的是
A.明矾净水:Al3++3H
2
O⇌Al(OH)
3
(胶体)+3H+
B.向AgCl浊液中通入H₂S,浊液变黑: 2AgCl+H₂S=Ag₂S+2H⁺+2Cl⁻
C.向Ca(HCO₃)₂溶液中加入足量的 NaOH溶液; Ca2++HCO−+OH−=CaCO ↓+ H₂O
3 3
D.向二元弱酸亚磷酸 (H₃PO₃)溶液中滴加过量的 NaOH 溶液: H₃PO₃+2OH⁻=
HPO2−+2H O
3 2
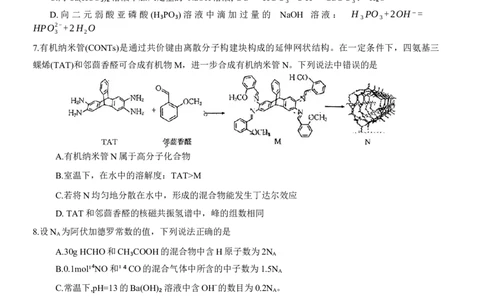
7.有机纳米管(CONTs)是通过共价键由离散分子构建块构成的延伸网状结构。在一定条件下,四氨基三
蝶烯(TAT)和邻茴香醛可合成有机物M,进一步合成有机纳米管N。下列说法中错误的是
A.有机纳米管N属于高分子化合物
B.室温下,在水中的溶解度:TAT>M
C.若将N均匀地分散在水中,形成的混合物能发生丁达尔效应
D. TAT和邻茴香醛的核磁共振氢谱中,峰的组数相同
8.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.30g HCHO和CH₃COOH的混合物中含H原子数为2N
A
B.0.1mol¹⁴NO 和¹⁴CO的混合气体中所含的中子数为1.5N
A
C.常温下,pH=13的Ba(OH)₂溶液中含OH⁻的数目为0.2N 。
A
D.23.0g乙醇与过量冰醋酸在浓硫酸、加热条件下反应,生成的乙酸乙酯分子数为0.5N
A
9.1825年偶然地发现了组成为 KCE·PtCl₂·C₂H₄·H₂O 的黄色晶体,其中含乙烯,配位化学确立后,证明其
中存在组成为[PtCl₃(C₂H₄)]⁻ 的配合物,铂的配合物顺式三氯二氨合铂[常称“顺铂”,化学式为
Pt(NH₃)₂Cl₂]具有抗癌活性。下列说法正确的是
A. C₂H₄ 为极性分子
B. H₂O的 VSEPR模型为V形
C. Pt(NH₃)₂Cl₂分子中含有4个σ键
D. NH₃分子中的 H—N—H键的键角小于顺铂中的H—N—H键
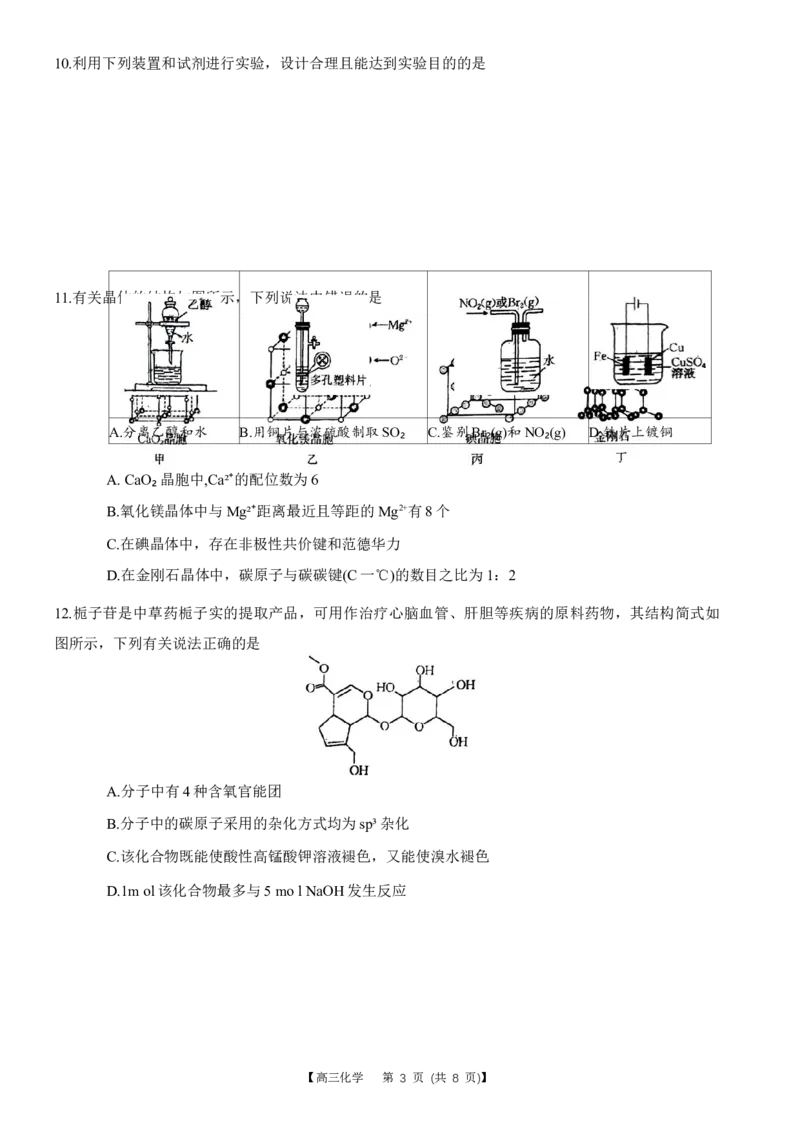
【高三化学 第 2 页 (共 8 页)】10.利用下列装置和试剂进行实验,设计合理且能达到实验目的的是
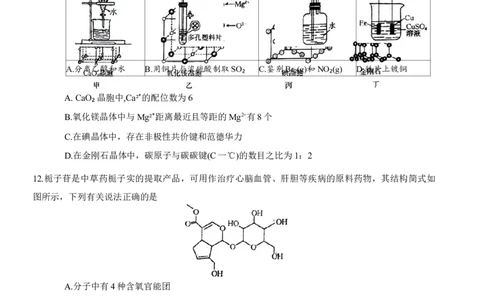
11.有关晶体的结构如图所示,下列说法中错误的是
A.分离乙醇和水 B.用铜片与浓硫酸制取SO₂ C.鉴别Br₂(g)和NO₂(g) D.铁片上镀铜
A. CaO₂晶胞中,Ca²⁺的配位数为6
B.氧化镁晶体中与Mg²⁺距离最近且等距的Mg2+有8个
C.在碘晶体中,存在非极性共价键和范德华力
D.在金刚石晶体中,碳原子与碳碳键(C一℃)的数目之比为1:2
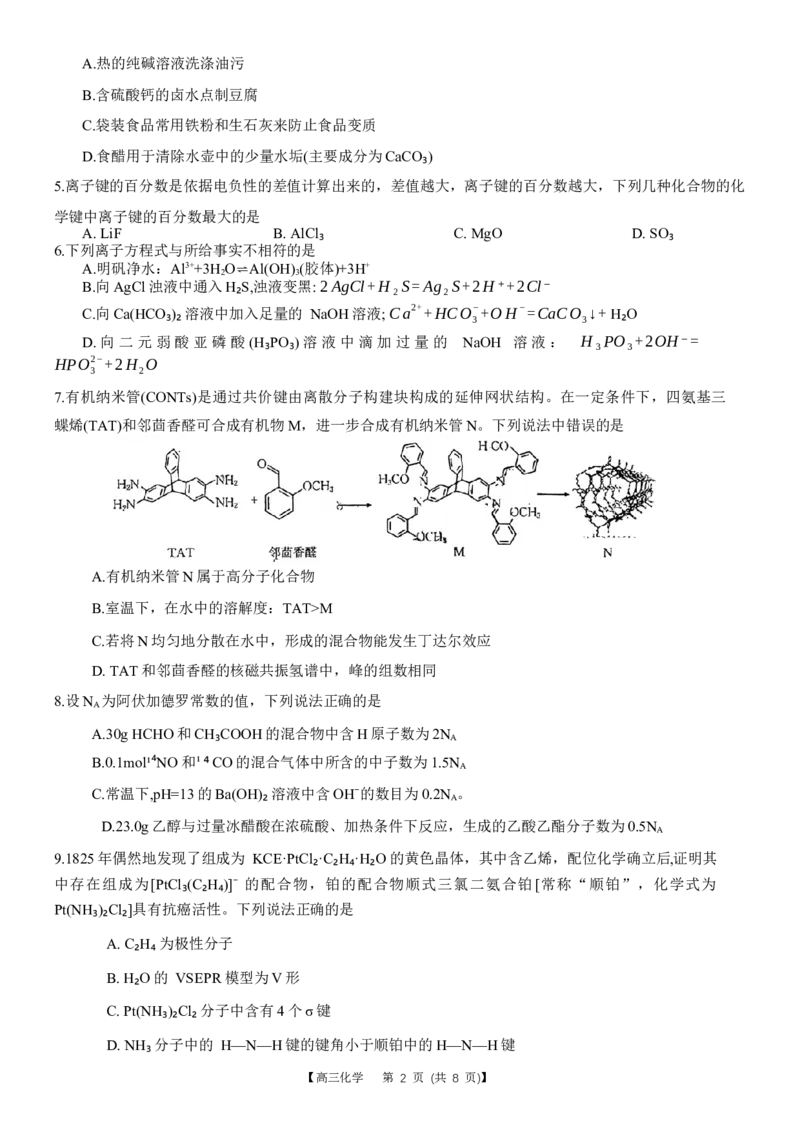
12.栀子苷是中草药栀子实的提取产品,可用作治疗心脑血管、肝胆等疾病的原料药物,其结构简式如
图所示,下列有关说法正确的是
A.分子中有4种含氧官能团
B.分子中的碳原子采用的杂化方式均为sp³杂化
C.该化合物既能使酸性高锰酸钾溶液褪色,又能使溴水褪色
D.1m ol该化合物最多与5 mo l NaOH发生反应
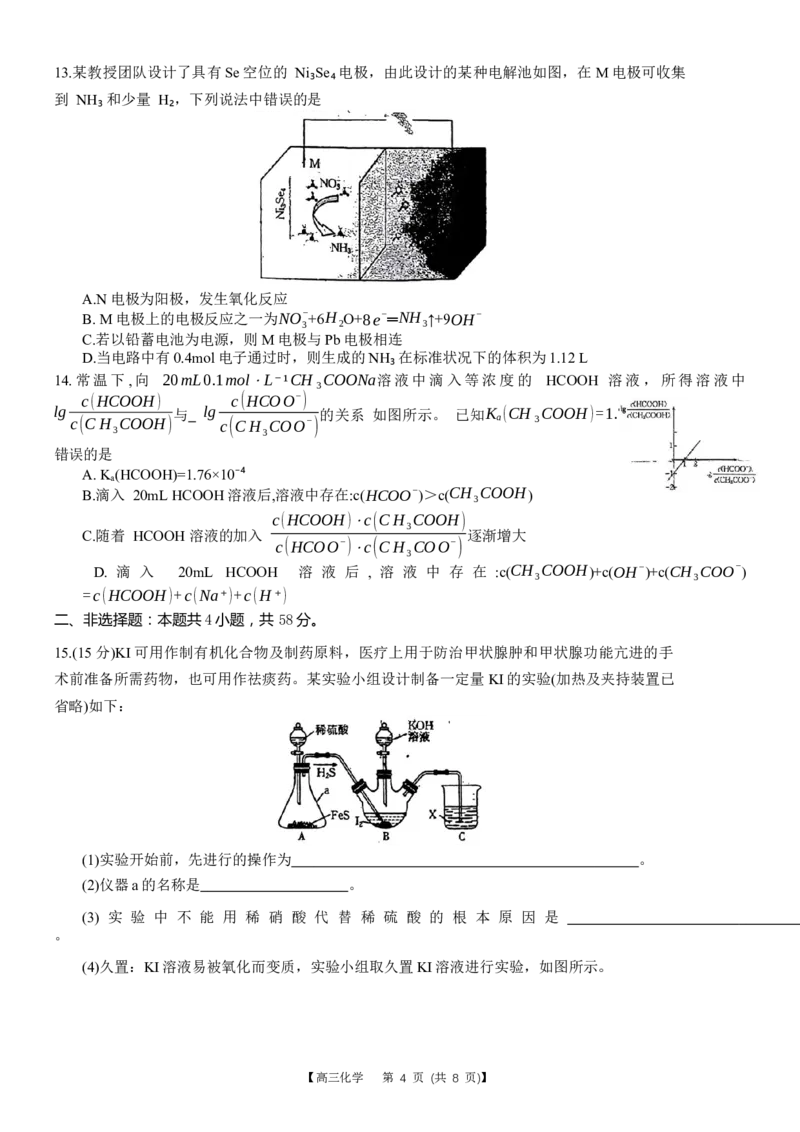
【高三化学 第 3 页 (共 8 页)】13.某教授团队设计了具有Se空位的 Ni₃Se₄电极,由此设计的某种电解池如图,在M电极可收集
到 NH₃ 和少量 H₂,下列说法中错误的是
A.N电极为阳极,发生氧化反应
B. M电极上的电极反应之一为NO− +6H O+8e−═NH ↑+9OH−
3 2 3
C.若以铅蓄电池为电源,则M电极与Pb电极相连
D.当电路中有0.4mol电子通过时,则生成的NH₃在标准状况下的体积为1.12 L
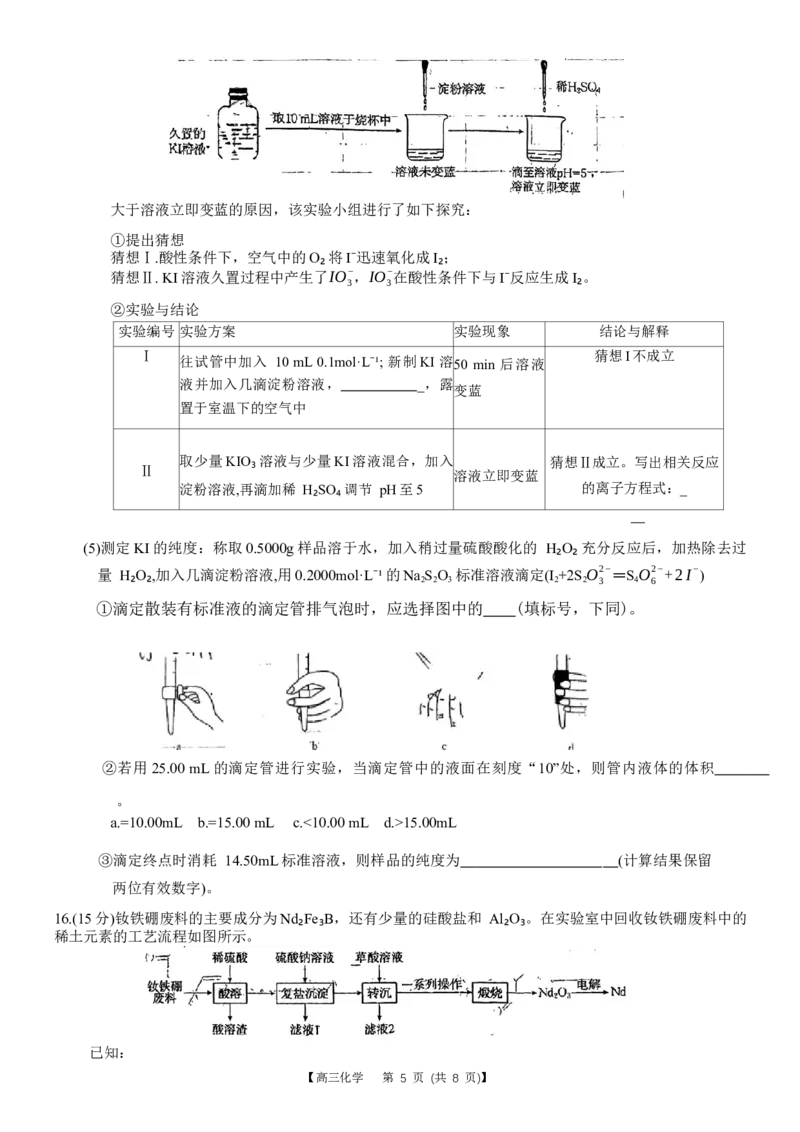
14.常温下,向 20mL0.1mol⋅L⁻¹CH₃COONa溶液中滴入等浓度的 HCOOH 溶液,所得溶液中
c(HCOOH) c(HCOO−)
lg 与 lg 的关系 如图所示。 已知Kₐ(CH₃COOH)=1.76×10⁻⁵,下列说法
c(CH COOH) c(CH COO−)
3 3
错误的是
A. Kₐ(HCOOH)=1.76×10⁻⁴
B.滴入 20mL HCOOH溶液后,溶液中存在:c(HCOO−)>c(CH COOH)
3
c(HCOOH)⋅c(CH COOH)
3
C.随着 HCOOH 溶液的加入 逐渐增大
c(HCOO−)⋅c(CH COO−)
3
D. 滴 入 20mL HCOOH 溶 液 后 , 溶 液 中 存 在 :c(CH COOH)+c(OH−)+c(CH COO− )
3 3
=c(HCOOH)+c(Na⁺)+c(H⁺)
二、非选择题:本题共4小题,共 58分。
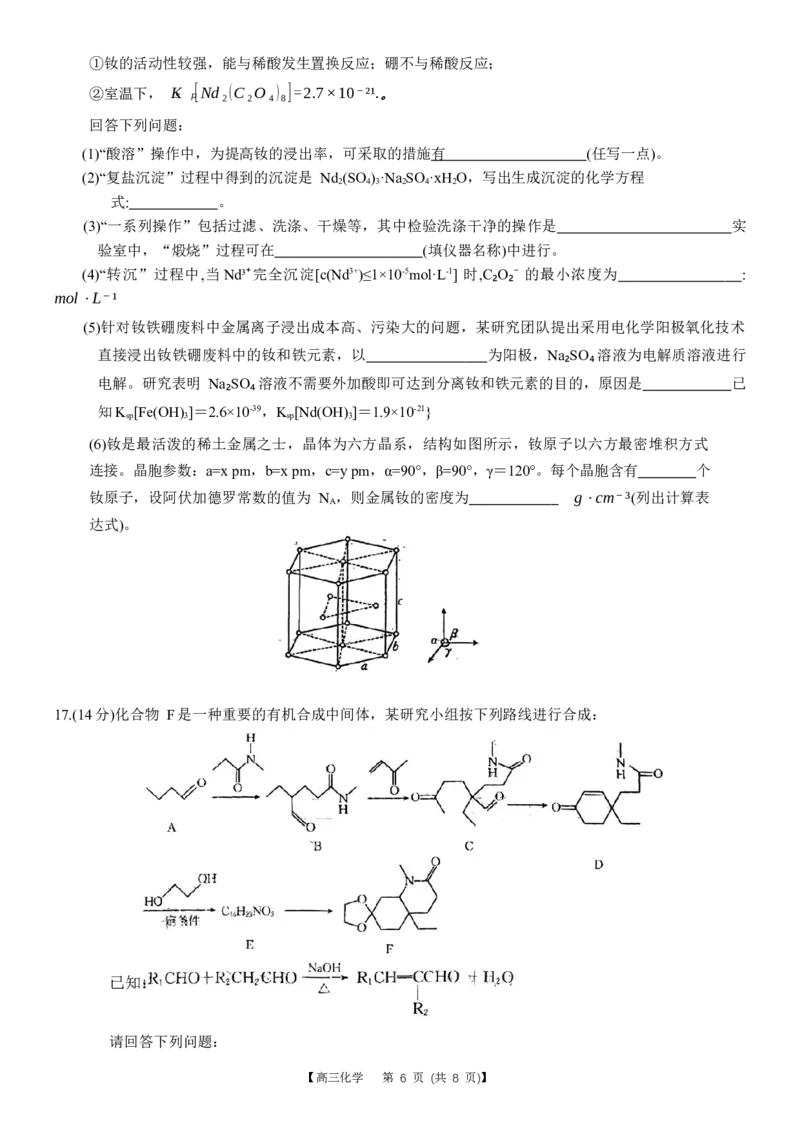
15.(15分)KI可用作制有机化合物及制药原料,医疗上用于防治甲状腺肿和甲状腺功能亢进的手
术前准备所需药物,也可用作祛痰药。某实验小组设计制备一定量KI的实验(加热及夹持装置已
省略)如下:
(1)实验开始前,先进行的操作为 。
(2)仪器a的名称是 。
(3) 实 验 中 不 能 用 稀 硝 酸 代 替 稀 硫 酸 的 根 本 原 因 是
。
(4)久置:KI溶液易被氧化而变质,实验小组取久置KI溶液进行实验,如图所示。
【高三化学 第 4 页 (共 8 页)】大于溶液立即变蓝的原因,该实验小组进行了如下探究:
①提出猜想
猜想Ⅰ.酸性条件下,空气中的O₂将I⁻迅速氧化成I₂;
猜想Ⅱ. KI溶液久置过程中产生了IO−,IO−在酸性条件下与I⁻反应生成I₂。
3 3
②实验与结论
实验编号 实验方案 实验现象 结论与解释
Ⅰ 猜想I不成立
往试管中加入 10 mL 0.1mol·L⁻¹; 新制KI 溶50 min 后溶液
液并加入几滴淀粉溶液, _,露
变蓝
置于室温下的空气中
取少量KIO₃溶液与少量KI溶液混合,加入 猜想Ⅱ成立。写出相关反应
Ⅱ
溶液立即变蓝
淀粉溶液,再滴加稀 H₂SO₄调节 pH至5 的离子方程式:_
(5)测定KI的纯度:称取0.5000g样品溶于水,加入稍过量硫酸酸化的 H₂O₂充分反应后,加热除去过
量 H₂O₂,加入几滴淀粉溶液,用0.2000mol·L⁻¹的Na S O 标准溶液滴定(I +2S O2−═S O2−+2I− )
2 2 3 2 2 3 4 6
①滴定散装有标准液的滴定管排气泡时,应选择图中的 (填标号,下同)。
②若用25.00 mL的滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积
。
a.=10.00mL b.=15.00 mL c.<10.00 mL d.>15.00mL
③滴定终点时消耗 14.50mL标准溶液,则样品的纯度为 (计算结果保留
两位有效数字)。
16.(15分)钕铁硼废料的主要成分为Nd₂Fe₃B,还有少量的硅酸盐和 Al₂O₃。在实验室中回收钕铁硼废料中的
稀土元素的工艺流程如图所示。
已知:
【高三化学 第 5 页 (共 8 页)】①钕的活动性较强,能与稀酸发生置换反应;硼不与稀酸反应;
②室温下, Kₛ ₚ[Nd₂(C₂O₄)₈]=2.7×10⁻²¹.。
回答下列问题:
(1)“酸溶”操作中,为提高钕的浸出率,可采取的措施有 (任写一点)。
(2)“复盐沉淀”过程中得到的沉淀是 Nd (SO ) ·Na SO ·xH O,写出生成沉淀的化学方程
2 4 3 2 4 2
式: 。
(3)“一系列操作”包括过滤、洗涤、干燥等,其中检验洗涤干净的操作是 实
验室中,“煅烧”过程可在 (填仪器名称)中进行。
(4)“转沉”过程中,当Nd³⁺完全沉淀[c(Nd3+)≤1×10-5mol·L-1] 时,C₂O₂⁻ 的最小浓度为 :
mol⋅L⁻¹
(5)针对钕铁硼废料中金属离子浸出成本高、污染大的问题,某研究团队提出采用电化学阳极氧化技术
直接浸出钕铁硼废料中的钕和铁元素,以 为阳极,Na₂SO₄溶液为电解质溶液进行
电解。研究表明 Na₂SO₄溶液不需要外加酸即可达到分离钕和铁元素的目的,原因是 已
知K [Fe(OH) ]=2.6×10-39,K [Nd(OH) ]=1.9×10-21}
sp 3 sp 3
(6)钕是最活泼的稀土金属之士,晶体为六方晶系,结构如图所示,钕原子以六方最密堆积方式
连接。晶胞参数:a=x pm,b=x pm,c=y pm,α=90°,β=90°,γ=120°。每个晶胞含有 个
钕原子,设阿伏加德罗常数的值为 N ,则金属钕的密度为 g⋅cm⁻³(列出计算表
A
达式)。
17.(14分)化合物 F是一种重要的有机合成中间体,某研究小组按下列路线进行合成:
已知:
请回答下列问题:
【高三化学 第 6 页 (共 8 页)】(1)有机物B所含的官能团名称是 ,B-→C的反应类型为
(2)化合物E的结构简式是 。
(3)写出D →E的化学方程式: 。
(4)1分子有机物F中含有的手性碳原子数为 。
(5)上述流程涉及的非金属元素中,电负性由大到小的顺序为 ,第一电
离能最大的为 (填元素符号)。
(6)有机物H是D的同分异构体,写出符合下列条件的 H的结构简式: (任写一种)。
①IR谱检测表明:分子中含有一个苯环,有C+-O—C键,无O——H、O—O键。
②¹H-NMR谱检测表明:分子中共有5种不同化学环境的氢原子。
③仅含有两种官能团..其中一种为一NH₂,且氨基与苯环直接相连。
18.(14分)研究CO₂资源的综合利用,对实现“碳达峰”和“碳中和”有重要意义。
(1)已知:
₂ ₂.CO ₃(g)+3H ₂(g)═CH ₁OH(g△)+HH⁻OⅠ(g4∽)9.5kJ·mol⁻¹=
Π.CO(g)+2H₂(g)⇌CH₃OH(g)△H₂=−90.4kJ⋅mol⁻¹
₂ ₂. CO ₂(g)+H ₃(g)═C△OH(g⁻Ⅲ)O+(Hg)
①△H₃= J⋅mol⁻¹。
②一定条件下,向体积为2L的恒容密闭容器中通入1m ol CO₂和3m ol H₂,发生上述反应,达
到平衡时,容器中CH₃OH(g)的物质的量为0.5mol,CO的物质的量为0.3mol,此时 H₂O(g)的浓
度为
mol·L⁻¹。
(2)CO₂在 Cu-ZnO催化下,同时发生反应Ⅰ、Ⅲ,此方法是解决温室效应和能源短缺问题的重要手
段。保持温度Т时,在容积不变的密闭容器中,充入一定量的CO₂及 H₂,起始及达到平衡时(tmin
时恰好达到平衡),容器内各气体物质的量及总压强如下表:
物质的量/mol 。
总压强/kPa
CO₂ H₂ CH₃OH(g) CO H₂O(g)
起始 0.5 0.9- 0 -01 0. po
平衡 n 0.3 p
若反应Ⅰ、Ⅲ均达到平衡时,p₀=1.4p,则表中n= ;0~t min 内,CO₂.的分压变化
率为
kPa⋅min⁻¹,反 应 Ⅰ 的 平 衡 常 数
Kₚ = ⁻²(用含p的式子表示)。
(kPa)
(3)CO₂催化加氢制甲烷涉及的反应主要有:
主反应:CO₂(g)+4H₂(g)⇌CH₄(g)+2H
2
O(g) △H₄<0
【高三化学 第 7 页 (共 8 页)】副反应:(CO₂(g)+H₂(g)⇌CO(g)+H₂O(g) △H₃
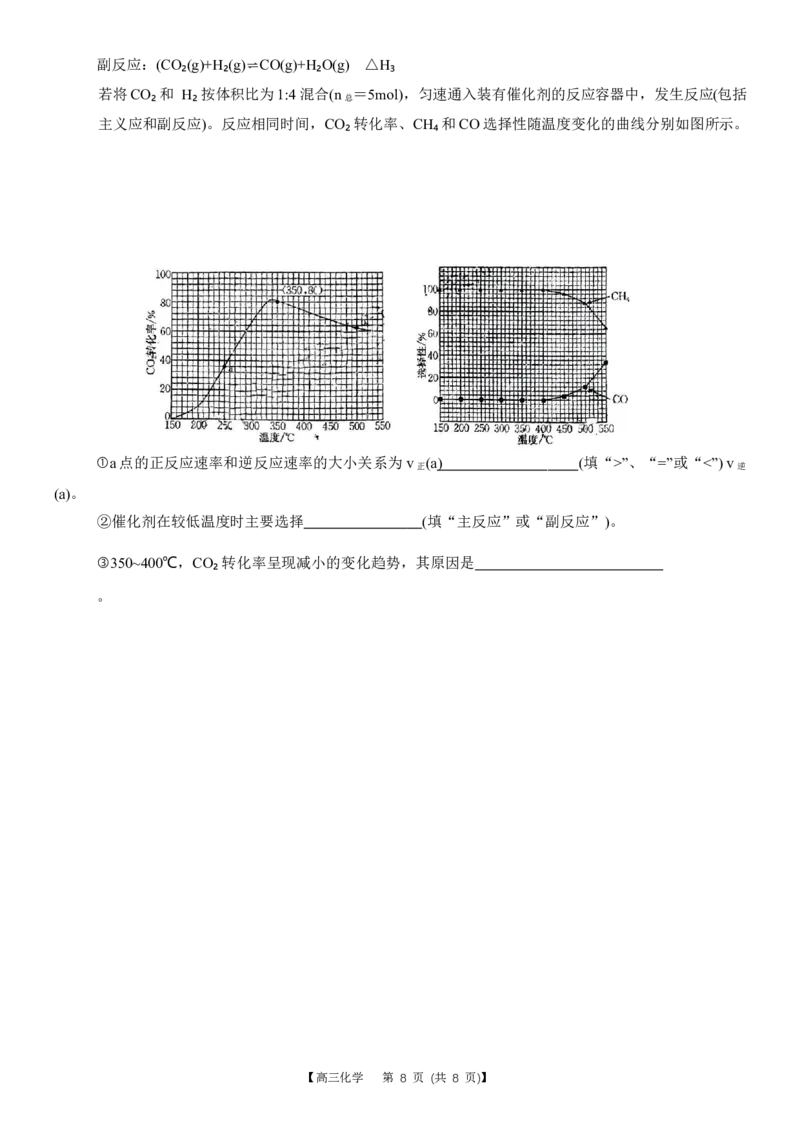
若将CO₂和 H₂按体积比为1:4 混合(n =5mol),匀速通入装有催化剂的反应容器中,发生反应(包括
总
主义应和副反应)。反应相同时间,CO₂转化率、CH₄和CO选择性随温度变化的曲线分别如图所示。
①a点的正反应速率和逆反应速率的大小关系为 v
正
(a ) (填“>”、“=”或“<”) v
逆
(a)。
②催化剂在较低温度时主要选择 (填“主反应”或“副反应”)。
③350~400℃,CO₂转化率呈现减小的变化趋势,其原因是
。
【高三化学 第 8 页 (共 8 页)】