文档内容
秘密★启用前 试卷类型:A
2025 届广东省普通高中毕业班调研考试(一)
会
化 学
究
本试卷共8页,20小题,满分100分。考试用时75分钟。
研
注意事项: 1.答卷前,考生务必用黑色字迹的钢笔或签字笔将自己的姓名、考生号、考场号和座位号填
写在答题卡上。用2B铅笔将试卷类型(A)填涂在答题卡相应位置上。将条形码横贴在右上
考
角“条形码粘贴处”。
2.作答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目选项的答案信息点涂
高
黑;如需改动,用橡皮擦干净后,再选涂其他答案,答案不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相
省
应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。不
按以上要求作答的答案无效。
东
4.作答选考题时,请先用2B铅笔填涂选做题的题号对应的信息点,再作答。漏涂、错涂、
多涂的,答案无效。
广
5.考生必须保持答题卡的整洁。考试结束后,将试卷和答题卡一并交回。
6.可能用到的相对原子质量:N14 Zn65
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小
题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.“葡萄美酒夜光杯”,酒具体现了历史进展。下列酒具中,主要由硅酸盐材料制成的是
会
究
研
A.清代彩绘龙纹蓝瓷壶 B.犀角雕玉兰花果纹杯 C.斫木云纹漆耳杯 D.青铜兽面纹爵
考
2.神舟十六号载人飞船展示了中国航天事业的强大实力和技术水平。下列叙述错误的是
A.空间站的砷化镓太阳能电池是将化学能转化为电能
高
B.飞船使用的Si N 隔热层属于新型无机非金属材料
3 4
C.空间站存储器所用的材料石墨省烯与C 互为同素异形体
60
D.飞船核心器件之一的石英晶体属于共价晶体
东
3.劳动创造幸福。下列劳动项目与所述的化学知识没有关联的是
选项 广劳动项目 化学知识
A 分析员用X射线衍射仪区分普通玻璃和水晶 普通玻璃属于非晶体,水晶属于晶体
B 泳池管理员用漂粉精对游泳池进行消毒 含氯消毒剂具有强酸性
C 实验员用加热法分离I 2 和NaCl I 2 易升华
D 维修工用NaOH和铝粉疏通厨卫管道 A1与NaOH溶液反应产生H
2
化学试题A 第1页(共8页)4.广州是岭南文化的集萃地。下列有关岭南文化的说法错误的是
A.“茶艺文化”:浸泡功夫茶利用了萃取原理,水作萃取剂
B.“戏剧文化”:现代粤剧舞台上灯光光柱的形成利用了丁达尔效应
会
C.“烟花文化”:广州海心沙新年烟花秀中绚烂多姿的颜色来自焰色试验
D.“粤菜文化”:盐焗鸡所用的粗盐由海水晒制而成,涉及复杂
究
的化学变化
5.下图是短周期某种非金属元素的“价-类”二维图,其中e是a和d的反应产物。下列推断错误的是
研
A.b和c均不是酸性氧化物
B.可存在a→b→c→d的转化
考
C.常温下,d的浓溶液不能与铁发生反应
D.可用与强碱的反应来检验e中的阳离高子
6.2023年诺贝尔奖授予开发出有效COVID-19mRNA疫苗的“核苷碱基修饰”项目。下图所示化合物
省
是腺嘌呤核苷(用R表示),可与硫酸反应生成硫酸盐(RH) SO 。下列说法错误的是
2 4
A.R是氨基酸的一种同系物
东
B.R能使酸性KMnO 溶液褪色
4
广
C.R能发生取代反应和加成反应
D.(RH) SO 水溶液中:2c(SO 2−)=c(RH+)+c(R)
2 4 4
7.下列实验操作规范且能达到目的的是
会
A.溶液的配制 B.氯气的提纯 C.氨气的收集 D.沉淀的过滤
究
8.我国科学家以N 、CO 及KHCO 等物质为原料通过电催化法制备尿素,设N 为阿伏加德罗常数的值。
2 2 3 A
下列说法正确的是 研
A.标准状况下,0.1molN 与CO 混合气体的体积为2.24L
2 2
考
B.2.8gN 含有的电子数目为2.8N
2 A
C.1mol尿素中所含有的σ键的数目为8N
高A 尿素
D.体积为1L的1mol·L−1的KHCO 溶液中,HCO −数目为N
3 3 A
省
9.谷氨酸单钠是味精的主要成分,利用发酵法制备该物质的流程如下,下列说法错误的是
东
广
A.可用碘水检验淀粉是否完全水解
B.葡萄糖与果糖是同分异构体
C.可用红外光谱仪测定谷氨酸中所含官能团的种类
D.1mol谷氨酸单钠最多消耗2molNaOH
化学试题A 第2页(共8页)10.一种可完全生物降解的Zn-Mo原电池结构如下图所示。电池使用过程中在Zn表面形成一层ZnO薄膜,
下列说法正确的是
会
究
A.Mo作原电池负极
B.电子由Zn经电解质流向Mo
研
C.Zn表面发生的电极反应:Zn -2e−+H O =ZnO+2H+
2
考
D.电路中转移0.02mol电子时,理论上消耗1.3gZn
11.含硫化合物的反应具有多样性。下列有关反应的离子方程式书写错误的是
高
A.用Na SO 溶液吸收SO 废气:SO 2−+SO +H₂O=2HSO −
2 3 2 3 2 3
B.海水提溴工艺中用SO 水溶液省还原Br :Br +SO +H₂O=H SO +2HBr
2 2 2 2 2 3
C.用Na CO 溶液处理锅炉水垢中的CaSO :CaSO (s)+CO 2−(aq)=CaCO (s)+SO 2−(aq)
2 3 4 4 3 3 4
东
D.Na S O 在酸性条件下分解:S O 2−+2H+=SO ↑+S↓+H₂O
2 2 3 2 3 2
12.下列陈述 I 与陈述广II 均正确,且具有因果关系的是
选项 陈述 I 陈述 II
A 工业合成氨中使用铁触媒调控反应 铁触媒能提高H 的平衡转化率
2
B AgCl 固体可完全溶于氨水 Ag+与NH 形成可溶的[Ag(NH ) ]+
3 3 2
C 港珠澳大桥的钢结构表面涂上了树脂涂料 钢铁在海水中易发生析氢腐蚀
D 甲苯能使酸性KMnO 溶液褪色 甲苯分子中含有会碳碳双键
4
13.由短周期非金属主族元素组成的化合物M E X Y 可治疗心绞痛。E、M、X、Y原子序数依次增大,
17 18 2 6
究
M的一种核素常用于测定文物的年代,E的基态原子最外层只有一种自旋方向的电子,Y元素原子的价层
电子排布式是nsnnp2n。下列说法一定正确的是 研
A.氢化物沸点:Y>M
考
B.元素的电负性:X0
广
B.曲线Y表示c(C H )随温度的变化关系
2 4
C.升高温度,v 加快,v 减慢,C H 平衡产率减小
逆 正 2 4
D.其他条件不变,2nmolCO 与6nmolH 在T₁℃下反应,
2 2
达到平衡时c(H )>c mol·L−1
2 1
化学试题A 第3页(共8页)15.化学兴趣小组采用次氯酸钙与稀盐酸反应制取氯气,并探究了氯气的性质。实验装置如图所示,下列
说法正确的是
A.湿润的 pH 试纸先变红后褪色,说明 Cl
2
会
有酸性和漂白性
B.f处出现红色沉淀是因为Fe2+被氧化为Fe3+,
究
Fe3+遇KSCN生成弱电解质Fe(SCN)
3
研
C.g处变为橙色,h处变为黄色,说明元素
非金属性:Cl>Br>I
考 i
D.等量Cl 分别单独缓慢通过g、h、i试管时,
2 i
生成的氧化产物的物质的量之比为1:1:1 高
16.我国多条高压直流电线路的瓷绝缘子出现铁帽腐蚀现象。在铁帽上加锌环能有效防止铁帽的腐蚀,防
省
护原理如图所示。下列说法错误的是
东
广
A.通电时,锌环是阳极,发生氧化反应
B.通电时,阴极上的电极反应为2H O+2e-=H ↑+2OH-
2 2
C.断电时,锌环上的电极反应为Zn2++2e-=Zn
会
D.断电和通电时,防止铁帽被腐蚀的化学原理不完全相同
究
二、非选择题:本题共4大题,共56分。
研
17.(14分)某学习小组按下图流程,在实验室模拟处理含苯酚的工业废水,并进行相关实验探究。
考
回答下列问题:
溶液
高
省
东
(1)操作I的名称是 。操作I、Ⅱ、Ⅲ共同用到的玻璃仪器除烧杯外还有 (填名称),流程
广
中可循环使用的物质是 。
(2)“水层2”中主要溶质为 (填化学式),其在生活中主要用途是 (填一个即可)。
化学试题A 第4页(共8页)(3)将所得苯酚配制成一定浓度的苯酚溶液,探究铁盐种类和pH对苯酚与Fe3+显色反应的影响。
查阅资料 i.[Fe(C H O) ]3−为紫色:
6 5 6
ii.Na+对苯酚与Fe3+的显色反应无影响;
会
ⅲ.[Fe(C H O) ]3−对特定波长光的吸收程度(用吸光度A表示)与[Fe(C H O) ]3−的浓度在一定范
6 5 6 6 5 6
围内成正比。 究
提出猜想 猜想1:Cl−对苯酚与Fe3+的显色反应有影响。
研
猜想2:SO 2−对苯酚与Fe3+的显色反应有影响。
4
猜想3:H+对苯酚与Fe3+的显色反应有
考
影响。
进行实验 常温下,用盐酸调节pH配制得到pH分别为a和b的0.1mol·L−1FeCl 溶液(a>b),用硫酸调节
3
高
pH配制得到pH分别为a和b的0.05mol·L−1Fe (SO ) 溶液。取5mL苯酚溶液于试管中,按实验1~4分别
2 4 3
再加入0.1mL含Fe3+的试剂,显色 省10min后用紫外-可见分光光度计测定该溶液的吸光度(本实验条件下,
pH改变对Fe3+水解程度的影响可忽略)。
东
序
含Fe3+试剂 含Fe3+的试剂
号 吸光度
广
0.1mol·L−1FeCl 溶液 0.05mol·L−1Fe (SO ) 溶液
3 2 4 3
A
1 pH=a / 1
5mL
苯酚 2 pH=b / A 2
溶液
A
3 / pH=a 3
会A
4
4 / pH=b
结果讨论 实验结果为A >A >A >A 。
1 2 3 4 究
①小组同学认为根据结果“A >A ”不足以证明猜想3成立的理由是 。
2 3
研
②为进一步验证猜想,小组同学设计了实验5和6,补充下表中相关内容。
(限选试剂:NaCl溶液、Na SO 溶液、NaCl固体、Na SO 固体)
2 考4 2 4
含Fe3+试剂 序 含Fe3+的试剂
高 再加入的试剂 吸光度
号
mol·L−1FeCl 溶液 mol·L−1Fe (SO ) 溶液
3 2 4 3
省
5 / pH=a NaCl固体 A
5mL 5
苯酚
溶液 东
6 pH=a / A
6
广
③根据实验1~6的结果,小组同学得出猜想1不成立,猜想2成立,且SO 2-对苯酚与Fe3+的显色反应起抑
4
制作用,得出此结论的依据是 。
④根据实验1~6的结果,小组同学得出猜想3成立,且H+对苯酚与Fe3+的显色反应有抑制作用,从化学平
衡角度解释其原因是 。
化学试题A 第5页(共8页)18.(14分)镍是重要战略金属资源,一种从某高镁低品位铜镍矿(主要成分为CuFeS 、FeS 、3NiO·4SiO ·H₂O、
2 2 2
3MgO·4SiO ·H O等)中回收 Cu、Ni 的工艺流程如图所示:
2 2
会
究
研
S、SiO2
考
已知:K [Ni(OH) ]=2×10-15 高
sp 2
回答下列问题:
省
(1)NaFe (SO ) (OH) 中,Fe元素的化合价为 。
3 4 2 6
(2)为提高“氧压浸出”的速率,可行的操作有 (任填一个)。
东
(3)“氧压浸出”中CuFeS 发生的化学反应方程式为 。
2
广
(4)“沉铁”时加入MgO先是除去过量的H+,后是调节溶液pH促使沉铁进行,沉铁反应的离子方程式
为 。
(5)“滤液”中c(Ni2+)=0.2mol·L−1,“沉镍”时控制pH为8.50,此时Ni2+的沉淀率为 。(结果保
留1位小数)
(6)NiAs的立方晶胞结构如图所示。
会
究
A
研
考
①Ni3+的价电子排布图为 。
高
②与A点处的Ni3+距离最近且相等的As3−有________个。
③设NiAs晶体最简式的式量为 省M
r
,晶体密度为ρg·cm-3,则该晶胞中最近的Ni3+之间的距离为
________nm。(列出计算式,N 为阿伏加德罗常数的值)。
A
东
广
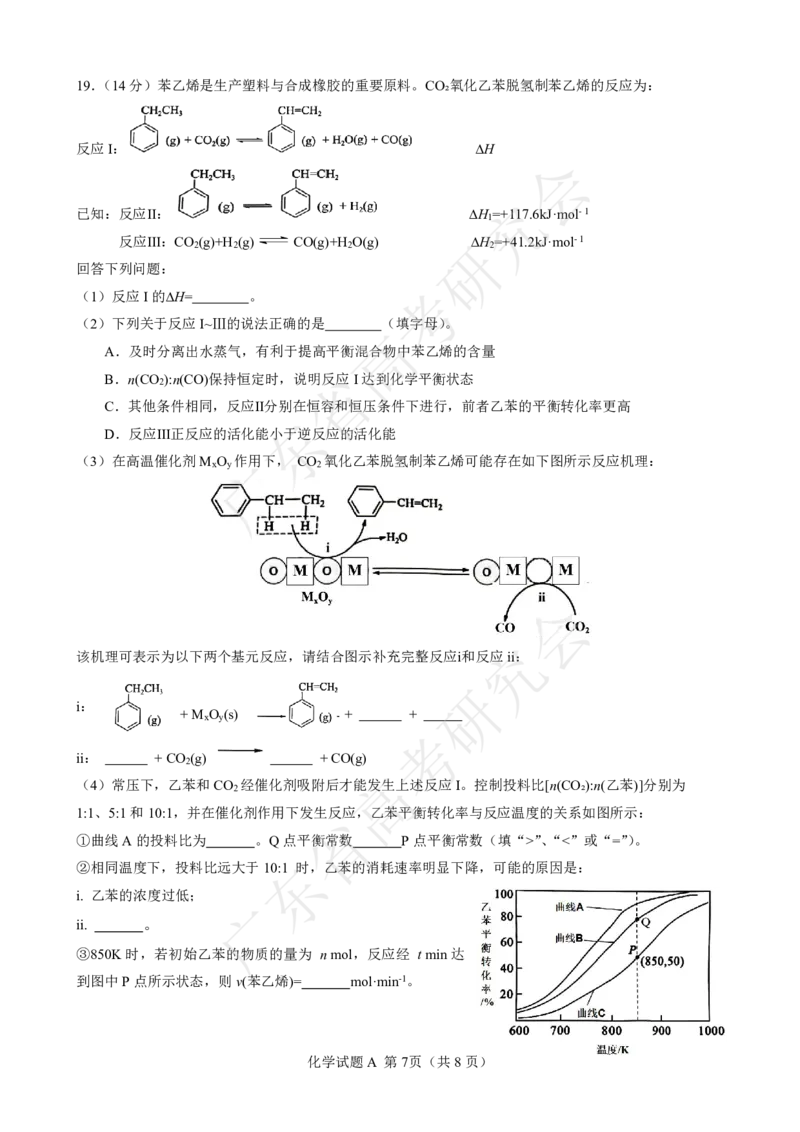
化学试题A 第6页(共8页)19.(14分)苯乙烯是生产塑料与合成橡胶的重要原料。CO₂氧化乙苯脱氢制苯乙烯的反应为:
反应I: ∆H
会
究
已知:反应Ⅱ: ∆H =+117.6kJ·mol-1
1
反应Ⅲ:CO
2
(g)+H
2
(g) CO(g)+H
2
O(g) 研∆H
2
=+41.2kJ·mol-1
回答下列问题:
考
(1)反应I的∆H= 。
(2)下列关于反应I~Ⅲ的说法正确的是 (填字母)。
高
A.及时分离出水蒸气,有利于提高平衡混合物中苯乙烯的含量
B.n(CO ):n(CO)保持恒定时,说省明反应I达到化学平衡状态
2
C.其他条件相同,反应Ⅱ分别在恒容和恒压条件下进行,前者乙苯的平衡转化率更高
东
D.反应Ⅲ正反应的活化能小于逆反应的活化能
(3)在高温催化剂M广O 作用下, CO 氧化乙苯脱氢制苯乙烯可能存在如下图所示反应机理:
x y 2
会
究
该机理可表示为以下两个基元反应,请结合图示补充完整反应ⅰ和反应ii:
研
i:
+M O (s) + +
x y
考
ii: +CO (g) +CO(g)
2
高
(4)常压下,乙苯和CO 经催化剂吸附后才能发生上述反应I。控制投料比[n(CO₂):n(乙苯)]分别为
2
1:1、5:1和10:1,并在催化剂作用下
省
发生反应,乙苯平衡转化率与反应温度的关系如图所示:
①曲线A的投料比为 。Q点平衡常数 P点平衡常数(填“>”、“<”或“=”)。
东
②相同温度下,投料比远大于10:1 时,乙苯的消耗速率明显下降,可能的原因是:
i. 乙苯的浓度过低;
广
ii. 。
③850K时,若初始乙苯的物质的量为 nmol,反应经 tmin达
到图中P点所示状态,则v(苯乙烯)= mol·min-1。
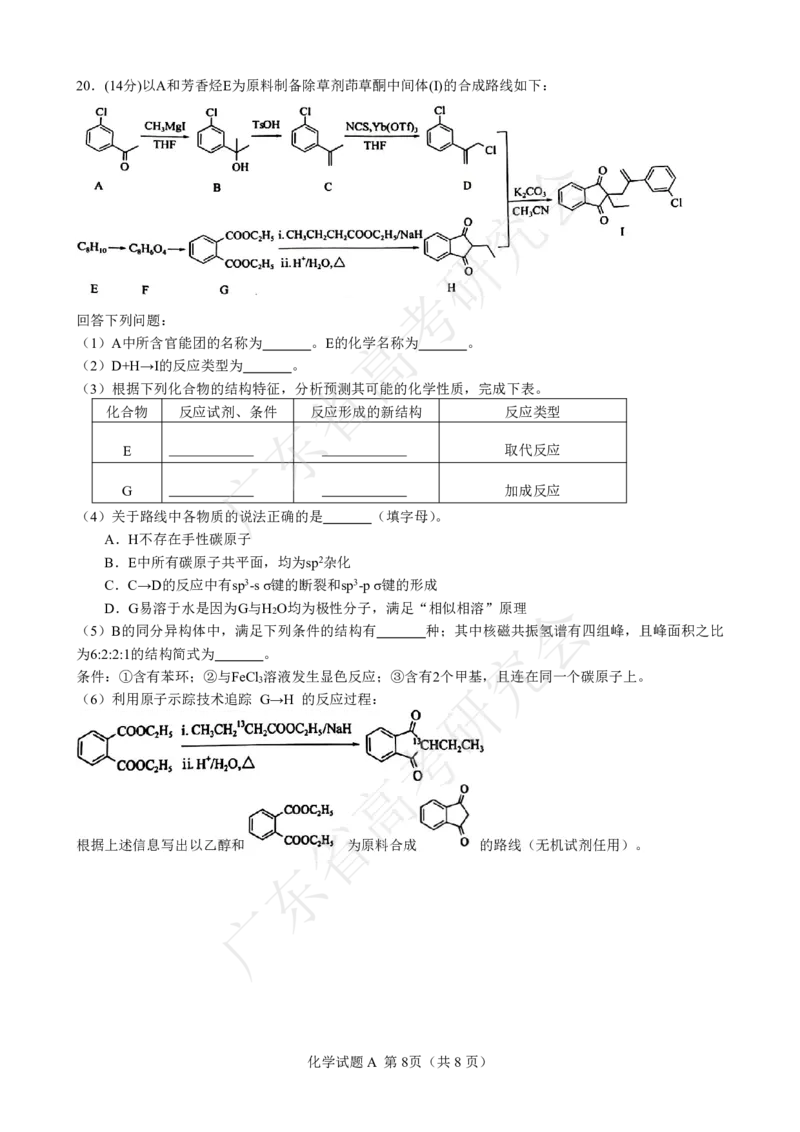
化学试题A 第7页(共8页)20.(14分)以A和芳香烃E为原料制备除草剂茚草酮中间体(Ⅰ)的合成路线如下:
会
究
研
考
回答下列问题:
高
(1)A中所含官能团的名称为 。E的化学名称为 。
(2)D+H→I的反应类型为 。
省
(3)根据下列化合物的结构特征,分析预测其可能的化学性质,完成下表。
化合物 反应试剂、条件 反应形成的新结构 反应类型
东
E 取代反应
广
G 加成反应
(4)关于路线中各物质的说法正确的是 (填字母)。
A.H不存在手性碳原子
B.E中所有碳原子共平面,均为sp2杂化
C.C→D的反应中有sp3-sσ键的断裂和sp3-pσ键的形成
会
D.G易溶于水是因为G与H O均为极性分子,满足“相似相溶”原理
2
(5)B的同分异构体中,满足下列条件的结构有 种;其中核磁共振氢谱有四组峰,且峰面积之比
究
为6:2:2:1的结构简式为 。
条件:①含有苯环;②与FeCl 溶液发生显色反应;③含有2个甲基,且连在同一个碳原子上。
3
研
(6)利用原子示踪技术追踪 G→H 的反应过程:
考
高
省
根据上述信息写出以乙醇和 为原料合成 的路线(无机试剂任用)。
东
广
化学试题A 第8页(共8页)