文档内容
5.1.1 硫及硫的氧化物(精练)
题组一 硫单质
1.(2021·辽宁·大连市第一中学高一期中)下列关于硫单质的叙述错误的是
A.硫(俗称硫黄)是一种黄色晶体 B.硫易溶于水,自然界中无单质硫存在
C.硫在空气中燃烧时生成二氧化硫 D.硫质脆,易研成粉末
2.(2021·黑龙江·哈师大附中高一期末)下列关于硫单质说法正确的是
A.硫单质是一种白色晶体 B.硫单质难溶于水
C.硫单质易溶于酒精 D.硫单质硬度大
3.(2021·云南·元阳县第一中学高一月考)下列说法中,不正确的是
A.硫是一种黄色、质脆的晶体
B.硫在反应中既可作氧化剂,又可作还原剂
C.硫易燃烧,其燃烧产物是大气污染物之一
D.硫与铁粉和铜粉分别反应,都可生成二价金属硫化物
4(2021·天津河北·高一期末)下列物质中的硫元素不能表现出还原性的是
A.HS B.SO C.HSO D.S
2 2 2 4
5.(2021·云南省华宁县第一中学高一期中)21 g铁粉与8 g硫粉混合加热,若不考虑其他损失,可生成硫
化亚铁的质量为
A.33 g B.24 g C.29 g D.22 g
6.(2021·上海市长征中学高一期中)下列有关硫的叙述中,错误的是
A.黑火药的成分中含硫 B.硫磺软膏可医治某些皮肤病
C.单质硫易溶于二硫化碳 D.单质硫只有氧化性
7.(2021·黑龙江·双鸭山一中高一月考)硫的氧化性不如氧气强,在下列叙述中不能说明这一事实的是
A.S+O SO ,O 是氧化剂、S是还原剂
2 2 2
B.S是淡黄色固体,O 是无色气体
2
C.氢硫酸放置在空气中易变浑浊(2H S+O=2S↓+2H O)
2 2 2
D.S和Cu反应只能生成Cu S(硫化亚铜),而O 与Cu反应生成CuO
2 2
8.(2021·吉林·延边朝鲜族自治州延边二中北校区高一期中)下列物质在一定条件下能够与硫黄发生反应,且硫作还原剂的是( )
A.O B.Fe C.H D.Cu
2 2
9.(2021·山西·太原市第五十六中学校高一月考)东汉魏伯阳在《周易参同契》中对汞的描述:“太阳流
珠,常欲去人……得火则飞,不见埃尘,将欲制之,黄芽为根。”这里的“黄芽”是指
A.金 B.硫磺 C.黄铜 D.黄铁矿
10.(2021·云南·罗平县第二中学高一月考)下列物质中,不能由单质通过化合反应得到的是
A.FeCl B.FeCl C.FeS D.Cu S
2 3 2
题组二 二氧化硫
1.(2021·辽宁·建平县实验中学高一期末)下列实验能说明SO 具有漂白性的是
2
A.SO 能使溴水褪色 B.SO 能使KMnO 溶液褪色
2 2 4
C.SO 能使滴有酚酞的NaOH溶液褪色 D.SO 能使品红溶液褪色
2 2
2.(2021·黑龙江·牡丹江市第十五中学高一期中)下列有关SO 的说法错误的是
2
A.可用澄清石灰水鉴别SO 和CO
2 2
B.SO 能使品红溶液褪色是因为它具有漂白性
2
C.将已被SO 漂白的品红溶液用酒精灯加热,可恢复原来的红色
2
D.SO 与O 混合加热,不能生成SO
2 2 3
3.(2021·北京市第五中学高一期中)I.利用下图装置制备 ,并研究 的性质。
(1)A装置利用亚硫酸钠和硫酸反应制备 ,写出化学方程式_______。
(2)填写下表
B中棉花的位置 ① ② ③ ④
所蘸试剂 石蕊试液 品红溶液 淀粉和碘水混合 氢硫酸液
现象 ___ ___ 褪色 浅黄色
体现 的性质 ___ ___ __ ___
(3) 和氯气按照体积比 通入水中,溶液的漂白性_______(填“增强”“减弱”“不变”)原因是
_______(用化学方程式表示)。
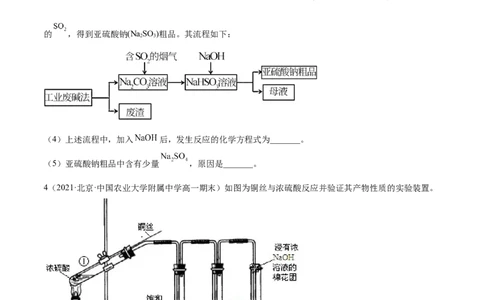
II.“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为 )吸收烟气中
的 ,得到亚硫酸钠(Na SO )粗品。其流程如下:
2 3
(4)上述流程中,加入 后,发生反应的化学方程式为_______。
(5)亚硫酸钠粗品中含有少量 ,原因是_______。
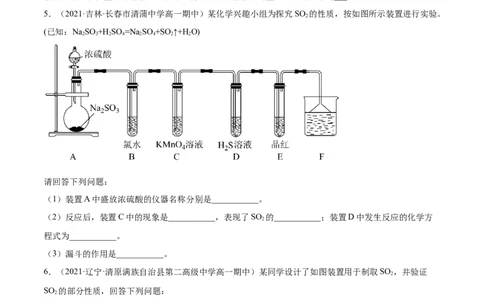
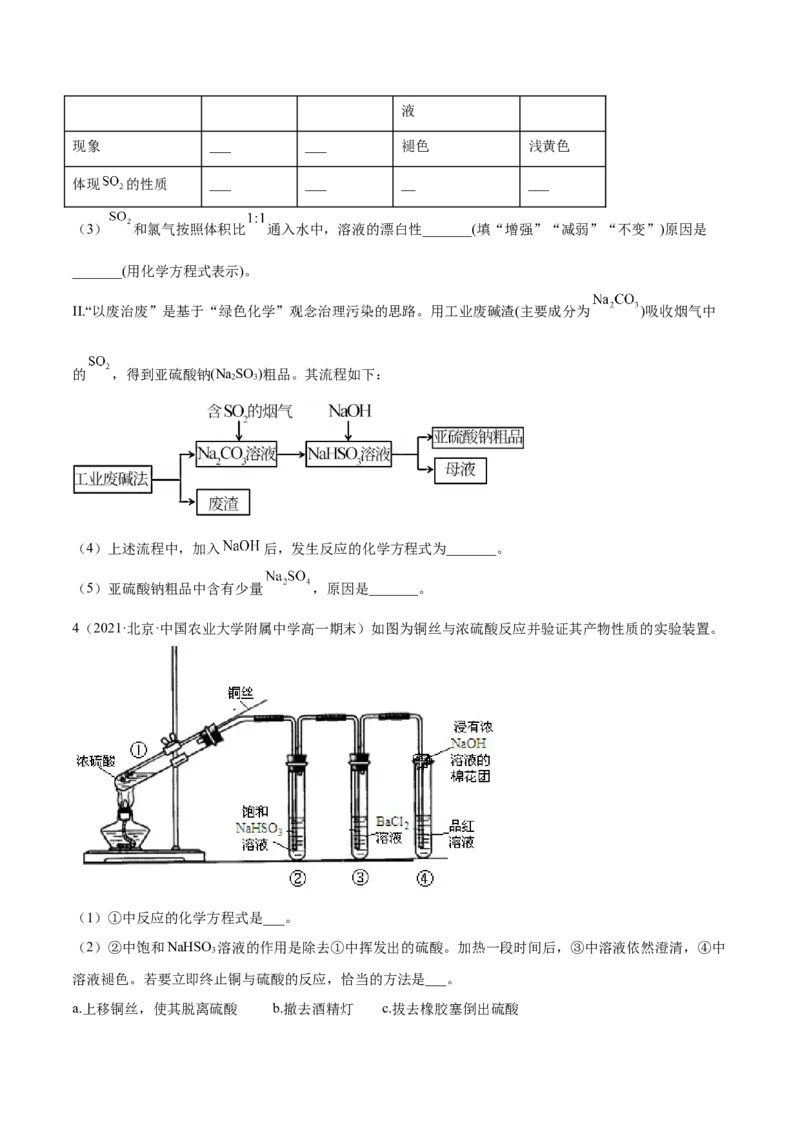
4(2021·北京·中国农业大学附属中学高一期末)如图为铜丝与浓硫酸反应并验证其产物性质的实验装置。
(1)①中反应的化学方程式是___。
(2)②中饱和NaHSO 溶液的作用是除去①中挥发出的硫酸。加热一段时间后,③中溶液依然澄清,④中
3
溶液褪色。若要立即终止铜与硫酸的反应,恰当的方法是___。
a.上移铜丝,使其脱离硫酸 b.撤去酒精灯 c.拔去橡胶塞倒出硫酸(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
加入试剂 现象 分析与解释
第一份 加入NaOH溶液 有白色沉淀生成 沉淀为___(写化学式)
第二份 加入氯水 有白色沉淀生成 沉淀为___(写化学式)
(4)④中棉花团的作用是___(用离子方程式表示)。
(5)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶
液呈蓝色。取少量蓝色溶液于试管中,滴加NaOH溶液至过量,出现的现象是___。
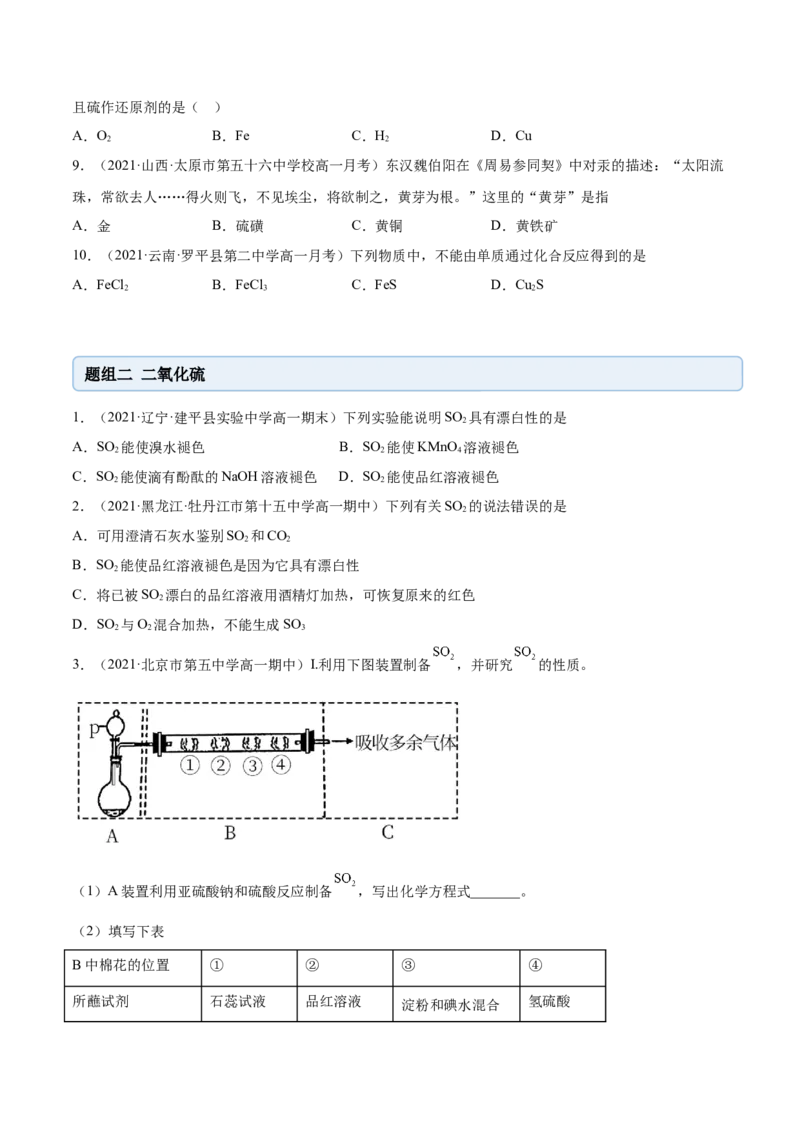
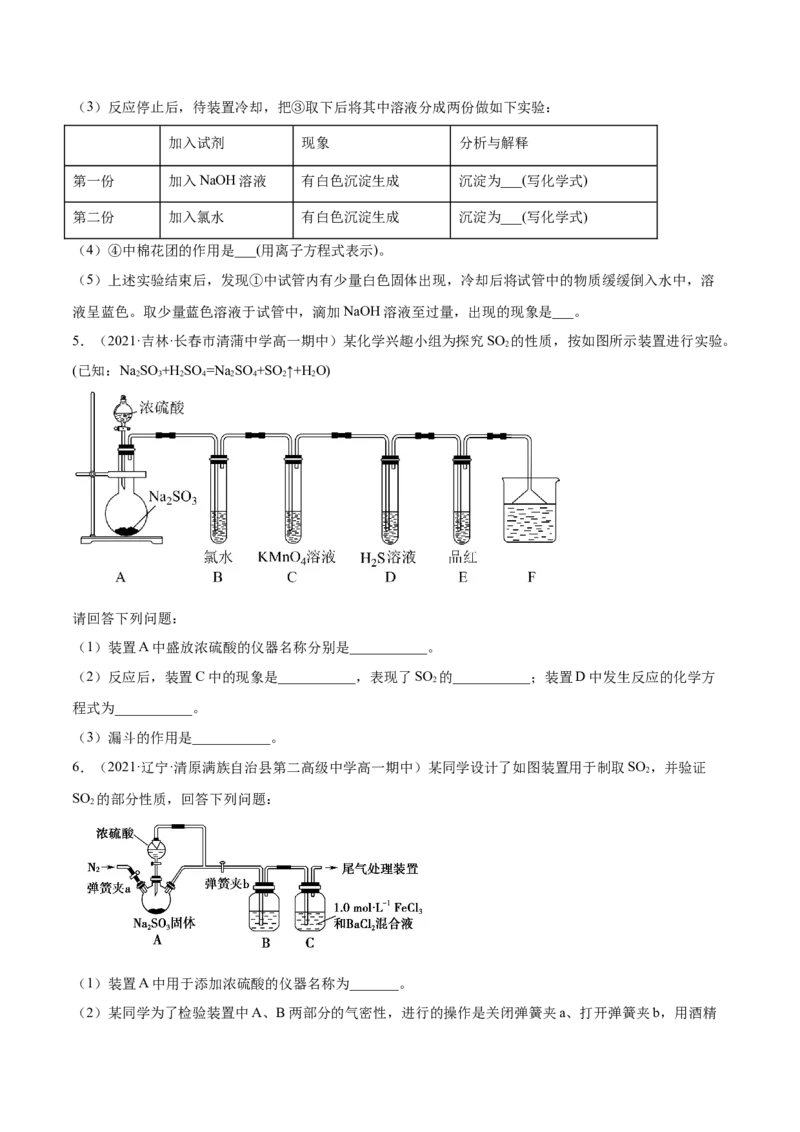
5.(2021·吉林·长春市清蒲中学高一期中)某化学兴趣小组为探究SO 的性质,按如图所示装置进行实验。
2
(已知:NaSO +H SO =Na SO +SO↑+H O)
2 3 2 4 2 4 2 2
请回答下列问题:
(1)装置A中盛放浓硫酸的仪器名称分别是___________。
(2)反应后,装置C中的现象是___________,表现了SO 的___________;装置D中发生反应的化学方
2
程式为___________。
(3)漏斗的作用是___________。
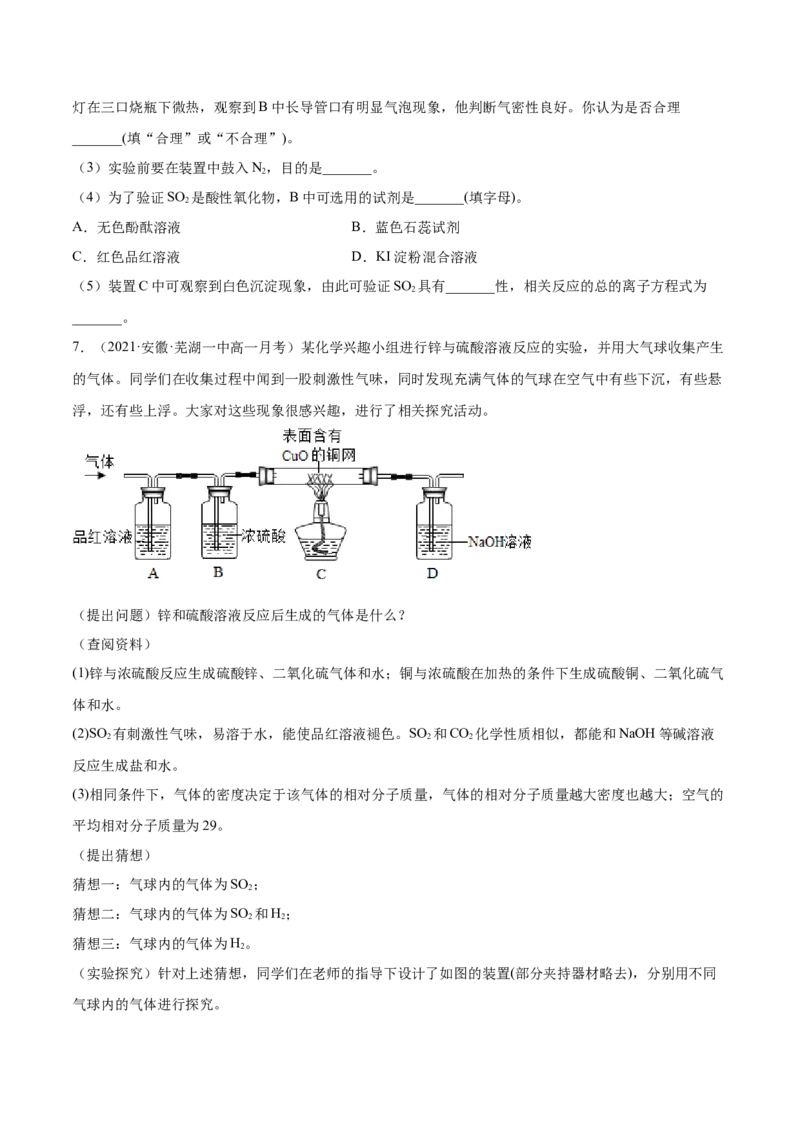
6.(2021·辽宁·清原满族自治县第二高级中学高一期中)某同学设计了如图装置用于制取SO ,并验证
2
SO 的部分性质,回答下列问题:
2
(1)装置A中用于添加浓硫酸的仪器名称为_______。
(2)某同学为了检验装置中A、B两部分的气密性,进行的操作是关闭弹簧夹a、打开弹簧夹b,用酒精灯在三口烧瓶下微热,观察到B中长导管口有明显气泡现象,他判断气密性良好。你认为是否合理
_______(填“合理”或“不合理”)。
(3)实验前要在装置中鼓入N,目的是_______。
2
(4)为了验证SO 是酸性氧化物,B中可选用的试剂是_______(填字母)。
2
A.无色酚酞溶液 B.蓝色石蕊试剂
C.红色品红溶液 D.KI淀粉混合溶液
(5)装置C中可观察到白色沉淀现象,由此可验证SO 具有_______性,相关反应的总的离子方程式为
2
_______。
7.(2021·安徽·芜湖一中高一月考)某化学兴趣小组进行锌与硫酸溶液反应的实验,并用大气球收集产生
的气体。同学们在收集过程中闻到一股刺激性气味,同时发现充满气体的气球在空气中有些下沉,有些悬
浮,还有些上浮。大家对这些现象很感兴趣,进行了相关探究活动。
(提出问题)锌和硫酸溶液反应后生成的气体是什么?
(查阅资料)
(1)锌与浓硫酸反应生成硫酸锌、二氧化硫气体和水;铜与浓硫酸在加热的条件下生成硫酸铜、二氧化硫气
体和水。
(2)SO 有刺激性气味,易溶于水,能使品红溶液褪色。SO 和CO 化学性质相似,都能和NaOH等碱溶液
2 2 2
反应生成盐和水。
(3)相同条件下,气体的密度决定于该气体的相对分子质量,气体的相对分子质量越大密度也越大;空气的
平均相对分子质量为29。
(提出猜想)
猜想一:气球内的气体为SO ;
2
猜想二:气球内的气体为SO 和H;
2 2
猜想三:气球内的气体为H。
2
(实验探究)针对上述猜想,同学们在老师的指导下设计了如图的装置(部分夹持器材略去),分别用不同
气球内的气体进行探究。(1)C装置在点燃酒精灯加热之前应先通一段时间的氮气,目的是___。
(2)甲同学观察到A中品红溶液褪色,C中无明显现象,说明猜想一正确。D瓶中氢氧化钠溶液的作用是
___。
(3)乙同学观察到___,说明猜想二正确。
(4)丙同学观察到A中品红溶液无明显现象,C中铜网表面黑色物质变红,说明猜想三正确。
(实验结论)通过实验探究与充分思考,聪明的你应该对锌与硫酸溶液反应产生的气体填充气球活动中的
异常现象能够很好的解释了。本次实验中锌粒与硫酸溶液反应先后生成二氧化硫气体和氢气。
(拓展反思)
(4)下列物质中不能由金属和稀硫酸反应直接得到的是___。
A.Al (SO ) B.Fe (SO ) C.MgSO D.ZnSO
2 4 3 2 4 3 4 4
(5)浓硫酸与铜在加热的条件下反应生成硫酸铜、二氧化硫气体和水,而稀硫酸与铜即使加热也不能反
应。这说明:某溶液的化学性质除了与溶质的性质有关外,还可能与下列中的有关___(填序号)。
A.溶质的质量分数 B.溶液的质量
C.溶液的体积 D.溶质的相对分子质量
(6)锌与铜分别和浓硫酸在一定条件下都可以反应产生二氧化硫,若选择铜与浓硫酸在加热的条件下反
应制取二氧化硫气体,其优点是___。
(7)实验中下沉的气球内一定含有的气体是___。(填化学式)
8.(2021·重庆市清华中学校高一月考)二氧化硫具有漂白性,工业上常用二氧化硫来漂白纸浆、毛、丝、
草帽等。此外二氧化硫还能够抑制霉菌和细菌的滋生,可用作防腐剂,甲组同学拟利用Mg粉与浓硫酸反
应制取22.4L(标准状况下)SO 。实验方案设计如下:取 粉与 的浓硫酸(含
2
)混合,加热充分反应,待Mg粉全部溶解后,干燥并收集气体。
(1)写出Mg粉与浓硫酸反应制备 的化学方程式:_______。
(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为___(填
化学式)。
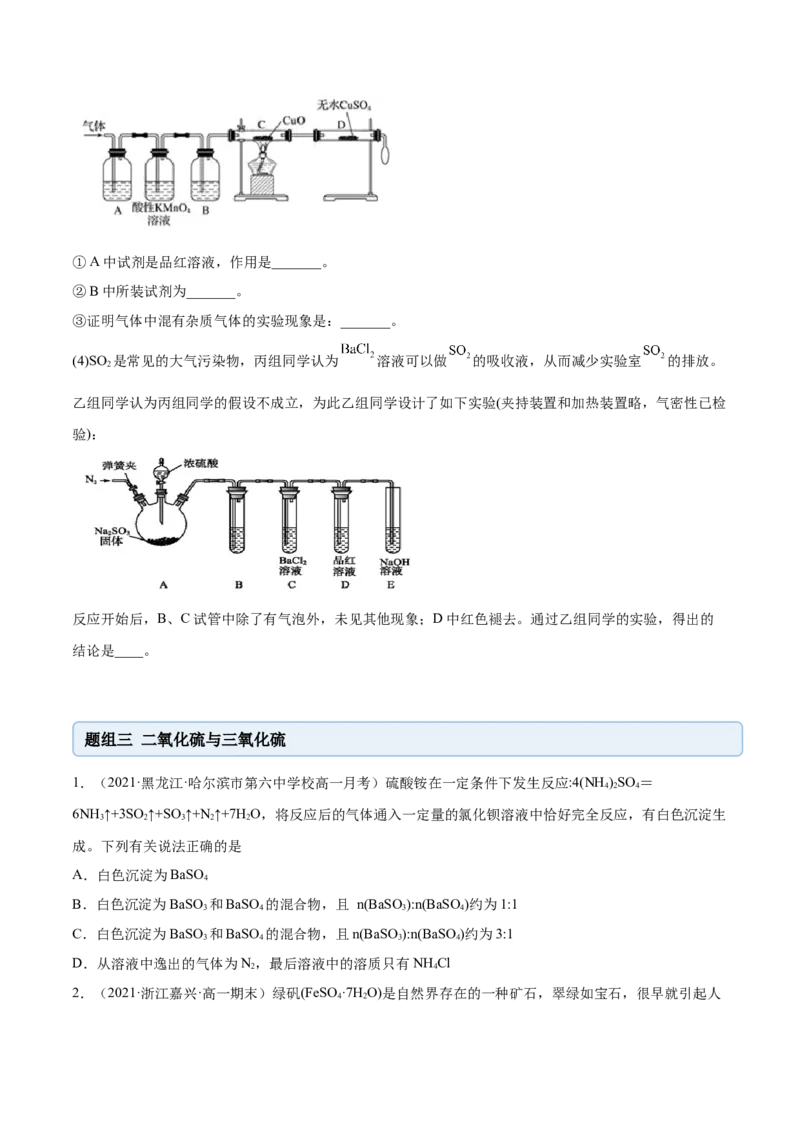
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实
验装置进行检验(已知酸性高锰酸钾溶液及B中试剂均过量)。①A中试剂是品红溶液,作用是_______。
②B中所装试剂为_______。
③证明气体中混有杂质气体的实验现象是:_______。
(4)SO 是常见的大气污染物,丙组同学认为 溶液可以做 的吸收液,从而减少实验室 的排放。
2
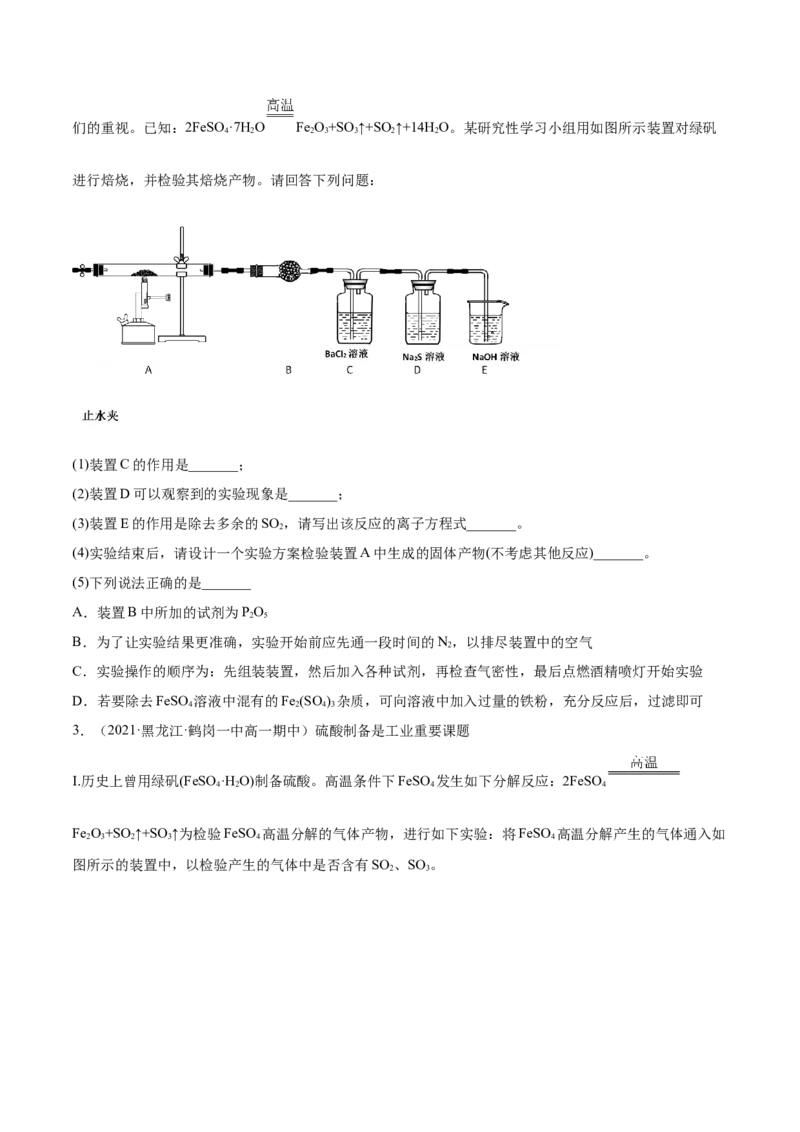
乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检
验):
反应开始后,B、C试管中除了有气泡外,未见其他现象;D中红色褪去。通过乙组同学的实验,得出的
结论是____。
题组三 二氧化硫与三氧化硫
1.(2021·黑龙江·哈尔滨市第六中学校高一月考)硫酸铵在一定条件下发生反应:4(NH )SO =
4 2 4
6NH ↑+3SO↑+SO↑+N ↑+7H O,将反应后的气体通入一定量的氯化钡溶液中恰好完全反应,有白色沉淀生
3 2 3 2 2
成。下列有关说法正确的是
A.白色沉淀为BaSO
4
B.白色沉淀为BaSO 和BaSO 的混合物,且 n(BaSO):n(BaSO)约为1:1
3 4 3 4
C.白色沉淀为BaSO 和BaSO 的混合物,且n(BaSO):n(BaSO)约为3:1
3 4 3 4
D.从溶液中逸出的气体为N,最后溶液中的溶质只有NH Cl
2 4
2.(2021·浙江嘉兴·高一期末)绿矾(FeSO ·7H O)是自然界存在的一种矿石,翠绿如宝石,很早就引起人
4 2们的重视。已知:2FeSO ·7H O Fe O+SO↑+SO↑+14H O。某研究性学习小组用如图所示装置对绿矾
4 2 2 3 3 2 2
进行焙烧,并检验其焙烧产物。请回答下列问题:
(1)装置C的作用是_______;
(2)装置D可以观察到的实验现象是_______;
(3)装置E的作用是除去多余的SO ,请写出该反应的离子方程式_______。
2
(4)实验结束后,请设计一个实验方案检验装置A中生成的固体产物(不考虑其他反应)_______。
(5)下列说法正确的是_______
A.装置B中所加的试剂为PO
2 5
B.为了让实验结果更准确,实验开始前应先通一段时间的N,以排尽装置中的空气
2
C.实验操作的顺序为:先组装装置,然后加入各种试剂,再检查气密性,最后点燃酒精喷灯开始实验
D.若要除去FeSO 溶液中混有的Fe (SO ) 杂质,可向溶液中加入过量的铁粉,充分反应后,过滤即可
4 2 4 3
3.(2021·黑龙江·鹤岗一中高一期中)硫酸制备是工业重要课题
Ⅰ.历史上曾用绿矾(FeSO ·H O)制备硫酸。高温条件下FeSO 发生如下分解反应:2FeSO
4 2 4 4
Fe O+SO↑+SO↑为检验FeSO 高温分解的气体产物,进行如下实验:将FeSO 高温分解产生的气体通入如
2 3 2 3 4 4
图所示的装置中,以检验产生的气体中是否含有SO 、SO 。
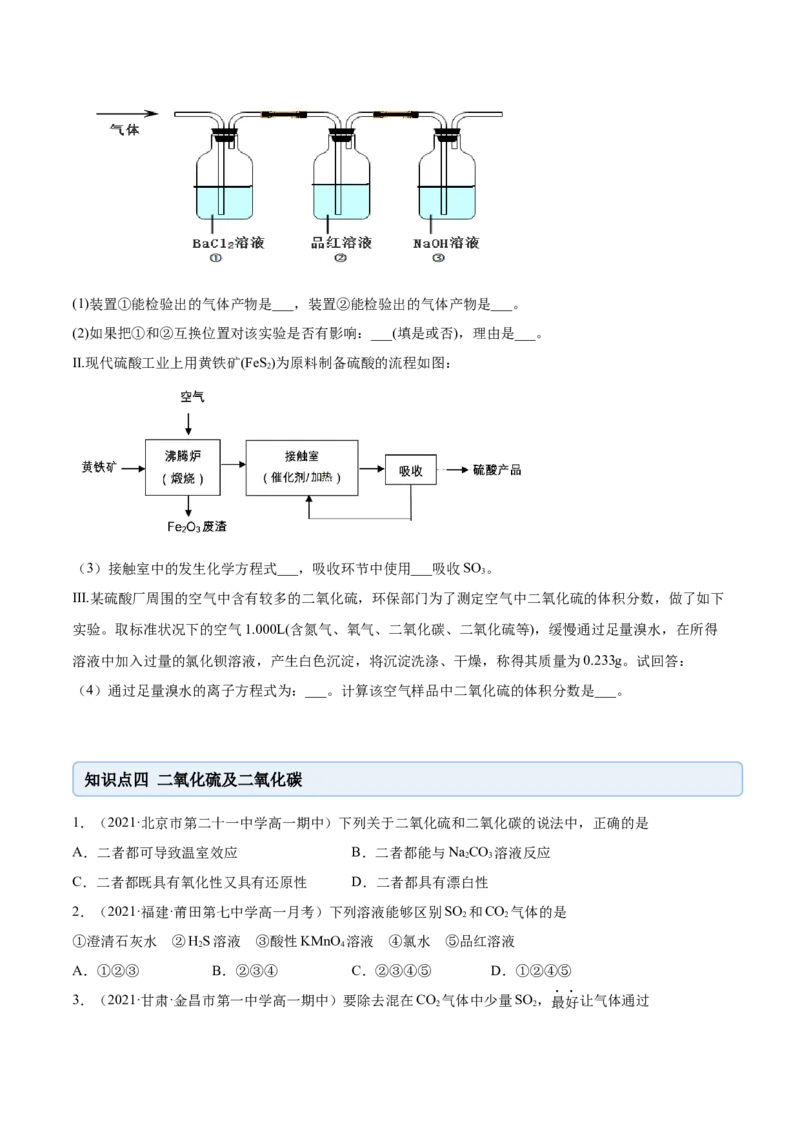
2 3(1)装置①能检验出的气体产物是___,装置②能检验出的气体产物是___。
(2)如果把①和②互换位置对该实验是否有影响:___(填是或否),理由是___。
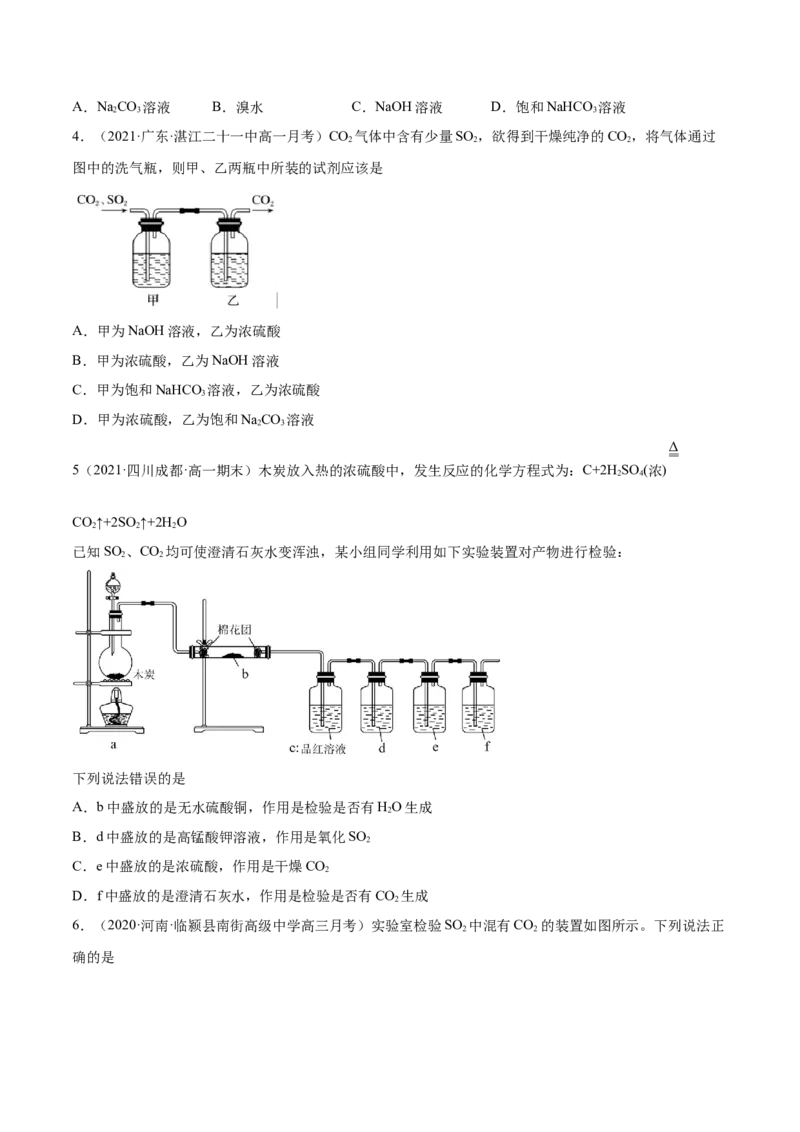
Ⅱ.现代硫酸工业上用黄铁矿(FeS )为原料制备硫酸的流程如图:
2
(3)接触室中的发生化学方程式___,吸收环节中使用___吸收SO 。
3
Ⅲ.某硫酸厂周围的空气中含有较多的二氧化硫,环保部门为了测定空气中二氧化硫的体积分数,做了如下
实验。取标准状况下的空气1.000L(含氮气、氧气、二氧化碳、二氧化硫等),缓慢通过足量溴水,在所得
溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.233g。试回答:
(4)通过足量溴水的离子方程式为:___。计算该空气样品中二氧化硫的体积分数是___。
知识点四 二氧化硫及二氧化碳
1.(2021·北京市第二十一中学高一期中)下列关于二氧化硫和二氧化碳的说法中,正确的是
A.二者都可导致温室效应 B.二者都能与NaCO 溶液反应
2 3
C.二者都既具有氧化性又具有还原性 D.二者都具有漂白性
2.(2021·福建·莆田第七中学高一月考)下列溶液能够区别SO 和CO 气体的是
2 2
①澄清石灰水 ②HS溶液 ③酸性KMnO 溶液 ④氯水 ⑤品红溶液
2 4
A.①②③ B.②③④ C.②③④⑤ D.①②④⑤
3.(2021·甘肃·金昌市第一中学高一期中)要除去混在CO 气体中少量SO ,最好让气体通过
2 2A.NaCO 溶液 B.溴水 C.NaOH溶液 D.饱和NaHCO 溶液
2 3 3
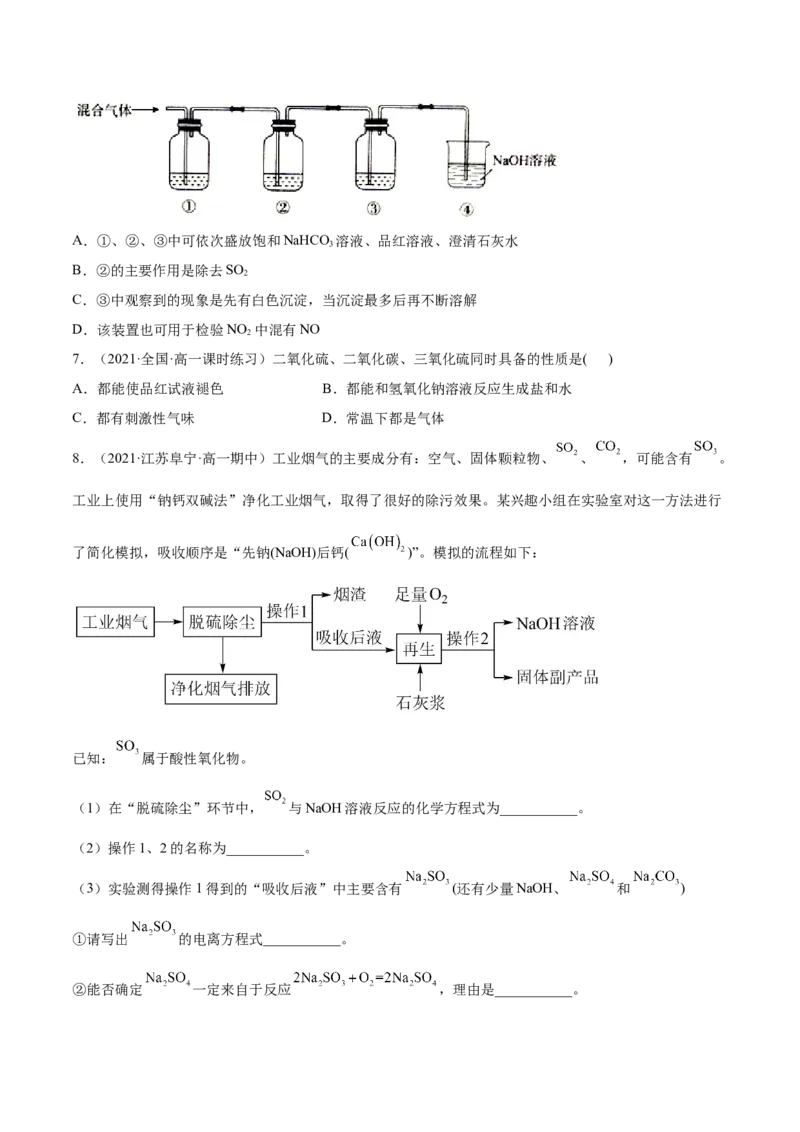
4.(2021·广东·湛江二十一中高一月考)CO 气体中含有少量SO ,欲得到干燥纯净的CO,将气体通过
2 2 2
图中的洗气瓶,则甲、乙两瓶中所装的试剂应该是
A.甲为NaOH溶液,乙为浓硫酸
B.甲为浓硫酸,乙为NaOH溶液
C.甲为饱和NaHCO 溶液,乙为浓硫酸
3
D.甲为浓硫酸,乙为饱和NaCO 溶液
2 3
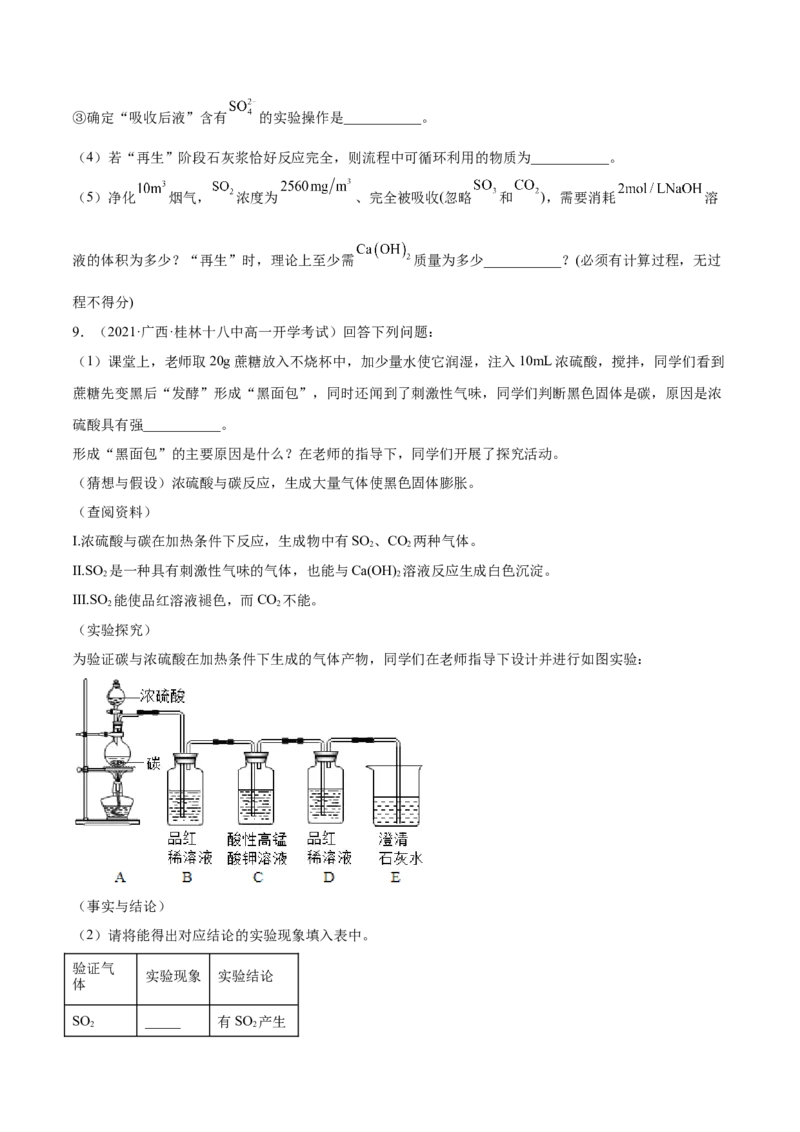
5(2021·四川成都·高一期末)木炭放入热的浓硫酸中,发生反应的化学方程式为:C+2H SO (浓)
2 4
CO↑+2SO↑+2H O
2 2 2
已知SO 、CO 均可使澄清石灰水变浑浊,某小组同学利用如下实验装置对产物进行检验:
2 2
下列说法错误的是
A.b中盛放的是无水硫酸铜,作用是检验是否有HO生成
2
B.d中盛放的是高锰酸钾溶液,作用是氧化SO
2
C.e中盛放的是浓硫酸,作用是干燥CO
2
D.f中盛放的是澄清石灰水,作用是检验是否有CO 生成
2
6.(2020·河南·临颍县南街高级中学高三月考)实验室检验SO 中混有CO 的装置如图所示。下列说法正
2 2
确的是A.①、②、③中可依次盛放饱和NaHCO 溶液、品红溶液、澄清石灰水
3
B.②的主要作用是除去SO
2
C.③中观察到的现象是先有白色沉淀,当沉淀最多后再不断溶解
D.该装置也可用于检验NO 中混有NO
2
7.(2021·全国·高一课时练习)二氧化硫、二氧化碳、三氧化硫同时具备的性质是( )
A.都能使品红试液褪色 B.都能和氢氧化钠溶液反应生成盐和水
C.都有刺激性气味 D.常温下都是气体
8.(2021·江苏阜宁·高一期中)工业烟气的主要成分有:空气、固体颗粒物、 、 ,可能含有 。
工业上使用“钠钙双碱法”净化工业烟气,取得了很好的除污效果。某兴趣小组在实验室对这一方法进行
了简化模拟,吸收顺序是“先钠(NaOH)后钙( )”。模拟的流程如下:
已知: 属于酸性氧化物。
(1)在“脱硫除尘”环节中, 与NaOH溶液反应的化学方程式为___________。
(2)操作1、2的名称为___________。
(3)实验测得操作1得到的“吸收后液”中主要含有 (还有少量NaOH、 和 )
①请写出 的电离方程式___________。
②能否确定 一定来自于反应 ,理由是___________。③确定“吸收后液”含有 的实验操作是___________。
(4)若“再生”阶段石灰浆恰好反应完全,则流程中可循环利用的物质为___________。
(5)净化 烟气, 浓度为 、完全被吸收(忽略 和 ),需要消耗 溶
液的体积为多少?“再生”时,理论上至少需 质量为多少___________?(必须有计算过程,无过
程不得分)
9.(2021·广西·桂林十八中高一开学考试)回答下列问题:
(1)课堂上,老师取20g蔗糖放入不烧杯中,加少量水使它润湿,注入10mL浓硫酸,搅拌,同学们看到
蔗糖先变黑后“发酵”形成“黑面包”,同时还闻到了刺激性气味,同学们判断黑色固体是碳,原因是浓
硫酸具有强___________。
形成“黑面包”的主要原因是什么?在老师的指导下,同学们开展了探究活动。
(猜想与假设)浓硫酸与碳反应,生成大量气体使黑色固体膨胀。
(查阅资料)
Ⅰ.浓硫酸与碳在加热条件下反应,生成物中有SO 、CO 两种气体。
2 2
Ⅱ.SO 是一种具有刺激性气味的气体,也能与Ca(OH) 溶液反应生成白色沉淀。
2 2
Ⅲ.SO 能使品红溶液褪色,而CO 不能。
2 2
(实验探究)
为验证碳与浓硫酸在加热条件下生成的气体产物,同学们在老师指导下设计并进行如图实验:
(事实与结论)
(2)请将能得出对应结论的实验现象填入表中。
验证气
实验现象 实验结论
体
SO _____ 有SO 产生
2 2CO _____ 有CO 产生
2 2
(3)碳与浓硫酸反应的化学方程式是___________。;浓硫酸与碳在加热条件下产生大量的SO 和CO,使
2 2
黑色固体膨胀,形成“黑面包”,猜想成立。
(反思与交流)
(4)小明同学提出,因老师的演示实验没有进行加热,所以同学们的探究实验无意义,其他同学一致否
定了他的说法,理由是___________。
(5)若B、E中试剂交换,___________(填“能”或“不能”)得出有CO 产生的结论,理由是
2
___________。
(6)C中酸性高锰酸钾溶液的作用是___________。倒卖拉黑不更新,淘宝唯一免费更新店铺:知二教育