文档内容
第一章 有机化合物的结构特点与研究方法
第二节 研究有机化合物的一般方法
1.2.1 分离、提纯
一、选择题
1. 海水淡化可解决淡水资源缺乏的问题。下列可应用于海水淡化技术的操作是( )
A. 蒸馏 B. 过滤 C. 萃取 D. 结晶
【答案】A
【解析】
A.海水中含有可溶性的电解质,从海水中获得溶剂水,需要通过蒸馏的操作,故A正确;
B.海水中含有可溶性的电解质,过滤得不到淡化水,故B错误;
C.萃取不能除去海水中的盐分,故C错误;
D.要获得淡化水,而不是提取海水中的盐分,所以不能采用结晶的方法,故D错误。
故选:A。
2. 下列实验操作中正确的是( )
A. 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B. 蒸馏操作时,应使温度计的水银球插入蒸馏烧瓶溶液中
C. 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
【答案】C
【解析】
蒸发时不能蒸干,则出现大量固体时停止加热,故A错误;
B.蒸馏时温度计测定馏分的温度,则温度计的水银球在蒸馏烧瓶的支管口处,故B错误;
C.分液时避免上下层液体混合,则分液漏斗中下层液体从下口放出,上层液体从上口倒出,故C正
确;
D.萃取时,溶质在不同溶剂中的溶解性不同,且不反应,溶剂互不相溶,不需要考虑密度,故 D错
误;
故选:C。
3. 提纯下列物质 括号中为少量杂质 ,选择试剂和分离方法都正确的是( )被提纯的物质 除杂试剂 分离方法
A. 甲烷 乙烯 酸性高锰酸钾溶液 洗气
B. 溴苯 氢氧化钠溶液 过滤
C. 乙酸 乙醇 饱和氢氧化钠溶液 过滤
D. 乙醇 生石灰 蒸馏
【解析】
A. 乙烯可以被高锰酸钾氧化为二氧化碳气体,引入了新杂质,故A错误;
B. 单质溴能与NaOH溶液反应生成溴化钠、次溴酸钠和水,溴化钠、次溴酸钠溶于水,溴苯不与
NaOH溶液反应也不溶于NaOH溶液,出现分层现象,用分液的方法分离,故B错误;
C. 乙醇溶于饱和氢氧化钠溶液,乙酸与氢氧化钠溶液反应得到溶于水的乙酸钠,不能除杂,故 C
错误;
D. 加入生石灰,水反应生成氢氧化钙,增大与乙醇的沸点差,可通过蒸馏将乙醇分离,故D正确。
故选D。
4. 下图是一些实验操作的装置,关于这些操作及装置的说法,正确的是( )
A. 甲为过滤装置,实验者用玻璃棒引流,且玻璃棒底端紧靠漏斗壁
B. 乙为蒸馏装置,实验者将蒸馏烧瓶置于水浴中,能更精确地控制温度;且冷凝管中的冷凝
水下进上出,利用逆流交换原理,冷却更充分
C. 丙为萃取操作,实验者用左手托住分液漏斗活塞,右手抵住玻璃塞,将分液漏斗按图所示
双手用力振荡,使液体混合
D. 丁为蒸发结晶装置,实验者用玻璃棒不断搅拌溶液,以促进液体挥发,烧杯底部垫上石棉
网,能让容器受热更加均匀
【答案】C
【解析】
A.玻璃棒靠紧三层滤纸,故A错误;
B.温度计测定馏分的温度,则温度计水银球应该置于蒸馏烧瓶支管口处,故B错误;
C.丙为萃取操作,实验者用左手托住分液漏斗活塞,右手抵住玻璃塞,将分液漏斗按图所示双手用力振荡,使液体混合,故C正确;
D.蒸发结晶应在蒸发皿中进行,故D错误。
5. 下列关于物质的分离、提纯实验中的一些操作或做法,正确的是
A. 在组装蒸馏装置时,温度计的水银球应伸入液面下
B. 在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加少量蒸馏水
C. 用苯萃取溴水时有机层应从下口放出
D. 在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后,要冷却到常温才过滤
【答案】B
【解析】
A.蒸馏时,测定馏分的温度,则温度计的水银球应在蒸馏烧瓶支管口处,非伸入液面下,故A错误;
B.水在加热过程中会蒸发,苯甲酸能溶于水,减少过滤时苯甲酸的损失,防止过饱和提前析出结晶,
加热溶解后还要加少量蒸馏水,故B正确;
C.用苯萃取溴水时,有机层在上层,应从上口放出,故C错误;
D.在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后要趁热过滤。粗苯甲酸中如果存在不溶解的杂质,
必须加热到苯甲酸溶解以后,趁热抽滤除去这些不溶解的杂质,然后慢慢冷却到有晶体析出,故D
错误。
6. 下列说法正确的是
选项 实验目的 所选主要仪器 铁架台等忽略 部分操作
用 浓 硫 酸 配 制500mL 容量瓶、烧杯、玻璃将量取好的浓硫酸放入容量瓶
A
硫酸溶液 棒、量筒、胶头滴管 中,加水溶解至刻度线
坩埚、酒精灯、玻璃棒、泥三当加热至大量固体出现时,停
B 从食盐水中得到NaCl晶体
角、三脚架 止加热,利用余热加热
蒸馏烧瓶、酒精灯、温度计、直
C 分离甲醇和甘油的混合物 温度计水银球插入液面以下
形冷凝管、锥形瓶、牛角管
分离时下层液体从分液漏斗下
D 用 萃取溴水中的 分液漏斗、烧杯
口放出,上层液体从上口倒出
【答案】D
【解析】
A.应该在烧杯中稀释浓硫酸,不能直接在容量瓶中稀释,该操作方法不合理,故A错误;
B.从食盐水中得到NaCl晶体的操作为蒸发,蒸发食盐水应该在蒸发皿中进行,不需要坩埚,故 B
错误;
C.可以通过蒸馏操作分离甲醇和甘油的混合物,但温度计的水银球不能插入溶液,应该放在蒸馏烧
瓶的支管口处,故C错误;D. 易溶于 ,溴的四氯化碳溶液与水分层,可用 萃取溴水中的 ,用到分液漏斗、
烧杯,分离时下层液体从分液漏斗下口放出,上层液体从上口倒出,故D正确;
故选D。
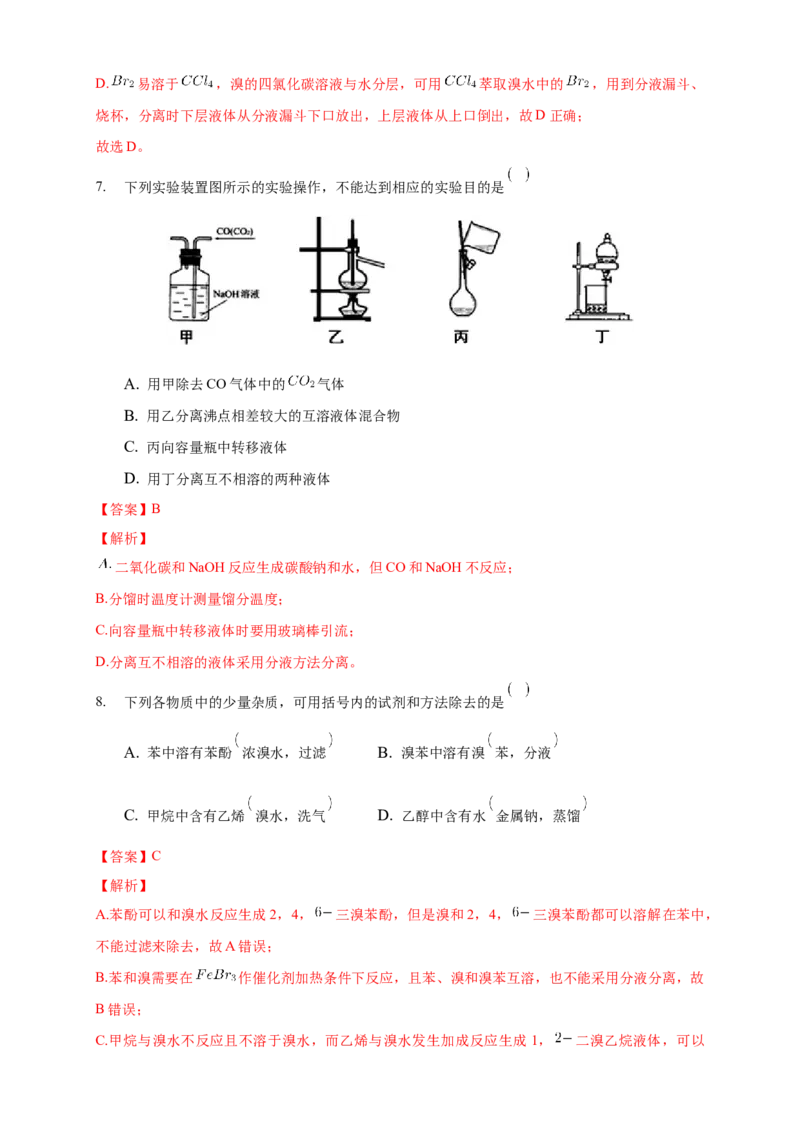
7. 下列实验装置图所示的实验操作,不能达到相应的实验目的是
A. 用甲除去CO气体中的 气体
B. 用乙分离沸点相差较大的互溶液体混合物
C. 丙向容量瓶中转移液体
D. 用丁分离互不相溶的两种液体
【答案】B
【解析】
二氧化碳和NaOH反应生成碳酸钠和水,但CO和NaOH不反应;
B.分馏时温度计测量馏分温度;
C.向容量瓶中转移液体时要用玻璃棒引流;
D.分离互不相溶的液体采用分液方法分离。
8. 下列各物质中的少量杂质,可用括号内的试剂和方法除去的是
A. 苯中溶有苯酚 浓溴水,过滤 B. 溴苯中溶有溴 苯,分液
C. 甲烷中含有乙烯 溴水,洗气 D. 乙醇中含有水 金属钠,蒸馏
【答案】C
【解析】
A.苯酚可以和溴水反应生成2,4, 三溴苯酚,但是溴和2,4, 三溴苯酚都可以溶解在苯中,
不能过滤来除去,故A错误;
B.苯和溴需要在 作催化剂加热条件下反应,且苯、溴和溴苯互溶,也不能采用分液分离,故
B错误;
C.甲烷与溴水不反应且不溶于溴水,而乙烯与溴水发生加成反应生成1, 二溴乙烷液体,可以利用溴水洗气除去甲烷中混有的乙烯,故C正确;
D.乙醇和水都能够与金属钠反应,故D错误。
故选C。
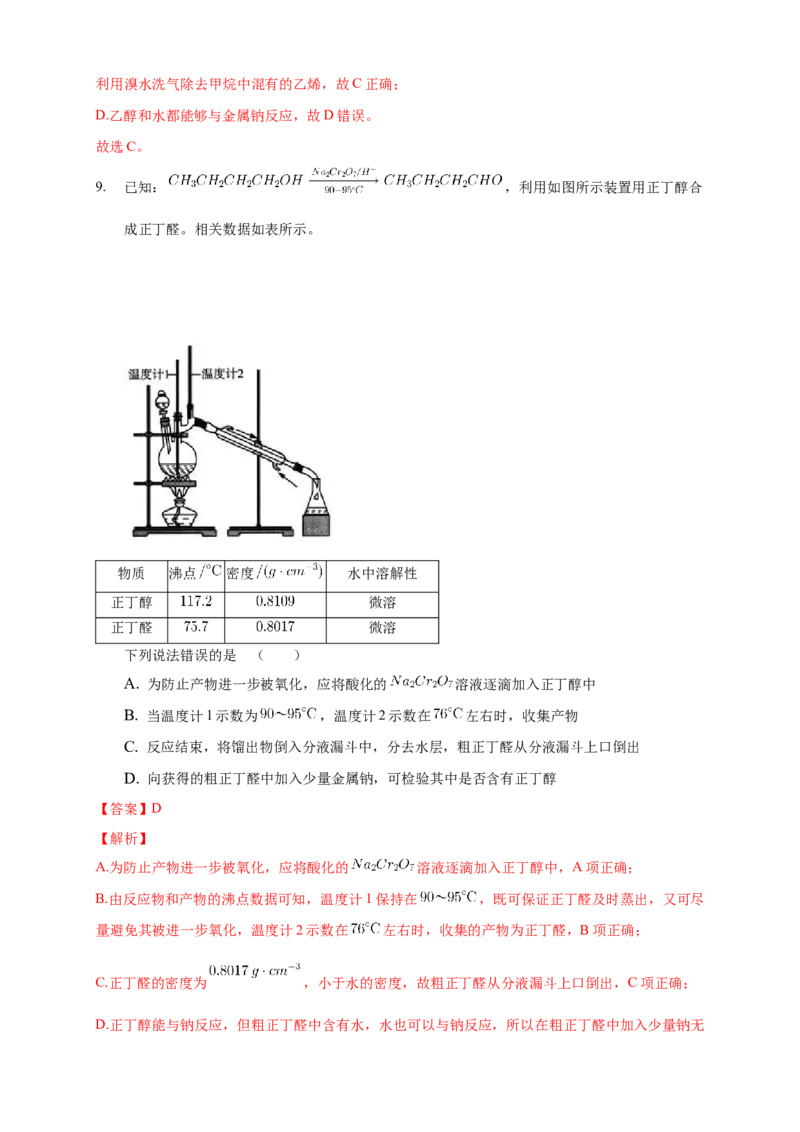
9. 已知: ,利用如图所示装置用正丁醇合
成正丁醛。相关数据如表所示。
物质 沸点 密度 水中溶解性
正丁醇 微溶
正丁醛 微溶
下列说法错误的是 ( )
A. 为防止产物进一步被氧化,应将酸化的 溶液逐滴加入正丁醇中
B. 当温度计1示数为 ,温度计2示数在 左右时,收集产物
C. 反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D. 向获得的粗正丁醛中加入少量金属钠,可检验其中是否含有正丁醇
【答案】D
【解析】
A.为防止产物进一步被氧化,应将酸化的 溶液逐滴加入正丁醇中,A项正确;
B.由反应物和产物的沸点数据可知,温度计1保持在 ,既可保证正丁醛及时蒸出,又可尽
量避免其被进一步氧化,温度计2示数在 左右时,收集的产物为正丁醛,B项正确;
C.正丁醛的密度为 ,小于水的密度,故粗正丁醛从分液漏斗上口倒出,C项正确;
D.正丁醇能与钠反应,但粗正丁醛中含有水,水也可以与钠反应,所以在粗正丁醛中加入少量钠无法检验其中是否含有正丁醇,D项错误。
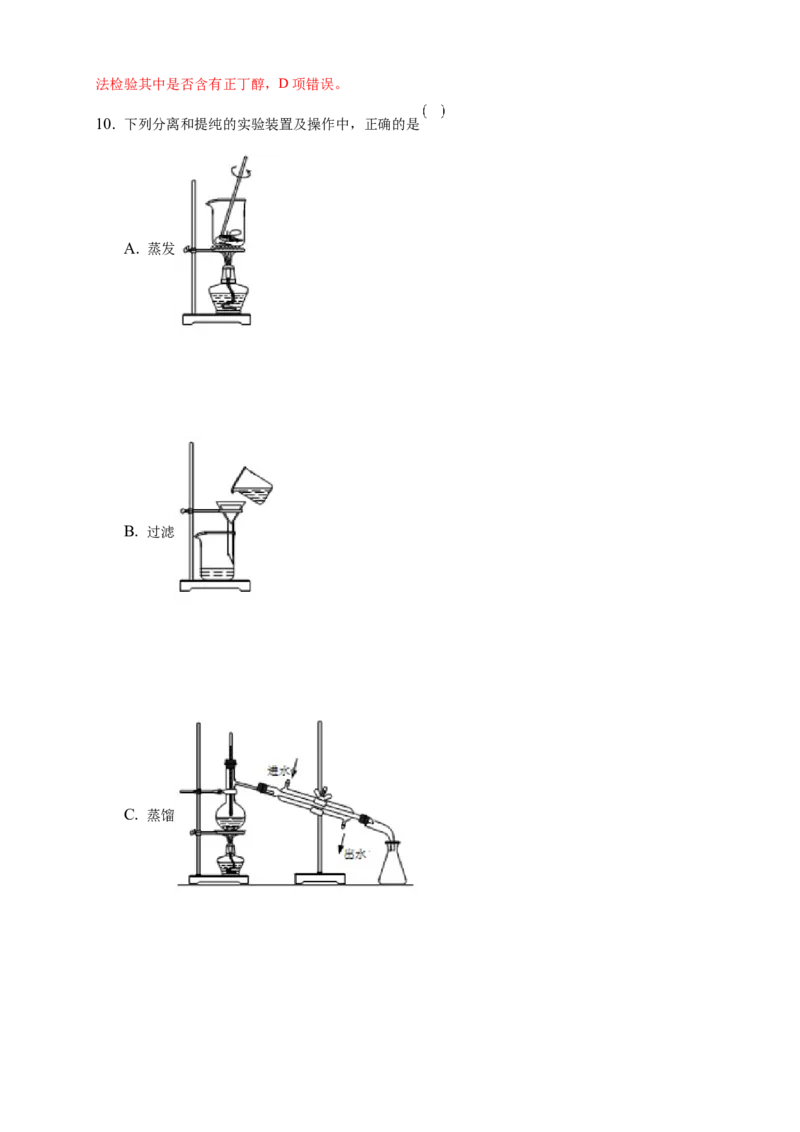
10. 下列分离和提纯的实验装置及操作中,正确的是
A. 蒸发
B. 过滤
C. 蒸馏D. 分液
【答案】D
【解析】
A.蒸发需要的仪器为蒸发皿,不能选烧杯,故A错误;
B.过滤需要玻璃棒引流,图中缺少玻璃棒,故B错误;
C.蒸馏时温度计测定馏分的温度、冷却水下进上出,则温度计的水银球应在支管口处,冷却水应下
口进水,故C错误;
D.利用分液漏斗分离分层的液体混合物,图中分液操作装置合理,故D正确。
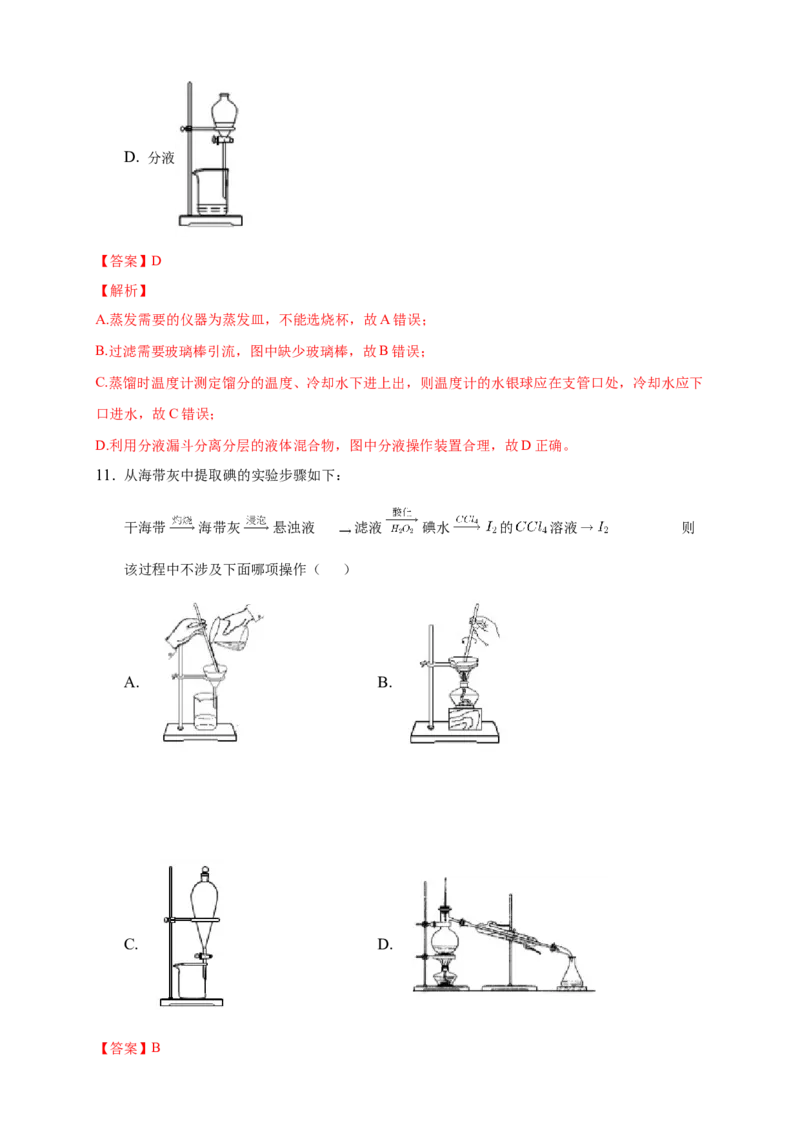
11. 从海带灰中提取碘的实验步骤如下:
干海带 海带灰 悬浊液 滤液 碘水 的 溶液 则
该过程中不涉及下面哪项操作( )
A. B.
C. D.
【答案】B【解析】
干海带 海带灰 悬浊液 滤液 碘水 的 溶液 从悬浊液到滤
液实现固液分离,因而需要过滤;从碘水到 的 溶液是萃取; 的 溶液的分离是要通
过蒸馏来分离的。
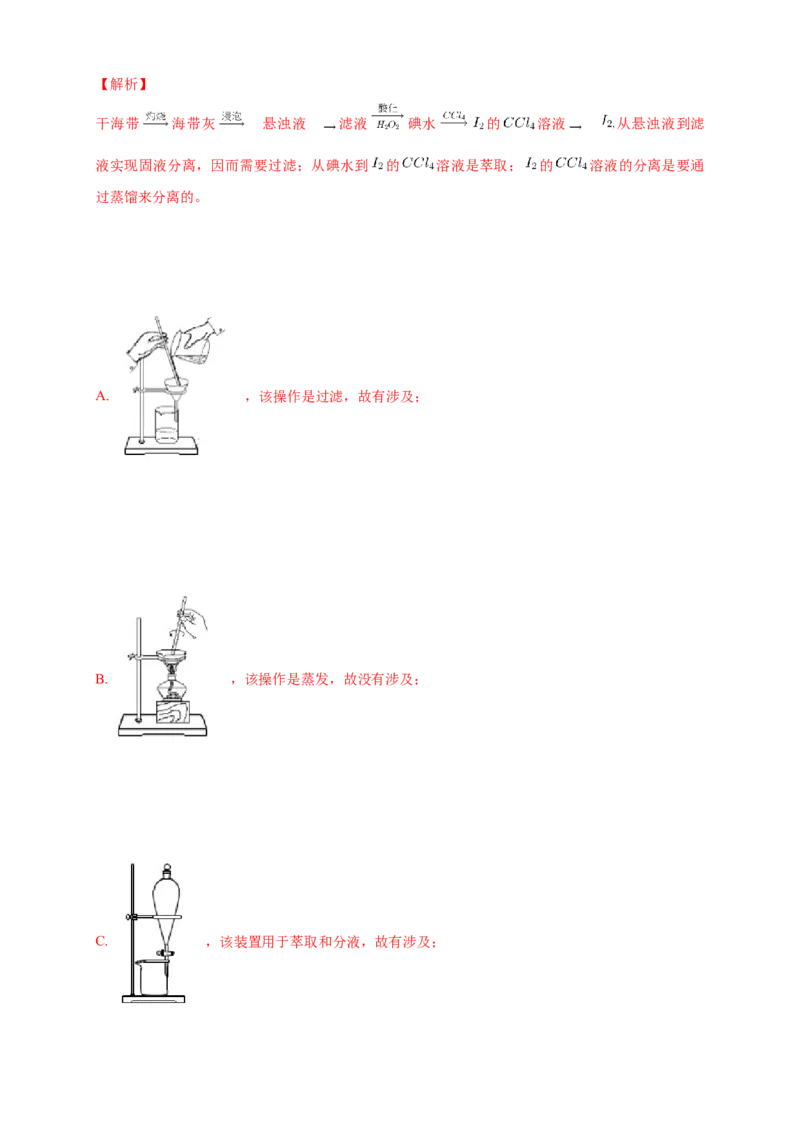
A. ,该操作是过滤,故有涉及;
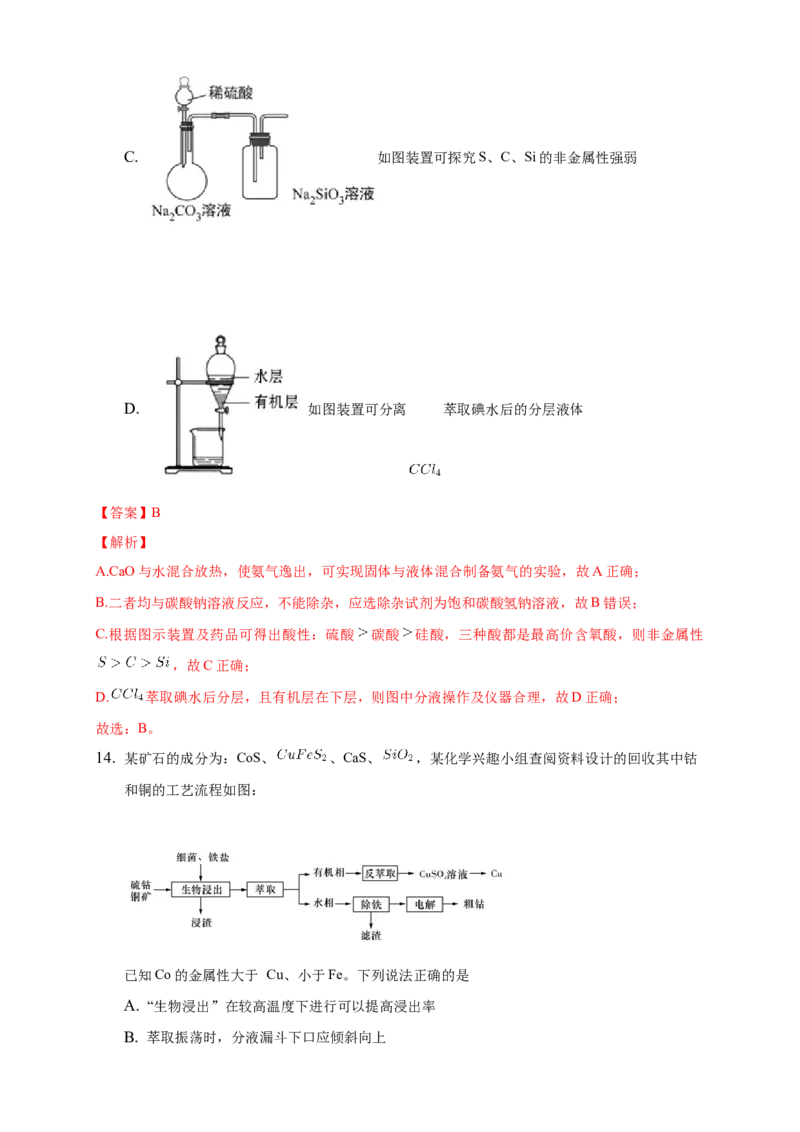
B. ,该操作是蒸发,故没有涉及;
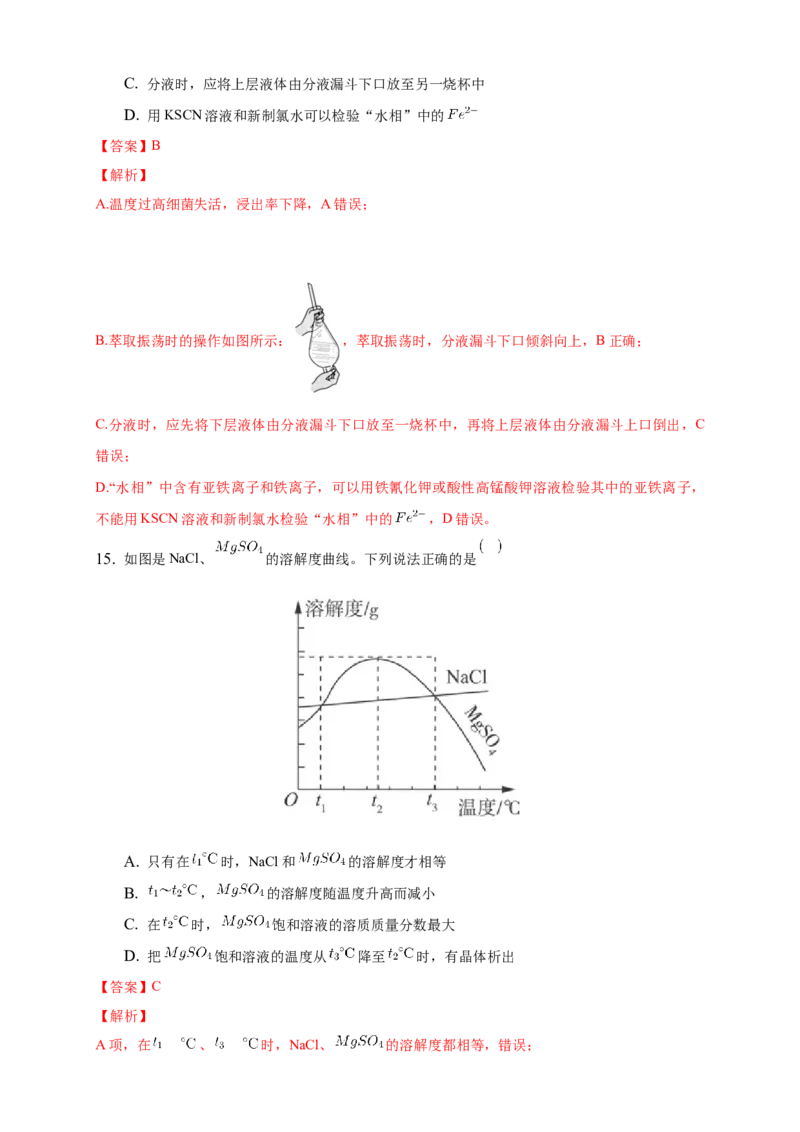
C. ,该装置用于萃取和分液,故有涉及;D. ,该装置用于蒸馏,故有涉及。
故选B。
12. 实验室中下列做法或说法正确的是
A. 用蒸发结晶的方法从碘水中提取碘单质
B. 面粉加工厂应标有“严禁烟火”的字样或图标
C. 用稀硫酸洗涤并灼烧铂丝后,再进行焰色反应
D. 蒸馏时,温度计的水银球应高于蒸馏烧瓶支管口
【答案】B
【解析】
A.用萃取分液的方法从碘水中提取碘单质,故A错误;
B.面粉加工厂应标有“严禁烟火”的字样或图标,以防止发生爆炸事故,故B正确;
C.用稀盐酸洗涤并灼烧铂丝后,再进行焰色反应,不能使用硫酸,故C错误;
D.蒸馏时,温度计的水银球应位于蒸馏烧瓶支管口处,故D错误。
13. 下列装置不能完成相应实验的是
A. 如图装置可用于制备氨气
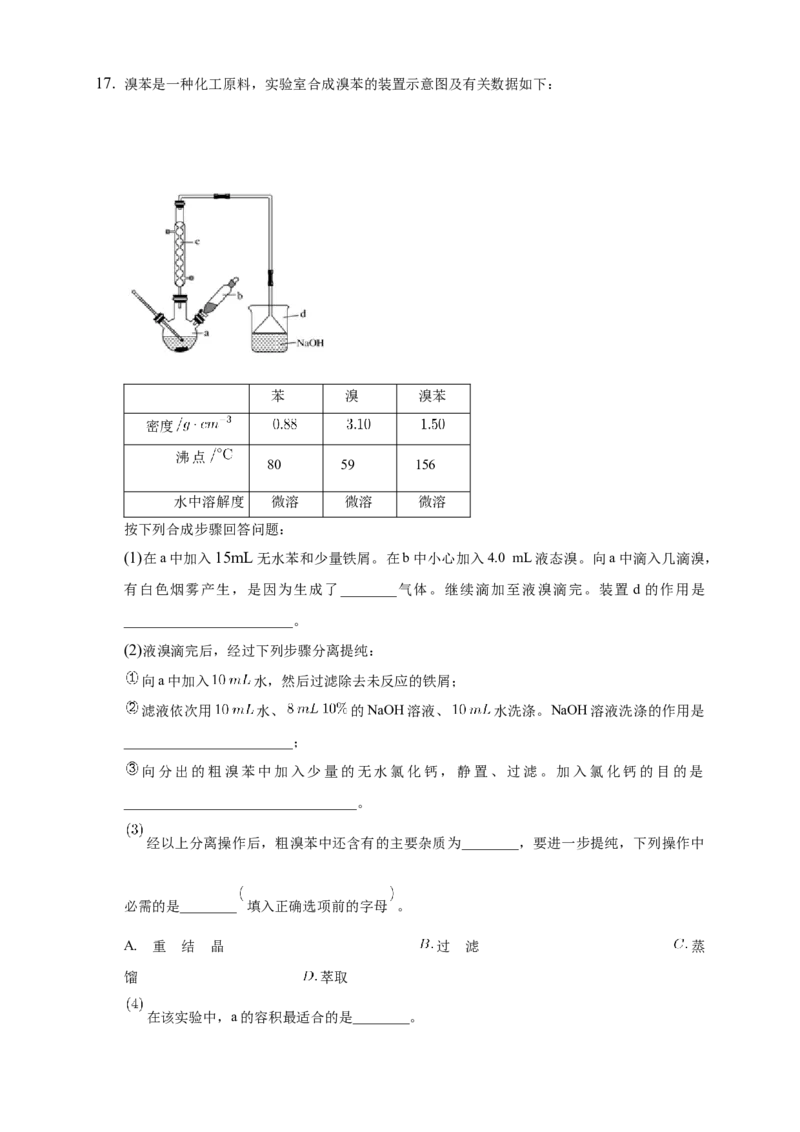
B. 如图装置可除去 中少量的 杂质C. 如图装置可探究S、C、Si的非金属性强弱
D. 如图装置可分离 萃取碘水后的分层液体
【答案】B
【解析】
A.CaO与水混合放热,使氨气逸出,可实现固体与液体混合制备氨气的实验,故A正确;
B.二者均与碳酸钠溶液反应,不能除杂,应选除杂试剂为饱和碳酸氢钠溶液,故B错误;
C.根据图示装置及药品可得出酸性:硫酸 碳酸 硅酸,三种酸都是最高价含氧酸,则非金属性
,故C正确;
D. 萃取碘水后分层,且有机层在下层,则图中分液操作及仪器合理,故D正确;
故选:B。
14. 某矿石的成分为:CoS、 、CaS、 ,某化学兴趣小组查阅资料设计的回收其中钴
和铜的工艺流程如图:
已知Co的金属性大于 Cu、小于Fe。下列说法正确的是
A. “生物浸出”在较高温度下进行可以提高浸出率
B. 萃取振荡时,分液漏斗下口应倾斜向上C. 分液时,应将上层液体由分液漏斗下口放至另一烧杯中
D. 用KSCN溶液和新制氯水可以检验“水相”中的
【答案】B
【解析】
A.温度过高细菌失活,浸出率下降,A错误;
B.萃取振荡时的操作如图所示: ,萃取振荡时,分液漏斗下口倾斜向上,B正确;
C.分液时,应先将下层液体由分液漏斗下口放至一烧杯中,再将上层液体由分液漏斗上口倒出,C
错误;
D.“水相”中含有亚铁离子和铁离子,可以用铁氰化钾或酸性高锰酸钾溶液检验其中的亚铁离子,
不能用KSCN溶液和新制氯水检验“水相”中的 ,D错误。
15. 如图是NaCl、 的溶解度曲线。下列说法正确的是
A. 只有在 时,NaCl和 的溶解度才相等
B. , 的溶解度随温度升高而减小
C. 在 时, 饱和溶液的溶质质量分数最大
D. 把 饱和溶液的温度从 降至 时,有晶体析出
【答案】C
【解析】
A项,在 、 时,NaCl、 的溶解度都相等,错误;B项, 之前, 的溶解度随温度的升高而增大, 之后,随温度的升高而降低,错误;
C项, ,S越大,w越大,正确;
D项,把 饱和溶液的温度从 降至 时,溶解度增大,由饱和溶液变成不饱和
溶液,不会有晶体析出,错误。
16. 下列除杂质 括号内的物质为少量杂质 的方法中不正确的是( )
A. 乙烯 二氧化硫 通过盛有NaOH溶液的洗气瓶
B. 苯 溴 :加入NaOH溶液振荡、静置、分液
C. 乙烷 乙烯 : 通过盛有溴水的洗气瓶
D. 乙酸乙酯 乙酸 :加入NaOH溶液振荡、静置、分液
【答案】D
【解析】
A. 能被NaOH溶液吸收,乙烯与NaOH溶液不反应,方法正确,故A正确;
B. 能被NaOH溶液吸收,苯与NaOH溶液不反应,方法正确,故B正确;
C.乙烯与溴水反应生成1, 二溴乙烷,为液体,乙烷不反应,方法正确,故C正确;
D.乙酸乙酯、乙酸均能与NaOH反应,故D错误。
故选D。
二、实验题17. 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
苯 溴 溴苯
密度
沸点
80 59 156
水中溶解度 微溶 微溶 微溶
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,
有白色烟雾产生,是因为生成了________气体。继续滴加至液溴滴完。装置 d 的作用是
________________________。
(2)液溴滴完后,经过下列步骤分离提纯:
向a中加入 水,然后过滤除去未反应的铁屑;
滤液依次用 水、 的NaOH溶液、 水洗涤。NaOH溶液洗涤的作用是
________________________;
向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是
_________________________________。
经以上分离操作后,粗溴苯中还含有的主要杂质为________,要进一步提纯,下列操作中
必需的是________ 填入正确选项前的字母 。
A. 重 结 晶 过 滤 蒸
馏 萃取
在该实验中,a的容积最适合的是________。A.
【答案】 ;吸收HBr和 ;
除去HBr和未反应的 ; 干燥;
苯;C;
【解析】
苯与液溴反应生成HBr,HBr与水蒸气结合呈白雾;液溴易挥发,而苯的卤代反应是放热的,
尾气中有HBr及挥发出的 ,用氢氧化钠溶液吸收,防止污染大气,
故答案为:HBr;吸收HBr和 ;
溴苯提纯的方法是:先水洗,把可溶物溶解在水中,然后过滤除去未反应的铁屑,再加
NaOH溶液,把未反应的 变成NaBr和NaBrO洗到水中,
故答案为:除去HBr和未反应的 ;
加入氯化钙的目的是干燥产品,
故答案为:干燥;
反应后得到的溴苯中溶有少量未反应的苯,利用沸点不同,苯的沸点小,被蒸馏出,溴苯留在
母液中,所以采取蒸馏的方法分离溴苯与苯,
故答案为:苯;C;
操作过程中,在a中加入15mL无水苯,向a中加入10mL水,在b中小心加入 液态溴,
所以a的容积最适合的是50mL,
故答案为:B。
三、推断题
18. 一种利用化肥中废催化剂 含CoO、Co、Al O 及少量 制取明矾和CoSO 粗产品的工艺
流程如下:已知: 相关金属离子形成氢氧化物沉淀的pH范围如下表所示:
在碱性条件下开始溶解时的pH为 ,完全溶解时的pH为11。
回答下列问题:
写出 的电子式:____________________。
下列措施一定能提高步骤I中 和 的浸取率的是___________ 填标号 。
将废催化剂粉磨为细颗粒
步骤I中的硫酸采用 的浓硫酸
适当提高浸取时的温度
步骤Ⅱ中,写出“氧化”过程中 被氧化的离子方程式:_____________________,若
“氧化”后再“调节 ”,造成的后果是______________________。
步骤III中加 应控制pH的范围为____________。
测定 粗产品中钴的质量分数的步骤如下:
准确称取 产品,先经预处理,然后加入过量的冰乙酸,在加热煮沸下。缓慢滴加 溶
液直至过量,生成不溶于乙酸的 ,再经过滤、洗涤及干燥,称量沉淀的质量为
。溶液氧化并沉淀 的离子方程式为_________________ 已知 被还原为
。
粗产品中钴元素的质量分数为__________ ,列出计算式 。
【答案】 ;
;
; 对 的分解有催化作用,造成原料利
用率低;
;
;
【解析】
【分析】
本题考查制备实验方案评价,为高频考点,侧重考查离子检验、化学反应方程式的书写、物质含量
测定等知识点,明确实验原理及物质性质是解本题关键,难点是题给信息的挖掘和运用,试题有利
于提高学生的分析能力及化学实验能力。
【解答】
为共价化合物,其电子式为 ,
故答案为:为 ;
将废催化剂粉磨为细颗粒,增大接触面积,提高浸取率,故正确;
的浓硫酸提供的氢离子浓度小,不能溶解金属及其氧化物,故错误;
适当提高浸取时的温度,有利于萃取反应的充分进行,故正确;故答案为:ac;
从整个流程分析,氧化前调节pH值为3,Ⅱ氧化后过滤是除去含铁物质,则氧化时把 转
化成氢氧化铁沉淀,则反应的离子方程式为:
若“氧化”后再“调节 ”, 转化成
, 没有形成沉淀,会催化过氧化氢的分解反应,造成过氧化氢的损失,
故答案为: ; 对 的分解有催化作用,造成
原料利用率低;
结合流程和已知条件,“沉钴”时需要将 完全沉淀,而 则完全溶解,故加
应控制pH的范围为 ,
故答案为: ;
溶液氧化并沉淀 为不溶于乙酸的 ,自身被还原为NO,离子方程
式为:
,
故答案为: ;
称量沉淀的质量为 ,即 ,根据 的方程式可得: 可得,
的物质的量为 ,质量为 ,则粗产品中钴元素的质量分数为 ,
故答案为: 。