文档内容
第一课时 化学平衡状态基础练习题解析版
1.14CO 与碳在高温条件下发生反应14CO+C 2CO,达到平衡后,平衡混合物中含14C的粒子有 ( )
2 2
A.14CO B.14CO、14CO C.14CO、14CO、14C D. 14CO
2 2 2
2.在一定条件下,使SO 和O 在一密闭容器中进行反应,下列说法中不正确的是 ( )
2 2
A.随着反应的进行,正反应速率逐渐减小,最后为零
B.随着反应的进行,正反应速率逐渐减小,最后不变
C.随着反应的进行,逆反应速率逐渐增大,最后不变
D.反应开始时,正反应速率最大,逆反应速率为零
3.一定条件下,将A、B、C三种物质各1mol通入一个密闭容器中发生反应:2A+B 2C,达到平衡时,B的物质的
量可能是( )
A. 1.5 mol B. 1 mol C. 0.5 mol D.0
4.判断A(g)+B(g) C(g)+D(g)是否达到平衡的依据是( )
A.压强不随时间改变
B.气体的密度不随时间改变
C.c(A)不随时间改变
D.单位时间内生成C和D的物质的量相等
5.在地壳内SiO 和HF存在以下平衡:SiO(s)+4HF(g) SiF(g)+2HO(g) △H=+148.9kJ/mol。如果上述反应在密
2 2 4 2
闭容器中发生,当反应达到平衡状态时( )
A.2v(正、HF)=v(逆、HO)
2
B.(H O)=v(SiF)
2 4
C.SiO 的质量保持不变
2
D.反应物不再转化为生成物
6.反应N(g)+3H(g) 2NH (g)在恒温恒容条件下进行,下列情况中,反应正向进行的是 (填字母,下
2 2 3
同);反应逆向进行的是 ;处于平衡状态的是 ;无法判断是否达到平衡的是
。
A.单位时间内消耗2molN ,同时生成4 mol NH
2 3
B.单位时间内消耗3molH ,同时生成2 mol NH
2 3
C.单位时间内生成2molN ,同时生成6 mol N-H键
2
D.混合气体的密度不再随时间而改变
E.容器中气体的压强不再随时间而改变
F.单位时间内生成2 mol NH ,同时又生成2molH-H键
3
7.(双选)一定条件下反应2AB(g) A(g)+B (g)达到平衡状态的标志是( )
2 2
A.单位时间内生成 mol A,同时消耗2n mol AB
2
B.容器内,3种气体AB、A、B 共存
2 2
C.AB的消耗速率等于A 的消耗速率的2倍
2
D.容器中各组分的物质的量分数不随时间变化
8.可逆反应:2NO 2NO+O 在密闭容器中反应,达到平衡状态的标志是( )
2 2
①单位时间内生成 nmol O 的同时生成2n mol NO
2 2
②单位时间内生成 nmol O 的同时生成2n mol NO
2
③用NO 、NO、O 的物质的量浓度变化表示反应速率的比为2:2:1的状态
2 2
④混合气体的颜色不再改变的状态
⑤混合气体平均相对分子质量不再改变的状态
A.①③④ B.②③⑤ C.①④⑤ D.①②③④⑤
9.对可逆反应4NH (g)+5O(g) 4NO(g)+6H O(g),下列叙述正确的是 ( )
3 2 2
A.达到平衡状态时,4v (O )=5v (NO)
正 2 逆
B.若单位时间内生成 xmol NO的同时,消耗xmolNH ,则反应达到平衡状态
3
C.恒容容器中气体密度不再改变不能说明达到平衡状态
D.化学反应速率关系:2v (NH )=3v (H O)
正 3 正 2
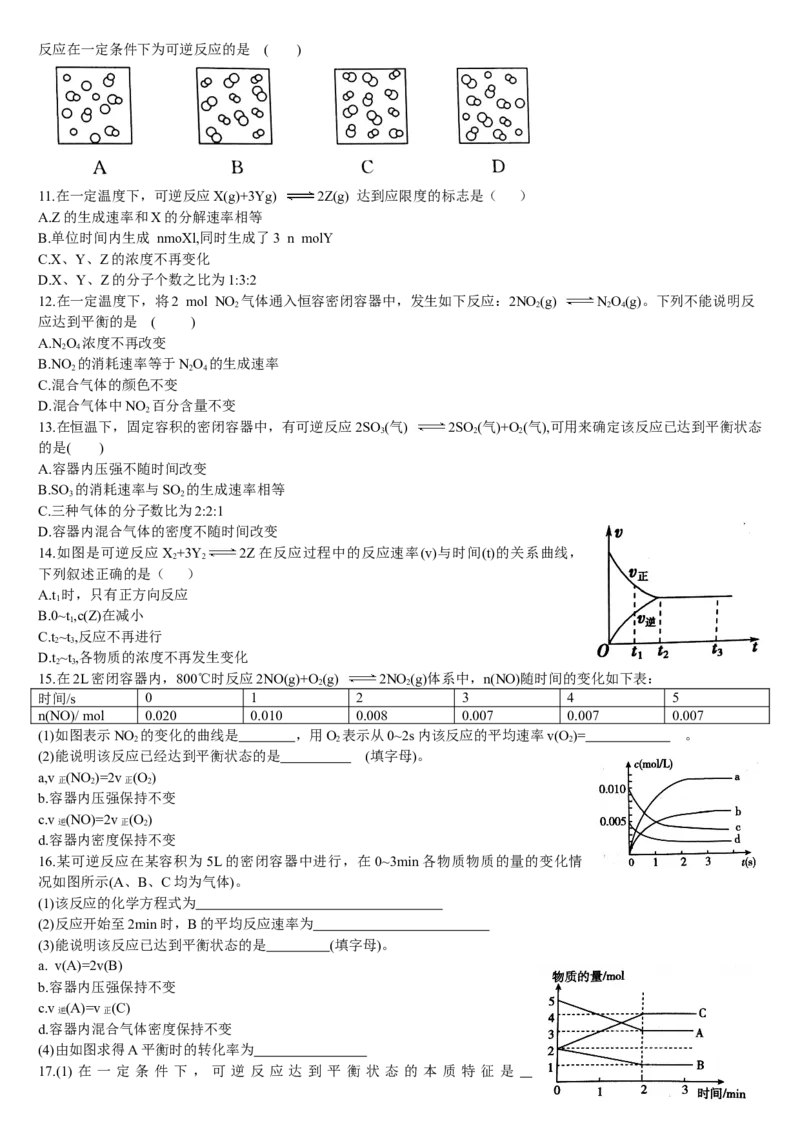
10.模型法是化学中把微观问题宏观化的最常见方法,对于2HBr(g) H(g)+Br (g)反应,下列四个图中可以表示该
2 2反应在一定条件下为可逆反应的是 ( )
11.在一定温度下,可逆反应X(g)+3Yg) 2Z(g) 达到应限度的标志是( )
A.Z的生成速率和X的分解速率相等
B.单位时间内生成 nmoXl,同时生成了3 n molY
C.X、Y、Z的浓度不再变化
D.X、Y、Z的分子个数之比为1:3:2
12.在一定温度下,将2 mol NO 气体通入恒容密闭容器中,发生如下反应:2NO (g) NO(g)。下列不能说明反
2 2 2 4
应达到平衡的是 ( )
A.NO 浓度不再改变
2 4
B.NO 的消耗速率等于NO 的生成速率
2 2 4
C.混合气体的颜色不变
D.混合气体中NO 百分含量不变
2
13.在恒温下,固定容积的密闭容器中,有可逆反应2SO (气) 2SO (气)+O (气),可用来确定该反应已达到平衡状态
3 2 2
的是( )
A.容器内压强不随时间改变
B.SO 的消耗速率与SO 的生成速率相等
3 2
C.三种气体的分子数比为2:2:1
D.容器内混合气体的密度不随时间改变
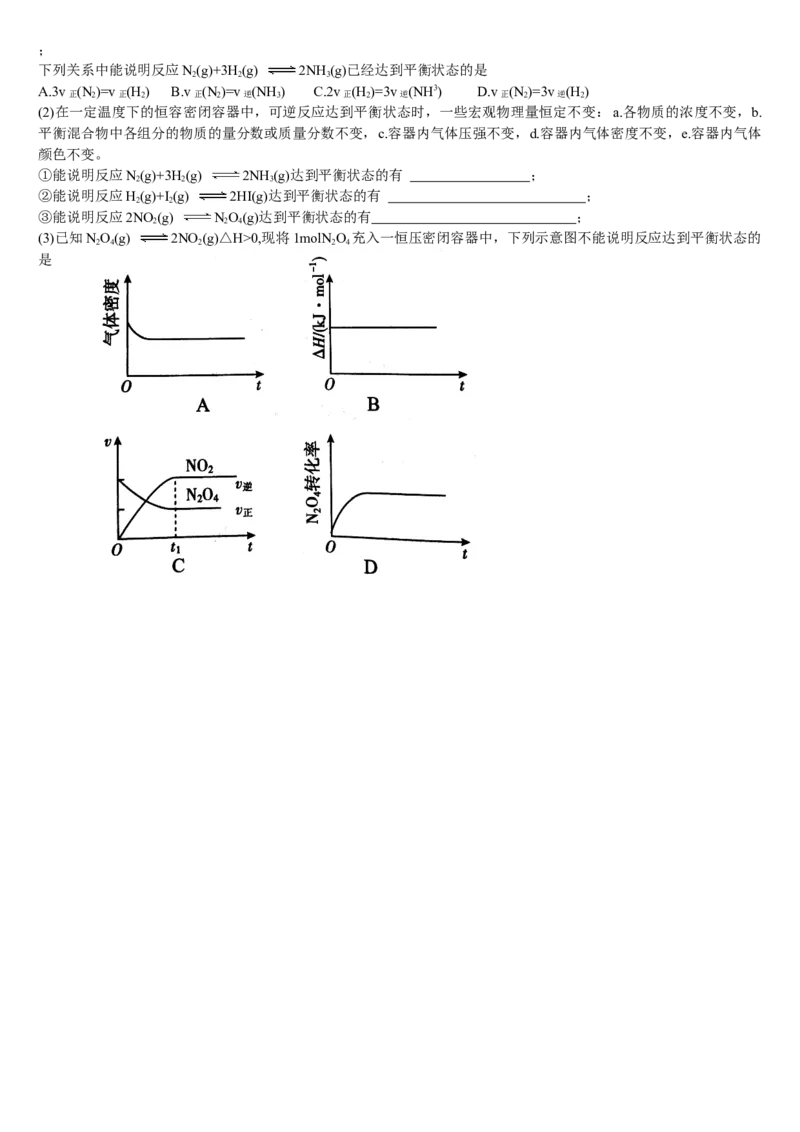
14.如图是可逆反应X+3Y 2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,
2 2
下列叙述正确的是( )
A.t 时,只有正方向反应
1
B.0~t ,c(Z)在减小
1
C.t~t,反应不再进行
2 3
D.t ~t,各物质的浓度不再发生变化
2 3
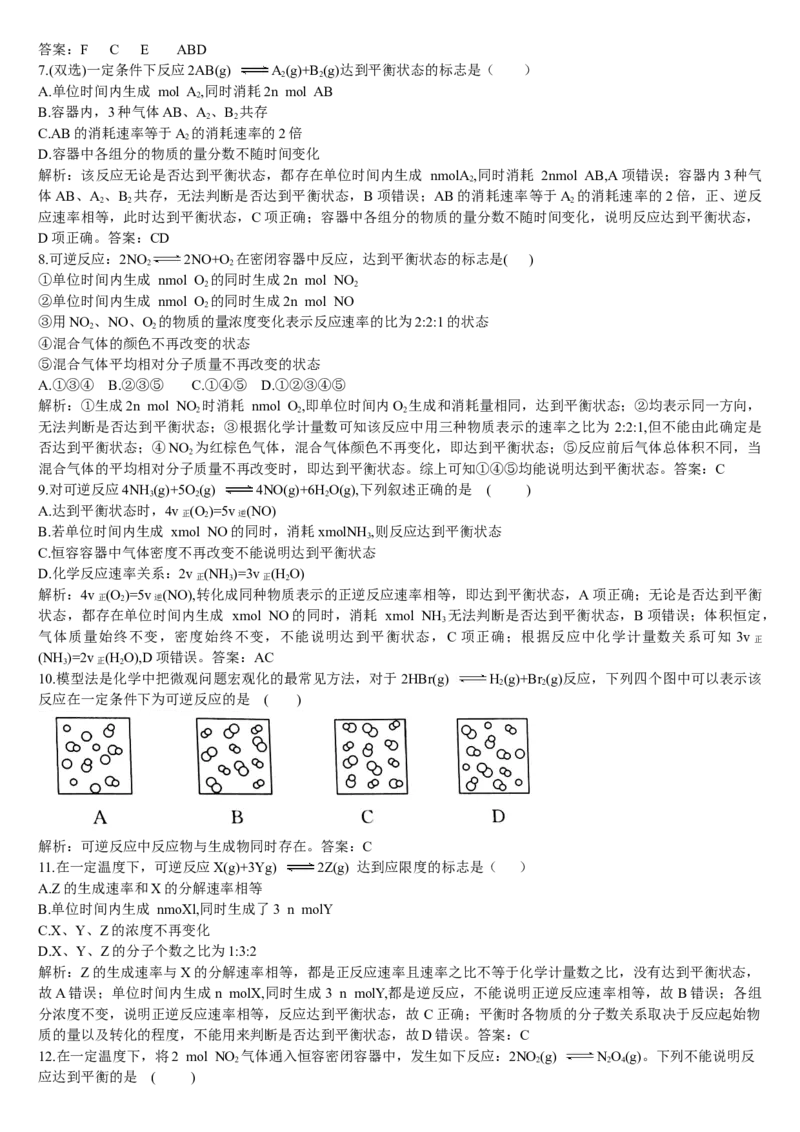
15.在2L密闭容器内,800℃时反应2NO(g)+O (g) 2NO (g)体系中,n(NO)随时间的变化如下表:
2 2
时间/s 0 1 2 3 4 5
n(NO)/ mol 0.020 0.010 0.008 0.007 0.007 0.007
(1)如图表示NO 的变化的曲线是 ,用O 表示从0~2s内该反应的平均速率v(O )= 。
2 2 2
(2)能说明该反应已经达到平衡状态的是 (填字母)。
a,v (NO )=2v (O )
正 2 正 2
b.容器内压强保持不变
c.v (NO)=2v (O )
逆 正 2
d.容器内密度保持不变
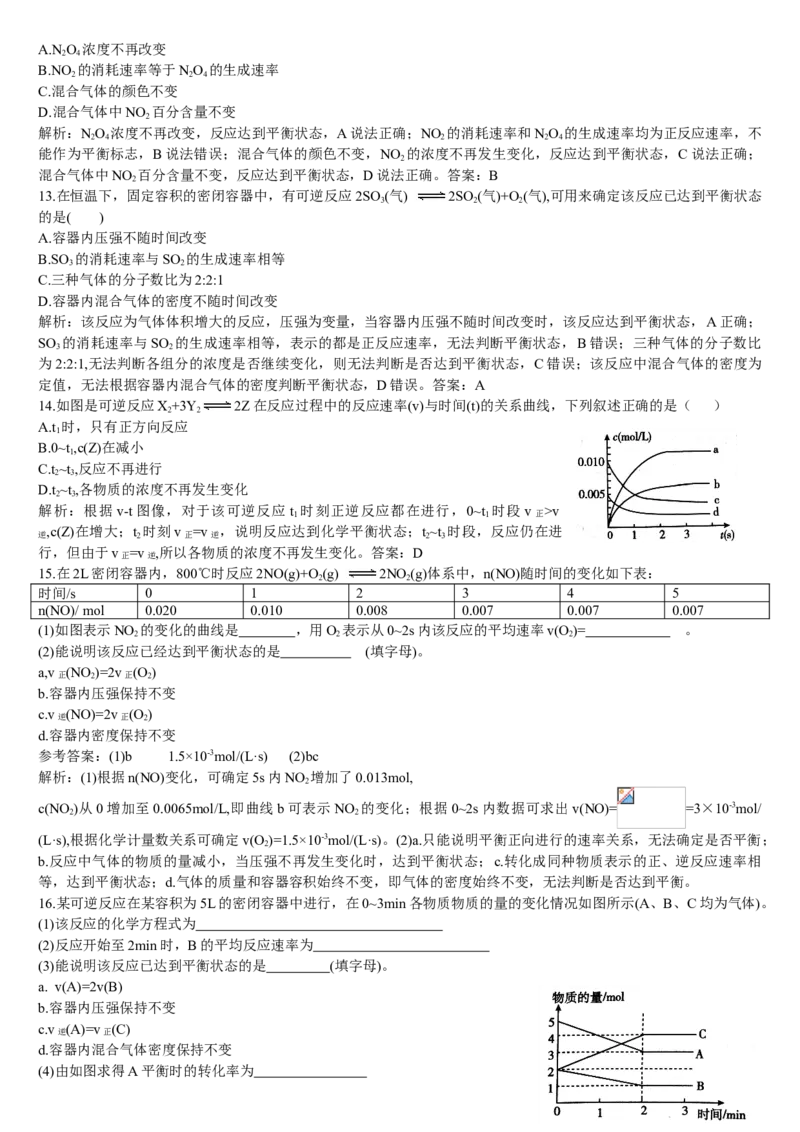
16.某可逆反应在某容积为 5L的密闭容器中进行,在 0~3min各物质物质的量的变化情
况如图所示(A、B、C均为气体)。
(1)该反应的化学方程式为
(2)反应开始至2min时,B的平均反应速率为
(3)能说明该反应已达到平衡状态的是 (填字母)。
a. v(A)=2v(B)
b.容器内压强保持不变
c.v (A)=v (C)
逆 正
d.容器内混合气体密度保持不变
(4)由如图求得A平衡时的转化率为
17.(1) 在 一 定 条 件 下 , 可 逆 反 应 达 到 平 衡 状 态 的 本 质 特 征 是;
下列关系中能说明反应N(g)+3H(g) 2NH (g)已经达到平衡状态的是
2 2 3
A.3v (N )=v (H ) B.v (N )=v (NH ) C.2v (H )=3v (NH3) D.v (N )=3v (H )
正 2 正 2 正 2 逆 3 正 2 逆 正 2 逆 2
(2)在一定温度下的恒容密闭容器中,可逆反应达到平衡状态时,一些宏观物理量恒定不变:a.各物质的浓度不变,b.
平衡混合物中各组分的物质的量分数或质量分数不变,c.容器内气体压强不变,d.容器内气体密度不变,e.容器内气体
颜色不变。
①能说明反应N(g)+3H(g) 2NH (g)达到平衡状态的有 ;
2 2 3
②能说明反应H(g)+I (g) 2HI(g)达到平衡状态的有 ;
2 2
③能说明反应2NO (g) NO(g)达到平衡状态的有 ;
2 2 4
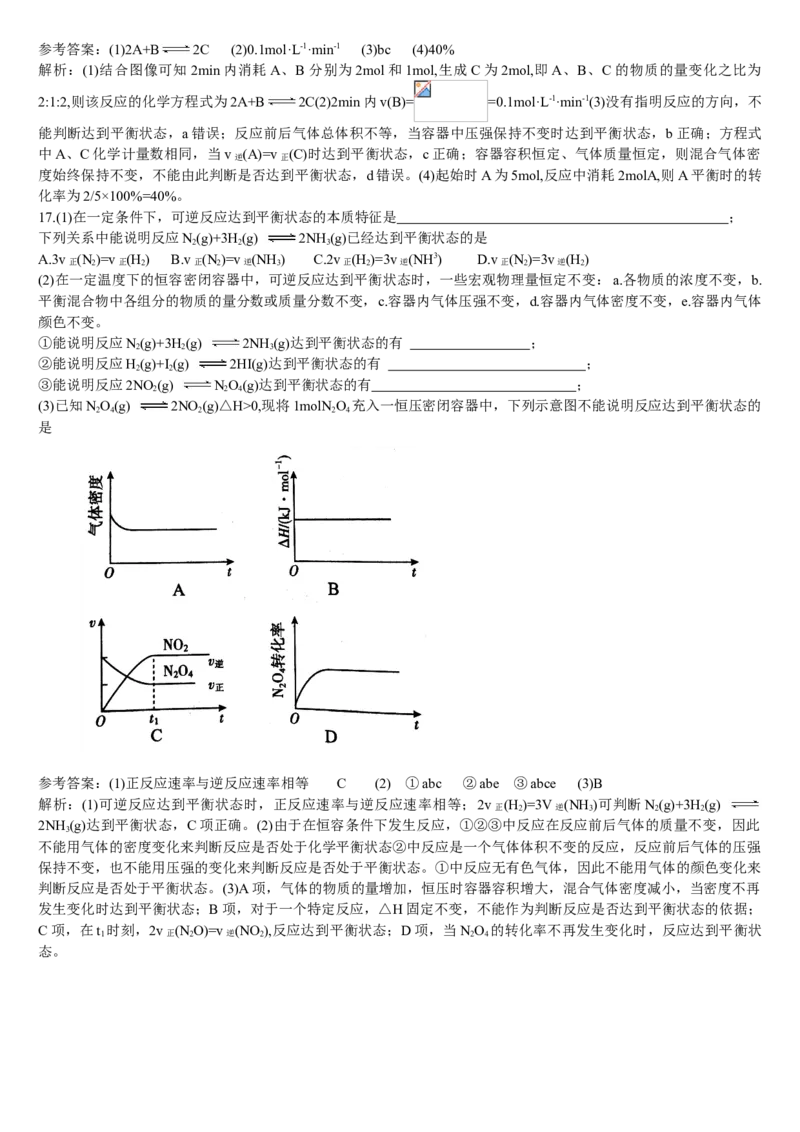
(3)已知NO(g) 2NO (g)△H>0,现将1molN O 充入一恒压密闭容器中,下列示意图不能说明反应达到平衡状态的
2 4 2 2 4
是第一课时 化学平衡状态基础练习题解析版
1.14CO 与碳在高温条件下发生反应14CO+C 2CO,达到平衡后,平衡混合物中含14C的粒子有 ( )
2 2
A.14CO B.14CO、14CO C.14CO、14CO、14C D. 14CO
2 2 2
解析:14CO 发生该反应时生成物CO中含14C,反应逆向进行时,所得CO 和C中也均含14C,结合上述分析,三种物质
2 2
中均含14C。答案:C
2.在一定条件下,使SO 和O 在一密闭容器中进行反应,下列说法中不正确的是 ( )
2 2
A.随着反应的进行,正反应速率逐渐减小,最后为零
B.随着反应的进行,正反应速率逐渐减小,最后不变
C.随着反应的进行,逆反应速率逐渐增大,最后不变
D.反应开始时,正反应速率最大,逆反应速率为零
解析:SO 和O 在密闭容器中开始发生反应时,反应物浓度最大,具有最大的正向速率,随着反应的进行,反应物浓
2 2
度减小,生成物浓度增大,正反应速率逐渐减小,逆反应速率逐渐增大,当正、逆反应速率相等时,达到化学平衡状
态,但正、逆反应速率均不为零。答案:A
3.一定条件下,将A、B、C三种物质各1mol通入一个密闭容器中发生反应:2A+B 2C,达到平衡时,B的物质的
量可能是( )
A. 1.5 mol B. 1 mol C. 0.5 mol D.0
解析:可逆反应不能进行彻底,若反应正向进行彻底,则B为0.5mol;若反应逆向进行彻底,则B为1.5mol。故平衡
时,0.5 molv(H 生成),故反应正向进行。
3 2 2 2 2答案:F C E ABD
7.(双选)一定条件下反应2AB(g) A(g)+B (g)达到平衡状态的标志是( )
2 2
A.单位时间内生成 mol A,同时消耗2n mol AB
2
B.容器内,3种气体AB、A、B 共存
2 2
C.AB的消耗速率等于A 的消耗速率的2倍
2
D.容器中各组分的物质的量分数不随时间变化
解析:该反应无论是否达到平衡状态,都存在单位时间内生成 nmolA ,同时消耗 2nmol AB,A项错误;容器内3种气
2
体AB、A 、B 共存,无法判断是否达到平衡状态,B项错误;AB的消耗速率等于A 的消耗速率的2倍,正、逆反
2 2 2
应速率相等,此时达到平衡状态,C项正确;容器中各组分的物质的量分数不随时间变化,说明反应达到平衡状态,
D项正确。答案:CD
8.可逆反应:2NO 2NO+O 在密闭容器中反应,达到平衡状态的标志是( )
2 2
①单位时间内生成 nmol O 的同时生成2n mol NO
2 2
②单位时间内生成 nmol O 的同时生成2n mol NO
2
③用NO 、NO、O 的物质的量浓度变化表示反应速率的比为2:2:1的状态
2 2
④混合气体的颜色不再改变的状态
⑤混合气体平均相对分子质量不再改变的状态
A.①③④ B.②③⑤ C.①④⑤ D.①②③④⑤
解析:①生成2n mol NO 时消耗 nmol O,即单位时间内O 生成和消耗量相同,达到平衡状态;②均表示同一方向,
2 2 2
无法判断是否达到平衡状态;③根据化学计量数可知该反应中用三种物质表示的速率之比为 2:2:1,但不能由此确定是
否达到平衡状态;④NO 为红棕色气体,混合气体颜色不再变化,即达到平衡状态;⑤反应前后气体总体积不同,当
2
混合气体的平均相对分子质量不再改变时,即达到平衡状态。综上可知①④⑤均能说明达到平衡状态。答案:C
9.对可逆反应4NH (g)+5O(g) 4NO(g)+6H O(g),下列叙述正确的是 ( )
3 2 2
A.达到平衡状态时,4v (O )=5v (NO)
正 2 逆
B.若单位时间内生成 xmol NO的同时,消耗xmolNH ,则反应达到平衡状态
3
C.恒容容器中气体密度不再改变不能说明达到平衡状态
D.化学反应速率关系:2v (NH )=3v (H O)
正 3 正 2
解析:4v (O )=5v (NO),转化成同种物质表示的正逆反应速率相等,即达到平衡状态,A项正确;无论是否达到平衡
正 2 逆
状态,都存在单位时间内生成 xmol NO的同时,消耗 xmol NH 无法判断是否达到平衡状态,B项错误;体积恒定,
3
气体质量始终不变,密度始终不变,不能说明达到平衡状态,C项正确;根据反应中化学计量数关系可知 3v
正
(NH )=2v (H O),D项错误。答案:AC
3 正 2
10.模型法是化学中把微观问题宏观化的最常见方法,对于2HBr(g) H(g)+Br (g)反应,下列四个图中可以表示该
2 2
反应在一定条件下为可逆反应的是 ( )
解析:可逆反应中反应物与生成物同时存在。答案:C
11.在一定温度下,可逆反应X(g)+3Yg) 2Z(g) 达到应限度的标志是( )
A.Z的生成速率和X的分解速率相等
B.单位时间内生成 nmoXl,同时生成了3 n molY
C.X、Y、Z的浓度不再变化
D.X、Y、Z的分子个数之比为1:3:2
解析:Z的生成速率与X的分解速率相等,都是正反应速率且速率之比不等于化学计量数之比,没有达到平衡状态,
故A错误;单位时间内生成n molX,同时生成3 n molY,都是逆反应,不能说明正逆反应速率相等,故 B错误;各组
分浓度不变,说明正逆反应速率相等,反应达到平衡状态,故 C正确;平衡时各物质的分子数关系取决于反应起始物
质的量以及转化的程度,不能用来判断是否达到平衡状态,故D错误。答案:C
12.在一定温度下,将2 mol NO 气体通入恒容密闭容器中,发生如下反应:2NO (g) NO(g)。下列不能说明反
2 2 2 4
应达到平衡的是 ( )A.NO 浓度不再改变
2 4
B.NO 的消耗速率等于NO 的生成速率
2 2 4
C.混合气体的颜色不变
D.混合气体中NO 百分含量不变
2
解析:NO 浓度不再改变,反应达到平衡状态,A说法正确;NO 的消耗速率和NO 的生成速率均为正反应速率,不
2 4 2 2 4
能作为平衡标志,B说法错误;混合气体的颜色不变,NO 的浓度不再发生变化,反应达到平衡状态,C说法正确;
2
混合气体中NO 百分含量不变,反应达到平衡状态,D说法正确。答案:B
2
13.在恒温下,固定容积的密闭容器中,有可逆反应2SO (气) 2SO (气)+O (气),可用来确定该反应已达到平衡状态
3 2 2
的是( )
A.容器内压强不随时间改变
B.SO 的消耗速率与SO 的生成速率相等
3 2
C.三种气体的分子数比为2:2:1
D.容器内混合气体的密度不随时间改变
解析:该反应为气体体积增大的反应,压强为变量,当容器内压强不随时间改变时,该反应达到平衡状态,A正确;
SO 的消耗速率与SO 的生成速率相等,表示的都是正反应速率,无法判断平衡状态,B错误;三种气体的分子数比
3 2
为2:2:1,无法判断各组分的浓度是否继续变化,则无法判断是否达到平衡状态,C错误;该反应中混合气体的密度为
定值,无法根据容器内混合气体的密度判断平衡状态,D错误。答案:A
14.如图是可逆反应X+3Y 2Z在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
2 2
A.t 时,只有正方向反应
1
B.0~t ,c(Z)在减小
1
C.t~t,反应不再进行
2 3
D.t ~t,各物质的浓度不再发生变化
2 3
解析:根据v-t图像,对于该可逆反应 t 时刻正逆反应都在进行,0~t 时段v >v
1 1 正
,c(Z)在增大;t 时刻v =v ,说明反应达到化学平衡状态;t~t 时段,反应仍在进
逆 2 正 逆 2 3
行,但由于v =v ,所以各物质的浓度不再发生变化。答案:D
正 逆
15.在2L密闭容器内,800℃时反应2NO(g)+O (g) 2NO (g)体系中,n(NO)随时间的变化如下表:
2 2
时间/s 0 1 2 3 4 5
n(NO)/ mol 0.020 0.010 0.008 0.007 0.007 0.007
(1)如图表示NO 的变化的曲线是 ,用O 表示从0~2s内该反应的平均速率v(O )= 。
2 2 2
(2)能说明该反应已经达到平衡状态的是 (填字母)。
a,v (NO )=2v (O )
正 2 正 2
b.容器内压强保持不变
c.v (NO)=2v (O )
逆 正 2
d.容器内密度保持不变
参考答案:(1)b 1.5×10-3mol/(L·s) (2)bc
解析:(1)根据n(NO)变化,可确定5s内NO 增加了0.013mol,
2
c(NO )从0增加至0.0065mol/L,即曲线b可表示NO 的变化;根据0~2s内数据可求出v(NO)= =3×10-3mol/
2 2
(L·s),根据化学计量数关系可确定v(O )=1.5×10-3mol/(L·s)。(2)a.只能说明平衡正向进行的速率关系,无法确定是否平衡;
2
b.反应中气体的物质的量减小,当压强不再发生变化时,达到平衡状态;c.转化成同种物质表示的正、逆反应速率相
等,达到平衡状态;d.气体的质量和容器容积始终不变,即气体的密度始终不变,无法判断是否达到平衡。
16.某可逆反应在某容积为5L的密闭容器中进行,在0~3min各物质物质的量的变化情况如图所示(A、B、C均为气体)。
(1)该反应的化学方程式为
(2)反应开始至2min时,B的平均反应速率为
(3)能说明该反应已达到平衡状态的是 (填字母)。
a. v(A)=2v(B)
b.容器内压强保持不变
c.v (A)=v (C)
逆 正
d.容器内混合气体密度保持不变
(4)由如图求得A平衡时的转化率为参考答案:(1)2A+B 2C (2)0.1mol·L-1·min-1 (3)bc (4)40%
解析:(1)结合图像可知2min内消耗A、B分别为2mol和1mol,生成C为2mol,即A、B、C的物质的量变化之比为
2:1:2,则该反应的化学方程式为2A+B 2C(2)2min内v(B)= =0.1mol·L-1·min-1(3)没有指明反应的方向,不
能判断达到平衡状态,a错误;反应前后气体总体积不等,当容器中压强保持不变时达到平衡状态,b正确;方程式
中A、C化学计量数相同,当v (A)=v (C)时达到平衡状态,c正确;容器容积恒定、气体质量恒定,则混合气体密
逆 正
度始终保持不变,不能由此判断是否达到平衡状态,d错误。(4)起始时A为5mol,反应中消耗2molA,则A平衡时的转
化率为2/5×100%=40%。
17.(1)在一定条件下,可逆反应达到平衡状态的本质特征是 ;
下列关系中能说明反应N(g)+3H(g) 2NH (g)已经达到平衡状态的是
2 2 3
A.3v (N )=v (H ) B.v (N )=v (NH ) C.2v (H )=3v (NH3) D.v (N )=3v (H )
正 2 正 2 正 2 逆 3 正 2 逆 正 2 逆 2
(2)在一定温度下的恒容密闭容器中,可逆反应达到平衡状态时,一些宏观物理量恒定不变:a.各物质的浓度不变,b.
平衡混合物中各组分的物质的量分数或质量分数不变,c.容器内气体压强不变,d.容器内气体密度不变,e.容器内气体
颜色不变。
①能说明反应N(g)+3H(g) 2NH (g)达到平衡状态的有 ;
2 2 3
②能说明反应H(g)+I (g) 2HI(g)达到平衡状态的有 ;
2 2
③能说明反应2NO (g) NO(g)达到平衡状态的有 ;
2 2 4
(3)已知NO(g) 2NO (g)△H>0,现将1molN O 充入一恒压密闭容器中,下列示意图不能说明反应达到平衡状态的
2 4 2 2 4
是
参考答案:(1)正反应速率与逆反应速率相等 C (2) ①abc ②abe ③abce (3)B
解析:(1)可逆反应达到平衡状态时,正反应速率与逆反应速率相等;2v (H )=3V (NH )可判断N(g)+3H(g)
正 2 逆 3 2 2
2NH (g)达到平衡状态,C项正确。(2)由于在恒容条件下发生反应,①②③中反应在反应前后气体的质量不变,因此
3
不能用气体的密度变化来判断反应是否处于化学平衡状态②中反应是一个气体体积不变的反应,反应前后气体的压强
保持不变,也不能用压强的变化来判断反应是否处于平衡状态。①中反应无有色气体,因此不能用气体的颜色变化来
判断反应是否处于平衡状态。(3)A项,气体的物质的量增加,恒压时容器容积增大,混合气体密度减小,当密度不再
发生变化时达到平衡状态;B项,对于一个特定反应,△H固定不变,不能作为判断反应是否达到平衡状态的依据;
C项,在t 时刻,2v (N O)=v (NO ),反应达到平衡状态;D项,当NO 的转化率不再发生变化时,反应达到平衡状
1 正 2 逆 2 2 4
态。