文档内容
4.2.2 电解原理的应用 练习(原卷版)
1.海水提镁的最后一步是将氯化镁电解获取金属镁,下列有关该电解过程的叙述中,正确的是(
)
A.两个电极必须都用惰性电极
B.阳极可以用金属电极,阴极必须是惰性电极
C.电解熔融状态的氯化镁
D.电解氯化镁的水溶液
2.下列金属只能用电解法冶炼获得的是( )
A.Na B.Cu
C.Fe D.Au
3.某同学组装了如图所示的电化学装置,电极Ⅰ为Zn,其他电极均为Cu,则下列说法正确的是(
)
A.电子移动:电极Ⅰ→电极Ⅳ→电极Ⅲ→电极Ⅱ
B.电极Ⅰ发生还原反应
C.电极Ⅳ逐渐溶解
D.电极Ⅲ的电极反应:Cu-2e-===Cu2+
A.阳极发生还原反应,其电极反应式为:Ni2++2e-===Ni
B.电解过程中,阳极减少的质量与阴极增加的质量相等
C.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
5.关于电解氯化钠水溶液(铁做阴极、石墨做阳极),下列叙述正确的是( )
A.若在阴极附近的溶液中滴入酚酞溶液,溶液呈无色
B.若在阳极附近的溶液中滴入KI溶液,溶液呈棕黄色
C.电解时在阳极得到氯气,在阴极得到金属钠
D.电解一段时间后,将全部电解液转移到烧杯中,充分搅拌后溶液呈中性
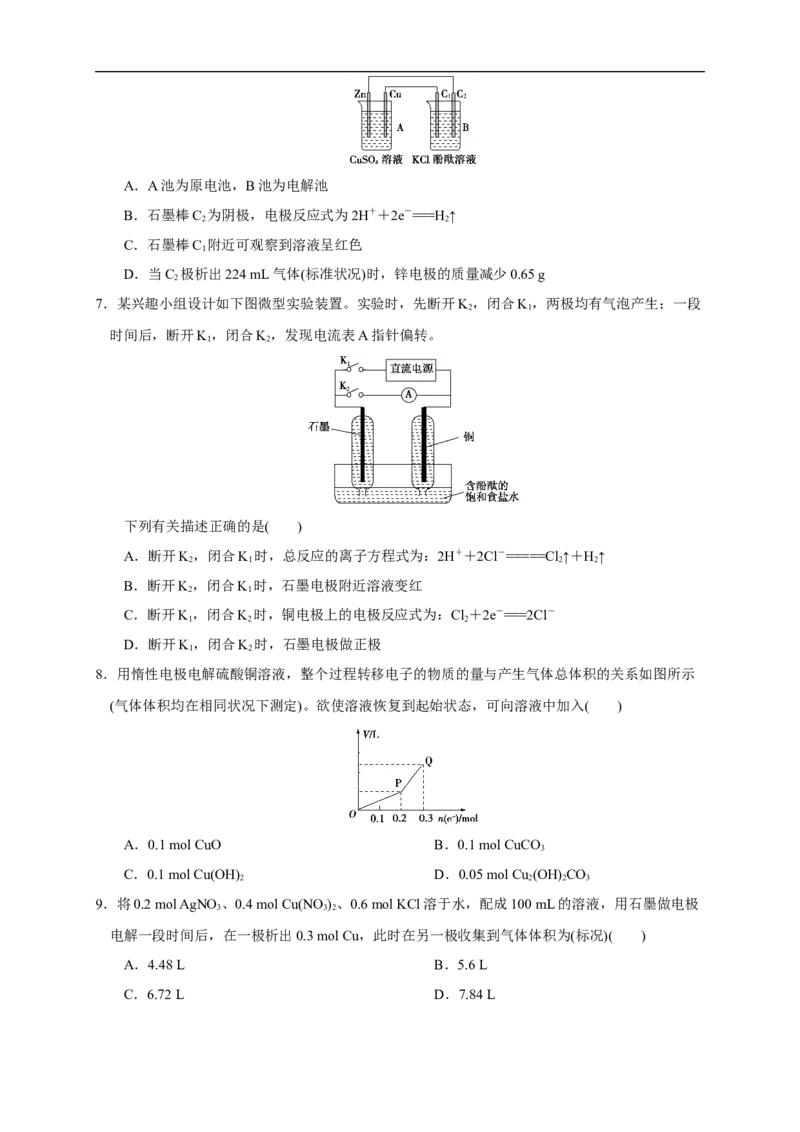
6.某学生按右图装置进行实验,下列说法不正确的是( )A.A池为原电池,B池为电解池
B.石墨棒C 为阴极,电极反应式为2H++2e-===H ↑
2 2
C.石墨棒C 附近可观察到溶液呈红色
1
D.当C 极析出224 mL气体(标准状况)时,锌电极的质量减少0.65 g
2
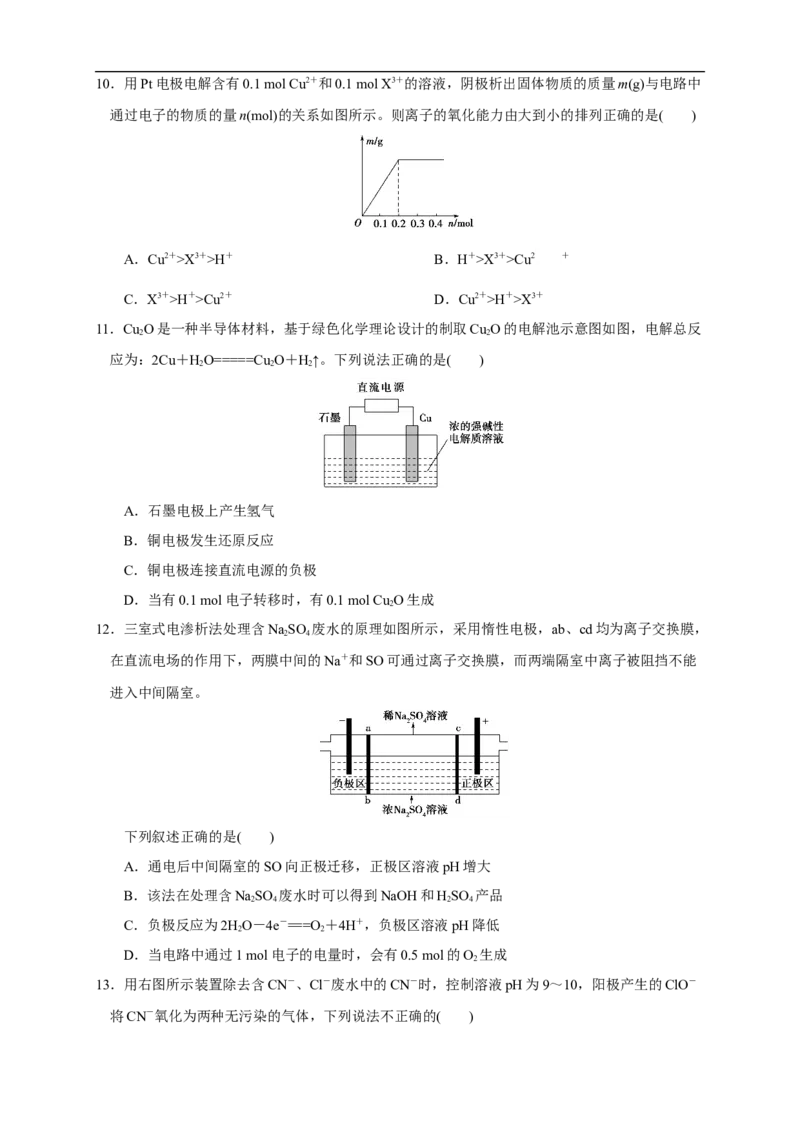
7.某兴趣小组设计如下图微型实验装置。实验时,先断开K,闭合K,两极均有气泡产生;一段
2 1
时间后,断开K,闭合K,发现电流表A指针偏转。
1 2
下列有关描述正确的是( )
A.断开K,闭合K 时,总反应的离子方程式为:2H++2Cl-=====Cl↑+H↑
2 1 2 2
B.断开K,闭合K 时,石墨电极附近溶液变红
2 1
C.断开K,闭合K 时,铜电极上的电极反应式为:Cl+2e-===2Cl-
1 2 2
D.断开K,闭合K 时,石墨电极做正极
1 2
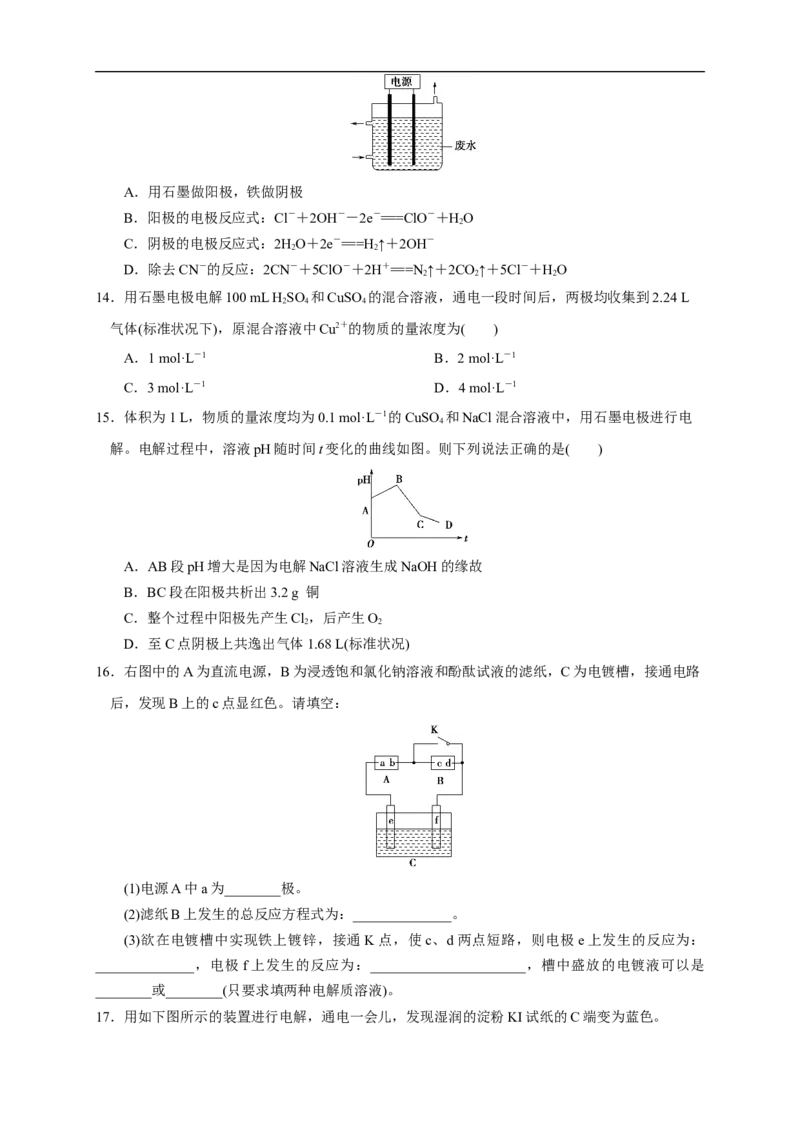
8.用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体总体积的关系如图所示
(气体体积均在相同状况下测定)。欲使溶液恢复到起始状态,可向溶液中加入( )
A.0.1 mol CuO B.0.1 mol CuCO
3
C.0.1 mol Cu(OH) D.0.05 mol Cu (OH) CO
2 2 2 3
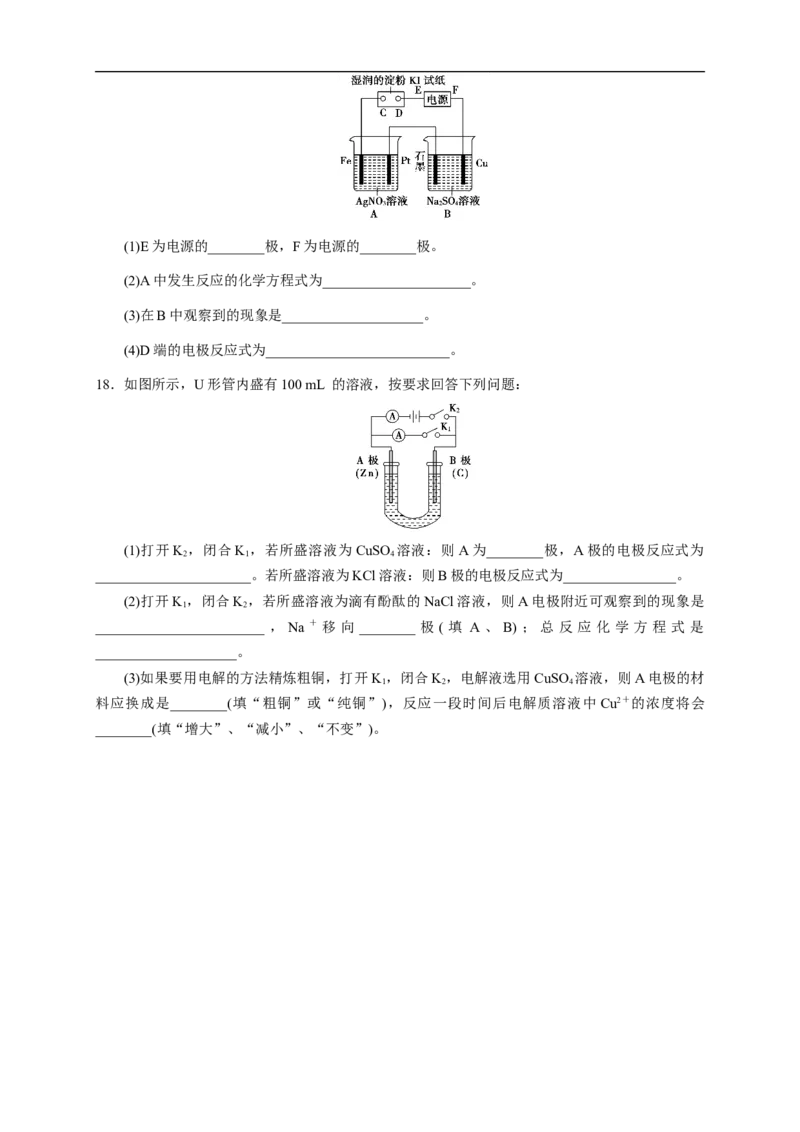
9.将0.2 mol AgNO 、0.4 mol Cu(NO )、0.6 mol KCl溶于水,配成100 mL的溶液,用石墨做电极
3 3 2
电解一段时间后,在一极析出0.3 mol Cu,此时在另一极收集到气体体积为(标况)( )
A.4.48 L B.5.6 L
C.6.72 L D.7.84 L10.用Pt电极电解含有0.1 mol Cu2+和0.1 mol X3+的溶液,阴极析出固体物质的质量m(g)与电路中
通过电子的物质的量n(mol)的关系如图所示。则离子的氧化能力由大到小的排列正确的是( )
A.Cu2+>X3+>H+ B.H+>X3+>Cu2 +
C.X3+>H+>Cu2+ D.Cu2+>H+>X3+
11.Cu O是一种半导体材料,基于绿色化学理论设计的制取Cu O的电解池示意图如图,电解总反
2 2
应为:2Cu+HO=====Cu O+H↑。下列说法正确的是( )
2 2 2
A.石墨电极上产生氢气
B.铜电极发生还原反应
C.铜电极连接直流电源的负极
D.当有0.1 mol电子转移时,有0.1 mol Cu O生成
2
12.三室式电渗析法处理含NaSO 废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,
2 4
在直流电场的作用下,两膜中间的Na+和SO可通过离子交换膜,而两端隔室中离子被阻挡不能
进入中间隔室。
下列叙述正确的是( )
A.通电后中间隔室的SO向正极迁移,正极区溶液pH增大
B.该法在处理含NaSO 废水时可以得到NaOH和HSO 产品
2 4 2 4
C.负极反应为2HO-4e-===O +4H+,负极区溶液pH降低
2 2
D.当电路中通过1 mol电子的电量时,会有0.5 mol的O 生成
2
13.用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-
将CN-氧化为两种无污染的气体,下列说法不正确的( )A.用石墨做阳极,铁做阴极
B.阳极的电极反应式:Cl-+2OH--2e-===ClO-+HO
2
C.阴极的电极反应式:2HO+2e-===H ↑+2OH-
2 2
D.除去CN-的反应:2CN-+5ClO-+2H+===N ↑+2CO↑+5Cl-+HO
2 2 2
14.用石墨电极电解100 mL H SO 和CuSO 的混合溶液,通电一段时间后,两极均收集到2.24 L
2 4 4
气体(标准状况下),原混合溶液中Cu2+的物质的量浓度为( )
A.1 mol·L-1 B.2 mol·L-1
C.3 mol·L-1 D.4 mol·L-1
15.体积为1 L,物质的量浓度均为0.1 mol·L-1的CuSO 和NaCl混合溶液中,用石墨电极进行电
4
解。电解过程中,溶液pH随时间t变化的曲线如图。则下列说法正确的是( )
A.AB段pH增大是因为电解NaCl溶液生成NaOH的缘故
B.BC段在阳极共析出3.2 g 铜
C.整个过程中阳极先产生Cl,后产生O
2 2
D.至C点阴极上共逸出气体1.68 L(标准状况)
16.右图中的A为直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路
后,发现B上的c点显红色。请填空:
(1)电源A中a为________极。
(2)滤纸B上发生的总反应方程式为:______________。
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为:
______________,电极f上发生的反应为:______________________,槽中盛放的电镀液可以是
________或________(只要求填两种电解质溶液)。
17.用如下图所示的装置进行电解,通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色。(1)E为电源的________极,F为电源的________极。
(2)A中发生反应的化学方程式为_____________________。
(3)在B中观察到的现象是____________________。
(4)D端的电极反应式为__________________________。
18.如图所示,U形管内盛有100 mL 的溶液,按要求回答下列问题:
(1)打开K ,闭合K ,若所盛溶液为CuSO 溶液:则A为________极,A极的电极反应式为
2 1 4
______________________。若所盛溶液为KCl溶液:则B极的电极反应式为________________。
(2)打开K ,闭合K ,若所盛溶液为滴有酚酞的NaCl溶液,则A电极附近可观察到的现象是
1 2
________________________ , Na + 移 向 ________ 极 ( 填 A 、 B) ; 总 反 应 化 学 方 程 式 是
____________________。
(3)如果要用电解的方法精炼粗铜,打开K ,闭合K ,电解液选用CuSO 溶液,则A电极的材
1 2 4
料应换成是________(填“粗铜”或“纯铜”),反应一段时间后电解质溶液中Cu2+的浓度将会
________(填“增大”、“减小”、“不变”)。