文档内容
第六章 化学反应与能量
第二节 化学反应的速率与限度(第1课时 化学反应的速率)
一、选择题(共12题)
1.在某一化学反应中,反应物A的浓度在2s内由1.0mol/L变成0.2mol/L,则在这2s内它的平均反应速率
为
A.0.08mol/(L·s) B.0.8mol/(L·s) C.0.4mol/(L·s) D.0.04mol/L
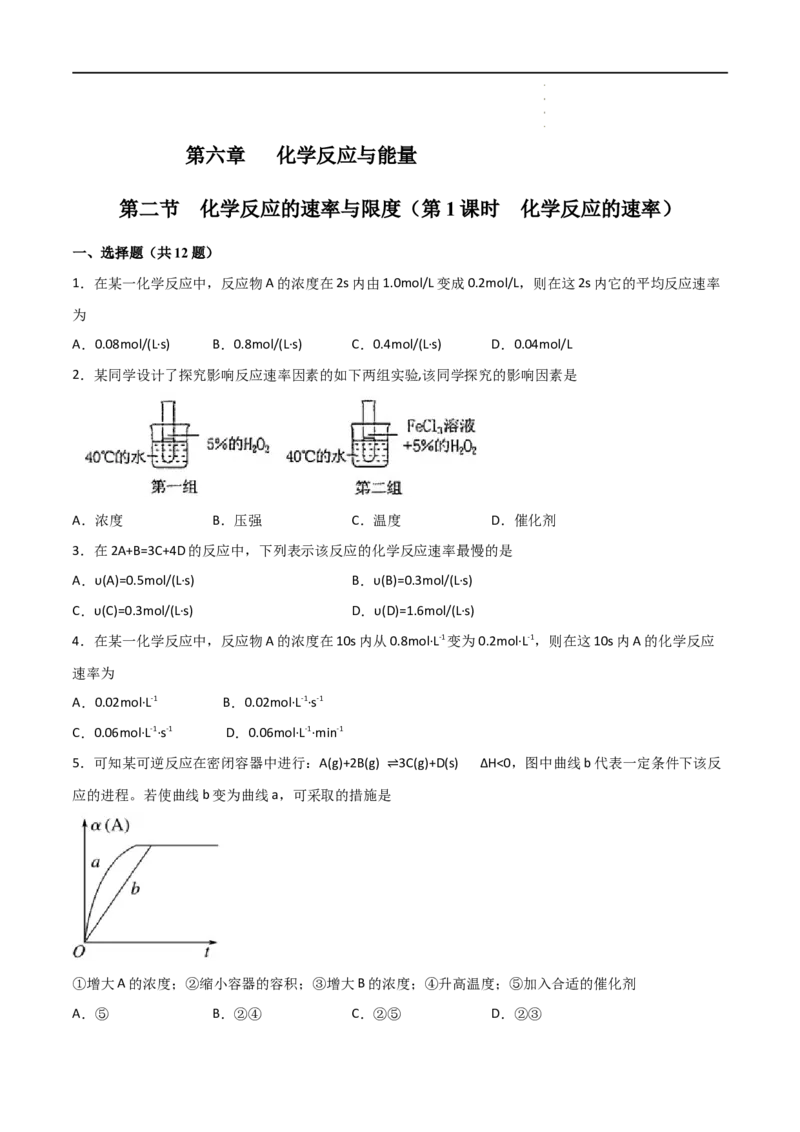
2.某同学设计了探究影响反应速率因素的如下两组实验,该同学探究的影响因素是
A.浓度 B.压强 C.温度 D.催化剂
3.在2A+B=3C+4D的反应中,下列表示该反应的化学反应速率最慢的是
A.υ(A)=0.5mol/(L·s) B.υ(B)=0.3mol/(L·s)
C.υ(C)=0.3mol/(L·s) D.υ(D)=1.6mol/(L·s)
4.在某一化学反应中,反应物A的浓度在10s内从0.8mol·L-1变为0.2mol·L-1,则在这10s内A的化学反应
速率为
A.0.02mol·L-1 B.0.02mol·L-1·s-1
C.0.06mol·L-1·s-1 D.0.06mol·L-1·min-1
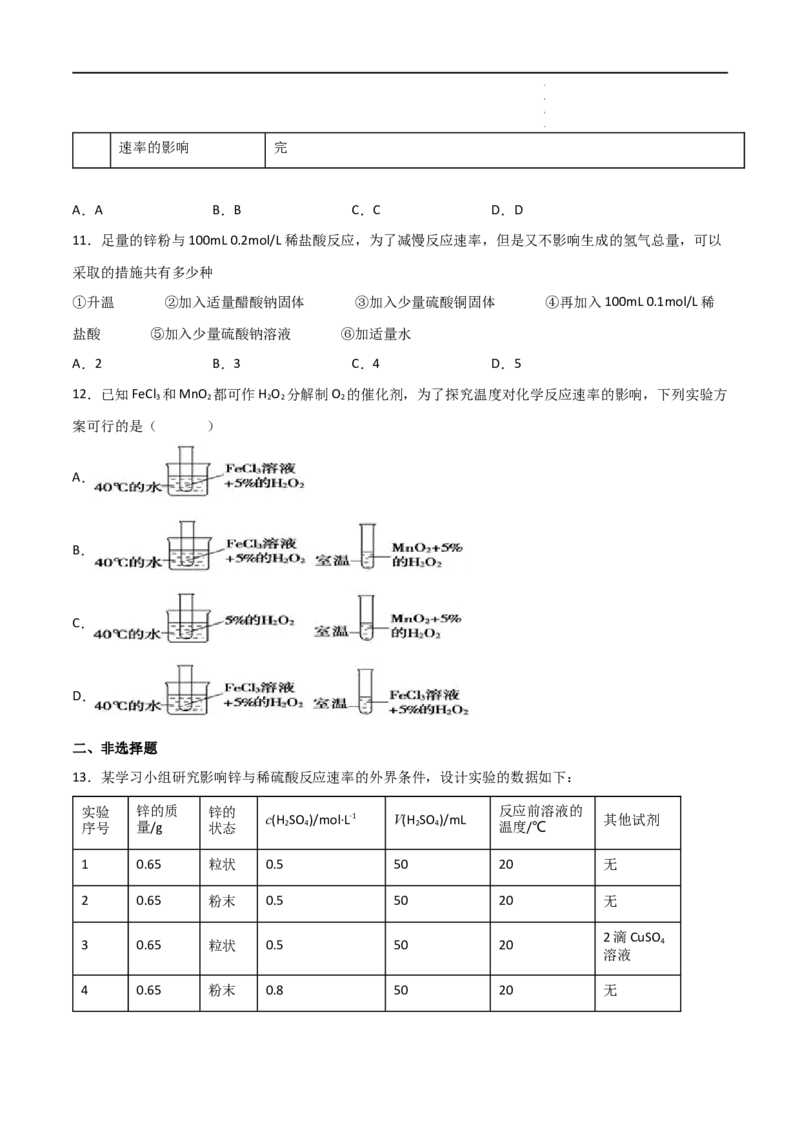
5.可知某可逆反应在密闭容器中进行:A(g)+2B(g) 3C(g)+D(s) ΔH<0,图中曲线b代表一定条件下该反
应的进程。若使曲线b变为曲线a,可采取的措施是⇌
①增大A的浓度;②缩小容器的容积;③增大B的浓度;④升高温度;⑤加入合适的催化剂
A.⑤ B.②④ C.②⑤ D.②③
学学科科网网((北北京京))股股份份有有限限公公司司6.控制变量法是化学实验的常用方法之一。下表探究影响H O 分解反应速率的因素是
2 2
温度 浓度 体积 催化剂
25℃ 5%H O 5mL FeCl
2 2 3
25℃ 5%H O 5mL MnO
2 2 2
A.温度 B.浓度 C.体积 D.催化剂
7.下列说法正确的是
A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以增大生成氢气的速率
B.100mL 2mol·L-1盐酸与锌片反应,加入适量的氯化钠溶液,反应速率不变
C.二氧化硫的催化氧化是一个放热反应,升高温度,反应速率降低
D.汽车尾气中的NO和CO可以缓慢反应生成N 和CO ,使用催化剂可以增大反应速率
2 2
8.在密闭容器中,SO 在400~500℃下催化氧化:2SO +O 2SO ,这是一个正反应放热的可逆反应。下
2 2 2 3
列操作中不能加快正反应速率的是
A.使用催化剂 B.适当提高反应温度
C.适当增加O 的用量 D.及时移走生成的SO
2 3
9.2A(g)+B(g) 3C(g)+4D(g)的反应,在不同条件下的反应的速率最慢的是
A.v(A)=0.5mol·L-1·min-1
B.v(B)=0.3mol·L-1·min-1
C.v(C)=1.2mol·L-1·min-1
D.v(D)=1.6mol·L-1·min-1
10.下列设计的实验方案能达到相应实验目的的是
选
实验目的 实验方案
项
取5mL 0.1mol/L KI溶液,滴加0.1mol/L FeCl 溶液5~6滴,充分反应,可根
A 探究化学反应的限度 3
据溶液中既含I 又含I-的实验事实判断该反应是可逆反应
2
比较Mg与Al的金属
B 常温下,将Mg、Al与NaOH溶液组成原电池
活动性
探究不同催化剂对同 相同条件下,向两支盛有等体积等浓度H O 溶液的试管中分别滴入5滴等
C 2 2
一反应速率的影响 浓度的CuSO 溶液和FeCl 溶液
4 3
D 探究浓度对化学反应 常温下,相同的铁片中分别加入足量的浓、稀硝酸,浓硝酸中铁片先溶解
学学科科网网((北北京京))股股份份有有限限公公司司速率的影响 完
A.A B.B C.C D.D
11.足量的锌粉与100mL 0.2mol/L稀盐酸反应,为了减慢反应速率,但是又不影响生成的氢气总量,可以
采取的措施共有多少种
①升温 ②加入适量醋酸钠固体 ③加入少量硫酸铜固体 ④再加入100mL 0.1mol/L稀
盐酸 ⑤加入少量硫酸钠溶液 ⑥加适量水
A.2 B.3 C.4 D.5
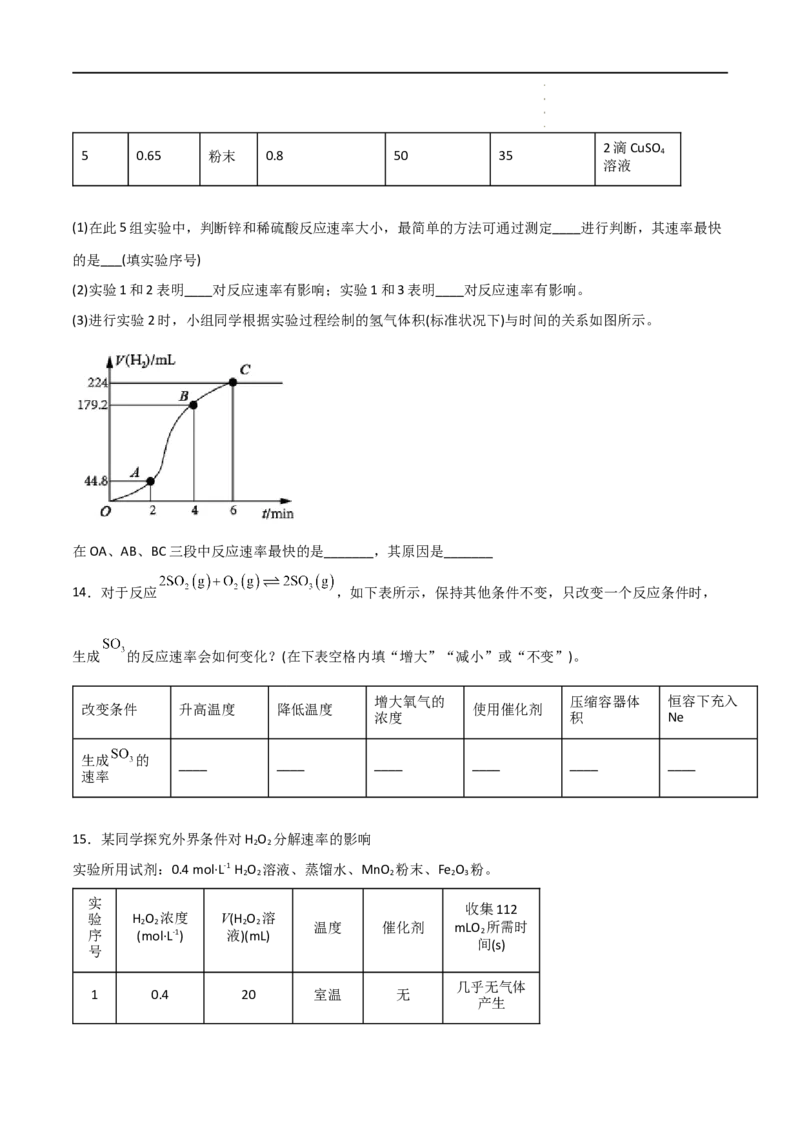
12.已知FeCl 和MnO 都可作H O 分解制O 的催化剂,为了探究温度对化学反应速率的影响,下列实验方
3 2 2 2 2
案可行的是( )
A.
B.
C.
D.
二、非选择题
13.某学习小组研究影响锌与稀硫酸反应速率的外界条件,设计实验的数据如下:
实验 锌的质 锌的 反应前溶液的
c(H SO )/mol·L-1 V(H SO )/mL 其他试剂
序号 量/g 状态 2 4 2 4 温度/℃
1 0.65 粒状 0.5 50 20 无
2 0.65 粉末 0.5 50 20 无
2滴CuSO
3 0.65 粒状 0.5 50 20 4
溶液
4 0.65 粉末 0.8 50 20 无
学学科科网网((北北京京))股股份份有有限限公公司司2滴CuSO
5 0.65 粉末 0.8 50 35 4
溶液
(1)在此5组实验中,判断锌和稀硫酸反应速率大小,最简单的方法可通过测定____进行判断,其速率最快
的是___(填实验序号)
(2)实验1和2表明____对反应速率有影响;实验1和3表明____对反应速率有影响。
(3)进行实验2时,小组同学根据实验过程绘制的氢气体积(标准状况下)与时间的关系如图所示。
在OA、AB、BC三段中反应速率最快的是_______,其原因是_______
14.对于反应 ,如下表所示,保持其他条件不变,只改变一个反应条件时,
生成 的反应速率会如何变化?(在下表空格内填“增大”“减小”或“不变”)。
增大氧气的 压缩容器体 恒容下充入
改变条件 升高温度 降低温度 使用催化剂
浓度 积 Ne
生成 的
____ ____ ____ ____ ____ ____
速率
15.某同学探究外界条件对H O 分解速率的影响
2 2
实验所用试剂:0.4 mol·L-1 H O 溶液、蒸馏水、MnO 粉末、Fe O 粉。
2 2 2 2 3
实
收集112
验 H O 浓度 V(H O 溶
2 2 2 2 温度 催化剂 mLO 所需时
序 (mol·L-1) 液)(mL) 2
间(s)
号
几乎无气体
1 0.4 20 室温 无
产生
学学科科网网((北北京京))股股份份有有限限公公司司50℃水
2 0.4 20 无 296
浴
3 0.4 20 室温 0.5 g a 45
0.5 g
4 0.4 20 室温 100
MnO 粉末
2
5 0.4 b 室温 a >45
(1)实验1、2的目的是其他条件相同时,研究____对H O 分解速率的影响。
2 2
(2)表中a处所用试剂为_。对比实验3、4可得出的结论是__。
(3)实验3、5是其他条件相同时,探究浓度对该化学反应速率的影响。b处取用10 mL 0.4 mol·L-1 H O 溶液,
2 2
还应添加的试剂及用量为___。
(4)控制其他条件相同,印刷电路板的金属粉末用0.4 mol·L-1 H O 溶液和3.0 mol·L-1 H SO 溶液处理。
2 2 2 4
①请配平方程式:___
Cu + H O + H+— Cu2+ + H O
2 2 2
②某同学在不同温度下完成该实验,测得铜的平均溶解速率分别为:
温度(℃) 20 30 40 50 60 70 80
铜的平均溶解速率
7.34 8.01 9.25 7.98 7.24 6.73 5.76
(×10-3 mol·L-1·min-1)
当温度高于40℃时,铜的平均溶解速率随着反应温度的升高而下降,其主要原因是:______。
学学科科网网((北北京京))股股份份有有限限公公司司学学科科网网((北北京京))股股份份有有限限公公司司