文档内容
1.2.1 电解质的电离 练习(解析版)
1.下列物质中,属于电解质的是( )
A.二氧化氮 B.蔗糖 C.铜 D.硝酸钾
【答案】D
【解析】二氧化氮和蔗糖不属于酸、碱、盐所以为非电解质;铜是单质既不是电解质也不是非
电解质;硝酸钾属于盐,所以是电解质。
2.化学兴趣小组在家中进行化学实验,按照左图连接好线路发现灯泡不亮,按照右图连接好线路
发现灯泡亮,由此得出的结论正确的是( )
A.NaCl是非电解质
B.NaCl溶液是电解质
C.NaCl在水溶液中电离出了可以自由移动的离子
D.NaCl溶液中,水电离出大量的离子
【答案】C
【解析】NaCl属于盐,所以是电解质,A错误。NaCl溶液是混合物所以不是电解质,B错
误;氯化钠固体溶于水后在水分子的作用下,发生电离,电离为可以移动的离子使溶液导电,C正
确;氯化钠溶于水是氯化钠发生了电离,水的电离实际很微弱,D错误。
3.下列叙述中正确的是( )
A.能电离出氢离子的化合物是酸
B.能电离出氢氧根离子的化合物是碱C.能电离出酸根阴离子的化合物是盐
D.由金属离子(或铵根离子)和酸根阴离子组成的化合物属于盐
【答案】D
【解析】酸、碱、盐是从电离角度对化合物的一种分类。电离出的阳离子全部是 H+的化合物
是酸,电离出的阴离子全部是OH-的化合物是碱,电离时只要能生成金属阳离子和酸根阴离子的
就是盐。所以A、B项说有氢离子、氢氧根离子就是酸、碱,显然错误,应该强调全部;C项说法
不够准确,因为有些盐还能电离出H+、OH-等。
4.对电解质的叙述正确的是( )
A.溶于水后得到的溶液能导电的物质
B.NaCl溶液在电流作用下电离成Na+和Cl-
C.NaCl是电解质故NaCl晶体能导电
D.氯化氢溶于水能导电,但气态氯化氢不能导电
【答案】D
【解析】电解质首先必须是化合物,所以A项说是物质就错误了;氯化钠电离是在水分子作用
下发生的,与是否有电流无关,B错误;氯化钠固体中离子不能移动,所以不导电,C错误;HCl
是电解质溶于水电离为氢离子和氯离子,溶液导电,气态氯化氢中存在的只有氯化氢分子,所以不
导电,D正确。
5.下列电离方程式中正确的是( )
A.HSO ===H+SO
2 4
B.Ca(OH) ===Ca2++(OH)
2
C.AlCl ===Al+3+3Cl-
3
D.Al (SO )===2Al3++3SO
2 4 3
【答案】D
【解析】(1)酸有一元酸和多元酸,碱有一元碱和多元碱,写电离方程式时,注意 H+和OH-的个数;盐的阴离子和阳离子也可能有多个,书写电离方程式时,同样要注意个数,故选项A和选项
B错;(2)书写电离方程式时,离子符号要正确,例:没有 H和(OH)这两种形式的离子;另外,离
子右上角的电荷数的书写不同于化合价,故选项C错。
6.下列电离方程式不正确的是( )
A.Ca(OH) ===Ca2++2OH-
2
B.KNO===K++NO
3
C.HSO ===2H++SO
2 4
D.NaSO ===Na+SO
2 3
【答案】D
【解析】NaSO 的电离方程式应该为NaSO ===2Na++SO。
2 3 2 3
7.NaHSO 在水溶液中能够电离出H+、Na+和SO。对于NaHSO 的分类不正确的是( )
4 4
A.NaHSO 是盐 B.NaHSO 是酸式盐
4 4
C.NaHSO 是钠盐 D.NaHSO 是酸
4 4
【答案】D
【解析】只有电离时生成的阳离子全部是氢离子的化合物才是酸,而NaHSO 电离出的阳离子
4
除了H+外还有Na+。
8.今有一种固体化合物X,X本身不导电,但熔融状态或溶于水中能够电离,下列关于该化合物
X的说法中,正确的是( )
A.X一定为电解质 B.X固体不导电的原因一定是该固体中不存在离子
C.X只能是盐类 D.X可以是任何化合物
【答案】A
【解析】电解质的定义就是:溶于水或熔融状态下能导电的化合物,A正确;固体不导电可能
是因为其中有离子但是离子不能移动,B错误;X可以是氢氧化钠之类的碱,C错误;D明显不合
理。9.下列物质的分类组合正确的是( )
A B C D
化合物 HCl NaOH Cu (OH) CO FeSO ·7H O
2 2 3 4 2
氧化物 HO NaO CO Fe O
2 2 3 4
电解质 浓盐酸 纯碱晶体 胆矾溶液 铁
【答案】B
【解析】A中浓盐酸为混合物;C中胆矾溶液为混合物;D中铁为单质。注意:纯碱晶体是含
10个结晶水的化合物——NaCO·10H O。
2 3 2
10.在溶液导电性实验中,往氢氧化钡溶液中滴加硫酸至过量,灯泡的明亮度变化是:明→暗→
明,下列说法正确的是( )
A.溶液的导电性与溶液中离子的浓度有关
B.溶液的导电性与溶液中离子数目的多少有关
C.灯泡最暗时溶液中无自由移动的离子
D.往氢氧化钡溶液中滴加盐酸与滴加硫酸时现象相同
【答案】A
【解析】溶液之所以能导电,是因溶液中有自由移动的离子,离子浓度越大,导电性越强,A
正确;溶液离子数目多,浓度不一定大,B错;BaSO 溶液中有自由移动的Ba2+和SO,只不过
4
BaSO 难溶,以上离子浓度较小,导电性较弱,或不易测出其导电性,C错;若在Ba(OH) 溶液中
4 2
滴加盐酸,Ba(OH) +2HCl===BaCl +2HO,BaCl 易溶于水,故灯泡一直亮,D错。
2 2 2 2
11.以下12种为中学化学中常见的物质:
①Cu ② NaCl ③ NaHSO ④ SO ⑤ HSO ⑥ C HOH ⑦CaCO ⑧ BaSO
4 3 2 4 2 5 3 4
⑨Cu(OH)
2
⑩Fe(OH) ⑪NaOH ⑫NH ·H O
3 3 2
请按下列分类标准回答问题:
(1)属于电解质的是_______________________________。(2)能电离出H+的是________,属于酸的是__________________。
(3)属于碱的是________,其中属于难溶性碱的是________。
(4)属于难溶盐的是________。
【答案】(1)②③⑤⑦⑧⑨⑩⑪⑫ (2)③⑤ ⑤ (3)⑨⑩⑪⑫ ⑨⑩ (4)⑦⑧
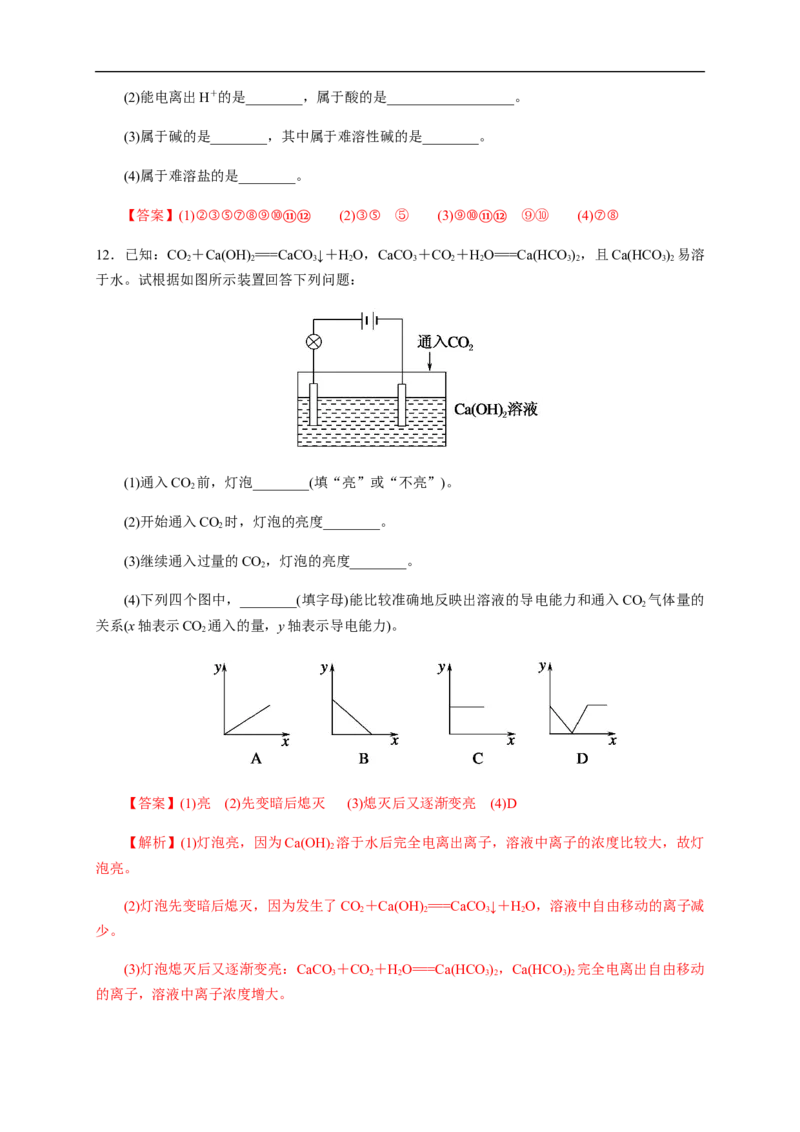
12.已知:CO +Ca(OH) ===CaCO ↓+HO,CaCO +CO +HO===Ca(HCO ) ,且Ca(HCO ) 易溶
2 2 3 2 3 2 2 3 2 3 2
于水。试根据如图所示装置回答下列问题:
(1)通入CO 前,灯泡________(填“亮”或“不亮”)。
2
(2)开始通入CO 时,灯泡的亮度________。
2
(3)继续通入过量的CO,灯泡的亮度________。
2
(4)下列四个图中,________(填字母)能比较准确地反映出溶液的导电能力和通入CO 气体量的
2
关系(x轴表示CO 通入的量,y轴表示导电能力)。
2
【答案】(1)亮 (2)先变暗后熄灭 (3)熄灭后又逐渐变亮 (4)D
【解析】(1)灯泡亮,因为Ca(OH) 溶于水后完全电离出离子,溶液中离子的浓度比较大,故灯
2
泡亮。
(2)灯泡先变暗后熄灭,因为发生了CO+Ca(OH) ===CaCO ↓+HO,溶液中自由移动的离子减
2 2 3 2
少。
(3)灯泡熄灭后又逐渐变亮:CaCO +CO +HO===Ca(HCO ) ,Ca(HCO ) 完全电离出自由移动
3 2 2 3 2 3 2
的离子,溶液中离子浓度增大。(4)由于通入CO 后溶液中自由移动的离子的浓度逐渐减小,所以一开始导电能力逐渐下降,随
2
着反应的进行,离子浓度逐渐增大,导电能力又逐渐增大,所以选D。