文档内容
1995 年吉林高考化学真题及答案
一、选择题(本题包括5小题,每小题3分,共15分.每小题只有一个选项符合题意.)
请分别比较1-3小题中前后2个值的大小.用(A),(B),(C),(D)表示前者和后者的关系.
1.(3分)N和Ne的原子半径( )
A.大于
B.小于
C.等于
D.不能肯定
2.(3分)F 和Br 的沸点( )
2 2
A.大于
B.小于
C.等于
D.不能肯定
3.(3分)17O和 16O原子的核外电子数( )
8 8
A.大于
B.小于
C.等于
D.不能肯定
4.(3分)据报道,1994年12月科学家发现了一种新元素,它的原子核内有161个中子,
质量数为272.该元素的原子序数为( )
A.111
B.161
C.272
D.433
5.(3分)下列物质中,既可与盐酸反应,又可与氢氧化钠溶液反应的是( )
A.NaHSO
4
B.NaHCO
3
C.NaSO
2 3
D.NHNO
4 3
第1页 | 共10页二、选择题(本题包括15小题,每小题3分,共45分.每小题有一个或两个选项符合题
意.若正确答案只包括一个选项,多选时,该题为0分:若正确答案包括两个选项.只选一
个且正确的给1分,选两个且都正确的给3分,但只要选错一个,该小题就为0分.)
6.(3分)下列溶液中,在空气里既不易被氧化,也不易分解,且可以用无色玻璃试剂瓶存
放的是( )
A.石炭酸
B.氢硫酸
C.氢氟酸
D.醋酸
7.(3分)在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振
荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶.则a和b
分别是( )
A.A
B.B
C.C
D.D
8.(3分)在体积为x L的密闭容器中通入a mol NO和b mol O,反应后容器内氮原子数和氧
2
原子数之比为( )
A.
B.
C.
D.
9.(3分)下列说法正确的是(N 表示阿伏加德罗常数的值)( )
0
A.在常温常压下,11.2L N 含有的分子数为0.5N
2 0
第2页 | 共10页B.在常温常压下,1mol Ne含有的原子数为N
0
C.71g Cl 所含原子数为2N
2 0
D.在同温同压时,相同体积的任何气体单质所含的原子数相同
10.(3分)下列离子方程式不正确的是( )
A.氢氧化钡溶液跟盐酸反应OH﹣+H+=HO
2
B.三氯化铁溶液跟过量氨水反应Fe3++3NH•HO=Fe(OH)↓3NH+
3 2 3 4
C.小苏打溶液跟烧碱溶液反应HCO﹣+OH﹣=CO2﹣+HO
3 3 2
D.氯气通入冷水中Cl+HO=Cl﹣+ClO﹣+2H+
2 2
11.(3分)在pH=1的溶液中,可以大量共存的离子组是( )
A.Na+,K+,S2﹣,Cl﹣
B.Al3+,Mg2+,SO2﹣,Cl﹣
4
C.K+,Na+,AlO﹣,NO﹣
2 3
D.K+,Na+,SO2﹣,SO2﹣
4 2 3
12.(3分)100毫升0.1摩/升醋酸与50毫升0.2摩/升氢氧化钠溶液混和,在所得溶液中
( )
A.[Na+]>[CHCOO﹣]>[OH﹣]>[H+]
3
B.[Na+]>[CHCOO﹣]>[H+]>[OH﹣]
3
C.[Na+]>[CHCOO﹣]>[H+]=[OH﹣]
3
D.[Na+]=[CHCOO﹣]>[OH﹣]>[H+]
3
13.(3分)100毫升6摩/升HSO 跟过量锌粉反应,在一定温度下,为了减缓反应进行的速
2 4
度,但又不影响生成氢气的总量.可向反应物中加入适量的( )
A.碳酸钠(固体)
B.水
C.硫酸钾溶液
D.硫酸铵(固体)
14.(3分)甲酸的下列性质中,可以证明它是弱电解质的是( )
A.1摩/升甲酸溶液的pH值约为2
B.甲酸能与水以任何比例互溶
C.10毫升1摩/升甲酸恰好与10毫升1摩/升NaOH溶液完全反应
D.在相同条件下,甲酸溶液的导电性比强酸溶液的弱
第3页 | 共10页15.(3分)下列物质能跟镁反应并生成氢气的是( )
A.甲酸溶液
B.氢氧化钠溶液
C.氯化铵溶液
D.碳酸钠溶液
16.(3分)在下列四种溶液中,分别加入少量固体二氧化锰,能产生气体的是( )
A.3%HO 溶液
2 2
B.1摩/升NaOH溶液
C.1摩/升KClO 溶液
3
D.1摩/升盐酸
17.(3分)将分别盛有熔融的氯化钾、氯化镁、氧化铝的三个电解槽串联,在一定条件下
通电一段时间后,析出钾、镁、铝的物质的量之比为( )
A.1:2:3
B.3:2:1
C.6:3:1
D.6:3:2
18.(3分)在一定温度下,可逆反应A(气)+3B(气) 2C(气)达到平衡的标志是( )
A.C生成的速度与C分解的速度相等
B.单位时间生成n摩尔A,同时生成3n摩尔B
C.A,B,C的浓度不再变化
D.A,B,C的分子数比为1:3:2
19.(3分)反应4NH+5O 4NO+6HO在5升的密闭容器中进行,半分钟后,NO的物质的量
3 2 2
增加了0.3摩尔,则此反应的平均速度 (表示反应物的消耗速度或生成物的生成速度)
为( )
A. O=0.01摩/升•秒
2
B. NO=0.008摩/升•秒
C. HO=0.003摩/升•秒
2
D. NH=0.002摩/升•秒
3
第4页 | 共10页20.(3分)如果定义有机物的同系列是一系列结构式符合AWB(其中n=0,1,2,3…
的化合物.式中A、B是任意一种基团(或氢原子),W为2价有机基团,又称为该同系列的
系差.同系列化合物的性质往往呈现规律性变化.下列四组化合物中,不可称为同系列的是
( )
A.CHCHCHCH CHCHCHCHCH CHCHCHCHCHCH
3 2 2 3 3 2 2 2 3 3 2 2 2 2 3
B.CHCH=CHCHO CHCH=CHCH=CHCHO CH(CH=CH)CHO
3 3 3 3
C.CHCHCH CHCHClCHCH CHCHClCHCHClCH
3 2 3 3 2 3 3 2 3
D.ClCHCHClCCl ClCHCHClCHCHClCCl ClCHCHClCHCHClCHCHClCCl
2 3 2 2 3 2 2 2 3
三、选择题(本题包括6小题,每小题4分,共24分,每小题只有一个选项符合题意.)
21.(4分)C、C、α、α,pH,pH 分别表示2种一元弱酸的物质的量浓度、电离度和溶
1 2 1 2 1 2
液的pH值,如果已知pH<pH,且α>α,则C 和C 的关系( )
1 2 1 2 1 2
A.C>C
1 2
B.C=C
1 2
C.C<C
1 2
D.无法确定
22.(4分)下列各组溶液,不用其它试剂就可以将它们区别开的是( )
A.盐酸、氢氧化钾、硫酸钾、碳酸钾
B.硝酸钠、盐酸、氯化铵、氢氧化钾
C.氯化钡、氯化钙、硫酸钠、硝酸钾
D.氢氧化钾、碳酸钾、硫酸镁、硫酸氢钾
23.(4分)24毫升浓度为0.05摩/升的NaSO 溶液,恰好与20毫升浓度为0.02摩/升的
2 3
KCrO 溶液完全反应,则元素Cr在被还原的产物中的化合价是( )
2 2 7
A.+6
B.+3
C.+2
D.0
24.(4分)(2010秋•日照期末)在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:
9,当1.6克X与Y完全反应后,生成4.4克R,则在此反应中Y和M的质量之比为( )
A.16:9
B.23:9
第5页 | 共10页C.32:9
D.46:9
25.(4分)常温下,向20升真空容器内通入a摩硫化氢和b摩二氧化硫(a和b都是正整
数,且a≤5,b≤5).反应完全后,容器内气体可能达到的最大密度约是( )
A.24.5克/升
B.14.4克/升
C.8克/升
D.5.1克/升
26.(4分)(2015春•随州期末)某温度下,在100克水中加入m克CuSO 或加入n克CuSO
4 4
•5HO,均可使溶液恰好达到饱和,则m与n的关系符合( )
2
A.m= n
B.m=
C.m=
D.m=
四、(本题包括2小题,共15分)
27.(6分)图(1)中瓶a内放入20毫升6摩/升盐酸,b是未充气的气球,里边放有4克
碳酸钙粉未,将它紧紧套在瓶a口上,胶管c套在瓶的侧口,并用弹簧夹d夹紧(瓶口和侧
口都不漏气).将图(1)的装置在托盘天平上称量,质量为W1克.根据实验现象填写下列
空白:
(1)把气球b中的碳酸钙粉末小心地倒入瓶中,立即产生许多气泡,气球逐渐胀大(图
Ⅱ).反应结束后,再次称量,质量为W2克.则W2和W1的关系是 .
(2)取25毫升6摩/升NaOH溶液.先用滴管取少量NaOH溶液,滴管插入胶管c口(为便
于操作,可以适当倾斜瓶a,注意防止漏气).打开d,将溶液挤入瓶中,立即夹紧d.可以
看到瓶内产生少量白色沉淀,轻轻摇动瓶a,沉淀随即消失.用同样方法再加入少量NaOH
溶液,又产生白色沉淀,轻摇,沉淀又消失.使沉淀消失的反应的化学方程式
是 .
(3)将全部NaOH溶液很快加入瓶中,夹紧d,瓶内产生大量白色沉淀,不再溶解.此时瓶
内温度 (填“不变“、“降低“或“升高“).
第6页 | 共10页(4)继续轻摇瓶a,气球逐渐缩小,直至恢复反应前的下垂状.写出这时发生的反应的化
学方程式 .
28.(9分)实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混和酸,加入反应器中.
②向室温下的混和酸中逐滴加入一定量的苯,充分振荡,混和均匀.
③在50﹣60℃下发生反应,直至反应结束.
④除去混和酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤.
⑤将用无水CaCl 干燥后的粗硝基苯进行蒸馏,得到纯硝基苯.
2
填写下列空白:
(1)配制一定比例浓硫酸与浓硝酸混和酸时,操作注意事项是: .
(2)步骤③中,为了使反应在50﹣60℃下进行,常用的方法是 .
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是 .
(4)步骤④中粗产品用5%NaOH溶液洗涤的目的是 .
(5)纯硝基苯是无色,密度比水 (填“小“或“大“),具有 气
味的油状液体.
五、(本题包括3小题,共16分).
29.(3分)一氧化氮是大气污染物之一.目前,有一种治理方法是在400℃左右、有催化剂
存在的情况下,用氨把一氧化氮还原为氮气和水.请写出该反应的化学方程
式 .
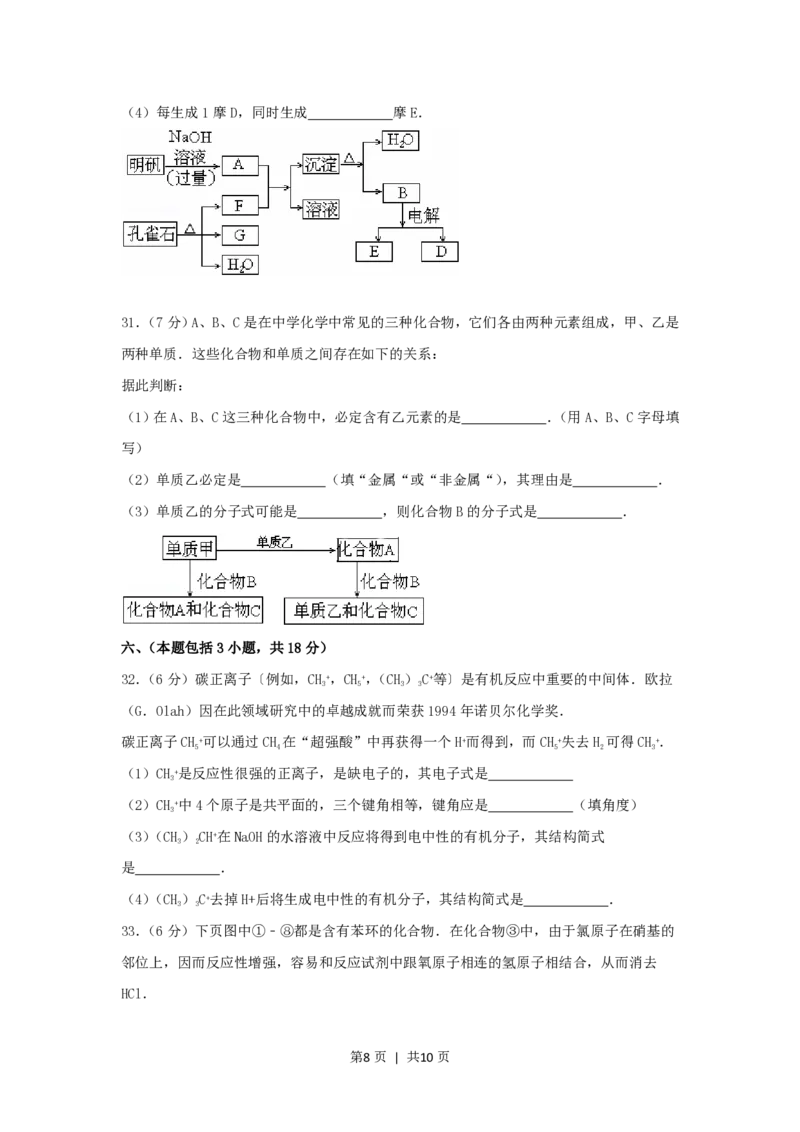
30.(6分)在一定条件下可实现下图所示物质之间的变化:
请填写以下空白:
(1)孔雀石的主要成分是CuCO•Cu(OH)(碱式碳酸铜),受热易分解.下图中的F
3 2
是 .
(2)写出明矾溶液与过量NaOH溶液反应的离子方程式: .
(3)图中所得G和D都为固体,混和后在高温下可发生反应,写出该反应的化学方程
式: .
第7页 | 共10页(4)每生成1摩D,同时生成 摩E.
31.(7分)A、B、C是在中学化学中常见的三种化合物,它们各由两种元素组成,甲、乙是
两种单质.这些化合物和单质之间存在如下的关系:
据此判断:
(1)在A、B、C这三种化合物中,必定含有乙元素的是 .(用A、B、C字母填
写)
(2)单质乙必定是 (填“金属“或“非金属“),其理由是 .
(3)单质乙的分子式可能是 ,则化合物B的分子式是 .
六、(本题包括3小题,共18分)
32.(6分)碳正离子〔例如,CH+,CH+,(CH)C+等〕是有机反应中重要的中间体.欧拉
3 5 3 3
(G.Olah)因在此领域研究中的卓越成就而荣获1994年诺贝尔化学奖.
碳正离子CH+可以通过CH 在“超强酸”中再获得一个H+而得到,而CH+失去H 可得CH+.
5 4 5 2 3
(1)CH+是反应性很强的正离子,是缺电子的,其电子式是
3
(2)CH+中4个原子是共平面的,三个键角相等,键角应是 (填角度)
3
(3)(CH)CH+在NaOH的水溶液中反应将得到电中性的有机分子,其结构简式
3 2
是 .
(4)(CH)C+去掉H+后将生成电中性的有机分子,其结构简式是 .
3 3
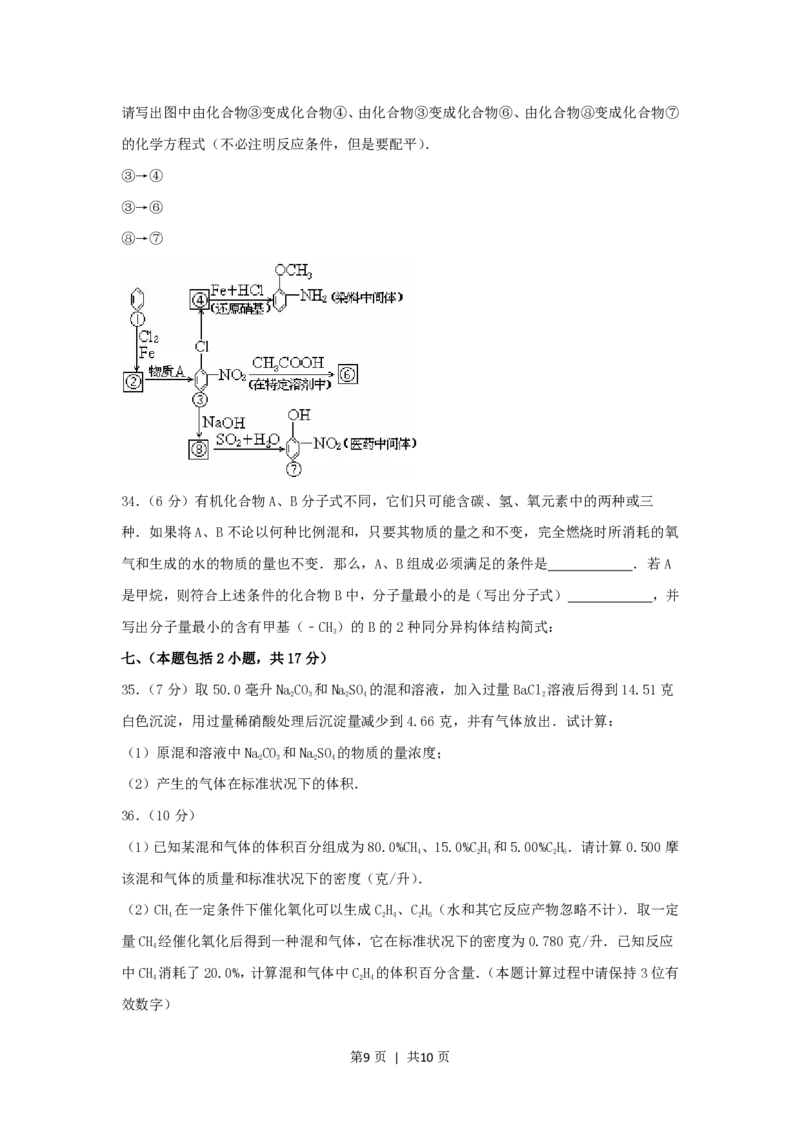
33.(6分)下页图中①﹣⑧都是含有苯环的化合物.在化合物③中,由于氯原子在硝基的
邻位上,因而反应性增强,容易和反应试剂中跟氧原子相连的氢原子相结合,从而消去
HCl.
第8页 | 共10页请写出图中由化合物③变成化合物④、由化合物③变成化合物⑥、由化合物⑧变成化合物⑦
的化学方程式(不必注明反应条件,但是要配平).
③→④
③→⑥
⑧→⑦
34.(6分)有机化合物A、B分子式不同,它们只可能含碳、氢、氧元素中的两种或三
种.如果将A、B不论以何种比例混和,只要其物质的量之和不变,完全燃烧时所消耗的氧
气和生成的水的物质的量也不变.那么,A、B组成必须满足的条件是 .若A
是甲烷,则符合上述条件的化合物B中,分子量最小的是(写出分子式) ,并
写出分子量最小的含有甲基(﹣CH)的B的2种同分异构体结构简式:
3
七、(本题包括2小题,共17分)
35.(7分)取50.0毫升NaCO 和NaSO 的混和溶液,加入过量BaCl 溶液后得到14.51克
2 3 2 4 2
白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66克,并有气体放出.试计算:
(1)原混和溶液中NaCO 和NaSO 的物质的量浓度;
2 3 2 4
(2)产生的气体在标准状况下的体积.
36.(10分)
(1)已知某混和气体的体积百分组成为80.0%CH、15.0%CH 和5.00%CH.请计算0.500摩
4 2 4 2 6
该混和气体的质量和标准状况下的密度(克/升).
(2)CH 在一定条件下催化氧化可以生成CH、CH(水和其它反应产物忽略不计).取一定
4 2 4 2 6
量CH 经催化氧化后得到一种混和气体,它在标准状况下的密度为0.780克/升.已知反应
4
中CH 消耗了20.0%,计算混和气体中CH 的体积百分含量.(本题计算过程中请保持3位有
4 2 4
效数字)
第9页 | 共10页参考答案
一、选择题(本题包括5小题,每小题3分,共15分.每小题只有一个选项符合题意.)请
分别比较1-3小题中前后2个值的大小.用(A),(B),(C),(D)表示前者和后者的关系.
1.B 2.B 3.C 4.A 5.B
二、选择题(本题包括15小题,每小题3分,共45分.每小题有一个或两个选项符合题意.
若正确答案只包括一个选项,多选时,该题为0分:若正确答案包括两个选项.只选一个且
正确的给1分,选两个且都正确的给3分,但只要选错一个,该小题就为0分.)
6.D 7.D 8.C 9.BC 10.D 11.B 12.A 13.BC 14.A 15.AC
16.A 17.D 18.AC 19.CD 20.C
三、选择题(本题包括6小题,每小题4分,共24分,每小题只有一个选项符合题意.)
21.D 22.D 23.B 24.A 25.B 26.B
四、(本题包括2小题,共15分)
27.w2=w1(或回答相等)Ca(OH)+2HCl=CaCl+2HO升高2NaOH+CO=NaCO+HO;
2 2 2 2 2 3 2
Ca(OH)+CO=CaCO↓+HO 28.先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和
2 2 3 2
冷却采取50~60℃水浴加热分液漏斗除去粗产品中残留的酸大苦杏仁
五、(本题包括3小题,共16分).
29.4NH+6NO 5N+6HO 30.CO(或二氧化碳)Al3++4OH-=AlO-+2HO3CuO+2Al
3 2 2 2 2 2
3Cu+AlO0.75 31.A、B非金属因为A+B→乙+C,且乙为单质,可知乙元素在A,B
2 3
中分别呈正、负价,所以乙是非金属S(或N)HS(或NH)
2 2 3
六、(本题包括3小题,共18分)
32.120°(CH)CHOH(CH)C=CH 33. 34.A、B的分子式中氢原子数相同,且
3 2 3 2 2
相差n个碳原子,同时相差2n个氧原子(n为正整数)CHO
2 4 2
七、(本题包括2小题,共17分)
35. 36.
第10页 | 共10页