文档内容
必修第一册 第一章 物质及其变化 章末单元测试题
榆次一中 李金虎
一、选择题(每小题只有一个正确选项,每小题3分,共45分)
1.化学为人类的进步做出了巨大贡献。下列过程中,不涉及化学反应的是( )
A.铁矿石炼铁 B.活字印刷
C.煤制药物 D.氯气制消毒液
2. 日常生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )
A.铜铸塑像上出现铜绿[Cu (OH) CO]
2 2 3
B.铁制菜刀生锈
C.大理石雕像被酸雨腐蚀毁坏
D.铝锅表面生成致密的氧化膜
3. 下列现象或新技术应用中,不涉及胶体性质的是( )
A.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀
B.使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血
C.清晨,在茂密的树林中,常常可以看到从枝叶间透过的一道道光柱
D.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
4. 分类法是化学学习中的一种重要方法。下列分类图正确的是( )
5. KOH是我国古代纺织业常用作漂洗的洗涤剂。古代制取KOH的流程如下:
上述流程中没有涉及的化学反应类型是
1
学科网(北京)股份有限公司A.化合反应 B.分解反应
C.置换反应 D.复分解反应
6. 无论在强酸还是强碱溶液中,下列各组离子一定能大量共存的是( )
A.K+、Na+、Cl-、HCO - B.Ca2+、K+、OH-、NO -
3 3
C.K+、Mg2+、NO -、SO 2- D.Na+、K+、Cl-、NO -
3 4 3
7.下列标明电子转移的方向和数目的化学方程式中正确的是( B )
8. 从海水中可以提取溴,主要反应为2Br-+Cl===Br +2Cl-。下列说法中正确的是( )
2 2
A.溴离子具有氧化性
B.氯气是还原剂
C.该反应属于复分解反应
D.氯气的氧化性比溴单质强
9. 下列各反应中,氧化反应与还原反应在同种元素中进行的是( )
A.Cl+2NaOH===NaCl+NaClO+HO
2 2
B.2KClO=====2KCl+3O↑
3 2
C.2KMnO =====KMnO +MnO +O↑
4 2 4 2 2
D.2HO=====2H↑+O↑
2 2 2
10.某溶液中含有较大量的Cl−、CO2-、OH− 3种阴离子,如果只取一次该溶液能够分别将3种阴
3
离子依次检验出来,下列实验操作顺序正确的是( )
①滴加过量的Mg(NO) 溶液 ②过滤 ③滴加AgNO 溶液 ④滴加过量的Ba(NO ) 溶液
3 2 3 3 2
A.①②④②③ B.④②①②③
C.①②③②④ D.④②③②①
11.实验室需配制一种仅含四种离子(不包括水电离出的离子)的无色混合溶液,且在混合溶液中四
种离子的物质的量浓度均相等。下面四个选项中能达到此目的的是( )
A.Na+、K+、SO 2-、Cl− B.Cu2+、K+、SO 2-、NO -
4 4 3
C.H+、K+、HCO -、Cl− D.Mg2+、Na+、Cl−、SO 2-
3 4
12.亚氨基锂(Li NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:
2
2
学科网(北京)股份有限公司LiNH+H ===LiNH +LiH,下列有关说法正确的是( )
2 2 2
A.LiNH中N的化合价是−1价
2
B.该反应中H 既是氧化剂又是还原剂
2
C.该反应是非氧化还原反应
D.该反应中被氧化的元素是氮,被还原的元素是氢
13.如图所示,“探险队员”——硫酸,不小心走进了有许多“吃人的野兽”(即能与硫酸发生化
学反应的物质)的小山,逃生线路有多种,但有一种线路是完全行不通,处处为陷阱,即为入
口→③→⑤→⑦→⑨→出口,则该线路涉及的物质为( )
A.NaCO、Fe(OH) 、Zn、Fe O
2 3 3 2 3
B.SO 、Cu、BaCl 、HCl
3 2
C.Zn、Fe(OH) 、KNO、CuO
3 3
D.SO 、Cu、NaCl、CuO
3
14. 常温下,在下列溶液中发生如下反应:
①16H++10Z-+2XO===2X2++5Z+8HO;
2 2
②2A2++B ===2A3++2B-;
2
③2B-+Z===B +2Z-。
2 2
由此判断下列说法错误的是( )
A.反应Z+2A2+===2A3++2Z-可以进行
2
B.Z元素在①③反应中均被还原
C.氧化性由强到弱的顺序是XO、Z、B 、A3+
2 2
D.还原性由强到弱的顺序是A2+、B-、Z-、X2+
15.三聚氰胺可由三聚氰酸[C N(OH) ]制备。三聚氰酸可用于消除汽车尾气中的NO ,已知三聚氰
3 3 3 2
酸中氮元素的化合价为-3价,有关反应原理为
①C N(OH) 3HCNO;
3 3 3
②8HCNO+6NO 7N+8CO+4HO。
2 2 2 2
下列说法正确的是( )
A.反应①中的两种物质是同一种物质
B.反应②中HCNO是氧化剂
C.反应②中NO 是还原剂
2
D.反应②中N 既是氧化产物,又是还原产物
2
二、填空题(本题包括5个小题,共55分)
16.(11分)取少量Fe O 粉末(红棕色)加入适量盐酸,反应后得到的溶液呈_________色。用此溶
2 3
3
学科网(北京)股份有限公司液分别做如下实验:
(1)取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方
程式为 ,此反应属于________反应。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl 溶液,继续煮
3
沸至溶液呈__________色,即制得Fe(OH) 胶体。
3
(3)取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl 溶液,振荡均匀后,将此烧
3
杯(编号甲)与盛有Fe(OH) 胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中
3
的液体,可以看到_______烧杯中的液体产生丁达尔效应。这个实验可以用来区别
___________。
17.(8分) 如下图是一块用FeCl 溶液与Cu反应制作的印刷电路板,其制作原理可用下式表示:
3
2FeCl +Cu===CuCl +2X。
3 2
(1)上式中X物质的化学式为________。
(2)在上述反应中,氧化剂为________,氧化产物为________,将两者的氧化性相比较,
________的氧化性更强。
(3)该反应的离子方程式为_______________________________。
18.(10分)过氧化氢HO(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒的作用来
2 2
清洗伤口。对于下列A~D涉及HO 的反应,填写空白:
2 2
A.NaO+2HCl===2NaCl+HO
2 2 2 2
B.Ag O+HO===2Ag+O↑+HO
2 2 2 2 2
C.2HO===2H O+O↑
2 2 2 2
D.3HO+Cr (SO )+10KOH===2K CrO+3KSO +8HO
2 2 2 4 3 2 4 2 4 2
(1)H O 仅体现氧化性的反应是 (填代号)。
2 2
(2)H O 既体现氧化性又体现还原性的反应是 (填代号)。
2 2
(3)完成NaClO 氧化FeCl 的离子方程式: ClO+ Fe2++ 6H + === Cl-+ Fe3++
3 2
3HO。
2
19.(14分)Ⅰ.2019年9月12日11时26分,我国在太原卫星发射中心用长征四号乙运载火箭,成功
将资源一号02D卫星发射升空。资源一号02D卫星将为国家自然资源资产管理和生态监理工
作提供稳定的数据保障,同时兼顾防灾减灾、环境保护、城乡建设、交通运输、应急管理等相
关领域应用需求。
(1)卫星改变运行的路线时需要喷火消耗燃料,其燃料一般是肼(N H)。肼中N的化合价是
2 4
,肼在空气中燃烧的化学方程式为NH +O=====N +2HO,请用双线桥法标出该反应中
2 4 2 2 2
4
学科网(北京)股份有限公司电子转移的方向和数目: 。
该反应中的氧化剂是 ,被氧化的元素是 ,每生成1个水分子转移 个电子。
(2)近几年来,太原市在环境保护方面采取了一系列措施,其中的喷雾车、洒水车都是为了降低
空气中的粉尘。含有粉尘的空气是否属于胶体 (填“是”或“否”),证明的方法是
。
Ⅱ.(3)黑火药是我国古代四大发明之一,其化学反应方程式为 S+2KNO +3C===K S+3CO↑+
3 2 2
N↑,①上述反应所涉及的物质中属于非电解质的是 ;②上述反应中被还原的元素是
2
。
(4)Fe O 可看作由 Fe O 和 FeO 组成。请写出 Fe O 与盐酸反应的化学方程式:
3 4 2 3 3 4
。
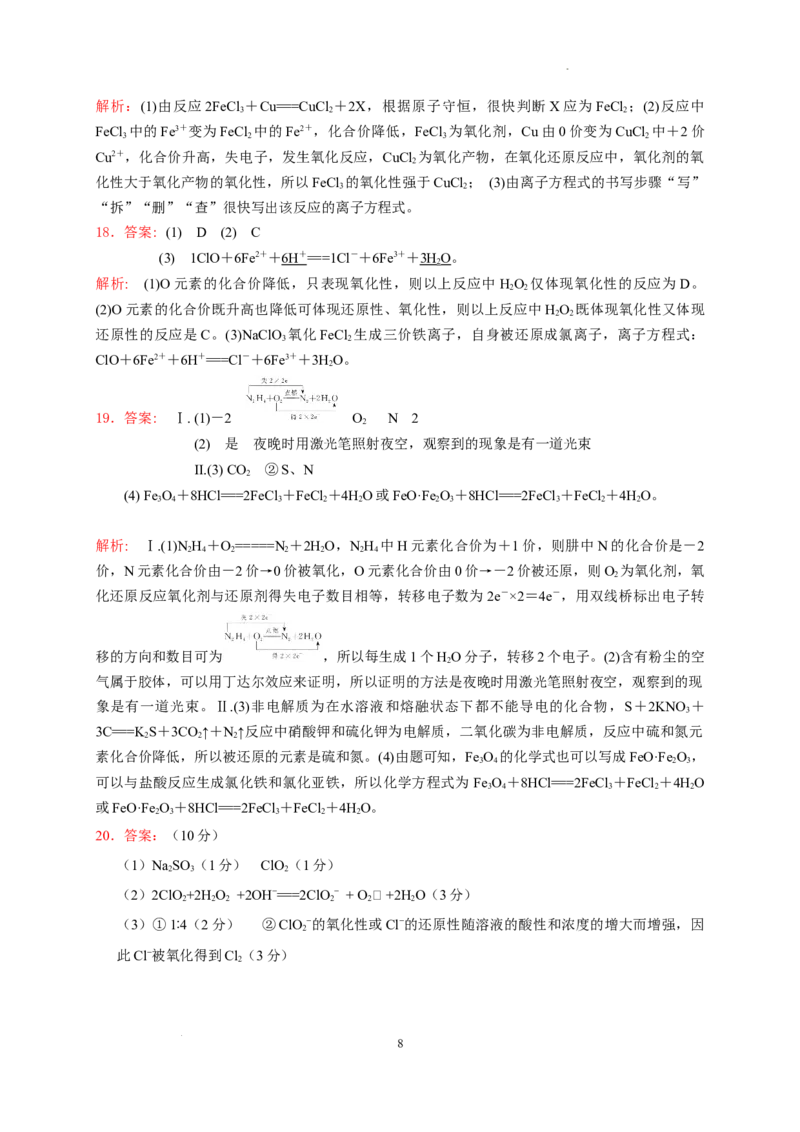
20.(12分)亚氯酸钠(NaClO)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱
2
性环境中稳定存在。某同学查阅资料后设计生产NaClO 的主要流程如下。(部分产品未标出)
2
(1)Ⅰ中发生反应的还原剂是____________、Ⅱ中的氧化剂是________(填化学式)。
(2)Ⅱ中反应的离子方程式是______________________________________。
(3)ClO 是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:
2
5NaClO+4HCl===5NaCl+4ClO ↑+ 2H O。
2 2 2
①该反应中氧化剂和还原剂的个数之比是________。
②研究表明:在上述过程中会发生副反应:NaClO+4HCl===NaCl+2Cl ↑+2H O,若反应开始
2 2 2
时盐酸浓度越大,则气体产物中Cl 的含量越大。请推测其原因是______。
2
1.答案:B
解析:铁矿石炼铁过程中有新的物质(如铁单质)生成,属于化学变化,涉及化学反应,故A不符合
题意;活字印刷过程中没有新的物质生成,属于物理变化,不涉及化学反应,故 B符合题意;用煤
为原料制取药物的过程中有新的物质生成,属于化学变化,涉及化学反应,故 C不符合题意;氯气
与氢氧化钠溶液反应生成次氯酸钠,有新的物质生成,属于化学变化,涉及化学反应,故D不符合
题意。
2.答案:C
解析:金属铜和氧气、二氧化碳、水发生化合反应生成铜绿,该反应中有元素化合价的变化,属于
氧化还原反应,故A不选;铁锈的主要成分是三氧化二铁,有元素化合价的变化,属于氧化还原反
5
学科网(北京)股份有限公司应,故B不选;酸雨腐蚀大理石雕像是因为碳酸钙能和酸反应,该反应中没有元素化合价的变化,
不是氧化还原反应,故C选;铝易被氧气氧化生成氧化铝,该反应中有元素化合价的变化,属于氧
化还原反应,故D不选。
3.答案:A
解析:A项为FeCl +3NaOH===Fe(OH) ↓+3NaCl,即生成沉淀而非胶体;血液是胶体,B项是胶体
3 3
的聚沉;C项为胶体的丁达尔效应;D项为血液的渗析,有毒物质可透过半透膜与血液分离,而血
液中蛋白质等分散质粒子不能透过半透膜仍留在血液中。
4.答案:C
解析:氧化物中CO既不是酸性氧化物,也不是碱性氧化物,A项错误;纯净物中的化合物分为电
解质和非电解质,单质也属于纯净物,但它既不是电解质,也不是非电解质,B项错误;置换反应
一定是氧化还原反应,而氧化还原反应不一定是置换反应,C项正确;化学反应不仅仅包括四种基
本反应类型,D项错误。
5.答案:C
解析:该流程中发生的反应依次是:CaCO CaO+CO ↑(分解反应),CaO+H O Ca(OH) (化
3 2 2 2
合反应),Ca(OH) +K CO CaCO ↓+2KOH(复分解反应)。
2 2 3 3
6.答案:D
解析:A项,若在强酸溶液中,大量H+与HCO反应会生成CO 气体;若在强碱溶液中,大量OH-
2
与HCO反应会生成HO和CO,错误。B项,大量Ca2+与OH-反应会生成微溶物Ca(OH) ,此外若
2 2
在强酸溶液中,OH-与H+反应会生成HO,错误。C项,若在强碱溶液中,大量OH-与Mg2+反应
2
会生成Mg(OH) 沉淀,错误。D项,无论是在强酸还是强碱溶液中,四种离子均可大量共存,正确。
2
7.答案:B
解析:A项,锌元素失去电子,氢元素得到电子,错误;B项,氯酸钾中氯元素由+5价降低到0
价,得到5个电子,HCl中氯元素由-1价升高到0价,共失去5个电子,正确;C项,2 个铁原子
失去6 个电子,3个氯气分子得到6 个电子,错误;D项,1 个铜原子失去2 个电子,硝酸中的
氮原子得到2 个电子,错误。
8.答案:D
解析:Br-是最低价,不可能具有氧化性,A项错误;从离子方程式可看出Cl 得电子,是氧化剂,
2
B项错误;从基本反应类型来看,该反应属于置换反应,C项错误;氯气将Br-氧化为Br ,说明
2
Cl 的氧化性比溴单质强。
2
9.答案:A
解析:A项中部分氯元素的化合价由0价升高到+1价,被氧化,同时部分氯元素的化合价由 0价
降低到-1价,被还原,氧化反应与还原反应在同种元素(氯元素)中进行,而另外三个选项得、失
电子均在不同元素中进行。
10.答案:B
6
学科网(北京)股份有限公司解析:检验Cl−要用到AgNO 溶液,干扰离子为OH−、CO2-;检验OH−要用到Mg(NO) 溶液,干扰
3 3 3 2
离子为CO2-,所以应先检验CO2-。综合分析实验操作顺序应为:④(检验CO2-)、②(除去BaCO 沉
3 3 3 3
淀)、①(检验OH−)、②[除去(Mg(OH) 沉淀]、③(检验Cl−)。
2
11.答案:D
解析:A项,若四种离子的浓度均相等,溶液中正、负电荷的总数不相等;B项,含有Cu2+,溶液
为蓝色;C项,H+和HCO -不能大量共存。
3
12.答案:B
解析:LiNH中氮的化合价为−3价,A错;该反应中H 中H元素化合价一部分变为+1价、一部分
2 2
变为−1价,H 既是氧化剂又是还原剂,B对;反应前后元素化合价发生了变化,该反应是氧化还
2
原反应,C错;该反应中被氧化和被还原的元素都是氢,D错。
13.答案:A
解析:该路线完全行不通,说明所有物质均与硫酸反应;NaCO、Fe(OH) 、Zn、Fe O 都能与硫酸
2 3 3 2 3
反应,故A符合题意;SO 、HCl不能与硫酸反应,故B不符合题意;KNO 不能与硫酸反应,故C
3 3
不符合题意;SO 、NaCl不能与硫酸反应,故D不符合题意。
3
14.答案:B
解析:Z元素在①反应中被氧化,B项错误。依据氧化剂的氧化性强于氧化产物,还原剂的还原性
强于还原产物,可得出:氧化性XO>Z >B >A3+,还原性A2+>B->Z->X2+,由还原性:A2+
2 2
>Z-可知,A项反应可以进行。
15.答案:D
解析:①中两种物质是两种不同的物质,A错误;反应②中NO 为氧化剂,HCNO为还原剂,N 既
2 2
是氧化产物也是还原产物。
16.答案:(10分)
棕黄
(1)FeCl +3NaOH===3NaCl+Fe(OH) ↓ 复分解反应
3 3
(2)红褐
(3)乙 胶体和溶液
解析: Fe O 粉末与盐酸反应生成氯化铁和水,因此反应后得到的溶液呈棕黄色。(1)取少量溶液
2 3
置于试管中,滴入几滴NaOH溶液,二者反应生成氢氧化铁红褐色沉淀和氯化钠,反应的化学方程
式为FeCl +3NaOH===3NaCl+Fe(OH) ↓,此反应属于复分解反应反应。(2)在小烧杯中加入20 mL
3 3
蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 FeCl 溶液,继续煮沸至溶液呈红褐色,即制得
3
Fe(OH) 胶体。(3)胶体可以产生丁达尔效应,溶液不能,可以用来区别溶液和胶体,所以可以看
3
到乙烧杯中的液体产生丁达尔效应。
17.答案:(1)FeCl (2)FeCl CuCl FeCl (3)2Fe3++Cu===Cu2++2Fe2+
2 3 2 3
7
学科网(北京)股份有限公司解析:(1)由反应2FeCl +Cu===CuCl +2X,根据原子守恒,很快判断X应为FeCl ;(2)反应中
3 2 2
FeCl 中的Fe3+变为FeCl 中的Fe2+,化合价降低,FeCl 为氧化剂,Cu由0价变为CuCl 中+2价
3 2 3 2
Cu2+,化合价升高,失电子,发生氧化反应,CuCl 为氧化产物,在氧化还原反应中,氧化剂的氧
2
化性大于氧化产物的氧化性,所以FeCl 的氧化性强于CuCl ; (3)由离子方程式的书写步骤“写”
3 2
“拆”“删”“查”很快写出该反应的离子方程式。
18.答案: (1) D (2) C
(3) 1ClO+6Fe2++ 6H + ===1Cl-+6Fe3++3HO。
2
解析: (1)O元素的化合价降低,只表现氧化性,则以上反应中 HO 仅体现氧化性的反应为D。
2 2
(2)O元素的化合价既升高也降低可体现还原性、氧化性,则以上反应中HO 既体现氧化性又体现
2 2
还原性的反应是C。(3)NaClO 氧化FeCl 生成三价铁离子,自身被还原成氯离子,离子方程式:
3 2
ClO+6Fe2++6H+===Cl-+6Fe3++3HO。
2
19.答案: Ⅰ. (1)-2 O N 2
2
(2) 是 夜晚时用激光笔照射夜空,观察到的现象是有一道光束
Ⅱ.(3) CO ②S、N
2
(4) Fe O+8HCl===2FeCl +FeCl +4HO或FeO·Fe O+8HCl===2FeCl +FeCl +4HO。
3 4 3 2 2 2 3 3 2 2
解析: Ⅰ.(1)N H +O=====N +2HO,NH 中H元素化合价为+1价,则肼中N的化合价是-2
2 4 2 2 2 2 4
价,N元素化合价由-2价→0价被氧化,O元素化合价由0价→-2价被还原,则O 为氧化剂,氧
2
化还原反应氧化剂与还原剂得失电子数目相等,转移电子数为2e-×2=4e-,用双线桥标出电子转
移的方向和数目可为 ,所以每生成1个HO分子,转移2个电子。(2)含有粉尘的空
2
气属于胶体,可以用丁达尔效应来证明,所以证明的方法是夜晚时用激光笔照射夜空,观察到的现
象是有一道光束。Ⅱ.(3)非电解质为在水溶液和熔融状态下都不能导电的化合物,S+2KNO +
3
3C===K S+3CO↑+N↑反应中硝酸钾和硫化钾为电解质,二氧化碳为非电解质,反应中硫和氮元
2 2 2
素化合价降低,所以被还原的元素是硫和氮。(4)由题可知,Fe O 的化学式也可以写成FeO·Fe O,
3 4 2 3
可以与盐酸反应生成氯化铁和氯化亚铁,所以化学方程式为 Fe O +8HCl===2FeCl +FeCl +4HO
3 4 3 2 2
或FeO·Fe O+8HCl===2FeCl +FeCl +4HO。
2 3 3 2 2
20.答案:(10分)
(1)NaSO (1分) ClO (1分)
2 3 2
(2)2ClO +2H O +2OH−===2ClO − + O +2HO(3分)
2 2 2 2 2 2
(3)①1∶4(2分) ②ClO −的氧化性或Cl−的还原性随溶液的酸性和浓度的增大而增强,因
2
此Cl−被氧化得到Cl(3分)
2
8
学科网(北京)股份有限公司(2)Ⅱ中ClO 转化为NaClO ,Cl元素化合价降低,ClO 作氧化剂,则HO 作还原剂,化合价升
2 2 2 2 2
高,生成 O ,则有 ClO +H O——O↑+ ClO ,溶液中加入了 NaOH,配平方程式可得:
2 2 2 2 2 2
2ClO +2H O+2OH− ===2ClO − +O +2HO 。 ( 3 ) ① 反 应
2 2 2 2 2 2
5NaClO+4HCl===5NaCl+4ClO ↑+2H O,NaClO 中Cl元素化合价由+3价分别变为−1价和+4价,
2 2 2 2
NaClO 既 是 氧 化 剂 又 是 还 原 剂 , 氧 化 剂 和 还 原 剂 个 数 之 比 是 1∶4 。
2
②NaClO+4HCl===NaCl+2Cl ↑+2H O,反应中,NaClO 作氧化剂,HCl作还原剂,反应开始时,
2 2 2 2
盐酸浓度越大,溶液酸性越强,气体产物的含量增大。可能原因是,溶液酸性增强,导致 NaClO
2
的氧化性增强,Cl−的还原性增强;或者Cl− 的浓度增大,导致Cl−还原性增强。
9
学科网(北京)股份有限公司10
学科网(北京)股份有限公司