文档内容
第一章第1节物质的分类及转化-课时作业2022-2023学年高
中化学人教版(2019)必修第一册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列属于酸性氧化物的是
A. B. C. D.
2.有些古文或谚语包含了丰富的化学知识。下列解释正确的是
A.《本草经集注》中有“孔雀石(碱式碳酸铜)投入苦酒中,涂铁皆作铜色”。碱式碳
酸铜属于碱类
B.“秋霜欲下手先知,灯底裁缝剪刀冷”中“剪刀冷”说明金属熔点低
C.“熬胆矾铁釜,久之亦化为铜”该过程发生了置换反应
D.“玉不琢不成器”,“百炼方能成钢”发生的均为化学变化
3.纳米孔气凝胶保温毡是由二氧化硅气凝胶和玻璃纤维组成的复合保温材料,该材料
具有保温性能好、防火性能卓越、稳定性高等优点。下列说法不正确的是
A.该材料能溶于水
B.该材料对铁质管道没有腐蚀性
C.二氧化硅可用来制造光导纤维
D.用激光笔照射二氧化硅气凝胶可产生丁达尔效应
4.下列关于氧化物分类的说法不正确的组合为( )
①金属氧化物也可以是酸性氧化物;②非金属氧化物一定是酸性氧化物;③碱性氧化
物一定是金属氧化物;④能与酸反应生成盐和水的氧化物一定是碱性氧化物;⑤能与
碱反应生成盐和水的氧化物一定是酸性氧化物
A.③④⑤ B.①②③ C.②④⑤ D.①②③④⑤
5.下列物质分类正确的是
碱 酸 酸性氧化物 纯净物
A NaOH HSO CO 冰水混合物
2 4 2
B 纯碱 HS CaO 石灰石
2
C NaOH NaHSO SO 液氨
4 2
D KOH HNO SO 碘酒
3 3A.A B.B C.C D.D
6.下列说法正确的是( )
A.向饱和FeCl 溶液中逐滴滴加NaOH溶液即可以制备Fe(OH) 胶体
3 3
B.明矾溶于水可产生具有吸附性的胶体粒子,常用于饮用水的杀菌消毒
C.多数合金比成分金属熔点低、硬度大
D.非金属氧化物一定属于酸性氧化物
7.下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
选项 a b c
A S SO SO
2 3
B HNO NO NO
3 2
C Si SiO HSiO
2 2 3
D NH NO NO
3 2
A.A B.B C.C D.D
8.下列关于胶体的说法正确的是
A.有人设想通过特殊的方法将碳酸钙加工成为纳米碳酸钙,纳米碳酸钙是与胶体相
似的分散系
B.氢氧化铁胶体、葡萄糖溶液用激光笔照射,均能观察到一条光亮的通道
C.明矾溶于水能形成胶体,可用于自来水的杀菌消毒
D.胶体的分散质粒子能通过滤纸
9.下列物质在一定条件下能一步实现转化的是( )
A.Cu→CuO→Cu(OH) B.N→NO →HNO
2 2 2 3
C.Na→NaOH→Na CO D.S→SO →HSO
2 3 3 2 4
10.下列物质的名称不正确的是( )
A.KAl(SO )·12H O:明矾
4 2 2
B.NaSO:硫代硫酸钠
2 2 3
C.CHCHOCH CH∶乙醚
3 2 2 3
D.(CH)CHCH C(CH):2,4,4-三甲基戊烷
3 2 2 3 3
11.下列叙述正确的是
①将FeCl 饱和溶液煮沸可得到带正电荷的Fe(OH) 胶体
3 3
②0.5 mol HSO 与0.5 mol Ba(OH) 完全反应所放出的热量即为中和热
2 4 2
③因为NaOH与NH Cl反应可以制取氨气,所以NaOH碱性大于NH ·H O,因此钠的
4 3 2
试卷第2页,共3页金属性大于N的
④向新制氯水中加入CaCO 可使溶液中HClO浓度增大
3
⑤Cu与HNO 溶液反应,由于HNO 浓度不同可发生不同的氧化还原反应
3 3
A.③④ B.②③⑤ C.④⑤ D.①⑤
12.下列物质转化在给定条件下不能实现的是
A.S SO HSO B.SiO NaSiO(aq)
3 2 4 2 2 3
HSiO(胶体)
2 3
C.Fe FeCl FeCl (aq) D.Al O NaAlO (aq)
3 2 2 3 2
AlCl (aq)
3
二、填空题
13.近年来我国在科技领域取得举世瞩目的成就:
(1)2019年12月27日“胖五”在文昌航天发射场顺利升空。“胖五”的燃料大部分是
零下183℃的①液氧和零下253℃的②液氢——这已经接近低温的极限,所以又被称为
“冰箭”。“胖五”的动力心脏——大推力氢氧发动
机和液氧③煤油发动机都是全新研制的。
(2)2019年3月10日我国长征三号乙运载火箭在西昌卫星发射中西完成第300次发射。
长征三号乙运载火箭一子级上部是装有液体液体④四氧化二氮(N O)的氧化剂箱,下部
2 4
是装有液体偏二甲肼[(CH )NNH]的燃烧剂。
3 2 2
(3)2019年1月3号,嫦娥四号探测器成功着陆在月球背面,标志着我国航天技术发展
进入了新阶段。探测器使用⑤钛合金等新材料,太空舱中利用⑥NiFeO 转化呼出的废
4
气。在上述短文标有序号的物质中,属于混合物的是____,属于单质的是____,属于氧化
物的是____,其主要成分属于有机物的是____,属于盐的是__。(填序号)
14.回答下列问题:
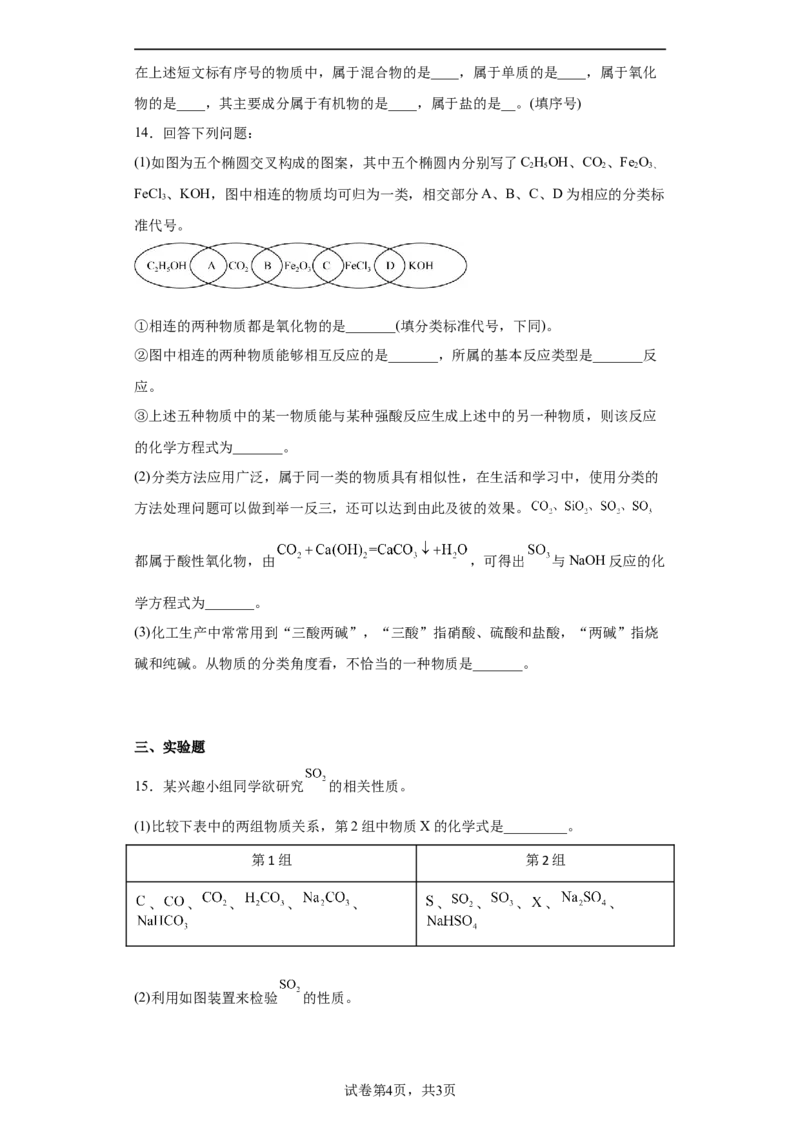
(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了C HOH、CO、Fe O
2 5 2 2 3、
FeCl 、KOH,图中相连的物质均可归为一类,相交部分A、B、C、D为相应的分类标
3
准代号。
①相连的两种物质都是氧化物的是_______(填分类标准代号,下同)。
②图中相连的两种物质能够相互反应的是_______,所属的基本反应类型是_______反
应。
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,则该反应
的化学方程式为_______。
(2)分类方法应用广泛,属于同一类的物质具有相似性,在生活和学习中,使用分类的
方法处理问题可以做到举一反三,还可以达到由此及彼的效果。
都属于酸性氧化物,由 ,可得出 与NaOH反应的化
学方程式为_______。
(3)化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧
碱和纯碱。从物质的分类角度看,不恰当的一种物质是_______。
三、实验题
15.某兴趣小组同学欲研究 的相关性质。
(1)比较下表中的两组物质关系,第2组中物质X的化学式是_________。
第1组 第2组
、 、 、 、 、 、 、 、 、 、
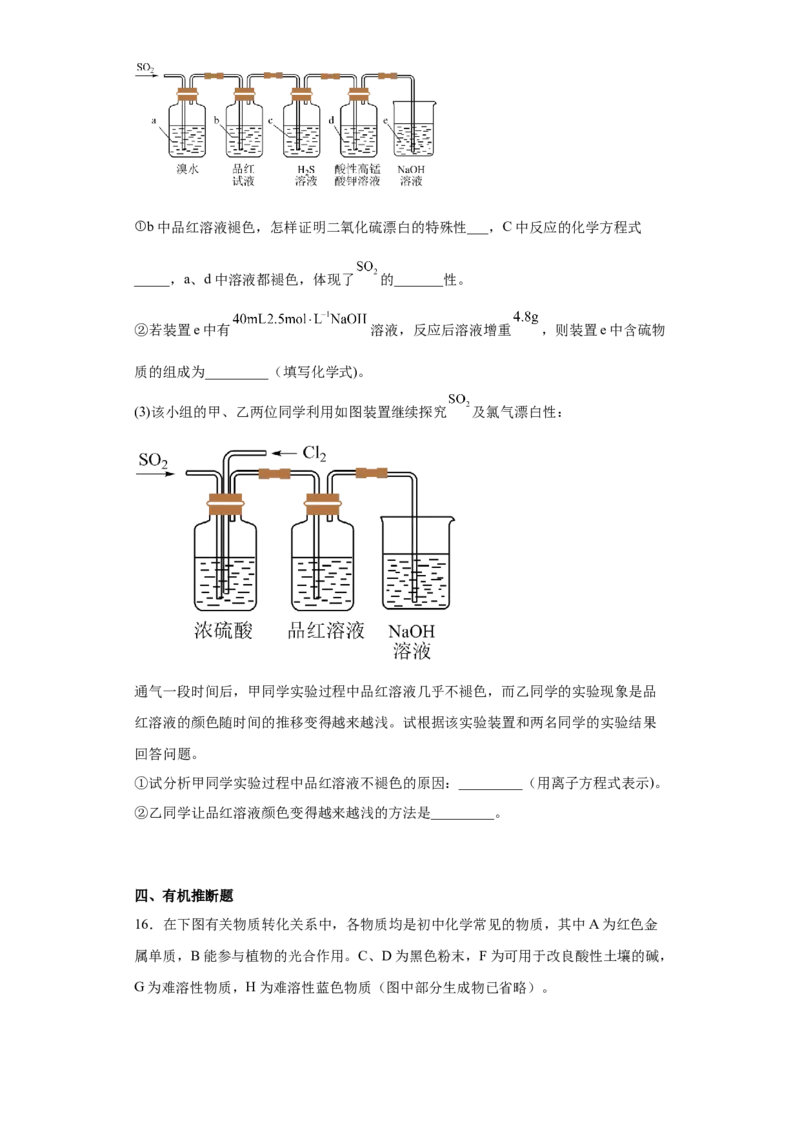
(2)利用如图装置来检验 的性质。
试卷第4页,共3页①b中品红溶液褪色,怎样证明二氧化硫漂白的特殊性___,C中反应的化学方程式
_____,a、d中溶液都褪色,体现了 的_______性。
②若装置e中有 溶液,反应后溶液增重 ,则装置e中含硫物
质的组成为_________(填写化学式)。
(3)该小组的甲、乙两位同学利用如图装置继续探究 及氯气漂白性:
通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品
红溶液的颜色随时间的推移变得越来越浅。试根据该实验装置和两名同学的实验结果
回答问题。
①试分析甲同学实验过程中品红溶液不褪色的原因:_________(用离子方程式表示)。
②乙同学让品红溶液颜色变得越来越浅的方法是_________。
四、有机推断题
16.在下图有关物质转化关系中,各物质均是初中化学常见的物质,其中A为红色金
属单质,B能参与植物的光合作用。C、D为黑色粉末,F为可用于改良酸性土壤的碱,
G为难溶性物质,H为难溶性蓝色物质(图中部分生成物已省略)。(1)用化学式表示: D________,G___________;
(2)写出E与F反应的化学方程式________________________;
(3)光合作用生成的淀粉在人体内变成葡萄糖(C H O),葡萄糖在酶的催化作用
6 12 6
下发生缓慢氧化,同时放出热量,写出葡萄糖发生缓慢氧化反应的化学方程式
______________。
试卷第6页,共3页参考答案:
1.B
【分析】能与碱反应生成盐和水的氧化物是酸性氧化物,据此解答。
【详解】A.NaOH溶于水电离出的阴离子全部是氢氧根离子,属于碱,A不符合;
B.CO 能与碱反应生成盐和水,属于酸性氧化物,B符合;
2
C. 与碱反应会有硝酸钠、亚硝酸钠两种盐,且发生氧化还原反应,不符合酸性氧化
物的定义,C不符合;
D.FeO能与酸反应生成盐和水,属于碱性氧化物,D不符合;
故选:B。
2.C
【详解】A.碱式碳酸铜属于盐,故A错误;
B.“剪刀冷”说明环境温度低,故B错误;
C.“熬胆矾铁釜,久之亦化为铜”该过程发生了硫酸铜和铁的置换反应,故C正确;
D.“玉不琢不成器”,该过程为物质形态改变过程,没有新物质生成,属于物理变化,
故D错误;
故答案选C。
3.A
【详解】A.该材料的主要成分是二氧化硅气凝胶和玻璃纤维,二者不溶于水,A错误;
B.该材料稳定性高,不与铁质管道发生反应,对铁质管道没有腐蚀性,B正确;
C.光导纤维的成分是二氧化硅,二氧化硅可用来制造光导纤维,C正确;
D.二氧化硅气凝胶是胶体,胶体能发生丁达尔效应,D正确;
答案选A。
4.C
【详解】①金属氧化物也可以是酸性氧化物,如MnO 为酸性氧化物,故①正确;
2 7
②非金属氧化物不一定是酸性氧化物,如CO、NO等为不成盐氧化物,故②错误;
③碱性氧化物是和酸反应生成盐和水的氧化物,一定是金属氧化物,故③正确;
④能与酸反应生成盐和水的氧化物不一定是碱性氧化物,如过氧化钠和盐酸反应生成盐和
水、氧气,但发生的是氧化还原反应,故④错误;
⑤能与碱反应生成盐和水的氧化物不一定是酸性氧化物,如NO 和碱反应生成盐和水,但
2
发生的是氧化还原反应,故⑤错误;
因此②④⑤错误,故答案选C。【点睛】本题考查了氧化物分类、氧化物的物质组成和反应、注意概念实质的理解应用,
注意知识积累,答题时注意学会利用举例排除法。
5.A
【详解】A.氢氧化钠是碱、硫酸是酸、二氧化碳是酸性氧化物、冰水混合物是只含有水
分子的纯净物,故A正确;
B.纯碱是盐、氧化钙是碱性氧化物、石灰石是主要成分为碳酸钙的混合物,故B错误;
C. 硫酸氢钠是盐,不是酸,故C错误;
D.碘酒是碘的酒精溶液,属于混合物,故D错误;
故选A。
6.C
【详解】A. 向饱和FeCl 溶液中逐滴滴加NaOH溶液生成氢氧化铁沉淀,应该将饱和氯化
3
铁溶液滴入沸腾的蒸馏水中继续加热至溶液呈红褐色即可以制备Fe(OH) 胶体,A错误;
3
B. 明矾溶于水可产生具有吸附性的氢氧化铝胶体粒子,常用于净水剂,不能用于饮用水的
杀菌消毒,B错误;
C. 多数合金比成分金属熔点低、硬度大,C正确;
D. 非金属氧化物不一定属于酸性氧化物,例如CO、NO等,D错误。
答案选C。
【点睛】选项B是解答的易错点,注意明矾作净水剂的原理与杀菌消毒原理的区别,一般
具有强氧化性的微粒可以杀菌消毒。
7.B
【详解】A.S可生成二氧化硫.二氧化硫和三氧化硫的反应为可逆反应,但SO 无法一步
3
生成S,故A错误;
B.HNO→NO(8HNO+3Cu=3Cu(NO )+2NO↑+4HO),NO→NO
3 3 3 2 2 2
(2NO+O =2NO),NO →NO(3NO +H O=2HNO +NO),NO →HNO
2 2 2 2 2 3 2 3
(3NO +H O=2HNO +NO),故B正确;C.SiO 不能直接生成HSiO,应先与氢氧化钠
2 2 3 2 2 3
等碱溶液反应生成硅酸钠,再与酸反应生成硅酸,故C错误;
D.NH 不能直接生成NO ,氨气被氧化生成NO,故D错误;
3 2
故选B。
8.D
【详解】A.纳米碳酸钙没有形成分散系,因此不具有与胶体相似的性质,A错误;
B.葡萄糖溶液用激光笔照射,不能观察到一条光亮的通道,B错误;
答案第2页,共2页C.明矾溶于水能形成胶体,能够吸附水中悬浮的固体,不具有强氧化性,因此不可用于自
来水的杀菌消毒,C错误;
D.胶体的分散质粒子的直径小于滤纸的缝隙直径,因此能通过滤纸,D正确;
故合理选项是D。
9.C
【分析】A.CuO不溶于水,无法一步反应得到Cu(OH);
2
B.氮气在放电或者加热的条件下转化为一氧化氮,无法一步转化为二氧化氮;
D.硫和氧气发生反应生成二氧化硫,二氧化硫进一步氧化变为三氧化硫;
【详解】A.CuO不溶于水,与水不反应,则CuO→Cu(OH) 不能一步实现,故A不选;
2
B.氮气在放电或高温下生成NO,则N→NO 不能一步实现,故B不选;
2 2
C.Na与水反应生成NaOH、NaOH与二氧化碳反应生成碳酸钠,均可一步实现转化,故C
选;
D.S燃烧生成二氧化硫,则S→SO 不能一步实现转化,故D不选;
3
故选:C。
10.D
【详解】A.明矾是十二水合硫酸铝钾,化学式为KAl(SO )·12H O,A正确;
4 2 2
B.硫代硫酸钠化学式是NaSO,B正确;
2 2 3
C.乙醚结构简式是CHCHOCH CH,C正确;
3 2 2 3
D.(CH)CHCH C(CH):违背烷烃命名选择主链时,应该从离支链较近的一端为起点给
3 2 2 3 3
主链碳原子编号的原则,要尽可能使支链编号最小,该物质正确命名为2,2,4-三甲基戊
烷,D错误;
故合理选项是D。
11.C
【详解】试题分析:①将饱和溶液FeCl 加入沸水中可得到带正电荷的Fe(OH) 胶体胶
3 3
粒,Fe(OH) 胶体不显电性,错误;②SO 2- Ba2+反应生成BaSO,需要放出热量,所以
3 4 和 4
0.5mol H SO 与0.5mol Ba(OH) 完全反应生成1mol水所放出的热量不是中和热,错误;
2 4 2
③NH ·H O不是N元素的最高价氧化物的水化物,不能判断金属性强弱,错误;④新制氯
3 2
水中存在平衡:Cl
2
+H
2
O⇌HCl+HClO,达到平衡后加入少量CaCO
3
(s),HCl与碳酸钙反
应,而HClO不反应,溶液中氢离子浓度减小,平衡向正反应方向移动,HClO浓度增加,
正确;⑤Cu与HNO 溶液反应,由于HNO 浓度不同可发生不同的氧化还原反应,与浓硝酸
3 3
反应生成二氧化氮,与稀硝酸反应生成一氧化氮,正确;故选C。考点:考查了胶体的制备、中和热概念、物质的性质以及平衡移动原理等相关知识。
12.A
【详解】A、硫在氧气中燃烧只能生成二氧化硫,故A错误;
B、SiO+2NaOH=Na SiO+H O ,NaSiO+2HCl=H SiO↓+2NaCl,故B正确;
2 2 3 2 2 3 2 3
C、2Fe+3Cl =2FeCl ,2FeCl +Fe=3FeCl ,故C正确;
2 3 3 2
D、氧化铝与氢氧化钠反应生成偏铝酸钠,偏铝酸钠溶液与过量的盐酸生成三氯化铝,故
D正确;
故选A。
13. ③⑤ ①② ④ ③ ⑥
【分析】根据混合物是由多种微粒构成的物质;单质是仅有一种元素组成的纯净物;氧化
物是由氧和另外一种元素组成的化合物;有机物是含有碳元素的化合物;盐是由金属阳离
子(或铵根离子)与酸根离子组成的化合物分析判断。
【详解】①液氧是液态O,属于单质;
2
②液氢是液态H,属于单质;
2
③煤油是由多种烃组成的混合物,烃是仅由碳、氢两种元素组成的化合物,属于有机物,
因此煤油属于有机物,同时也属于混合物;
④四氧化二氮分子式是NO,是由氧、氮两种元素组成的化合物,属于氧化物;
2 4
⑤钛合金属于合金,合金属于混合物;
⑥NiFeO 是由Ni2+与 通过离子键结合形成的化合物,属于盐。
4
综上所述可知:属于混合物的是③⑤;属于单质的是①②;属于氧化物的是④;其主要成
分属于有机物的是③;属于盐的是⑥。
【点睛】本题考查物质的分类。掌握有关概念及物质的组成成分是解答的关键。
14.(1) B D 复分解 Fe O+6HCl=2FeCl +3H O
2 3 3 2
(2)2NaOH+SO =Na SO +H O
3 2 4 2
(3)纯碱即NaCO
2 3
【详解】(1)①氧化物是指由两种元素其中一种是氧元素的化合物,故CO 和Fe O 属于
2 2 3
氧化物,则组成相连的两种物质都是氧化物的是B,故答案为:B;
②已知C HOH与CO,CO 与Fe O,Fe O 与FeCl 均不反应,FeCl 与KOH能够反应生
2 5 2 2 2 3 2 3 3 3
成Fe(OH) 沉淀和KCl,图中相连的两种物质能够相互反应的是D,方程式为:
3
答案第4页,共2页FeCl +3KOH=Fe(OH) ↓+3KCl,该反应所属的基本反应类型是复分解反应,故答案为:D;
3 3
复分解;
③上述五种物质中的某一物质能与某种强酸反应生成上述中的另一种物质,即Fe O 和HCl
2 3
反应生成FeCl 和HO,则该反应的化学方程式为Fe O+6HCl=2FeCl +3H O,故答案为:
3 2 2 3 3 2
Fe O+6HCl=2FeCl +3H O;
2 3 3 2
(2)由 ,即酸性氧化物和碱反应生成盐和水,故可得出
与NaOH反应的化学方程式为:2NaOH+SO =Na SO +H O,故答案为:
3 2 4 2
2NaOH+SO =Na SO +H O;
3 2 4 2
(3)酸是指在水溶液中电离出的阳离子全部为H+的化合物,故硝酸、硫酸和盐酸均属于
酸,而碱是指在水溶液中电离出的阴离子全部为OH-的化合物,故烧碱即NaOH属于碱,
而纯碱为NaCO 不是碱,而是盐,故从物质的分类角度看,不恰当的一种物质是纯碱即
2 3
NaCO,故答案为:纯碱即NaCO。
2 3 2 3
15. 加热褪色后的溶液恢复红色
还原 和
氯气和二氧化硫不是等物质的量通入
【分析】根据物质的分类排列顺序,可以推断X为硫酸;二氧化硫通过溴水时,溴水褪色,
证明二氧化硫有还原性;二氧化硫通过品红溶液时,溶液褪色,证明二氧化硫有漂白性;
二氧化硫通过硫化氢溶液时,有淡黄色沉淀生成,证明二氧化硫有氧化性;二氧化硫通过
酸性高锰酸钾溶液时,溶液褪色,证明二氧化硫有还原性;最后是尾气处理装置。
【详解】(1)根据物质的分类排列顺序,可以推断X为硫酸第2组中物质X的化学式是
。
(2)①b中品红溶液褪色,加热褪色后的溶液恢复红色可以证明二氧化硫漂白的特殊性,即
漂白后生成物不稳定,受热分解后恢复原来的颜色。C中二氧化硫通过硫化氢溶液时,有
淡黄色沉淀生成,反应的化学方程式为 ,a,d中溶液都褪色,体现了 的还原性。
②若装置e中有 溶液, 的物质的量为0.1mol,若其完全转化
为 ,则可吸收0.05mol ,质量增加3.2g;若其完全转化为 ,则可吸收
0.1mol ,质量增加6.4g;反应后溶液实际增重 ,恰好介于这两个值之间,则装置
e中含硫物质的组成为 和 。
(3)通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红
溶液的颜色随时间的推移变得越来越浅。
①甲同学实验过程中品红溶液不褪色,是因为其通入 和氯气的体积比恰好为1:1,两者
恰好反应生成硫酸和盐酸,而硫酸与盐酸均不具有漂白性;离子方程式为
。
②乙同学的实验现象是品红溶液的颜色随时间的推移变得越来越浅,则乙同学通入的气体
中两种组分的体积比或物质的量之比不是1:1,其中无论哪种过量均可使品红溶液褪色,故
其让品红溶液颜色变得越来越浅的方法是:氯气和二氧化硫不是等物质的量通入。
【点睛】在分析装置e中含硫物质的组成时,可以使用极值法分析。该反应有两个极端情
况,即完全转化为正盐或酸式盐,根据钠元素守恒可以确定吸收二氧化硫的质量,与实际
质量的增加进行对比,即可确定其组成。
16. C BaSO CuSO +Ca(OH) =Cu(OH) ↓+CaSO C H O+6O
4 4 2 2 4 6 12 6 2
6CO+6H O
2 2
【分析】根据各物质均是初中化学常见的物质,A为红色金属单质,所以A是铜,B能参
与植物的光合作用,C、D为黑色粉末,C、D高温会生成铜和B,所以B是二氧化碳,
C、D是氧化铜和碳,C和X生成的E会与氯化钡反应,所以C是氧化铜,D是碳,F为可
用于改良酸性土壤的碱,所以F是氢氧化钙,G为难溶性物质,H为难溶性蓝色物质,所
以E是硫酸铜,硫酸铜和氯化钡反应生成硫酸钡沉淀和氯化铜,所以G是硫酸钡,X是硫
酸,硫酸铜和氢氧化钙反应生成硫酸钙和氢氧化铜沉淀,所以H是氢氧化铜,I是硫酸钙,
答案第6页,共2页然后将推出的物质进行验证即可。
【详解】根据以上分析可知A是铜,B是二氧化碳,C是氧化铜,D是碳,E是硫酸铜,F
是氢氧化钙,G是硫酸钡,X是硫酸,H是氢氧化铜,I是硫酸钙,则
(1)根据以上分析可知D、G的化学式分别是C、BaSO;
4
(2)E与F的反应是氢氧化钙和硫酸铜反应生成硫酸钙和氢氧化铜沉淀,化学方程式为
CuSO +Ca(OH) =Cu(OH) ↓+CaSO ;
4 2 2 4
(3)因为葡萄糖发生缓慢氧化反应生成二氧化碳和水,故化学方程式为C H O+6O
6 12 6 2
6CO+6H O。
2 2
【点睛】在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转
化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可。答案第8页,共2页