文档内容
湖南省常德市汉寿县第一中学2024-2025学年
高一下学期2月月考化学试卷
可能用到的相对原子质量:H-1 N-14 O-16 Na-23 V-51 Fe-56 Cu-64
一、单选题(每题 3 分,共 42 分)
1.在某年端午节前夕,中央电视台新闻频道的《媒体广场》栏目报道了用硫酸铜处理过的
“返青粽叶”,食用其包裹的粽子有害健康。硫酸铜属于
A.酸 B.碱 C.氧化物 D.盐
2.实验室既可用浓盐酸与 在加热时反应制备 ,也可用 与浓盐酸在常温下
反应制备 ,下列有关说法不正确的是
A. 的氧化性比 的强
B.用饱和 溶液除去 中混有的HCl
C.用排气法收集 时,不需要利用其他试剂就能确定集气瓶中已收集满
D.足量 与含 个HCl的浓盐酸在加热条件下反应,得到 的个数小于
3.下列对物质的分类正确的是
选项 酸 碱 盐 酸性氧化物 碱性氧化物
A 烧碱 干冰 CaO
B HCl
C HClO 胆矾 FeO
D 纯碱 NaCl CuO
A.A B.B C.C D.D
4.离子反应在物质制备和分离、物质提纯和鉴定,以及消除水中污染物等方面都有广泛的
应用。下列说法正确的是
A.NaHCO 在水溶液中的电离:NaHCO = Na++H++CO
3 3B.氨水能导电,所以氨水是电解质
C.用铜与稀硝酸反应制备一氧化氮:
D.使酚酞溶液呈红色的溶液中: 、 、 、 能大量共存
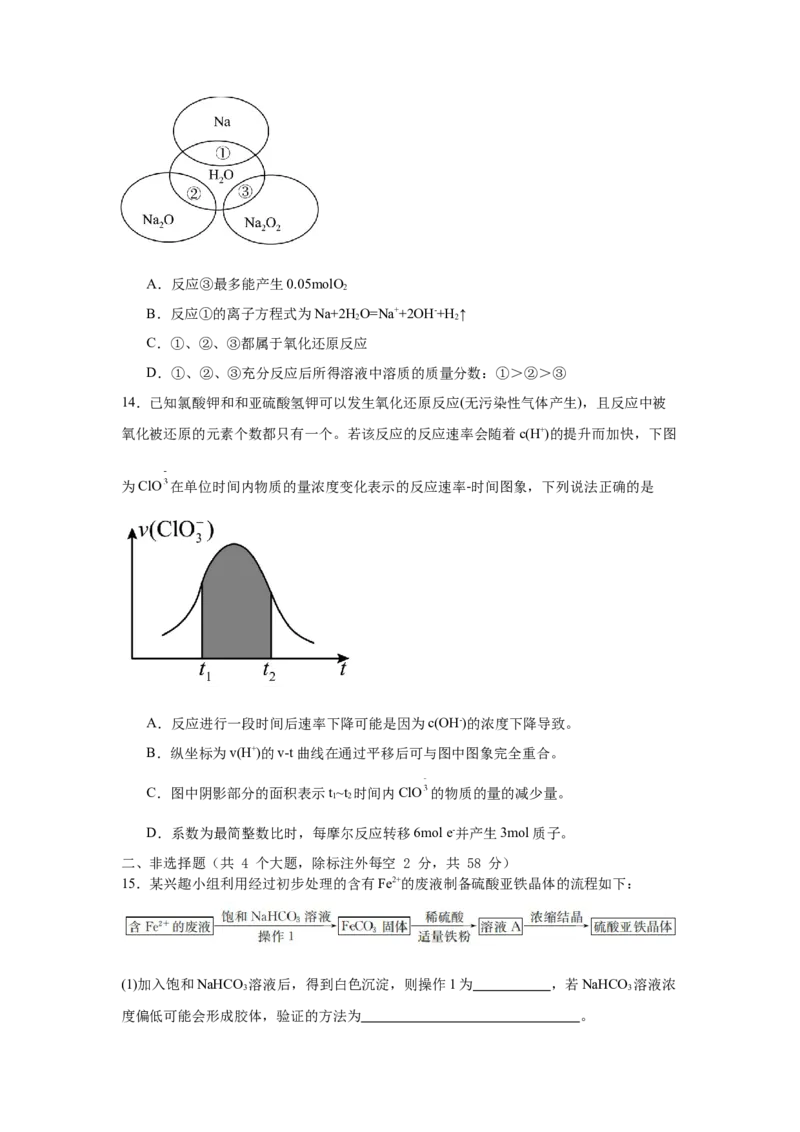
5.某些短周期主族元素的原子序数和主要化合价的关系如图所示。下列说法错误的是
A.②分别与①、④均可构成直线形分子
B.最高价氧化物对应的水化物的碱性:⑤>⑥
C.④与⑤形成的二元化合物中阴阳离子个数比为1:1
D.③、⑦的简单氢化物均能与其最高价氧化物对应水化物反应
6.铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝是同主族元素,元素
符号是Tl,以下对铊的性质推断不正确的是
A.铊是易导电的银白色金属 B.能生成+3价离子
C.氧化铊是两性氧化物 D.Tl3+的氧化性比Al3+弱
7.下列物质中既含有离子键又含有非极性共价键的是
A. B. C. D.
8.室温下,下列实验操作、现象和结论均正确的是
选
实验操作 现象 结论
项
向某溶液中依次滴入几滴 溶液和 溶液先无明显现
A 该溶液中含
新制氯水 象,后变红向浓度均为0.1 的 和 混合
B 先出现黄色沉淀 还原性强于
溶液中滴加0.1 溶液
C 向待测液中加入盐酸酸化的 溶液 有白色沉淀生成 待测液中含有
发出黄色火焰, 金属钠在空气中加
D 将一小块金属钠放在蒸发皿里,加热
生成淡黄色固体 热生成过氧化钠
A.A B.B C.C D.D
9.下列实验中金属或氧化物可以完全溶解的是
A.1mol Cu与含2mol HSO 的浓硫酸共热
2 4
B.1mol MnO 与含2mol HO 的溶液共热
2 2 2
C.常温下1mol Al投入足量的浓硫酸中
D.常温下1mol Cu投入含4mol HNO 的浓硝酸中
3
10.下列关于物质的量的正确说法是
A.可以理解为物质的质量 B.就是物质的粒子数目
C.表示一定数目微粒集合体的物理量 D.符号 ,单位n
11.200℃时, 和水蒸气的混合气体共23.2g与足量的 充分反应后,固体质量增
加了7.2g,则原混合气体中 与 的质量为
A.8.8g,14.4g B.8.6g,14.6g C.8.0g,15.2g D.8.5g,14.7g
12.氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原
产物的还原性。现有以下反应:①Cl+2KBr=2KCl+Br ②KClO +6HCl=
2 2 3
3Cl↑+KCl+3H O(KCl中-1价Cl全部来自于HCl中-1价的Cl)③2KBrO +Cl=Br +2KClO 下
2 2 3 2 2 3
列说法正确的是
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱的顺序为 KBrO >KClO >Cl>Br
3 3 2 2
C.反应②中还原剂与氧化剂的物质的量之比为6∶1
D.反应③中22.4LCl 完全反应,转移电子的物质的量为10mol
2
13.如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应。已知钠及其氧化物
的物质的量均为0.1mol,水的质量为100g。下列说法正确的是A.反应③最多能产生0.05molO
2
B.反应①的离子方程式为Na+2HO=Na++2OH-+H ↑
2 2
C.①、②、③都属于氧化还原反应
D.①、②、③充分反应后所得溶液中溶质的质量分数:①>②>③
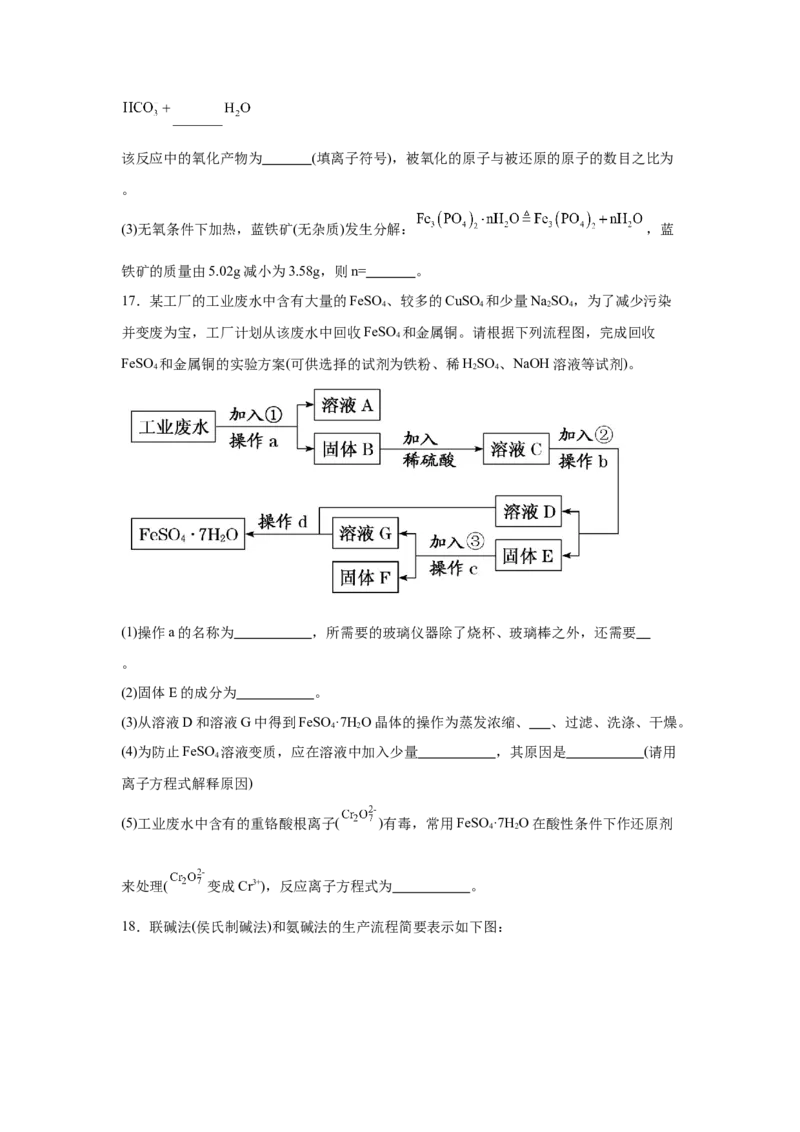
14.已知氯酸钾和和亚硫酸氢钾可以发生氧化还原反应(无污染性气体产生),且反应中被
氧化被还原的元素个数都只有一个。若该反应的反应速率会随着c(H+)的提升而加快,下图
为ClO 在单位时间内物质的量浓度变化表示的反应速率-时间图象,下列说法正确的是
A.反应进行一段时间后速率下降可能是因为c(OH-)的浓度下降导致。
B.纵坐标为v(H+)的v-t曲线在通过平移后可与图中图象完全重合。
C.图中阴影部分的面积表示t~t 时间内ClO 的物质的量的减少量。
1 2
D.系数为最简整数比时,每摩尔反应转移6mol e-并产生3mol质子。
二、非选择题(共 4 个大题,除标注外每空 2 分,共 58 分)
15.某兴趣小组利用经过初步处理的含有Fe2+的废液制备硫酸亚铁晶体的流程如下:
(1)加入饱和NaHCO 溶液后,得到白色沉淀,则操作1为 ,若NaHCO 溶液浓
3 3
度偏低可能会形成胶体,验证的方法为 。(2)加入铁粉的作用是 。
(3)测定废液中Fe2+的浓度可使用已知浓度的酸性高锰酸钾溶液。配平下面方程式,并用双
线桥法表示电子转移过程:KMnO +FeSO+H SO =MnSO +K SO +Fe (SO )+H O;
4 4 2 4 4 2 4 2 4 3 2
。
(4)已知Fe+与NaHCO 按物质的量1:2的比例恰好完全反应,该反应的离子方程式为
3
。
(5)硫酸亚铁在空气中煅烧生成Fe O 和一种酸性氧化物,该反应的化学方程式为
2 3
,该反应中每产生1mol Fe O,转移的电子数为 个。
2 3
16.一方面,磷矿藏在地球上分布不均匀且储量有限;另一方面,污水中含有较多的磷元
素。因此在污水处理生物污泥中的蓝铁矿 因其潜在的特殊用途以及经济
价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
(1)水处理时,加入的高铁酸钾( )作为净水消毒剂,发生反应的化学方程式为
。
① 中Fe的化合价为 价,上述反应涉及的物质中属于盐的是 。
②高铁酸钾可用于净水消毒的原因是
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:
。
_______ _______ _______ _______ ______________
该反应中的氧化产物为 (填离子符号),被氧化的原子与被还原的原子的数目之比为
。
(3)无氧条件下加热,蓝铁矿(无杂质)发生分解: ,蓝
铁矿的质量由5.02g减小为3.58g,则n= 。
17.某工厂的工业废水中含有大量的FeSO 、较多的CuSO 和少量NaSO ,为了减少污染
4 4 2 4
并变废为宝,工厂计划从该废水中回收FeSO 和金属铜。请根据下列流程图,完成回收
4
FeSO 和金属铜的实验方案(可供选择的试剂为铁粉、稀HSO 、NaOH溶液等试剂)。
4 2 4
(1)操作a的名称为 ,所需要的玻璃仪器除了烧杯、玻璃棒之外,还需要
。
(2)固体E的成分为 。
(3)从溶液D和溶液G中得到FeSO ·7H O晶体的操作为蒸发浓缩、 、过滤、洗涤、干燥。
4 2
(4)为防止FeSO 溶液变质,应在溶液中加入少量 ,其原因是 (请用
4
离子方程式解释原因)
(5)工业废水中含有的重铬酸根离子( )有毒,常用FeSO ·7H O在酸性条件下作还原剂
4 2
来处理( 变成Cr3+),反应离子方程式为 。
18.联碱法(侯氏制碱法)和氨碱法的生产流程简要表示如下图:(1)沉淀池中发生反应的化学方程式为 。
(2)X是 ,Y是 (填化学式)。
(3)Z中除了溶解的氨气、食盐外,其它溶质还有 ;排出液W中的溶质除了氢氧化
钙外,还有 。
(4)从理论上分析,在氨碱法生产过程中 (填“需要”或“不需要”)补充氨气。
(5)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确的是 (填序号)。
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气目的是使氯化铵更多析出
c.加入食盐细粉目的是提高 的浓度,促进碳酸氢钠结晶析出
(6)联碱法与氨碱法相比,指出联碱法的一项优点 。
参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 D B A D C C C A D C
题号 11 12 13 14
答案 A B A D
15.(1) 过滤 丁达尔效应(2)防止亚铁离子被氧化
(3)2,10,8,2,1,5,8;
(4)
(5) 2N
A
16.(1) +6 有强氧化性,可以杀灭细菌,生成的氢氧化铁胶
体具有吸附性,能吸附水中的悬浮物
(2) 8;1;15;8;1;21 1:8
(3)8
17.(1) 过滤 漏斗
(2)Fe和Cu
(3)冷却结晶
(4) 铁粉 Fe+2Fe3+=3Fe2+
(5)6Fe2++ +14H+=6Fe3++2Cr3++7H O
2
18.
、NaCl 不需要 b 不产生无用的