文档内容
【冲刺期末】高二化学期末单元复习测试
第三单元 水溶液中的离子反应与平衡
(时间:90分钟 满分:100分)
一、选择题(本题共15小题,每小题3分,共45分。每小题只有一个选项符合题意)
1.(2020河北唐山高二上期末)亚硫酸与氢硫酸都是二元弱酸,下列事实中,不能比较亚硫酸与氢硫酸的酸性
强弱的是
A. 亚硫酸的还原性比氢硫酸弱
B. 相同条件下,导电能力亚硫酸强于氢硫酸
C. 0.10 mol·L-1的亚硫酸和氢硫酸溶液的pH分别为2.1和4.5
D. 亚硫酸可以与碳酸氢钠溶液反应,而氢硫酸不能
2.(2020陕西西安中学高二上期中)由表格中电离常数判断下列反应可以发生的是
弱酸 HClO HCO
2 3
电离平衡常数 K=4.3×10-7
1
K=3.2×10-8
(25 ℃) K=4.7×10-11
2
A. NaClO+NaHCO === HClO+Na CO
3 2 3
B. NaClO+CO +H O=== HClO+NaHCO
2 2 3
C. 2NaClO+CO +H O=== 2HClO+Na CO
2 2 2 3
D. 2HClO+Na CO=== 2NaClO+CO ↑+H O
2 3 2 2
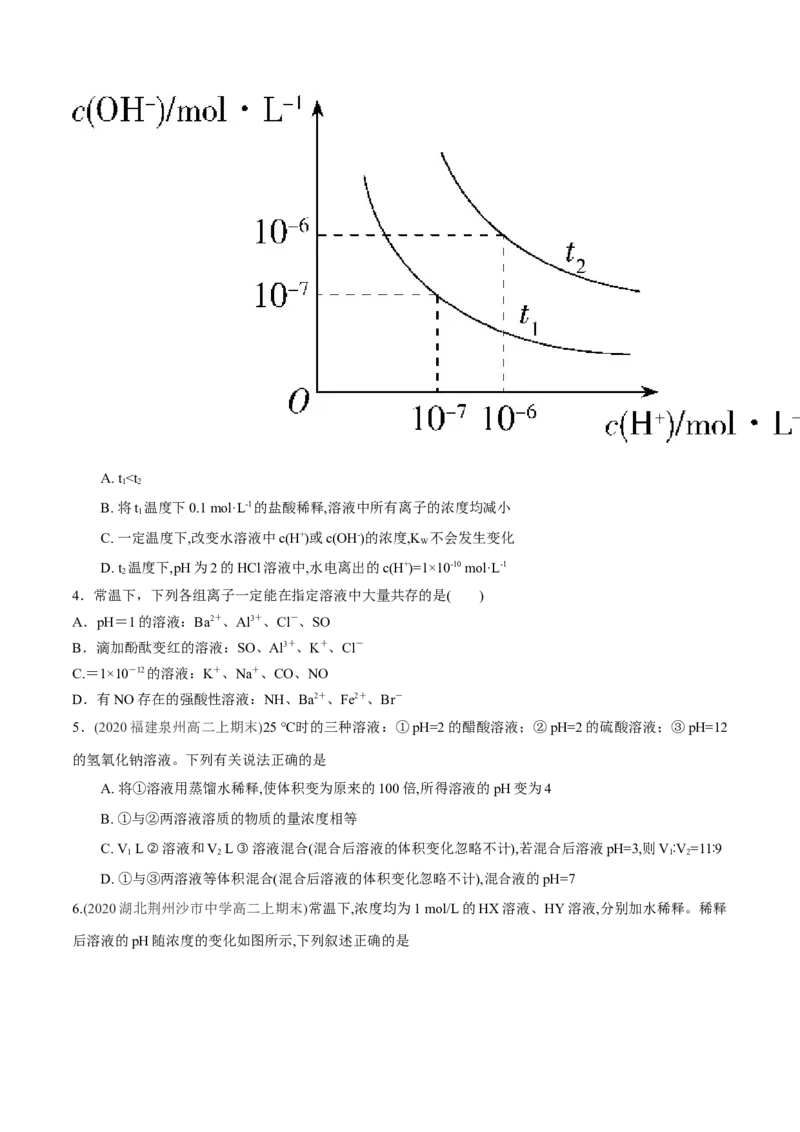
3.(2020河南南阳一中高二上月考)已知在t 、t 温度下水的电离平衡曲线如图所示,则下列说法中不正确的
1 2
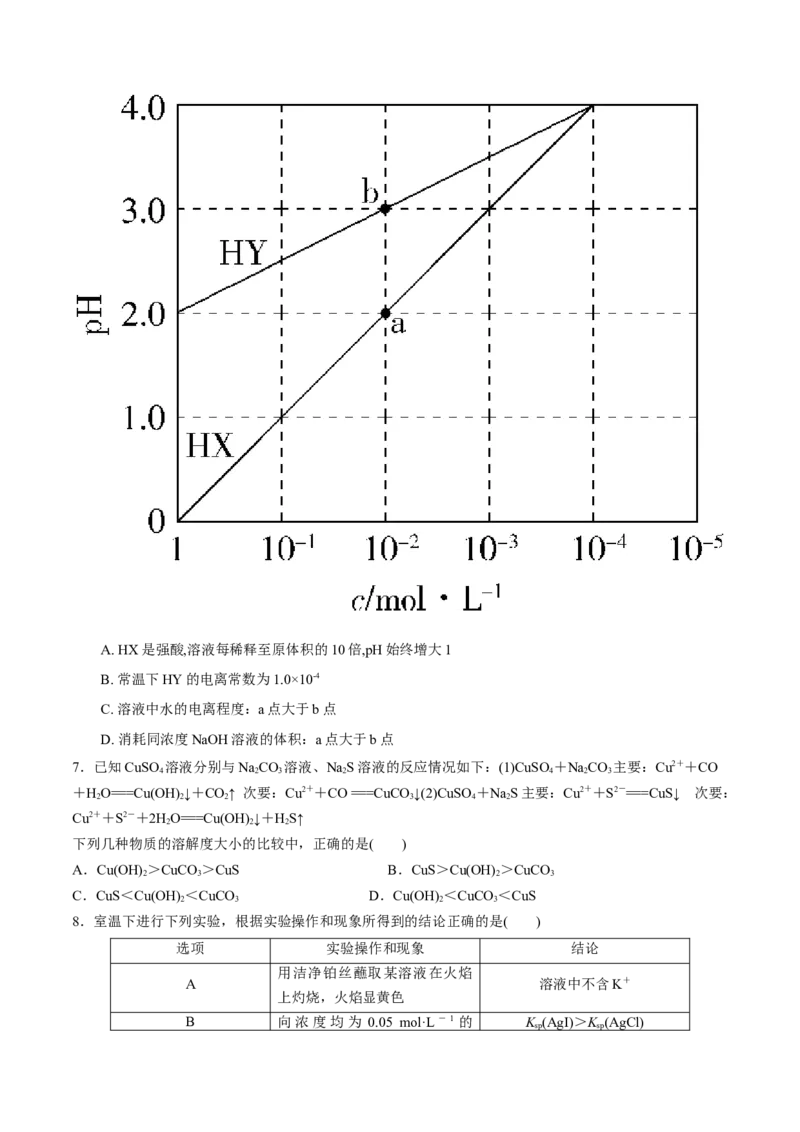
是A. tc(K+)>c(OH-)
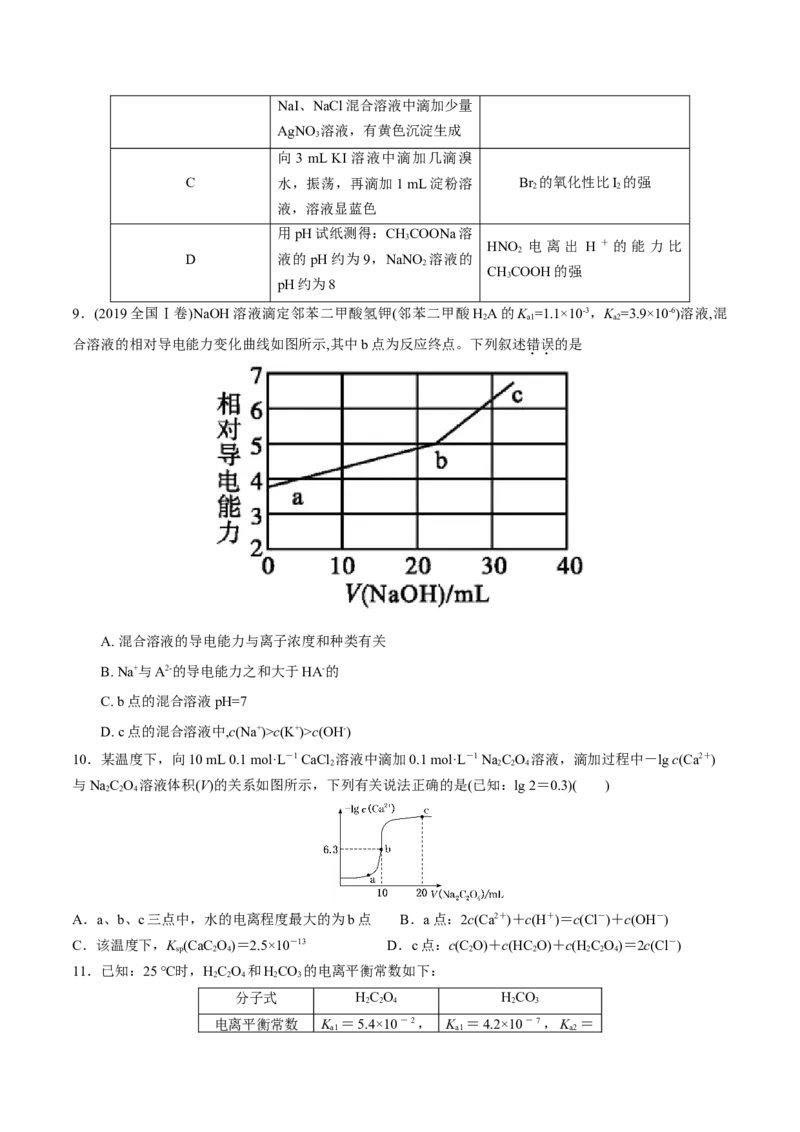
10.某温度下,向10 mL 0.1 mol·L-1 CaCl 溶液中滴加0.1 mol·L-1 Na C O 溶液,滴加过程中-lg c(Ca2+)
2 2 2 4
与NaC O 溶液体积(V)的关系如图所示,下列有关说法正确的是(已知:lg 2=0.3)( )
2 2 4
A.a、b、c三点中,水的电离程度最大的为b点 B.a点:2c(Ca2+)+c(H+)=c(Cl-)+c(OH-)
C.该温度下,K (CaC O)=2.5×10-13 D.c点:c(C O)+c(HC O)+c(H C O)=2c(Cl-)
sp 2 4 2 2 2 2 4
11.已知:25 ℃时,HC O 和HCO 的电离平衡常数如下:
2 2 4 2 3
分子式 HC O HCO
2 2 4 2 3
电离平衡常数 K =5.4×10-2, K =4.2×10-7,K =
a1 a1 a2K =5.4×10-5 5.6×10-11
a2
以下操作均在25 ℃条件下进行,则下列说法不正确的是( )
A.KHC O 溶液呈酸性,KHCO 溶液呈碱性
2 4 3
B.在KHC O 溶液中通入足量CO 生成的盐只有KHCO
2 4 2 3
C.分别向20 mL 0.1 mol·L-1 H C O 和HCO 溶液中加入0.1 mol·L-1 NaOH溶液至中性前者消耗NaOH多
2 2 4 2 3
D.将等物质的量浓度的HC O 和NaOH溶液等体积混合,所得溶液中各微粒浓度大小顺序为
2 2 4
c(Na+)>c(HC O)>c(C O)>c(H C O)
2 2 2 2 4
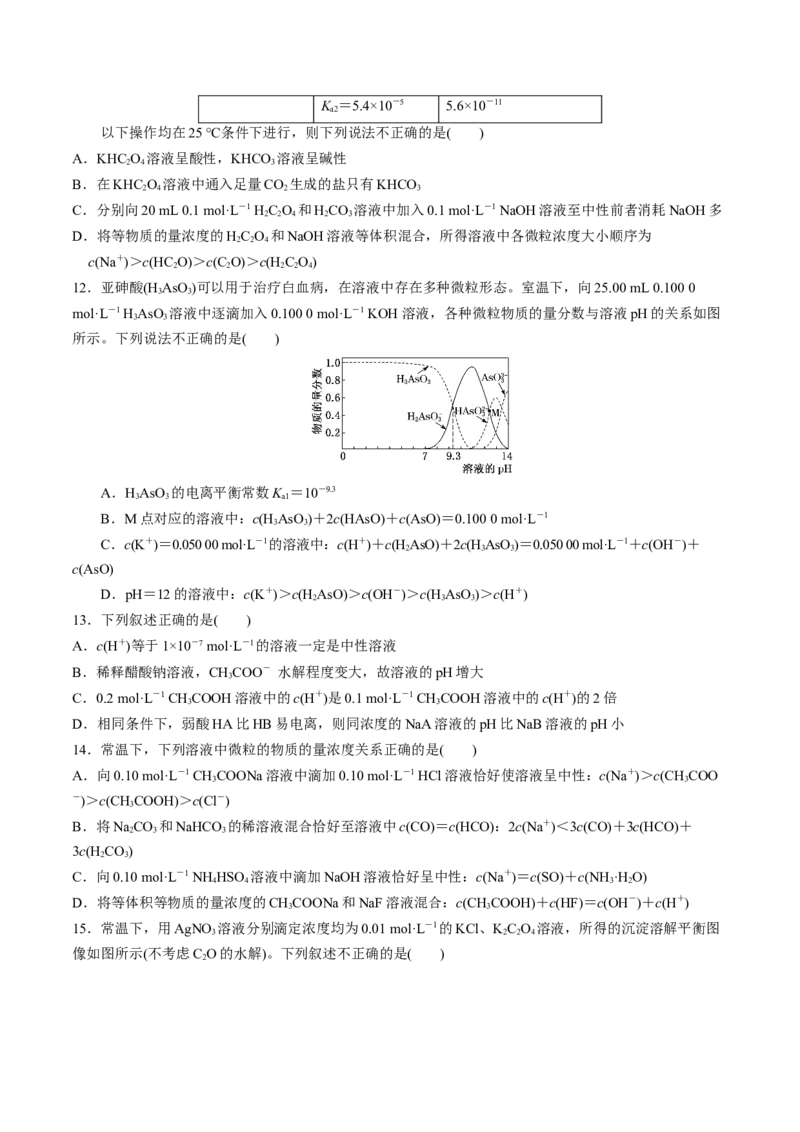
12.亚砷酸(H AsO )可以用于治疗白血病,在溶液中存在多种微粒形态。室温下,向25.00 mL 0.100 0
3 3
mol·L-1 H AsO 溶液中逐滴加入0.100 0 mol·L-1 KOH 溶液,各种微粒物质的量分数与溶液pH的关系如图
3 3
所示。下列说法不正确的是( )
A.HAsO 的电离平衡常数K =10-9.3
3 3 a1
B.M点对应的溶液中:c(H AsO )+2c(HAsO)+c(AsO)=0.100 0 mol·L-1
3 3
C.c(K+)=0.050 00 mol·L-1的溶液中:c(H+)+c(H AsO)+2c(H AsO )=0.050 00 mol·L-1+c(OH-)+
2 3 3
c(AsO)
D.pH=12的溶液中:c(K+)>c(H AsO)>c(OH-)>c(H AsO )>c(H+)
2 3 3
13.下列叙述正确的是( )
A.c(H+)等于1×10-7 mol·L-1的溶液一定是中性溶液
B.稀释醋酸钠溶液,CHCOO- 水解程度变大,故溶液的pH增大
3
C.0.2 mol·L-1 CH COOH溶液中的c(H+)是0.1 mol·L-1 CH COOH溶液中的c(H+)的2倍
3 3
D.相同条件下,弱酸HA比HB易电离,则同浓度的NaA溶液的pH比NaB溶液的pH小
14.常温下,下列溶液中微粒的物质的量浓度关系正确的是( )
A.向0.10 mol·L-1 CH COONa溶液中滴加0.10 mol·L-1 HCl溶液恰好使溶液呈中性:c(Na+)>c(CHCOO
3 3
-)>c(CHCOOH)>c(Cl-)
3
B.将NaCO 和NaHCO 的稀溶液混合恰好至溶液中c(CO)=c(HCO):2c(Na+)<3c(CO)+3c(HCO)+
2 3 3
3c(H CO)
2 3
C.向0.10 mol·L-1 NHHSO 溶液中滴加NaOH溶液恰好呈中性:c(Na+)=c(SO)+c(NH ·H O)
4 4 3 2
D.将等体积等物质的量浓度的CHCOONa和NaF溶液混合:c(CHCOOH)+c(HF)=c(OH-)+c(H+)
3 3
15.常温下,用AgNO 溶液分别滴定浓度均为0.01 mol·L-1的KCl、KC O 溶液,所得的沉淀溶解平衡图
3 2 2 4
像如图所示(不考虑C O的水解)。下列叙述不正确的是( )
2A.K (Ag C O)等于10-10 B.n点表示Ag C O 的不饱和溶液
sp 2 2 4 2 2 4
C.向c(Cl-)=c(C O)的混合液中滴入AgNO 溶液时,先生成Ag C O 沉淀
2 3 2 2 4
D.Ag C O(s)+2Cl-(aq)2AgCl(s)+C O(aq)的平衡常数为108
2 2 4 2
二、非选择题(本题共5小题,共55分)
16.(10分)在氨水中存在下列电离平衡:NH·H O +OH-。
3 2
(1)下列情况能引起电离平衡正向移动的有 (填字母,下同)。
①加NH Cl固体 ②加NaOH溶液 ③通入HCl ④加CHCOOH溶液 ⑤加水 ⑥加压
4 3
a. ①③⑤ b. ①④⑥
c. ③④⑤ d. ①②④
(2)在含有酚酞的0.1 mol·L-1氨水中加入少量的NH Cl晶体,则溶液颜色 。
4
a. 变蓝色 b. 变深
c. 变浅 d. 不变
(3)在一定温度下,用水缓慢稀释1 mol·L-1氨水的过程中,溶液中随着水量的增加:
①n(OH-) (填“增大”“减小”或“不变”,下同);
② ; ③ 。
17.(10分)我国国标推荐的食品、药品中Ca元素含量的测定方法之一为利用NaC O 使处理后的样品中的
2 2 4
Ca2+形成沉淀,过滤、洗涤,然后将所得CaC O 固体溶于过量的强酸,最后使用已知浓度的KMnO 溶液通过滴
2 4 4
定来测定溶液中Ca2+的含量。回答以下问题:
(1)KMnO 溶液应该用 (填“酸式”或“碱式”)滴定管盛装,除滴定管外,还需要的玻璃仪器有
4
__________________________(写出两种即可)。
(2)试写出滴定过程中发生反应的离子方程式: 。
(3)滴定终点的颜色变化为溶液由 色变为 色。
(4)以下操作会导致测定结果偏高的是 (填字母)。
a. 装入KMnO 溶液前未润洗滴定管
4
b. 滴定结束后俯视读数
c. 滴定结束后,滴定管尖端悬有一滴溶液d. 滴定过程中,振荡时将少量待测液洒出
(5)某同学对上述实验方案进行了改进并用于测定某品牌的钙片(主要成分为CaCO )中钙元素的含量,其
3
实验过程如下:取2.00 g样品放入锥形瓶中,用酸式滴定管向锥形瓶内加入20.00 mL浓度为0.10 mol·L-1的
盐酸(盐酸过量),充分反应一段时间,用酒精灯将锥形瓶内液体加热至沸腾,数分钟后,冷却至室温,加入2~3滴
酸碱指示剂,用浓度为0.10 mol·L-1的NaOH溶液滴定至终点,消耗NaOH溶液8.00 mL。[提示:Ca(OH) 微溶
2
于水,pH较低时不会产生沉淀]据此回答:
①为使现象明显、结果准确,滴定过程中的酸碱指示剂应选择 (填“石蕊”“甲基橙”或“酚
酞”)溶液。
②实验过程中将锥形瓶内液体煮沸的目的是 。
③则此2.00 g钙片中CaCO 的质量为 g。
3
18.(10分)在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)常温下,将0.2 mol·L-1某一元酸HA溶液和0.1 mol·L-1 NaOH溶液等体积混合后溶液pH大于7,若混
合液体积等于两溶液体积之和,则混合液中下列关系正确的是__________(填字母)。
A.c(HA)