文档内容
第 11 课 碳酸钠和碳酸氢钠 焰色试验
[学习目标]
课标要点 学科素养
碳酸钠、碳酸氢钠的性质 通过对“碳酸钠、碳酸氢钠的性质”的学习增强科学探究水平
通过对“碳酸钠、碳酸氢钠的相互转化”的学习,能建立认知
碳酸钠、碳酸氢钠的相互转化
模型,并能运用模型解释化学现象,揭示现象的本质和规律
1.探究并比较碳酸钠与碳酸氢钠的性质,增强科学探究与创新意识。
2.了解焰色试验。
[学习过程]
知识点一 碳酸钠和碳酸氢钠
教材学习
仔细阅读教材,思考下列问题:
[实验1] 探究NaCO 和NaHCO 的溶解性及其水溶液的酸碱性
2 3 3
盐 1 g Na CO 1 g NaHCO
2 3 3
(1)观察NaCO 和NaHCO 的
2 3 3
____________ ____________
外观并进行描述
(2)向两支分别装有NaCO、
2 3
NaHCO 的试管中分别滴入 加水结块,变成晶体,温度
3
加水部分溶解,温度计示数
几滴水,振荡,观察现象; 计示数上升,说明有放热现
下降,说明有吸热现象
将温度计分别插入其中,温 象
度计的示数有何变化
(3)继续向(2)的试管中分别加
入5 mL水,用力振荡,有何 完全溶解 固体量减少,部分溶解
现象
(4)分别向(3)所得溶液中滴入
溶液呈红色 溶液呈浅红色
1~2滴酚酞溶液,有何现象
NaCO 加少量水变成__________________;
2 3
NaCO、NaHCO 都能溶于水,____________溶解度较大;
2 3 3
初步结论
NaCO 溶解______,NaHCO 溶解______;
2 3 3
NaCO、NaHCO 溶液都呈碱性,____________溶液的碱性稍强
2 3 3
注意: (1)Na CO 、NaHCO 均易溶于水,但相同温度下,NaHCO 的溶解度比NaCO 小很多,故向饱
2 3 2 3 3 2 3
和NaCO 溶液中通入CO 有NaHCO 晶体析出,反应的化学方程式为NaCO+HO+CO===2NaHCO ↓。
2 3 2 3 2 3 2 2 3
(2)Na CO 粉末遇水生成碳酸钠晶体(Na CO·xHO);碳酸钠晶体在干燥空气里逐渐失去结晶水变成
2 3 2 3 2
学科网(北京)股份有限公司NaCO 粉末。
2 3
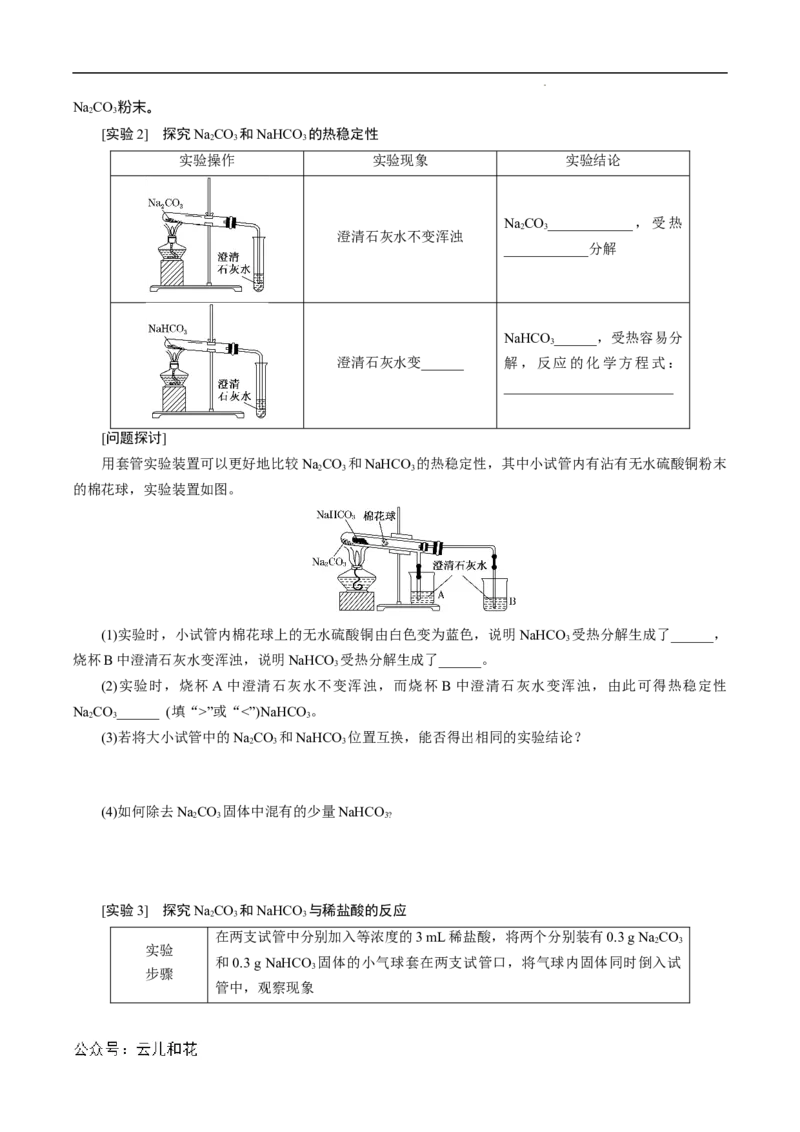
[实验2] 探究NaCO 和NaHCO 的热稳定性
2 3 3
实验操作 实验现象 实验结论
NaCO____________,受热
2 3
澄清石灰水不变浑浊
____________分解
NaHCO ______,受热容易分
3
澄清石灰水变______ 解,反应的化学方程式:
________________________
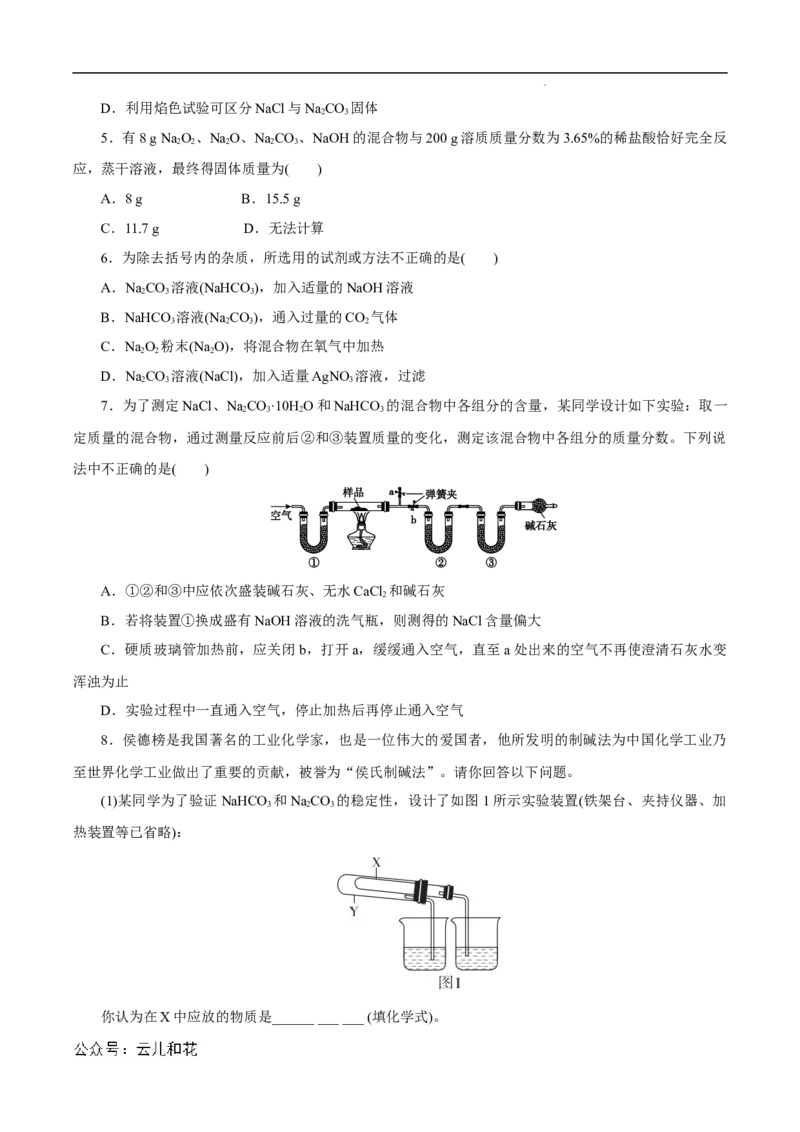
[问题探讨]
用套管实验装置可以更好地比较NaCO 和NaHCO 的热稳定性,其中小试管内有沾有无水硫酸铜粉末
2 3 3
的棉花球,实验装置如图。
(1)实验时,小试管内棉花球上的无水硫酸铜由白色变为蓝色,说明NaHCO 受热分解生成了______,
3
烧杯B中澄清石灰水变浑浊,说明NaHCO 受热分解生成了______。
3
(2)实验时,烧杯A中澄清石灰水不变浑浊,而烧杯 B中澄清石灰水变浑浊,由此可得热稳定性
NaCO______ (填“>”或“<”)NaHCO。
2 3 3
(3)若将大小试管中的NaCO 和NaHCO 位置互换,能否得出相同的实验结论?
2 3 3
(4)如何除去NaCO 固体中混有的少量NaHCO
2 3 3?
[实验3] 探究NaCO 和NaHCO 与稀盐酸的反应
2 3 3
在两支试管中分别加入等浓度的3 mL稀盐酸,将两个分别装有0.3 g Na CO
2 3
实验
和0.3 g NaHCO 固体的小气球套在两支试管口,将气球内固体同时倒入试
3
步骤
管中,观察现象
学科网(北京)股份有限公司实验
操作
实验 两支试管中都产生无色气泡,气球膨胀,加入碳酸氢钠的试管中产生气泡的
现象 速率更快,气球膨胀得更大
[问题探讨]
(1)向稀盐酸中加入NaCO ,反应的化学方程式:______________________________,离子方程式为
2 3
______________________________。
(2)向稀盐酸中加入NaHCO ,反应的化学方程式:______________________________,离子方程式为
3
______________________________。
(3)Na CO 、NaHCO 都能和稀盐酸反应产生 CO ,但反应速率 NaCO______ (填“>”“<”或
2 3 3 2 2 3
“=”)NaHCO 。
3
(4)能否用稀盐酸鉴别等浓度的NaCO 和NaHCO 溶液?
2 3 3
知识精讲
1.Na CO 与NaHCO 性质的比较
2 3 3
碳酸钠(Na CO) 碳酸氢钠(NaHCO )
2 3 3
俗名 纯碱或苏打 小苏打
色、态 白色粉末(Na CO·10H O为晶体) 细小、白色粉末
2 3 2
溶解性 易溶于水 在水中溶解度比NaCO 小
2 3
溶液的酸碱性 显碱性 显碱性
稳定,受热难分解;但结晶碳酸钠 不 稳 定 , 受 热 易 分 解 :
热稳定性
(Na CO·10H O)易风化 2NaHCO =====NaCO+HO+CO↑
2 3 2 3 2 3 2 2
与酸反应(与 NaCO +2HCl===2NaCl+HO+ NaHCO + HCl===NaCl + HO +
2 3 2 3 2
HCl) CO↑ CO↑(反应速率比NaCO 快)
2 2 2 3
与碱反应[与 2NaHCO + Ca(OH) ===CaCO ↓ +
3 2 3
NaCO+Ca(OH) ===CaCO ↓+
2 3 2 3
Ca(OH) 、 NaCO+2HO
2 2 3 2
2NaOH(NaCO 与NaOH不反应)
2 3
NaOH] NaHCO +NaOH===NaCO+HO
3 2 3 2
与可溶性钙
盐、钡盐反应 NaCO+CaCl ===CaCO ↓+2NaCl
2 3 2 3
不反应
(与CaCl 、 NaCO+BaCl ===BaCO ↓+2NaCl
2 2 3 2 3
BaCl )
2
相互转化 NaCONaHCO
2 3 3
用途 用于玻璃、肥皂、洗涤剂、造纸、 制发酵剂、灭火器、医疗上用于治疗
学科网(北京)股份有限公司纺织等工业 胃酸过多
2.碳酸钠与碳酸氢钠的鉴别方法
碳酸钠和碳酸氢钠都能与Ca(OH) 、Ba(OH) 溶液反应产生沉淀,故不能用Ca(OH) 、Ba(OH) 溶液鉴
2 2 2 2
别。
3.互滴法鉴别NaCO 溶液和稀盐酸
2 3
NaCO 溶液和稀盐酸反应时,滴加顺序不同,反应现象不同。
2 3
(1)向NaCO 溶液中滴加盐酸时,开始时无气泡产生,后产生气泡,原因是首先发生反应:NaCO +
2 3 2 3
HCl===NaCl+NaHCO ,然后发生反应:NaHCO +HCl===NaCl+CO↑+HO。
3 3 2 2
(2)向盐酸中滴加 NaCO 溶液时,会立即产生大量气泡,该过程中发生的反应为 NaCO +
2 3 2 3
2HCl===2NaCl+CO↑+HO。
2 2
4.NaCO 和NaHCO 的相互转化
2 3 3
(1)NaHCO 固体加热可得NaCO 固体。
3 2 3
(2)Na CO 溶液中不断通入足量CO 气体可得NaHCO 溶液。
2 3 2 3
(3)NaHCO 溶液中滴加适量的NaOH溶液可得NaCO 溶液。
3 2 3
5.除杂
混合物(括号内为杂质) 除杂方法及试剂
NaCO 固体(NaHCO ) 加热
2 3 3
NaHCO 溶液(Na CO) 通入足量CO 气体
3 2 3 2
NaCO 溶液(NaHCO ) 加入适量NaOH溶液
2 3 3
典题例析
[例1]下列关于NaCO 与NaHCO 的性质判断正确的是( )
2 3 3
A.常温下溶解度:NaCONaHCO
2 3 3
D.与澄清石灰水反应,均有白色沉淀生成
学科网(北京)股份有限公司[例2]纯碱和小苏打是厨房中两种常见的用品,它们都是白色固体。下列区分这两种物质的方法中正确
的是( )
A.分别用砂锅加热两种样品,全部分解挥发,没有残留物的是小苏打
B.用洁净铁丝蘸取两种样品在煤气灯火焰上灼烧,火焰颜色发生明显变化的是小苏打
C.在两只小玻璃杯中分别加入少量的两种样品,再加入等体积等浓度的食醋,产生气泡快的是小苏
打
D.先将两种样品配成溶液,分别加入等量的石灰水,无白色沉淀生成的是小苏打
[例3]下列有关NaCO 和NaHCO 的说法中,正确的是( )
2 3 3
A.NaCO 和NaHCO 溶于水都会放出热量
2 3 3
B.等质量的两种固体,分别与等浓度的盐酸完全反应,消耗盐酸的体积一样多
C.等质量的两种固体,分别与过量盐酸反应,生成CO 的质量相等
2
D.取相同浓度的两种溶液,分别滴入酚酞,溶液颜色较深的是NaCO 溶液
2 3
[例4]可用于判断碳酸氢钠粉末中混有碳酸钠的实验方法是( )
A.加热时有气体放出
B.滴加盐酸时有气泡放出
C.溶于水后滴加BaCl 稀溶液,有白色沉淀生成
2
D.溶于水后滴加澄清石灰水,有白色沉淀生成
[例5]有两支试管分别装有NaCO 溶液和NaHCO 溶液,下列操作或判断正确的是( )
2 3 3
选项 操作 判断
A. 分别加入澄清石灰水 产生沉淀的是NaCO 溶液
2 3
B. 分别加入等浓度的稀盐酸 反应较剧烈的是NaCO 溶液
2 3
C. 分别加入CaCl 溶液 产生沉淀的为NaCO 溶液
2 2 3
D. 逐渐加入等浓度的稀盐酸 立即产生气泡的是NaCO 溶液
2 3
知识点二 焰色试验
教材学习
仔细阅读教材,思考下列问题:
(1)焰色试验:很多金属或它们的化合物在火焰上灼烧时都会使火焰呈现出特征颜色,根据火焰呈现的
特征颜色,可以判断试样所含的金属元素,化学上把这样的定性分析操作称为焰色试验。焰色试验属于
______变化,根据焰色试验呈现的特征颜色,可以检验__________的存在,如钠的焰色为_________、 钾
的焰色为__________(透过蓝色钴玻璃)。
(2)操作步骤:“洗、烧、蘸、烧”
学科网(北京)股份有限公司①洗:用______________洗涤铂丝或铁丝(不能用玻璃棒)。
②烧:将洗净的铂丝或铁丝放在酒精灯(或煤气灯)火焰上灼烧至_____________________时为止。
③蘸:用铂丝蘸取少量待测液或者待测物质。
④烧:置于火焰上灼烧,观察火焰的颜色。
【小结】焰色试验应用中的注意事项
①不是所有的金属都可呈现焰色,金属单质与它的化合物的焰色颜色相同。
②焰色试验是物理过程,是元素的特性。
③观察钾的焰色时,要透过蓝色钴玻璃观察,这样可以滤去黄光,避免其中含钠杂质所产生的黄色光
的干扰。
知识精讲
1.焰色试验
根据火焰呈现的特征颜色,可以判断试样所含的金属元素,化学上把这样的定性分析操作称为焰色试
验。
2.操作步骤
3.几种常见金属元素的焰色
金属元素 锂 钠 钾 钙 锶 钡 铜
_____ ______
颜色 紫红色 紫色(透过蓝色钴玻璃) 砖红色 洋红色 _____色
色 色
4.应用
(1)检验金属元素的存在,如鉴别NaCl和KCl溶液。
(2)利用焰色试验制节日烟火。
注意:
(1)焰色试验可用来鉴别一些金属元素,这种鉴别物质的方法属于物理方法,而不是化学方法。
(2)清洗铂丝时不能用稀硫酸代替盐酸,因为硫酸的熔沸点较高,难挥发。
(3)观察钾的焰色试验时,要透过蓝色钴玻璃观察,这样做的目的是滤去黄光,避免少量钠元素对鉴别
钾元素的干扰。
典题例析
[例1]某物质灼烧时火焰呈黄色,下列判断正确的是( )
学科网(北京)股份有限公司A.该物质一定是钠的化合物
B.该物质一定含钠元素
C.该物质一定是金属钠
D.该物质中一定含钠离子
[例2]利用焰色试验既可以制作五彩缤纷的节日烟花,亦可以定性鉴别某些金属盐。灼烧立德粉
(ZnS·BaSO )样品时,钡的焰色为( )
4
A.黄色 B.红色
C.紫色 D.黄绿色
[例3]奥运会闭幕式上,燃放了大量的烟花,五彩缤纷的焰火十分好看。研究表明,焰火颜色的产生
与烟花中含有钠、钾、钙、钡、铜、锶等金属元素有关。下列有关说法不正确的是( )
A.五彩缤纷的焰火的形成是因为上述金属元素产生了不同的焰色
B.每次做焰色试验前都要用盐酸洗净铂丝并在火焰上灼烧至与原来的火焰颜色相同
C.KCl与KNO 灼烧时火焰的颜色不相同
3
D.观察钾及其化合物的焰色需要透过蓝色钴玻璃
[效果检测]
1.下列关于NaCO 的叙述中,正确的是( )
2 3
A.NaCO 是治疗胃酸过多的一种药剂
2 3
B.往碳酸钠稀溶液中加入少量稀盐酸,可观察到有大量气泡产生
C.除去NaCO 溶液中的NaSO ,加入适量的Ba(OH) 溶液,过滤
2 3 2 4 2
D.NaCO 在不同反应中既能吸收CO,又能参加反应放出CO
2 3 2 2
2.除去NaHCO 溶液中混有的少量NaCO 可采取的方法是( )
3 2 3
A.通入二氧化碳气体 B.加入氢氧化钡溶液
C.加入澄清石灰水 D.加入稀盐酸
3.a g纯净的碳酸钠和a g碳酸钠与碳酸氢钠的混合物相比,下列描述正确的是( )
A.分别和盐酸反应时,混合物的耗酸量大
B.分别和足量盐酸反应时,混合物放出的CO 多
2
C.分别配制成等体积溶液,混合物碱性强
D.分别配制成等体积溶液,混合物溶液中Na+的浓度大
4.五彩缤纷的焰火与化学中“焰色试验”知识相关。下列说法中正确的是( )
A.焰色试验是化学变化
B.用稀硫酸清洗做焰色试验的铂丝
C.K的焰色试验应透过蓝色钴玻璃观察
学科网(北京)股份有限公司D.利用焰色试验可区分NaCl与NaCO 固体
2 3
5.有8 g Na O 、NaO、NaCO 、NaOH的混合物与200 g溶质质量分数为3.65%的稀盐酸恰好完全反
2 2 2 2 3
应,蒸干溶液,最终得固体质量为( )
A.8 g B.15.5 g
C.11.7 g D.无法计算
6.为除去括号内的杂质,所选用的试剂或方法不正确的是( )
A.NaCO 溶液(NaHCO ),加入适量的NaOH溶液
2 3 3
B.NaHCO 溶液(Na CO),通入过量的CO 气体
3 2 3 2
C.NaO 粉末(Na O),将混合物在氧气中加热
2 2 2
D.NaCO 溶液(NaCl),加入适量AgNO 溶液,过滤
2 3 3
7.为了测定NaCl、NaCO·10H O和NaHCO 的混合物中各组分的含量,某同学设计如下实验:取一
2 3 2 3
定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各组分的质量分数。下列说
法中不正确的是( )
A.①②和③中应依次盛装碱石灰、无水CaCl 和碱石灰
2
B.若将装置①换成盛有NaOH溶液的洗气瓶,则测得的NaCl含量偏大
C.硬质玻璃管加热前,应关闭b,打开a,缓缓通入空气,直至a处出来的空气不再使澄清石灰水变
浑浊为止
D.实验过程中一直通入空气,停止加热后再停止通入空气
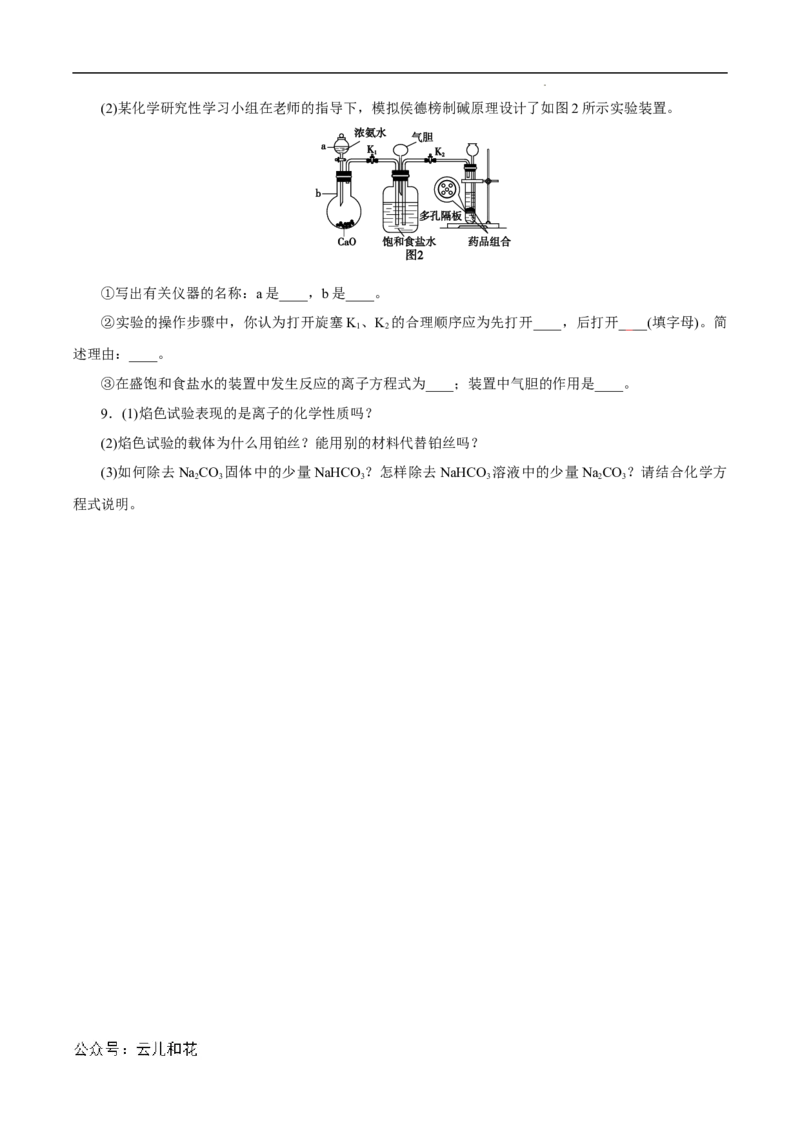
8.侯德榜是我国著名的工业化学家,也是一位伟大的爱国者,他所发明的制碱法为中国化学工业乃
至世界化学工业做出了重要的贡献,被誉为“侯氏制碱法”。请你回答以下问题。
(1)某同学为了验证NaHCO 和NaCO 的稳定性,设计了如图1所示实验装置(铁架台、夹持仪器、加
3 2 3
热装置等已省略):
你认为在X中应放的物质是______ ___ ___ (填化学式)。
学科网(北京)股份有限公司(2)某化学研究性学习小组在老师的指导下,模拟侯德榜制碱原理设计了如图2所示实验装置。
①写出有关仪器的名称:a是____,b是____。
②实验的操作步骤中,你认为打开旋塞K 、K 的合理顺序应为先打开____,后打开____(填字母)。简
1 2
述理由:____。
③在盛饱和食盐水的装置中发生反应的离子方程式为____;装置中气胆的作用是____。
9.(1)焰色试验表现的是离子的化学性质吗?
(2)焰色试验的载体为什么用铂丝?能用别的材料代替铂丝吗?
(3)如何除去NaCO 固体中的少量NaHCO ?怎样除去NaHCO 溶液中的少量NaCO ?请结合化学方
2 3 3 3 2 3
程式说明。
学科网(北京)股份有限公司