文档内容
课时作业
A篇·知识对点训练
知识点1 硫的性质
1.洗涤试管内壁上附着的硫黄,可选用的方法是( )
A.用CS 洗涤 B.通入H 加热
2 2
C.加热试管使硫熔化 D.用酒精洗涤
答案 A
解析 硫黄易溶于CS ,故可用CS 洗涤试管内壁上附着的硫黄。
2 2
2.下列说法不正确的是( )
①硫是一种黄色的能溶于水的晶体 ②火山喷出物中含有大量含硫化合物
③硫在空气中燃烧的产物是二氧化硫 ④硫在纯氧中燃烧的产物是三氧化硫
A.①② B.②③ C.③④ D.①④
答案 D
解析 硫是一种难溶于水的黄色晶体;硫不论在空气中还是纯氧中,燃烧的
产物都是SO 。
2
3.下列说法中不正确的是( )
A.在自然界中有游离态的硫存在
B.试管内壁的硫粉可以用热的碱液除去
C.硫与金属反应,生成低价态的金属化合物
D.硫的氧化性比氯气的强
答案 D
解析 游离态的硫存在于火山喷口附近或地壳的岩层里,A正确;S可以与
热的碱液反应,B正确;硫的氧化性较弱,与变价金属化合时,只能生成低价态
金属硫化物,如S与Fe、Cu反应,生成FeS、Cu S;氯气的氧化性较强,Cl 与
2 2
Fe、Cu反应生成高价态金属化合物FeCl 、CuCl ,C正确,D错误。
3 2
知识点2 硫的氧化物
4.下列关于SO 和SO 的叙述正确的是( )
2 3A.标准状况下,都是无色气体,都易溶于水
B.都是酸性氧化物,其水溶液都是强酸
C.都可使品红溶液褪色,加热时红色又能再现
D.都能跟碱溶液反应
答案 D
解析 标准状况下,SO 是无色固体,A错误;SO 溶于水生成H SO ,其为
3 2 2 3
弱酸,B错误;SO 能使品红溶液褪色,加热时红色再现,SO 则不能,C错误;
2 3
SO 和SO 都是酸性氧化物,都能跟碱反应,D正确。
2 3
5.当我们查看葡萄酒标签上的成分信息时,常发现其成分中含有少量
SO 。下列关于SO 的说法正确的是( )
2 2
A.SO 属于非法添加剂,不该添加到葡萄酒中
2
B.SO 具有还原性,少量的SO 可防止葡萄酒氧化变质
2 2
C.SO 具有还原性,不能用浓硫酸干燥
2
D.SO 可以使酸性KMnO 溶液褪色,体现了它的漂白性
2 4
答案 B
解析 葡萄酒中的适量二氧化硫可以起到防腐、杀菌、抗氧化的作用,适量
的二氧化硫对人体是无害的,可以添加到葡萄酒中,A错误;因为二氧化硫中硫
元素为+4价,有还原性,可以抗氧化,B正确;二氧化硫和硫酸中硫元素是相
邻价态,不能发生氧化还原反应,能用浓硫酸干燥,C错误;二氧化硫使酸性高
锰酸钾溶液褪色体现了二氧化硫的还原性,不是漂白性,D错误。
6.下列有关SO 的说法正确的是( )
2
A.SO 和SO 均是酸性氧化物
2 3
B.SO 的漂白原理和氯气的漂白原理相同
2
C.在SO +2H S===3S+2H O反应中,氧化产物和还原产物的物质的量之
2 2 2
比为1∶2
D.把某气体通入澄清的石灰水中,石灰水变浑浊,该气体一定是SO
2
答案 A解析 SO 和SO 都可以和碱反应生成相应的盐和H O,都是酸性氧化物,A
2 3 2
正确;SO 与有机色素化合生成不稳定的无色物质,而 Cl 与 H O 反应生成的
2 2 2
HClO具有强氧化性,将有机色素氧化为无色物质,故两者漂白原理不同,B错
误;该反应中,氧化产物与还原产物的物质的量之比为 2∶1,C错误;能使澄
清石灰水变浑浊的气体有CO 、SO ,D错误。
2 2
7.下列实验报告记录的实验现象正确的是( )
答案 B
解析 SO 水溶液显酸性,加入石蕊试液中,石蕊变红色;加入品红溶液中,
2
品红褪色;加入Ba(NO ) 溶液中,H SO 被NO氧化成SO生成BaSO 白色沉淀;
3 2 2 3 4
加入NaOH和BaCl 混合溶液中,H SO 和NaOH生成Na SO ,Na SO 与BaCl
2 2 3 2 3 2 3 2
生成BaSO 白色沉淀。
3
8.将SO 和SO 两种气体的混合物通入BaCl 溶液,其结果是( )
2 3 2
A.两种气体都被吸收,并有BaSO 沉淀生成
4
B.只有BaSO 沉淀,SO 通入溶液中无沉淀生成
4 2
C.生成BaSO 和BaSO 沉淀
4 3D.只生成BaSO 沉淀,SO 从溶液中逸出
3 3
答案 B
解析 SO +H O===H SO ,H SO +BaCl ===BaSO ↓+2HCl;但 SO 与
3 2 2 4 2 4 2 4 2
BaCl 溶液不反应,故选B。
2
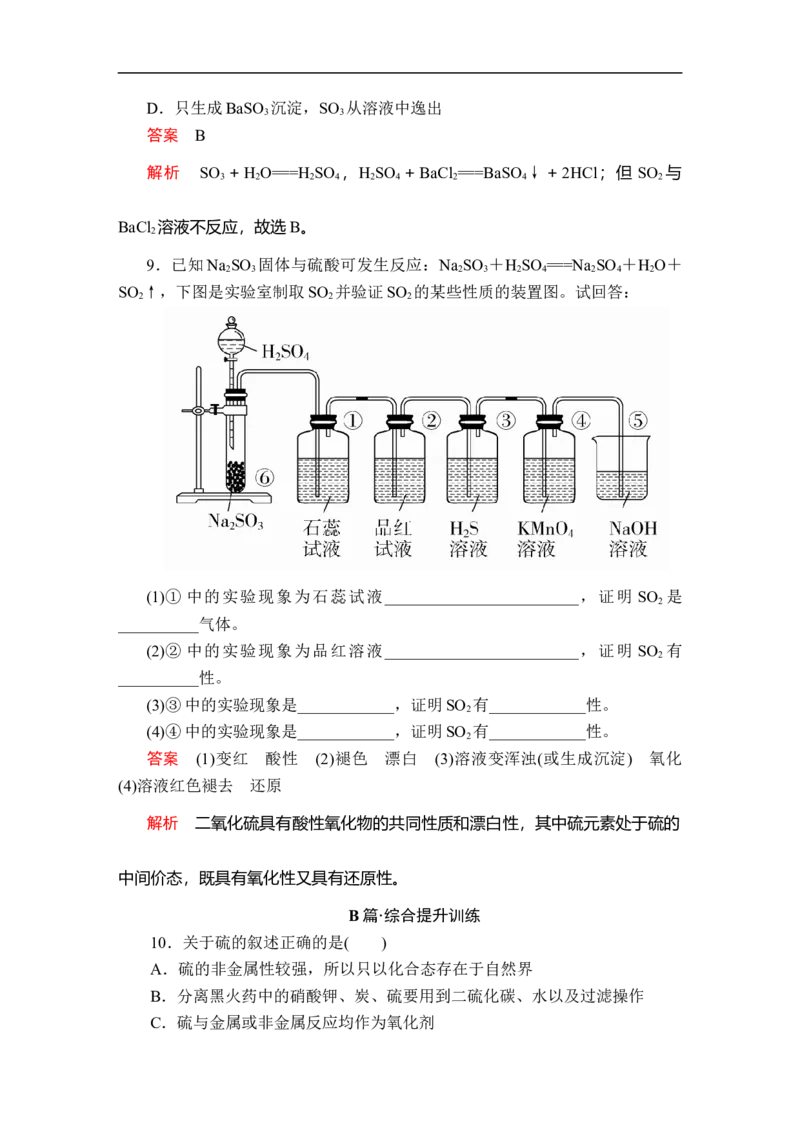
9.已知Na SO 固体与硫酸可发生反应:Na SO +H SO ===Na SO +H O+
2 3 2 3 2 4 2 4 2
SO ↑,下图是实验室制取SO 并验证SO 的某些性质的装置图。试回答:
2 2 2
(1)① 中的实验现象为石蕊试液________________________,证明 SO 是
2
__________气体。
(2)② 中的实验现象为品红溶液________________________,证明 SO 有
2
__________性。
(3)③中的实验现象是____________,证明SO 有____________性。
2
(4)④中的实验现象是____________,证明SO 有____________性。
2
答案 (1)变红 酸性 (2)褪色 漂白 (3)溶液变浑浊(或生成沉淀) 氧化
(4)溶液红色褪去 还原
解析 二氧化硫具有酸性氧化物的共同性质和漂白性,其中硫元素处于硫的
中间价态,既具有氧化性又具有还原性。
B篇·综合提升训练
10.关于硫的叙述正确的是( )
A.硫的非金属性较强,所以只以化合态存在于自然界
B.分离黑火药中的硝酸钾、炭、硫要用到二硫化碳、水以及过滤操作
C.硫与金属或非金属反应均作为氧化剂D.3.2 g硫与6.4 g铜反应能得到9.6 g纯净硫化物
答案 B
解析 硫在自然界中以游离态和化合态两种形式存在,A错误;先将题中三
种物质溶于水后过滤,可分离出硫和炭的混合物,然后利用 CS 可以从混合物中
2
分离出硫,B正确;硫与非金属反应时也可能作还原剂,如 S+O =====SO ,C
2 2
错误;硫与铜发生的反应为2Cu+S=====Cu S,故此时S过量,生成8.0 g硫化
2
物,有1.6 g硫剩余,D错误。
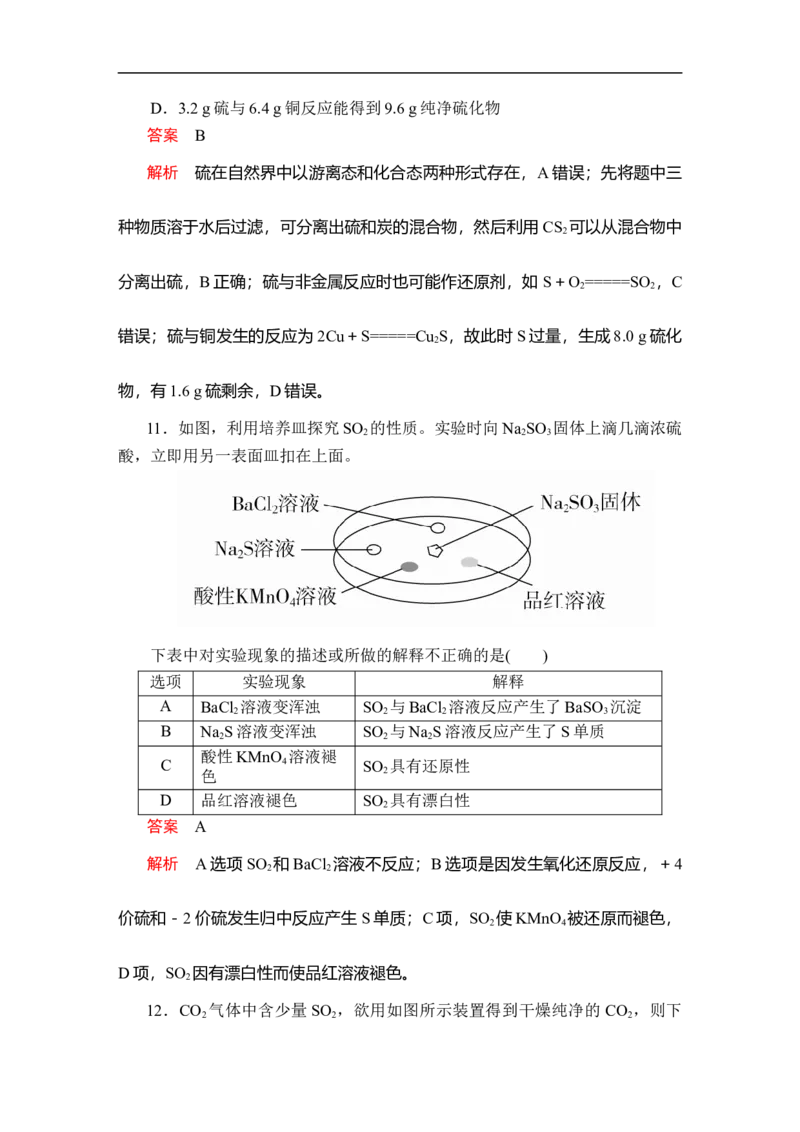
11.如图,利用培养皿探究SO 的性质。实验时向Na SO 固体上滴几滴浓硫
2 2 3
酸,立即用另一表面皿扣在上面。
下表中对实验现象的描述或所做的解释不正确的是( )
选项 实验现象 解释
A BaCl 溶液变浑浊 SO 与BaCl 溶液反应产生了BaSO 沉淀
2 2 2 3
B Na S溶液变浑浊 SO 与Na S溶液反应产生了S单质
2 2 2
酸性KMnO 溶液褪
C 4 SO 具有还原性
色 2
D 品红溶液褪色 SO 具有漂白性
2
答案 A
解析 A选项SO 和BaCl 溶液不反应;B选项是因发生氧化还原反应,+4
2 2
价硫和-2价硫发生归中反应产生 S单质;C项,SO 使KMnO 被还原而褪色,
2 4
D项,SO 因有漂白性而使品红溶液褪色。
2
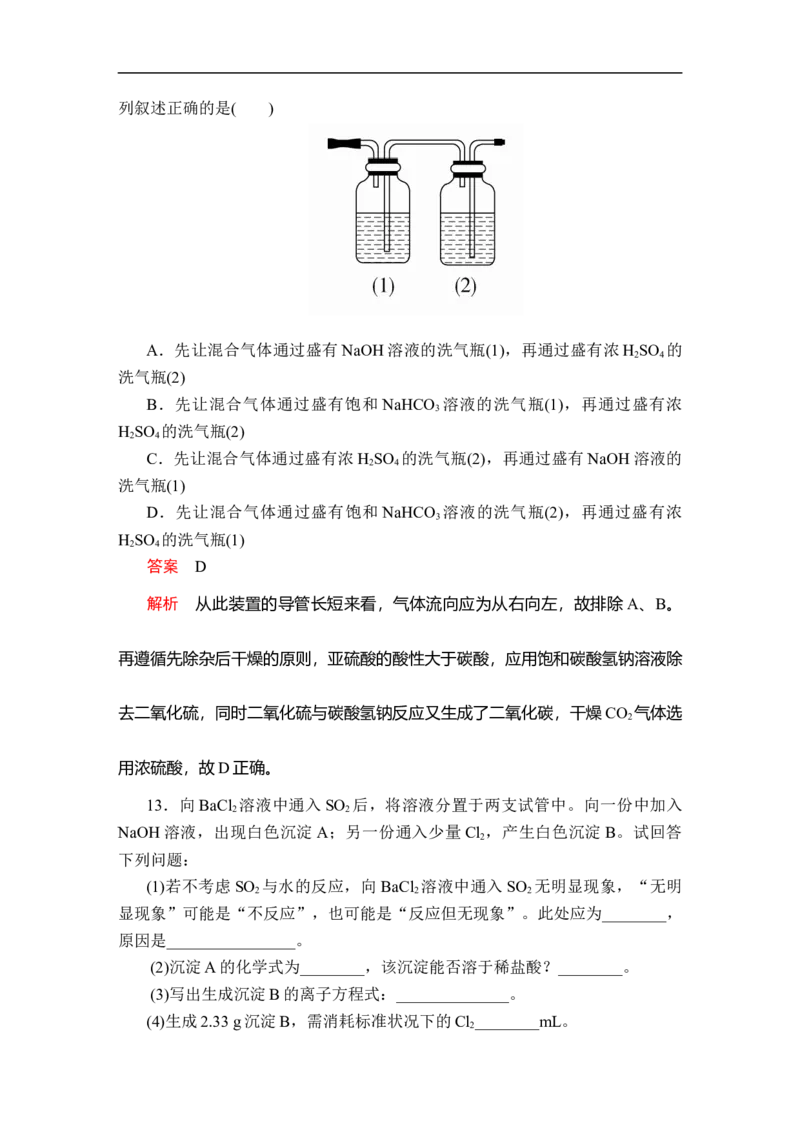
12.CO 气体中含少量 SO ,欲用如图所示装置得到干燥纯净的 CO ,则下
2 2 2列叙述正确的是( )
A.先让混合气体通过盛有NaOH溶液的洗气瓶(1),再通过盛有浓H SO 的
2 4
洗气瓶(2)
B.先让混合气体通过盛有饱和 NaHCO 溶液的洗气瓶(1),再通过盛有浓
3
H SO 的洗气瓶(2)
2 4
C.先让混合气体通过盛有浓H SO 的洗气瓶(2),再通过盛有NaOH溶液的
2 4
洗气瓶(1)
D.先让混合气体通过盛有饱和 NaHCO 溶液的洗气瓶(2),再通过盛有浓
3
H SO 的洗气瓶(1)
2 4
答案 D
解析 从此装置的导管长短来看,气体流向应为从右向左,故排除A、B。
再遵循先除杂后干燥的原则,亚硫酸的酸性大于碳酸,应用饱和碳酸氢钠溶液除
去二氧化硫,同时二氧化硫与碳酸氢钠反应又生成了二氧化碳,干燥CO 气体选
2
用浓硫酸,故D正确。
13.向BaCl 溶液中通入SO 后,将溶液分置于两支试管中。向一份中加入
2 2
NaOH溶液,出现白色沉淀 A;另一份通入少量Cl ,产生白色沉淀 B。试回答
2
下列问题:
(1)若不考虑SO 与水的反应,向 BaCl 溶液中通入SO 无明显现象,“无明
2 2 2
显现象”可能是“不反应”,也可能是“反应但无现象”。此处应为________,
原因是________________。
(2)沉淀A的化学式为________,该沉淀能否溶于稀盐酸?________。
(3)写出生成沉淀B的离子方程式:______________。
(4)生成2.33 g沉淀B,需消耗标准状况下的Cl ________mL。
2答案 (1)不反应 弱酸不能制强酸 (2)BaSO 能
3
(3)Ba2++SO +Cl +2H O===BaSO ↓+2Cl-+4H+ (4)224
2 2 2 4
解析 加入NaOH溶液发生的反应为
Ba2++SO +2OH-===BaSO ↓+H O;①
2 3 2
通入Cl 发生的反应为
2
Ba2++SO +Cl +2H O===BaSO ↓+2Cl-+4H+。②
2 2 2 4
由方程式②:BaSO ~ Cl
4 2
233 g 22400 mL
2.33 g V(Cl )
2
故V(Cl )=224 mL。
2
14.某化学兴趣小组为了探究常温下某非金属氧化物形成的未知气体的成分,
该小组成员将气体通入澄清石灰水,发现澄清石灰水变浑浊,持续通入发现浑浊
又变澄清,由此该小组成员对气体的成分提出猜想。
【提出猜想】
猜想1:________________;
猜想2:__________;
猜想3:_______。
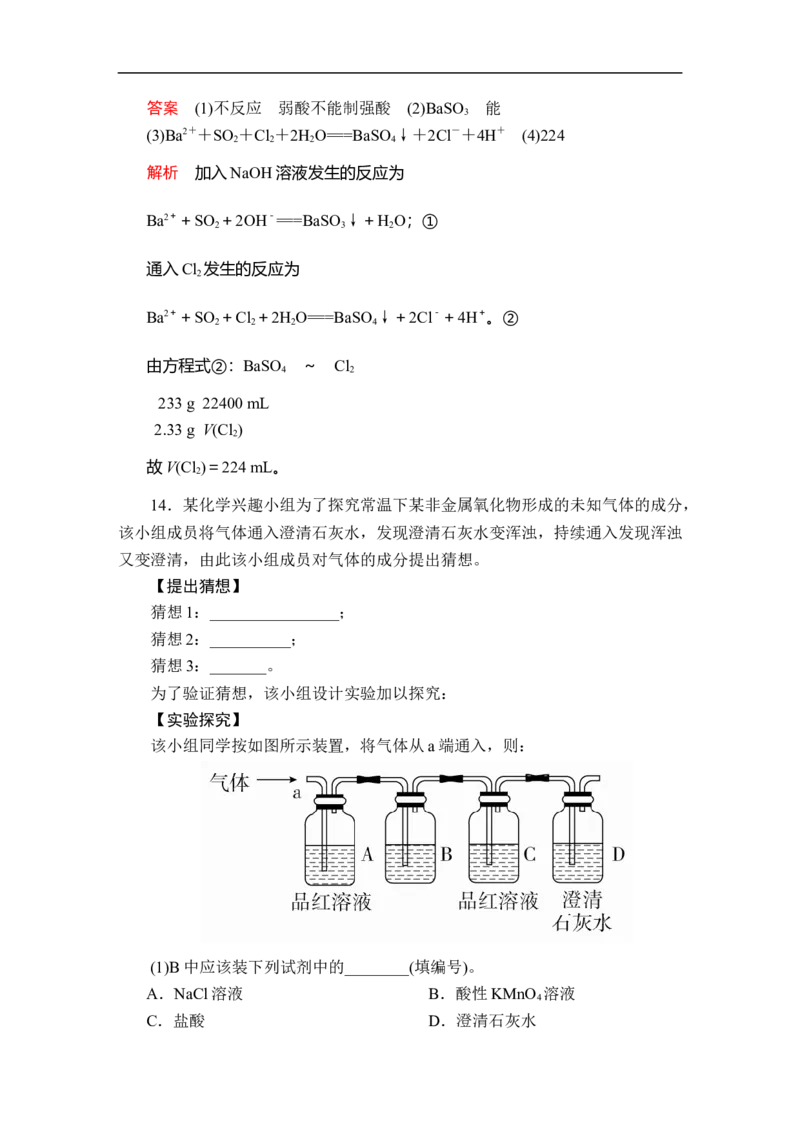
为了验证猜想,该小组设计实验加以探究:
【实验探究】
该小组同学按如图所示装置,将气体从a端通入,则:
(1)B中应该装下列试剂中的________(填编号)。
A.NaCl溶液 B.酸性KMnO 溶液
4
C.盐酸 D.澄清石灰水(2)A中品红溶液的作用是________________。
(3)D中澄清石灰水的作用是________________。
通过该实验,该小组同学观察到以下三个实验现象:
①A中品红溶液褪色;②C中品红溶液不褪色;
③D中澄清石灰水变浑浊。
【得出结论】
(4)由上述现象该小组同学确认该气体的成分为________________。
答案 【提出猜想】 气体为CO 气体为SO 气体为CO 和SO 的混合
2 2 2 2
气体
【实验探究】 (1)B
(2)验证混合气体中是否含有SO
2
(3)验证混合气体中是否含有CO
2
【得出结论】 (4)CO 和SO 的混合气体
2 2
解析 根据所学知识,能使澄清石灰水先变浑浊又变澄清的气体只有CO 和
2
SO ,所以提出的猜想是猜想1:气体为CO ;猜想2:气体为SO ;猜想3:气
2 2 2
体为CO 和SO 的混合气体。要验证气体的成分,必须先验证SO 是否存在,并
2 2 2
除尽,再检验CO 气体的存在,以防SO 干扰CO 的检验。
2 2 2