文档内容
人教版(2019)必修第二册第八章第二节 化学品的合理使
用课时训练一
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.我国科学家的科技创新成果斐然,下列成果中获得诺贝尔奖的是
A.侯德榜联合制碱法 B.钮经义等在1965年合成结晶牛胰岛
素
C.屠呦呦发现抗疟新药青蒿素 D.徐光宪建立稀土串级萃取理论
2.下列说法不正确的是
A.苯甲酸可以用于合成香料、药物等,其钠盐也是常用的食品防腐剂
B.硬化油不易被空气氧化变质,可作为制造肥皂和人造油的原料
C.甲醛又称福尔马林,具有杀菌、防腐性能,可用于制作生物标本
D.N,N-二甲基甲酰胺是生产多种化学纤维的溶剂,也用于合成农药、医药等
3.化学与生产、生活密切相关。下列说法错误的是
A.在燃煤中加入石灰石,有利于防治酸雨
B.84消毒液应避光密封保存
C.食品包装袋中的生石灰有防氧化作用
D.补铁剂搭配维生素C服用有助于铁的吸收
4.下列物质的用途说法正确的是
A.NH HCO 受热易分解,因此可用做化肥
4 3
B.碳酸钠可作为治疗胃溃疡病人胃酸过多症的药物
C.铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物
D.中秋佳节月饼中小袋包装的生石灰可用来防止月饼氧化变质
5.下列关于农药和肥料的说法正确的是
A.草木灰含有KCO,可作为钾肥使用
2 3
B.含磷化合物都可以作为磷肥直接使用
C.氮肥只能通过人工合成而得到
D.农药都对人体无害,可以大量使用农药
6.中和反应在工农业生产和日常生活中有广泛的用途。下列应用与中和反应原理无关
的是
A.施用熟石灰改良酸性土壤
B.服用含Al(OH) 的药物治疗胃酸过多
3C.用熟石灰和硫酸铜配制波尔多液
D.用NaOH溶液洗涤石油产品中的残余硫酸
7.化学与生活密切相关。下列说法错误的是
A.通常使用聚氯乙烯制食品保鲜袋
B.对自来水消毒,二氧化氯比氯气效果好
C.可用草木灰修复酸雨浸蚀后的土壤
D.低氟地区使用含氟牙膏有利于保护牙齿
8.已知土壤胶体粒子带负电荷,能吸收土壤中的正离子,有利于有些植物对正离子的
吸收;向土壤中施用含氮量相等的下列化肥,从化学式分析其中肥效最低的是
A.NH NO B.NH Cl C.NH HCO D.(NH )SO
4 3 4 4 3 4 2 4
9.有关合理用药的下列说法中,错误的是
A.对症下药是合理用药的首要原则
B.能被充分、快速吸收而无刺激性的药物,可在饭前口服
C.一种药物的用量,是经过严格的科学实验和大量的临床研究确定的
D.服药一般用温开水,止咳糖浆也可用水冲服
10.下列说法错误的是
A.氢键,离子键和共价键都属于化学键
B.化学家门捷列夫编制了第一张元素周期表
C.药剂师和营养师必须具备化学相关专业知识
D.石灰石是制造玻璃和水泥的主要原料之一
11.化学品的正确使用,关乎人体健康与环境保护。下列叙述正确的是
A.凡是有添加剂的食品均对人体健康不利
B.汽油是大宗化学品,属纯净物
C.化肥的超量使用不仅造成浪费,还可能污染环境
D.处方类药品是可不经医生直接购买服用
12.能够在人体血管中通行的药物分子运输车——“纳米药物分子运输车”在中国科
学院上海硅酸盐研究所研制成功,该“运输车”可提高肿瘤的治疗效果,其结构如图
所示。下列有关说法错误的是
试卷第2页,共3页A.包装上印“OTC”标识的药物为非处方药
B.油脂、蔗糖等这类含碳化合物属于有机物
C.分散质粒子直径在1~100nm的分散系为胶体,该“运输车”分散于水中所得的分
散系不属于胶体
D.该“运输车”中铁元素的价态为+3价
13.化学使人类生活更美好。下列叙述不正确的是
A.合理使用医用酒精,可有效杀菌消毒
B.港珠澳大桥中使用的水泥属于硅酸盐
C.三星堆出土的玛瑙饰品与水晶的成分不同
D.我国自主研发的“奋斗者”深海潜水器使用的钛合金具有耐高压、耐低温的特性
14.下列有关化学品的说法不正确的是
A.阿司匹林是一种重要的天然药物,具有解热镇痛作用
B.亚硝酸钠能防止肉制品变质,但有一定毒性
C.农药在农作物病虫害的综合防治中占有重要地位
D.毒品对个人和社会危害极大,每一个人都应远离毒品
15.古诗词是我国传统文化的瑰宝。下列诗词解读错误的是
A.“常恐秋节至,焜黄华叶衰”,树叶由绿变黄是发生了化学变化
B.“落红不是无情物,化作春泥更护花”蕴含着自然界中的碳、氮循环
C.“朝坛雾卷,曙岭烟沉”,雾有丁达尔现象是因为胶体粒子对光有散射作用
D.“心忧炭贱愿天寒”中的炭与“嫦娥五号”卫星所用的碳纤维互为同素异形体
二、填空题
16.胃病是人类易患的疾病,“氢氧化铝”是市场上一种常见的胃药,下表是它的说
明书。
[药品名称]复方氢氧化铝片
[成分]每片含主要成分氢氧化铝 、硅酸镁 、颠茄流浸膏
[辅料]淀粉、硬脂酸镁
[适应症]用于缓解胃酸过多引起的胃痛、胃灼热感(烧心)、反酸,也可用于慢性胃
炎
[用法用量]口服。成人一次2~4片,一日3次。饭前半小时或胃痛发作时嚼碎后服
(1)氢氧化铝可中和胃酸(盐酸),该反应的化学方程式为
________________________________________。
(2)药片中除含有铝元素外,还含有镁、硅等元素,将药品溶解在稀硫酸中,得到一种白色沉淀,此反应的离子方程式为_____________________________,说明
____________。将溶液分成两份,向一份中逐滴加入氢氧化钠溶液至过量,现象为
____________________;另一份逐滴加入氨水至过量,现象为
____________________________________,反应的离子方程式为_______________
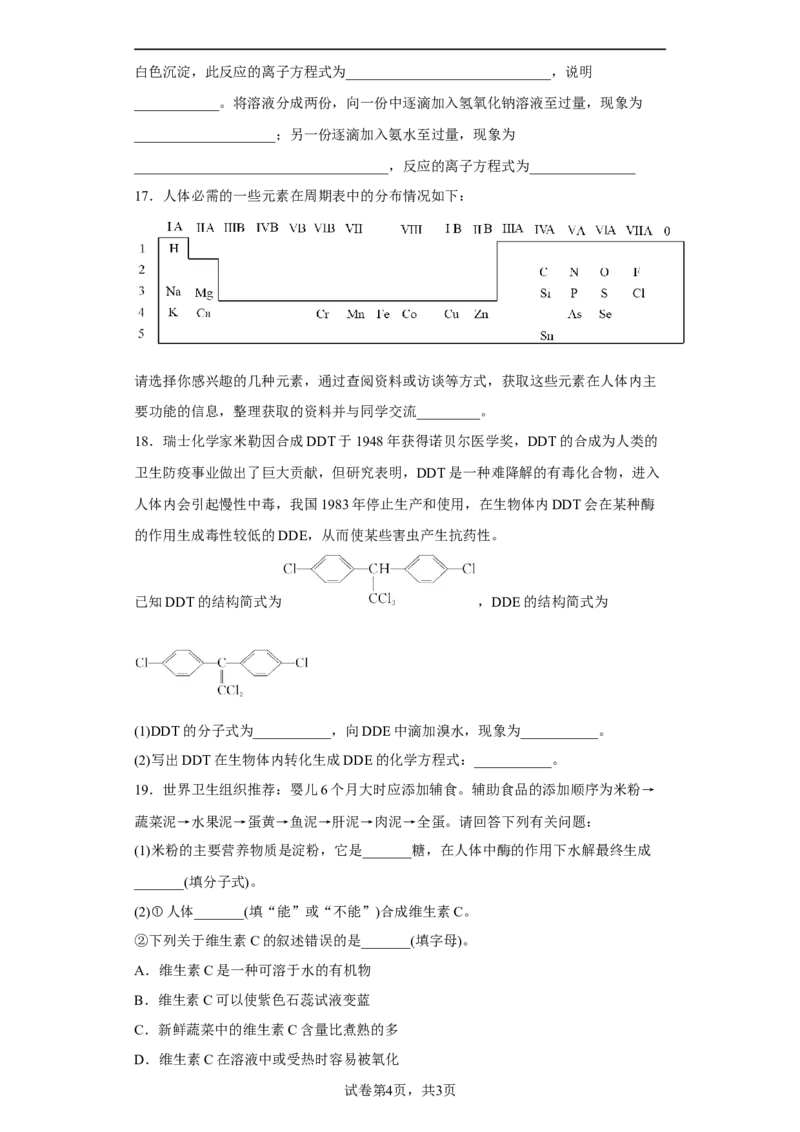
17.人体必需的一些元素在周期表中的分布情况如下:
请选择你感兴趣的几种元素,通过查阅资料或访谈等方式,获取这些元素在人体内主
要功能的信息,整理获取的资料并与同学交流_________。
18.瑞士化学家米勒因合成DDT于1948年获得诺贝尔医学奖,DDT的合成为人类的
卫生防疫事业做出了巨大贡献,但研究表明,DDT是一种难降解的有毒化合物,进入
人体内会引起慢性中毒,我国1983年停止生产和使用,在生物体内DDT会在某种酶
的作用生成毒性较低的DDE,从而使某些害虫产生抗药性。
已知DDT的结构简式为 ,DDE的结构简式为
(1)DDT的分子式为___________,向DDE中滴加溴水,现象为___________。
(2)写出DDT在生物体内转化生成DDE的化学方程式:___________。
19.世界卫生组织推荐:婴儿6个月大时应添加辅食。辅助食品的添加顺序为米粉→
蔬菜泥→水果泥→蛋黄→鱼泥→肝泥→肉泥→全蛋。请回答下列有关问题:
(1)米粉的主要营养物质是淀粉,它是_______糖,在人体中酶的作用下水解最终生成
_______(填分子式)。
(2)①人体_______(填“能”或“不能”)合成维生素C。
②下列关于维生素C的叙述错误的是_______(填字母)。
A.维生素C是一种可溶于水的有机物
B.维生素C可以使紫色石蕊试液变蓝
C.新鲜蔬菜中的维生素C含量比煮熟的多
D.维生素C在溶液中或受热时容易被氧化
试卷第4页,共3页E维生素C可在铁制容器内配制成溶液使用
(3)宝宝食用蛋黄,可以补充奶类中铁的匮乏。铁属于_______(填“常量元素”或“微
量元素”),人体缺铁将会导致_______(填字母)。
A.记忆能力下降 B.免疫能力下降
C.对温度的适应能力下降 D.缺铁性贫血
(4)①6个月内的婴儿消化道黏膜屏障发育尚不完全,而蛋清中的蛋白质分子较小,容
易透过肠壁黏膜进入血液,引起过敏反应。蛋白质在人体内水解的最终产物为_______。
②为了保障婴儿的健康,很多国家已明确规定婴儿食品内不能加入任何_______(填
“着色剂”或“营养强化剂”)。
(5)某抗酸药的有效成分是氢氧化铝,写出其中和胃里过多的盐酸时发生反应的化学方
程式:_______。
20.人们吃的冷热酸甜、形形色色的食物,都要经过胃的消化,天长日久可能对胃造
成了各种伤害,因此人们发明了各种各样的治疗胃病的药物,其中一类抗酸药能有效
地治疗因胃酸过多引起的胃痛、胃胀等,其有效成分除了中学化学中熟知的氧化镁、
氢氧化镁、氢氧化铝、碳酸钙、碳酸氢钠等外,还有一些我们不太熟悉的物质如双羟
基铝碳酸钠、柠檬酸钠、三硅酸镁等。联系我们所学知识,试完成下列各题:
(1)人的胃液中含有盐酸,可以为胃蛋白酶提供酸性环境,同时还可以杀死随食物进入
胃部的细菌,但胃液酸度过高会患胃酸过多症,下列物质不宜用作治疗胃酸过多症的
药物的主要成分的是_______。
A.小苏打粉B.Al(OH) 粉C.氧化钙粉D.纯碳酸钙粉
3
(2)胃镜检查发现胃少量出血,说明胃溃疡已深及黏膜下层,此种情况下胃溃疡患者胃
酸过多可考虑选用上小题中的_______(填字母)。
(3)某品牌抗酸药的主要成分有糖衣、碳酸镁、氢氧化铝、淀粉。
①写出该抗酸药发挥功效时的化学方程式:_______、_______。
②淀粉在抗酸药中作填充剂、黏合剂,淀粉在人体内酶的催化作用下发生水解反应,
最终转化为_______(写分子式)。
三、实验题
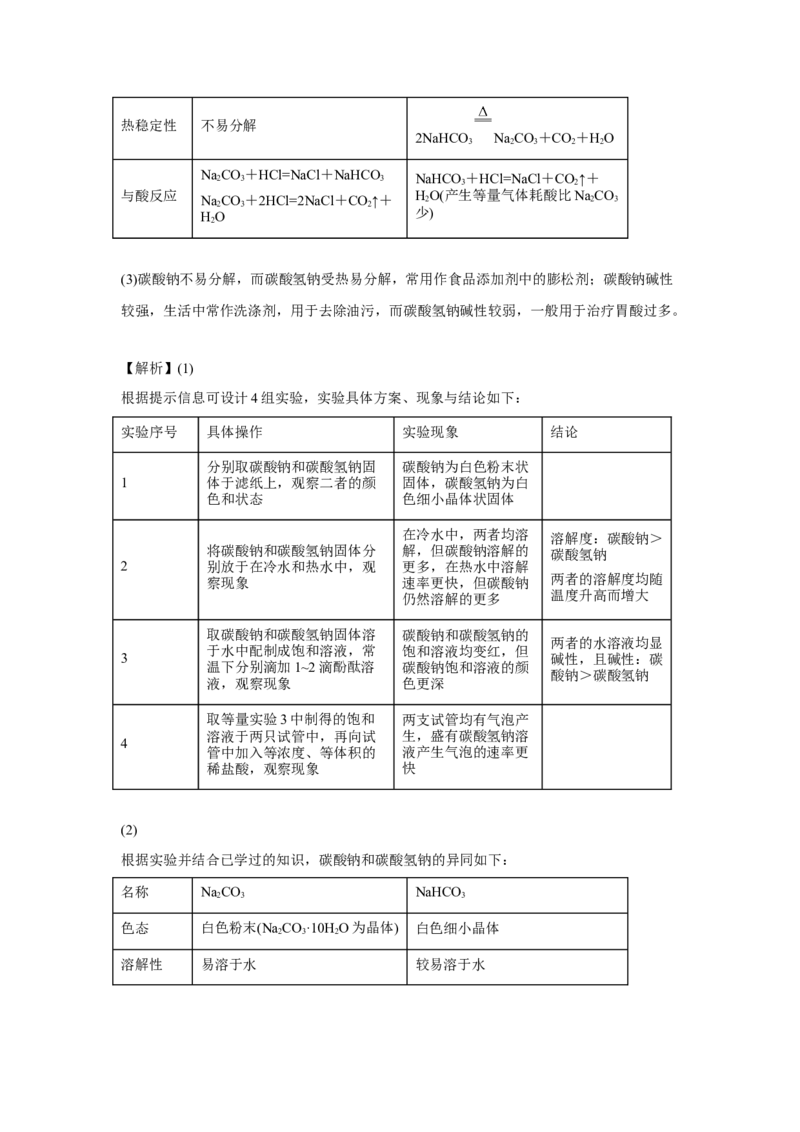
21.碳酸钠和碳酸氢钠在食品工业中均可用作食品添加剂,它们也是生活中常见的日
用化学品。
(1)为了解碳酸钠和碳酸氢钠的性质,请根据以下提示设计实验并完成实验报告。
___________①观察二者的颜色和状态;
②观察其在冷水和热水中的溶解情况;
③测定其饱和溶液的pH;
④向其溶液中分别逐滴加入盐酸,观察现象。
(2)根据以上实验的结果和已学过的知识,列表比较碳酸钠和碳酸氢钠性质的异同。
___________
(3)举例说明碳酸钠和碳酸氢钠在日常生活或食品工业中的用途,根据二者的性质进行
解释,并与同学讨论。___________
22.请你参与识别化肥的探究活动。有五种化肥分别是硫酸钾、氯化钾、碳酸氢铵、
氯化铵和硝酸铵。
第一步:称取五种化肥各10 g,分别研细。
第二步:硝酸铵和熟石灰反应的化学方程式是___________。
第三步:另取三种铵盐各少量,分别盛于三支试管中,均滴入少量盐酸,无明显现象
的是___________,有气泡放出的是___________,反应的化学方程式是___________。
第四步:另取氯化铵和硝酸铵两种铵盐进行识别,写出识别时发生反应的化学方程式:
___________。
第五步:取两种钾盐,分别在试管中配成溶液,各滴入几滴氯化钡溶液,生成白色沉
淀的钾盐是______,无明显现象的钾盐是______。
试卷第6页,共3页参考答案:
1.C
【详解】屠呦呦发现抗疟新药青蒿素的成果获得诺贝尔奖,故C符合题意。
综上所述,答案为C。
2.C
【详解】A.苯甲酸可以用于合成香料、药物等,苯甲酸钠是常用的食品防腐剂,A正确;
B.硬化油是饱和脂肪酸甘油酯,不易被空气氧化变质,可作为制造肥皂和人造油的原料,
B正确;
C.含甲醛 的溶液称福尔马林,C错误;
D.N,N-二甲基甲酰胺可用于多种化学纤维的溶剂,也用于合成农药、医药等,D正确;
故选C。
3.C
【详解】A. 在燃煤中加入石灰石,发生反应 ,
, ,故有利于防治酸雨,故A正确;
B. 84消毒液的有效成分是NaClO,存在水解反应 ,HClO
见光易分解,促进水解反应正向进行,使84消毒液失效,故应避光密封保存,故B正确;
C. 食品包装袋中的生石灰起干燥作用,生石灰无还原性,故C错误;
D. 人体吸收的铁元素为亚铁离子,而亚铁离子易被氧化,维生素C具有还原性,维生素
C具有抗氧化的作用,故补铁剂搭配维生素C服用有助于铁的吸收,故D正确;
故选C。
4.C
【详解】A.NH HCO 可用做化肥,是因为它溶于水后电离产生的 能被植物吸收,为
4 3
植物提供营养元素,A不正确;
B.碳酸钠虽然能与胃酸反应,但它的碱性过强,会腐蚀胃壁,所以不能作为治疗胃酸过
多症的药物,B不正确;
C.铝制餐具表面的保护膜为氧化铝,能溶于酸或碱,所以不宜用来蒸煮或长时间存放酸性或碱性食物,C正确;
D.中秋月饼袋中放有小袋包装的生石灰,生石灰具有吸水性,可用来防止月饼受潮变质,
D不正确;
故选C。
5.A
【详解】A.草木灰含有KCO,KCO 属于可溶性钾盐,故可作为钾肥使用,故A正确;
2 3 2 3
B.含磷化合物不一定都可以作为磷肥直接使用,故B错误;
C.氮肥不一定只能通过人工合成而得到,例如自然固氮等,故C错误;
D.农药都对人体有害,不可以大量使用农药,故D错误;
故选:A。
6.C
【详解】A.施用熟石灰改良酸性土壤时,利用熟石灰的碱性,中和土壤的酸性,A不符
合题意;
B.服用含Al(OH) 的药物治疗胃酸过多时,利用Al(OH) 的碱性中和胃酸的酸性,B不符
3 3
合题意;
C.用熟石灰和硫酸铜配制波尔多液,发生的是碱和盐的复分解反应,不是酸碱中和反应,
C符合题意;
D.用NaOH溶液洗涤石油产品中的残余硫酸,NaOH与硫酸发生中和反应,D不符合题意;
故选C。
7.A
【详解】A.聚氯乙烯塑料受热会产生有毒物质,不可用来制食品保鲜袋,故A错误;
B.ClO 中氯元素的化合价为+4价,Cl 的化合价为0价,所以单位质量的ClO 比Cl 的物
2 2 2 2
质的量大,得电子数目多,与Cl 相比是一种高效消毒剂,故B正确;
2
C.草木灰的主要成分是KCO,水溶液显碱性能够与硫酸等反应,可以用来治理土壤酸化,
2 3
故C正确;
D.用含氟牙膏可在牙齿表面形成坚硬难溶的Ca (PO )F,有利于保护牙齿,故D正确;
5 4 3
答案为A。
8.A
【详解】A.NH NO 中含N微粒为 和 ,土壤胶体粒子带负电,能吸收 ,但
4 3
答案第2页,共2页不能吸收 , 会随水土流失,从而使肥效损失,A符合题意;
B.NH Cl中含N微粒为 ,土壤胶体粒子能吸收 并加以利用,从而有效利用此氮
4
肥,B不符合题意;
C.NH HCO 中含N微粒为 ,能被土壤胶体粒子吸收利用,从而有效利用此氮肥,C
4 3
不符合题意;
D.(NH )SO 中含N微粒为 ,能被土壤胶体粒子吸收,使肥分得以有效利用,D不符
4 2 4
合题意;
故选A。
9.D
【详解】A.根据病情需要,恰当选择药物,以达到好的治疗效果,故A正确;
B.无刺激性的药物,对胃和消化道不产生刺激,可以可在饭前口服,故B正确;
C.药物的用量是经过严格的科学实验和大量的临床研究确定的,故C正确;
D.止咳糖浆用水冲服会被稀释效果减弱,故D错误。
故选D。
10.A
【详解】A.离子键和共价键都属于化学键,氢键属于分子间作用力,A说法错误;
B.第一张元素周期表是俄国化学家门捷列夫编制的,B说法正确;
C.药剂师和营养师的工作分别与药剂和营养物质有关,因此必须具备相关的化学专业知
识才能胜任相关工作,C说法正确;
D.制造玻璃的主要原料是石灰石、石英和纯碱,制造水泥的主要原料是石灰石和黏土,D
说法正确;
综上所述,本题选A。
11.C
【详解】A.合理使用食品添加剂,对丰富食品生产和促进人体健康有好处,可以食用,
但不能过量,A错误;
B.汽油是石油分馏产品,其中含有多种烃,仍然是混合物,B错误;
C.化肥可以使植物长势更好,但若使用超量,不仅会造成物质浪费,还可能污染土壤和水源,C正确;
D.处方类药品必须经医生开处方后在医生的指导下购买服用,而非处方药品可不经医生
直接购买服用,D错误;
故合理选项是C。
12.D
【详解】A.“OTC”代表非处方药,R代表处方药,A正确;
B.油脂、蔗糖均含碳元素,不根据其组成和结构特点,属于有机物,B正确;
C.该"纳米药物分子车”的直径为20Onm,而胶体分散质粒子直径为1~100nm,所以
该"纳米药物分子车"分散于水中所得的分散系不属于胶体,C正确;
D.由图可知,该有机物中含有四氧化三铁,其中有+2价和+3价铁,D错误;
故选D。
13.C
【详解】A.医用酒精为75%的乙醇水溶液,能使蛋白质变性,可用于杀菌消毒,A正确;
B.水泥属于无机非金属材料,其主要成分为硅酸盐,B正确;
C.玛瑙与水晶的主要成分均为 ,C错误;
D.海底深处的压强大、气温低,所以深海潜水器使用的钛合金应具有耐高压、耐低温的
特性,D正确;
故选C。
14.A
【详解】A.阿司匹林是一种重要的合成药物,化学名称为乙酰水杨酸,具有解热镇痛作
用,A错误;
B.亚硝酸钠具有还原性,因此能防止肉制品氧化变质,但有一定毒性,因此一定要注意
量的使用在安全范围,B正确;
C.农药可以治疗病虫害,提高农作物的产量,因此在农作物病虫害的综合防治中占有重
要地位,C正确;
D.毒品对中枢神经系统和周围神经系统都有很大的损害,可产生异常的兴奋、抑制等作
用,出现一系列神经、精神症状,如失眠、烦躁、惊厥、麻痹、记忆力下降、主动性降低、
性格孤僻、意志消沉、周围神经炎等。对心血管系统、呼吸系统、消化系统和生殖系统等
都会造成严重的危害。吸毒使免疫力下降,还会成为感染艾滋病、乙肝等血液传染病的高
危人群。可见毒品对个人和社会危害极大,每一个人都应远离毒品,D正确;
答案第4页,共2页故合理选项是A。
15.D
【详解】A. “常恐秋节至,焜黄华叶衰”,树叶由绿变黄是树叶中叶绿素分解,被叶绿
素掩盖的红色素、黄色素露出而显红色、黄色,有新物质产生,发生了化学变化,故A正
确;
B. “落红不是无情物,化作春泥更护花”,花等有机物落到泥土中,植物体中的蛋白质、
纤维素等含C、N的物质分解后变成有机肥供植物使用,蕴含着自然界中的碳、氮循环,
故B正确;
C. “朝坛雾卷,曙岭烟沉”,雾有丁达尔现象是因为胶体粒子对光有散射作用,形成
“光亮的通路”,故C正确;
D.碳纤维是一种新型无机非金属材料,是含碳量在90%以上的高强度高模量纤维,主要
成分是碳的单质,“心忧炭贱愿天寒”中的炭,炭黑的主要成分也为碳,不能互称为同素
异形体,金刚石、石墨、活性炭等由碳元素组成的不同的单质才能互称为同素异形体,故
D错误;
故选D。
16. Al(OH) +3HCl=AlCl +3H O MgSiO +2H+=H SiO↓+Mg2+ 硫酸的酸性比
3 3 2 3 2 3
硅酸的强 先有白色沉淀产生且逐渐增多,后沉淀又逐渐减少到一定量后不再减
少 有白色沉淀产生且逐渐增多至一定量后不再改变 Mg2+
+2NH∙H O=Mg(OH)↓+2 ,Al3++3NH∙H O=Al(OH) ↓+3
3 2 2 3 2 3
【详解】(1)氢氧化铝可与盐酸反应生成氯化铝和水,反应的方程式为
Al(OH) +3HCl=AlCl +3H O;
3 3 2
(2)硅酸镁与硫酸反应生成白色沉淀硅酸,离子方程式为MgSiO +2H+=H SiO↓+Mg2+;根据
3 2 3
强酸制弱酸原理,说明硫酸的酸性比硅酸的强;硫酸铝、硫酸镁能与NaOH反应生成氢氧
化铝、氢氧化镁,随NaOH的加入,溶液中铝离子、镁离子反应完全时,氢氧化铝与
NaOH反应生成偏铝酸钠溶液,可观察到先有白色沉淀产生且逐渐增多,后沉淀又逐渐减
少到一定量后不再减少;而氨水不能与氢氧化铝反应,则加入氨水至过量时,可观察到有
白色沉淀产生且逐渐增多至一定量后不再改变;反应的离子方程式为Mg2+
+2NH∙H O=Mg(OH)↓+2 ,Al3++3NH∙H O=Al(OH) ↓+3 。
3 2 2 3 2 317.碳对于现有已知的所有生命系统都是不可或缺的,没有它,生命不可能存在。
钠是人体中一种重要无机元素,是细胞外液中带正电的主要离子,参与水的代谢,保证体
内水的平衡,调节体内水分与渗透压;维持体内酸和碱的平衡;是胰液、胆汁、汗和泪水
的组成成分;对ATP(腺嘌呤核苷三磷酸)的生产和利用、肌肉运动、心血管功能、能量
代谢都有关系;糖代谢、氧的利用也需有钠的参与;维持血压正常;增强神经肌肉兴奋性。
钾可以调节细胞内适宜的渗透压和体液的酸碱平衡,参与细胞内糖和蛋白质的代谢。有助
于维持神经健康、心跳规律正常,可以预防中风,并协助肌肉正常收缩。在摄入高钠而导
致高血压时,钾具有降血压作用。
钙是人类骨、齿的主要无机成分,也是神经传递、肌肉收缩、血液凝结、激素释放和乳汁
分泌等所必需的元素。钙约占人体质量的1.4%,参与新陈代谢,每天必须补充钙;人体中
钙含量不足或过剩都会影响生长发育和健康。
磷和钙都是骨骼牙齿的重要构成材料;保持体内ATP代谢的平衡;磷是组成遗传物质核酸
的基本成分之一,而核苷酸是生命中传递信息和调控细胞代谢的重要物质——核糖核酸
(RNA)和脱氧核糖核酸(DNA)的基本组成单位;参与体内的酸碱平衡的调节,参与体
内能量的代谢。
铁是血红蛋白的重要部分,而血红蛋白功能是向细胞输送氧气,并将二氧化碳带出细胞;
铁元素催化促进β-胡萝卜素转化为维生素A、嘌呤与胶原的合成,抗体的产生,脂类从血
液中转运以及药物在肝脏的解毒等;铁与免疫的关系也比较密切;铁可以提高机体的免疫
力,增加中性白细胞和吞噬细胞的吞噬功能;可使机体的抗感染能力增强。
【详解】碳对于现有已知的所有生命系统都是不可或缺的,没有它,生命不可能存在。
钠是人体中一种重要无机元素,是细胞外液中带正电的主要离子,参与水的代谢,保证体
内水的平衡,调节体内水分与渗透压;维持体内酸和碱的平衡;是胰液、胆汁、汗和泪水
的组成成分;对ATP(腺嘌呤核苷三磷酸)的生产和利用、肌肉运动、心血管功能、能量
代谢都有关系;糖代谢、氧的利用也需有钠的参与;维持血压正常;增强神经肌肉兴奋性。
钾可以调节细胞内适宜的渗透压和体液的酸碱平衡,参与细胞内糖和蛋白质的代谢。有助
于维持神经健康、心跳规律正常,可以预防中风,并协助肌肉正常收缩。在摄入高钠而导
致高血压时,钾具有降血压作用。
钙是人类骨、齿的主要无机成分,也是神经传递、肌肉收缩、血液凝结、激素释放和乳汁
分泌等所必需的元素。钙约占人体质量的1.4%,参与新陈代谢,每天必须补充钙;人体中
钙含量不足或过剩都会影响生长发育和健康。
答案第6页,共2页磷和钙都是骨骼牙齿的重要构成材料;保持体内ATP代谢的平衡;磷是组成遗传物质核酸
的基本成分之一,而核苷酸是生命中传递信息和调控细胞代谢的重要物质——核糖核酸
(RNA)和脱氧核糖核酸(DNA)的基本组成单位;参与体内的酸碱平衡的调节,参与体
内能量的代谢。
铁是血红蛋白的重要部分,而血红蛋白功能是向细胞输送氧气,并将二氧化碳带出细胞;
铁元素催化促进β-胡萝卜素转化为维生素A、嘌呤与胶原的合成,抗体的产生,脂类从血
液中转运以及药物在肝脏的解毒等;铁与免疫的关系也比较密切;铁可以提高机体的免疫
力,增加中性白细胞 和吞噬细胞的吞噬功能;可使机体的抗感染能力增强。
18.(1) C HCl 溴水褪色
14 9 5
(2) +HCl
【解析】略
19. 多 C H O 不能 BE 微量元素 ABCD
6 12 6
氨基酸 着色剂 Al(OH) +3HCl=AlCl +3H O
3 3 2
【详解】(1)淀粉的化学式为(C H O)n,淀粉属于多糖,淀粉在人体中可以被水解,最终水
6 10 5
解产物为葡萄糖,化学式为C H O;
6 12 6
(2)①维生素C为人体所需要的重要影响物质,人体不能直接合成维生素C,必须从食物中
摄取;
②A.维生素C为水溶性维生素,维生素C可以溶于水,A正确;
B.维生素C水溶液呈酸性,可以使紫色石蕊试液变红,B错误;
C.维生素C在高温下可以发生氧化,因此新鲜蔬菜中的维生素C含量比煮熟的多,C正
确;
D.维生素C受热易被氧化,生成脱氢维生素C,D正确;
E.维生素C具有酸性,可以与铁制容器反应,不能用铁制容器配制维生素C溶液,E错误;
故选择BE;
(3)铁属于微量元素,人体缺铁会导致记忆力下降、免疫力下降、对温度的适应能力下降、
缺铁性贫血,故答案选ABCD;
(4)①蛋白质可以在人体中水解,水解的最终产物为氨基酸;
②婴儿对食品添加剂的代谢能力较弱,因此国家规定:婴儿食品中不能添加任何着色剂;
(5)胃酸的主要成分为盐酸,服用Al(OH) 可以中和胃酸,反应的化学方程式为
3Al(OH) +3HCl=AlCl +3H O。
3 3 2
20. C B
C H O
6 12 6
【详解】(1)CaO溶于水生成强碱并放出大量的热,不能用于治疗胃酸过多症,答案选C;
(2)患胃溃疡较重者,不能服用与胃酸反应放出CO 气体的抗酸药,为避免加速胃穿孔,可
2
服用含Al(OH) 粉的药物,答案选B;
3
(3)①能发挥药效的是碳酸镁与氢氧化铝,发挥功效时的化学方程式为
、 ;
②淀粉水解的最终产物是葡萄糖,分子式为C H O。
6 12 6
21.(1)
实验序号 具体操作 实验现象 结论
分别取碳酸钠和碳酸氢钠固 碳酸钠为白色粉末状
1 体于滤纸上,观察二者的颜 固体,碳酸氢钠为白
色和状态 色细小晶体状固体
在冷水中,两者均溶 溶解度:碳酸钠>
将碳酸钠和碳酸氢钠固体分 解,但碳酸钠溶解的 碳酸氢钠
2 别放于在冷水和热水中,观 更多,在热水中溶解
察现象 速率更快,但碳酸钠 两者的溶解度均随
仍然溶解的更多 温度升高而增大
取碳酸钠和碳酸氢钠固体溶 碳酸钠和碳酸氢钠的
两者的水溶液均显
于水中配制成饱和溶液,常 饱和溶液均变红,但
3 碱性,且碱性:碳
温下分别滴加1~2滴酚酞溶 碳酸钠饱和溶液的颜
酸钠>碳酸氢钠
液,观察现象 色更深
取等量实验3中制得的饱和 两支试管均有气泡产
溶液于两只试管中,再向试 生,盛有碳酸氢钠溶
4
管中加入等浓度、等体积的 液产生气泡的速率更
稀盐酸,观察现象 快
(2)
名称 NaCO NaHCO
2 3 3
色态 白色粉末(Na CO·10H O为晶体) 白色细小晶体
2 3 2
溶解性 易溶于水 较易溶于水
答案第8页,共2页热稳定性 不易分解
2NaHCO NaCO+CO+HO
3 2 3 2 2
Na 2 CO 3 +HCl=NaCl+NaHCO 3 NaHCO 3 +HCl=NaCl+CO 2 ↑+
与酸反应 NaCO+2HCl=2NaCl+CO↑+ H 2 O(产生等量气体耗酸比Na 2 CO 3
2 3 2
HO
少)
2
(3)碳酸钠不易分解,而碳酸氢钠受热易分解,常用作食品添加剂中的膨松剂;碳酸钠碱性
较强,生活中常作洗涤剂,用于去除油污,而碳酸氢钠碱性较弱,一般用于治疗胃酸过多。
【解析】(1)
根据提示信息可设计4组实验,实验具体方案、现象与结论如下:
实验序号 具体操作 实验现象 结论
分别取碳酸钠和碳酸氢钠固 碳酸钠为白色粉末状
1 体于滤纸上,观察二者的颜 固体,碳酸氢钠为白
色和状态 色细小晶体状固体
在冷水中,两者均溶 溶解度:碳酸钠>
将碳酸钠和碳酸氢钠固体分 解,但碳酸钠溶解的 碳酸氢钠
2 别放于在冷水和热水中,观 更多,在热水中溶解
察现象 速率更快,但碳酸钠 两者的溶解度均随
仍然溶解的更多 温度升高而增大
取碳酸钠和碳酸氢钠固体溶 碳酸钠和碳酸氢钠的
两者的水溶液均显
于水中配制成饱和溶液,常 饱和溶液均变红,但
3 碱性,且碱性:碳
温下分别滴加1~2滴酚酞溶 碳酸钠饱和溶液的颜
酸钠>碳酸氢钠
液,观察现象 色更深
取等量实验3中制得的饱和 两支试管均有气泡产
溶液于两只试管中,再向试 生,盛有碳酸氢钠溶
4
管中加入等浓度、等体积的 液产生气泡的速率更
稀盐酸,观察现象 快
(2)
根据实验并结合已学过的知识,碳酸钠和碳酸氢钠的异同如下:
名称 NaCO NaHCO
2 3 3
色态 白色粉末(Na CO·10H O为晶体) 白色细小晶体
2 3 2
溶解性 易溶于水 较易溶于水热稳定性 不易分解
2NaHCO NaCO+CO+HO
3 2 3 2 2
Na 2 CO 3 +HCl=NaCl+NaHCO 3 NaHCO 3 +HCl=NaCl+CO 2 ↑+
与酸反应 NaCO+2HCl=2NaCl+CO↑+ H 2 O(产生等量气体耗酸比Na 2 CO 3
2 3 2
HO
少)
2
(3)
根据二者的性质,碳酸钠不易分解,而碳酸氢钠受热易分解,常用作食品添加剂中的膨松
剂;碳酸钠碱性较强,生活中常作洗涤剂,用于去除油污,而碳酸氢钠碱性较弱,一般用
于治疗胃酸过多。
22. 2NH NO +Ca(OH) Ca(NO )+2NH ↑+2HO 氯化铵和硝酸铵
4 3 2 3 2 3 2
碳酸氢铵 NH HCO +HCl=NHCl+CO↑+HO NH Cl+AgNO=NHNO +
4 3 4 2 2 4 3 4 3
AgCl↓ KSO KCl
2 4
【分析】由物质的性质可知,三种铵盐中能与盐酸反应生成二氧化碳气体的是碳酸氢铵,
能与硝酸银溶液反应生成氯化银白色沉淀的是氯化铵,无明显现象的为硝酸铵;两种钾盐
中能与硫酸钡溶液反应生成白色沉淀的是硫酸钾,无明显现象的为氯化钾。
【详解】第二步:硝酸铵和熟石灰共热反应生成硝酸钙、氨气和水,反应的化学方程式为
2NH NO +Ca(OH) Ca(NO )+2NH ↑+2HO,故答案为:2NH NO +Ca(OH) Ca(NO )
4 3 2 3 2 3 2 4 3 2 3 2
+2NH ↑+2HO;
3 2
第三步:由分析可知,三种铵盐中能与盐酸反应生成二氧化碳气体的是碳酸氢铵,碳酸氢
铵与盐酸反应生成氯化铵、二氧化碳和水,反应的化学方程式为NH HCO +HCl=NHCl+
4 3 4
CO↑+HO,无明显现象的为氯化铵和硝酸铵,故答案为:氯化铵和硝酸铵;二氧化碳;
2 2
NH HCO +HCl=NHCl+CO↑+HO;
4 3 4 2 2
第四步:氯化铵和硝酸铵两种铵盐中,氯化铵能与硝酸银溶液反应生成氯化银白色沉淀和
硝酸铵,反应的化学方程式为NH Cl+AgNO=NHNO +AgCl↓,而硝酸铵不能与硝酸银溶
4 3 4 3
液反应,故答案为:NH Cl+AgNO=NHNO +AgCl↓;
4 3 4 3
第五步:两种钾盐中能与硫酸钡溶液反应生成白色沉淀的是硫酸钾,无明显现象的为氯化
钾,故答案为:KSO ;2KCl。
2 4
答案第10页,共2页