文档内容
第四章 化学反应与电能 章末单元测试题
榆次一中 李金虎
一、选择题(本题共有15小题,每小题3分,共45分,每小题只有一个正确选项)
1. 下列过程需要通电后才可以发生或进行的是( )
①电离 ②电泳 ③电解 ④电镀 ⑤电化学腐蚀
A.①② B.②③④ C.②③④⑤ D.全部
2. 下列叙述中,正确的是( )
①电解池是将化学能转变成电能的装置
②原电池是将电能转变成化学能的装置
③金属和石墨导电均为物理变化,电解质溶液导电是化学变化
④不能自发进行的氧化还原反应,通过电解的原理有可能实现
⑤电镀过程相当于金属的“迁移”,可视为物理变化
A.①②③④ B.③④
C.③④⑤ D.④
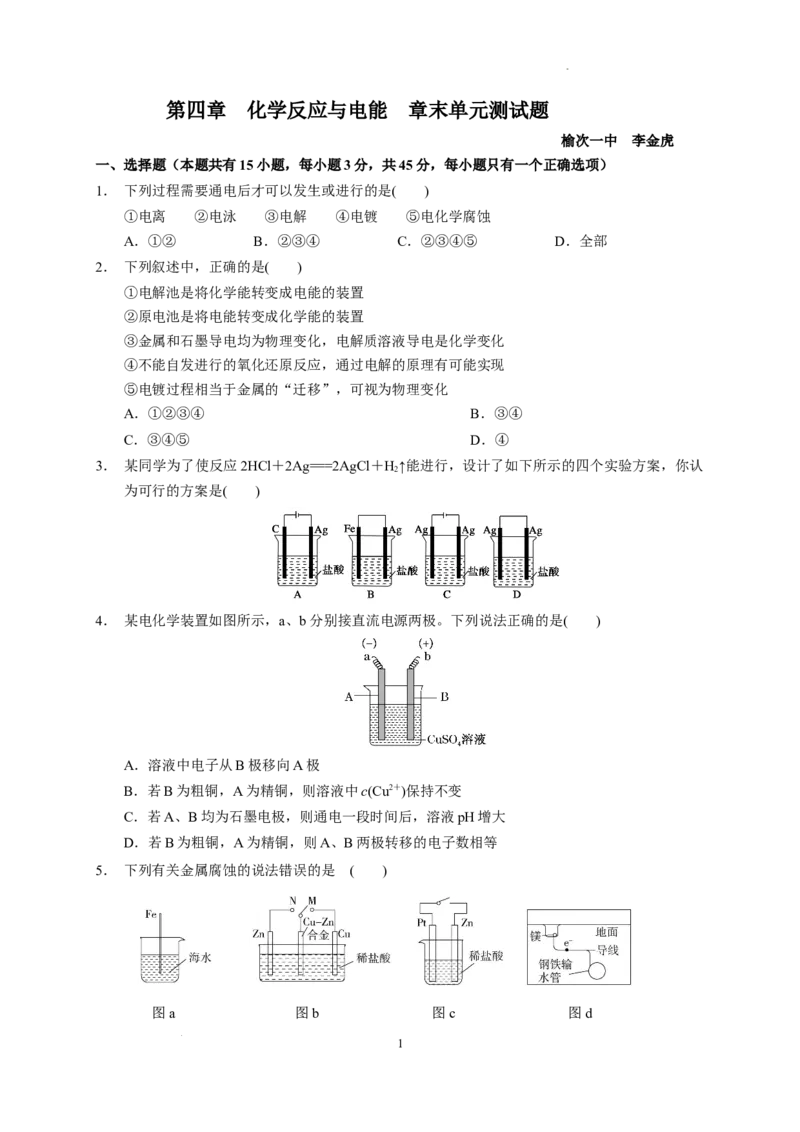
3. 某同学为了使反应2HCl+2Ag===2AgCl+H↑能进行,设计了如下所示的四个实验方案,你认
2
为可行的方案是( )
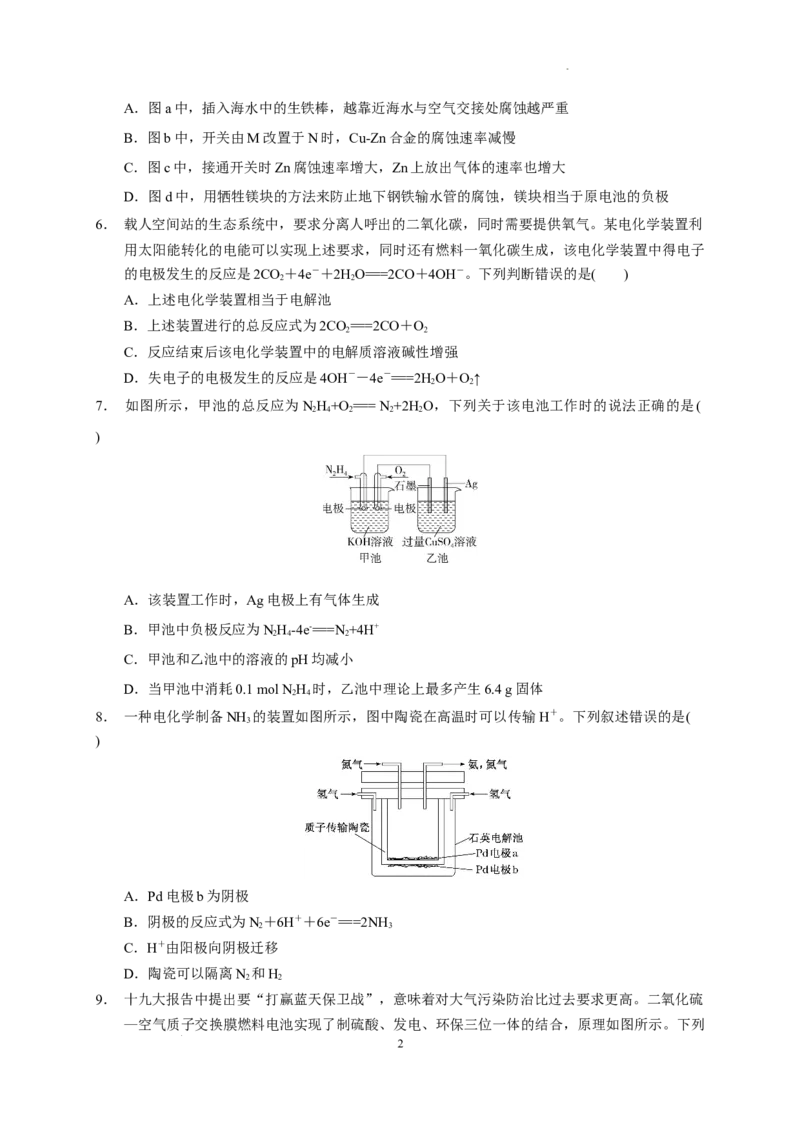
4. 某电化学装置如图所示,a、b分别接直流电源两极。下列说法正确的是( )
A.溶液中电子从B极移向A极
B.若B为粗铜,A为精铜,则溶液中c(Cu2+)保持不变
C.若A、B均为石墨电极,则通电一段时间后,溶液pH增大
D.若B为粗铜,A为精铜,则A、B两极转移的电子数相等
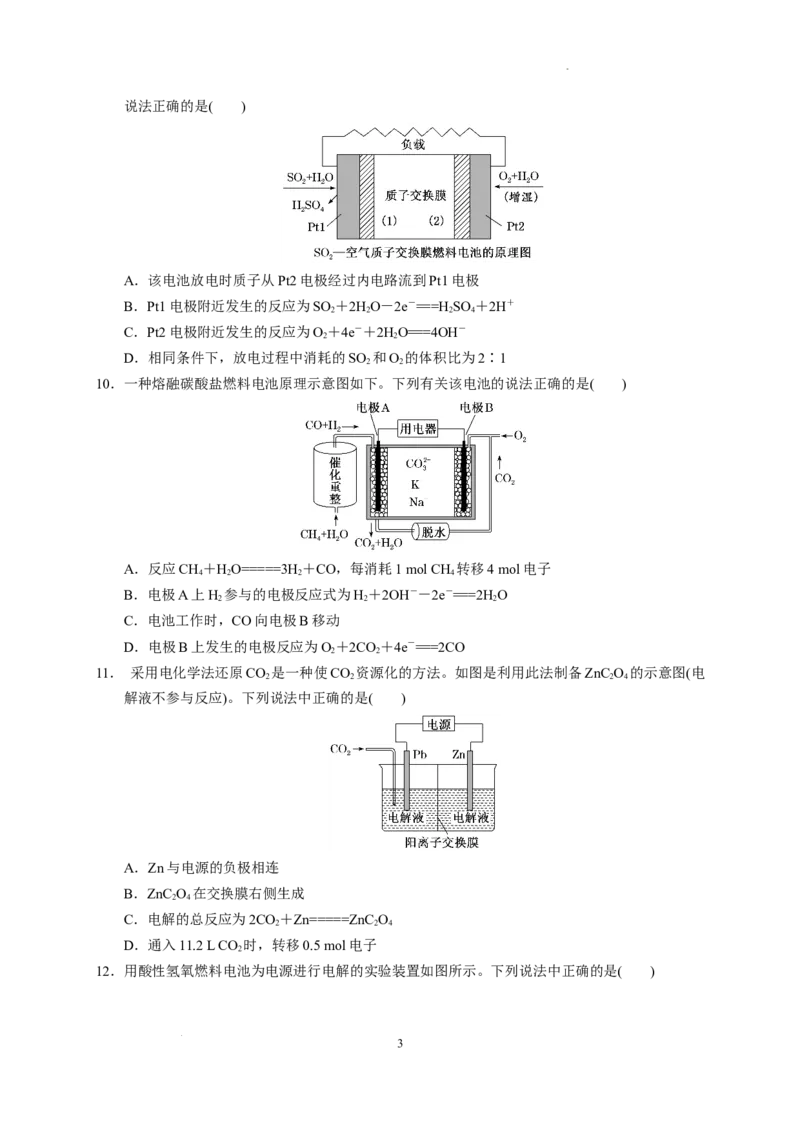
5. 下列有关金属腐蚀的说法错误的是 ( )
图a 图b 图c 图d
1
学科网(北京)股份有限公司A.图a中,插入海水中的生铁棒,越靠近海水与空气交接处腐蚀越严重
B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减慢
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,用牺牲镁块的方法来防止地下钢铁输水管的腐蚀,镁块相当于原电池的负极
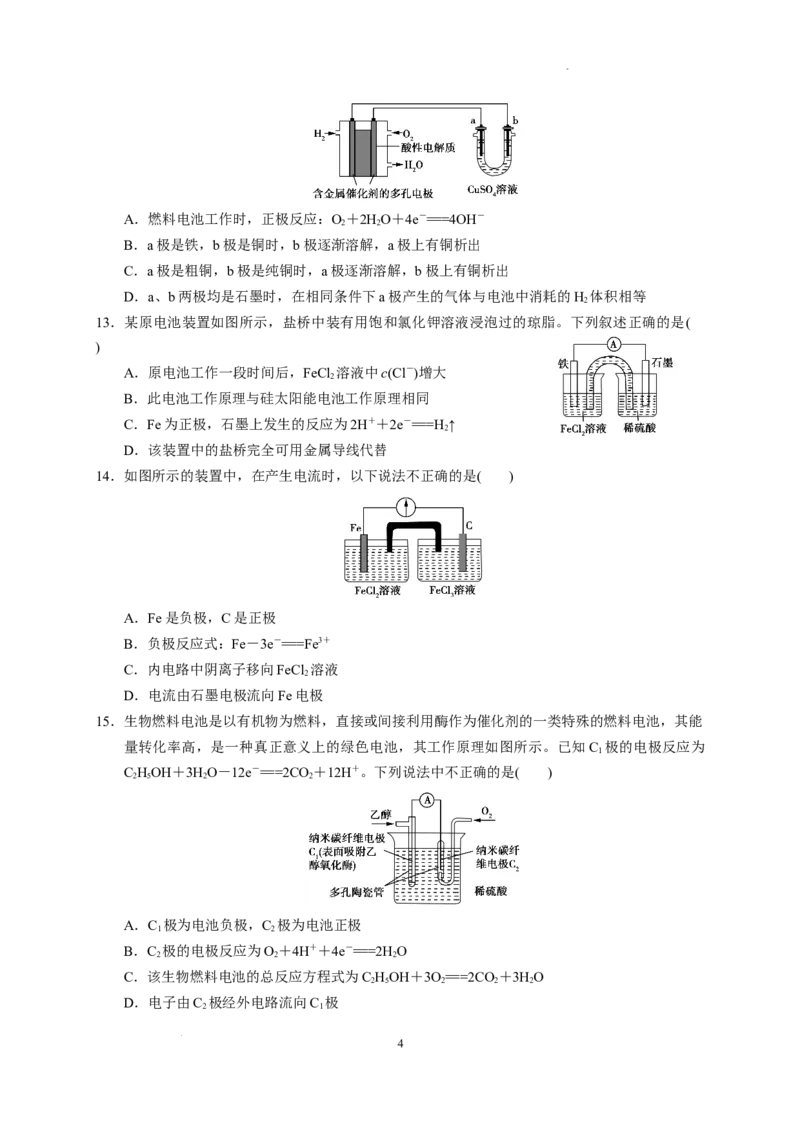
6. 载人空间站的生态系统中,要求分离人呼出的二氧化碳,同时需要提供氧气。某电化学装置利
用太阳能转化的电能可以实现上述要求,同时还有燃料一氧化碳生成,该电化学装置中得电子
的电极发生的反应是2CO+4e-+2HO===2CO+4OH-。下列判断错误的是( )
2 2
A.上述电化学装置相当于电解池
B.上述装置进行的总反应式为2CO===2CO+O
2 2
C.反应结束后该电化学装置中的电解质溶液碱性增强
D.失电子的电极发生的反应是4OH--4e-===2H O+O↑
2 2
7. 如图所示,甲池的总反应为NH+O === N +2H O,下列关于该电池工作时的说法正确的是(
2 4 2 2 2
)
A.该装置工作时,Ag电极上有气体生成
B.甲池中负极反应为NH-4e-===N +4H+
2 4 2
C.甲池和乙池中的溶液的pH均减小
D.当甲池中消耗0.1 mol NH 时,乙池中理论上最多产生6.4 g固体
2 4
8. 一种电化学制备NH 的装置如图所示,图中陶瓷在高温时可以传输H+。下列叙述错误的是(
3
)
A.Pd电极b为阴极
B.阴极的反应式为N+6H++6e-===2NH
2 3
C.H+由阳极向阴极迁移
D.陶瓷可以隔离N 和H
2 2
9. 十九大报告中提出要“打赢蓝天保卫战”,意味着对大气污染防治比过去要求更高。二氧化硫
—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所示。下列
2
学科网(北京)股份有限公司说法正确的是( )
A.该电池放电时质子从Pt2电极经过内电路流到Pt1电极
B.Pt1电极附近发生的反应为SO +2HO-2e-===H SO +2H+
2 2 2 4
C.Pt2电极附近发生的反应为O+4e-+2HO===4OH-
2 2
D.相同条件下,放电过程中消耗的SO 和O 的体积比为2∶1
2 2
10.一种熔融碳酸盐燃料电池原理示意图如下。下列有关该电池的说法正确的是( )
A.反应CH+HO=====3H+CO,每消耗1 mol CH 转移4 mol电子
4 2 2 4
B.电极A上H 参与的电极反应式为H+2OH--2e-===2H O
2 2 2
C.电池工作时,CO向电极B移动
D.电极B上发生的电极反应为O+2CO+4e-===2CO
2 2
11. 采用电化学法还原CO 是一种使CO 资源化的方法。如图是利用此法制备ZnC O 的示意图(电
2 2 2 4
解液不参与反应)。下列说法中正确的是( )
A.Zn与电源的负极相连
B.ZnC O 在交换膜右侧生成
2 4
C.电解的总反应为2CO+Zn=====ZnC O
2 2 4
D.通入11.2 L CO 时,转移0.5 mol电子
2
12.用酸性氢氧燃料电池为电源进行电解的实验装置如图所示。下列说法中正确的是( )
3
学科网(北京)股份有限公司A.燃料电池工作时,正极反应:O+2HO+4e-===4OH-
2 2
B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出
D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H 体积相等
2
13.某原电池装置如图所示,盐桥中装有用饱和氯化钾溶液浸泡过的琼脂。下列叙述正确的是(
)
A.原电池工作一段时间后,FeCl 溶液中c(Cl-)增大
2
B.此电池工作原理与硅太阳能电池工作原理相同
C.Fe为正极,石墨上发生的反应为2H++2e-===H ↑
2
D.该装置中的盐桥完全可用金属导线代替
14.如图所示的装置中,在产生电流时,以下说法不正确的是( )
A.Fe是负极,C是正极
B.负极反应式:Fe-3e-===Fe3+
C.内电路中阴离子移向FeCl 溶液
2
D.电流由石墨电极流向Fe电极
15.生物燃料电池是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能
量转化率高,是一种真正意义上的绿色电池,其工作原理如图所示。已知C 极的电极反应为
1
C HOH+3HO-12e-===2CO +12H+。下列说法中不正确的是( )
2 5 2 2
A.C 极为电池负极,C 极为电池正极
1 2
B.C 极的电极反应为O+4H++4e-===2H O
2 2 2
C.该生物燃料电池的总反应方程式为C HOH+3O===2CO +3HO
2 5 2 2 2
D.电子由C 极经外电路流向C 极
2 1
4
学科网(北京)股份有限公司二、填空题(本题包括5个小题,共55分)
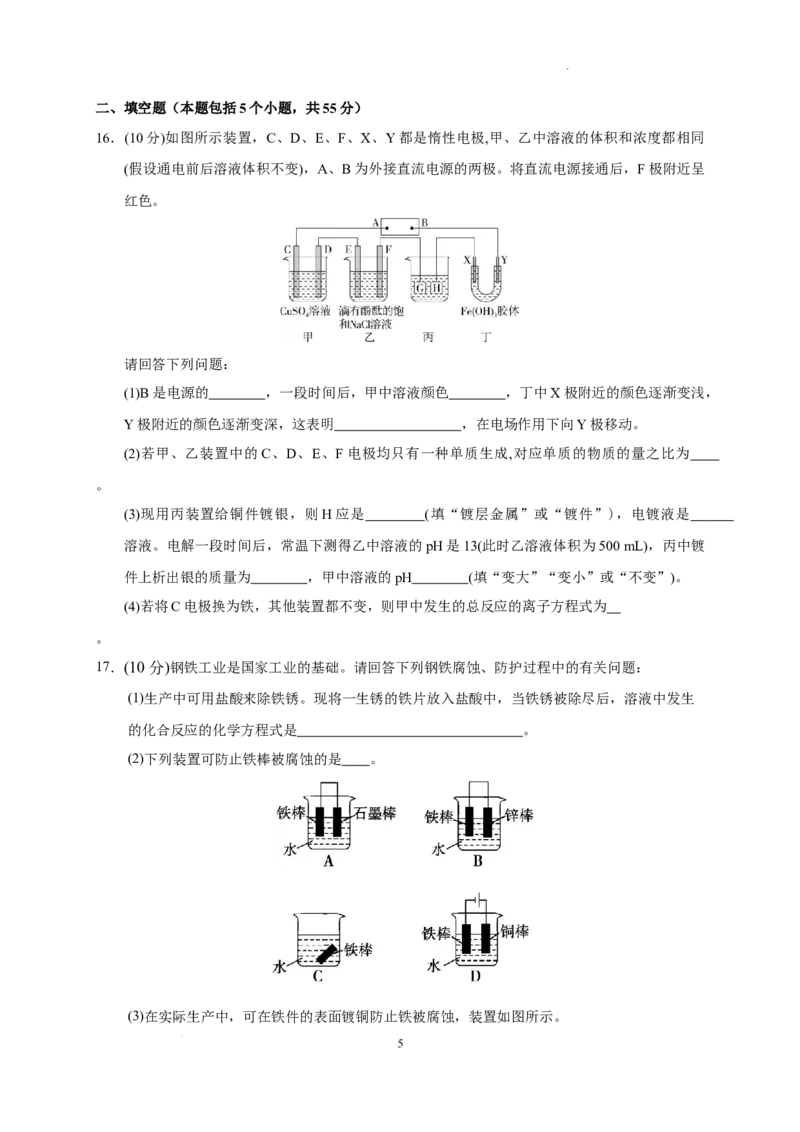
16.(10分)如图所示装置,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同
(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈
红色。
请回答下列问题:
(1)B是电源的 ,一段时间后,甲中溶液颜色 ,丁中X极附近的颜色逐渐变浅,
Y极附近的颜色逐渐变深,这表明 ,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为
。
(3)现用丙装置给铜件镀银,则H应是 (填“镀层金属”或“镀件”),电镀液是
溶液。电解一段时间后,常温下测得乙中溶液的pH是13(此时乙溶液体积为500 mL),丙中镀
件上析出银的质量为 ,甲中溶液的pH (填“变大”“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为
。
17.(10分)钢铁工业是国家工业的基础。请回答下列钢铁腐蚀、防护过程中的有关问题:
(1)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生
的化合反应的化学方程式是 。
(2)下列装置可防止铁棒被腐蚀的是 。
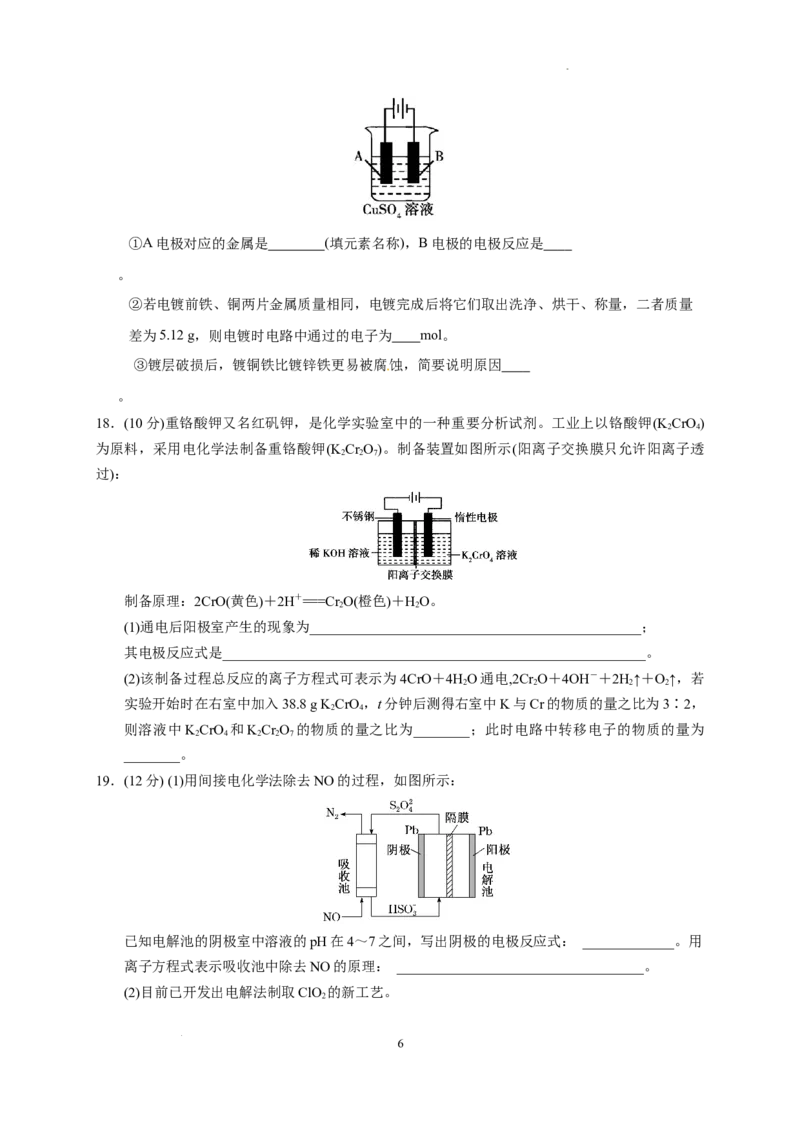
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀,装置如图所示。
5
学科网(北京)股份有限公司①A电极对应的金属是 (填元素名称),B电极的电极反应是
。
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量
差为5.12 g,则电镀时电路中通过的电子为 mol。
③镀层破损后,镀铜铁比镀锌铁更易被腐蚀,简要说明原因
。
18.(10分)重铬酸钾又名红矾钾,是化学实验室中的一种重要分析试剂。工业上以铬酸钾(K CrO)
2 4
为原料,采用电化学法制备重铬酸钾(K Cr O)。制备装置如图所示(阳离子交换膜只允许阳离子透
2 2 7
过):
制备原理:2CrO(黄色)+2H+===Cr O(橙色)+HO。
2 2
(1)通电后阳极室产生的现象为_______________________________________________;
其电极反应式是____________________________________________________________。
(2)该制备过程总反应的离子方程式可表示为4CrO+4HO通电,2Cr O+4OH-+2H↑+O↑,若
2 2 2 2
实验开始时在右室中加入38.8 g K CrO,t分钟后测得右室中K与Cr的物质的量之比为3∶2,
2 4
则溶液中KCrO 和KCr O 的物质的量之比为________;此时电路中转移电子的物质的量为
2 4 2 2 7
________。
19.(12分) (1)用间接电化学法除去NO的过程,如图所示:
已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式: _____________。用
离子方程式表示吸收池中除去NO的原理: ___________________________________。
(2)目前已开发出电解法制取ClO 的新工艺。
2
6
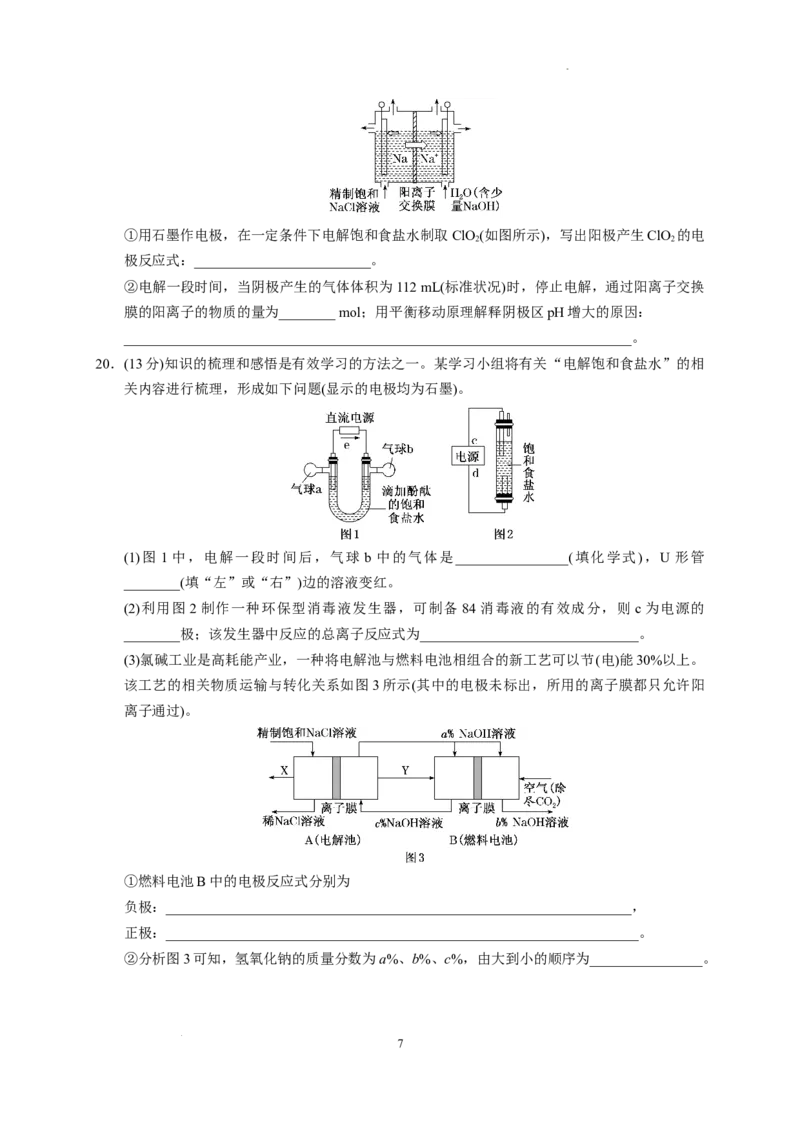
学科网(北京)股份有限公司①用石墨作电极,在一定条件下电解饱和食盐水制取ClO (如图所示),写出阳极产生ClO 的电
2 2
极反应式:_________________________。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解,通过阳离子交换
膜的阳离子的物质的量为________ mol;用平衡移动原理解释阴极区pH增大的原因:
________________________________________________________________________。
20.(13分)知识的梳理和感悟是有效学习的方法之一。某学习小组将有关“电解饱和食盐水”的相
关内容进行梳理,形成如下问题(显示的电极均为石墨)。
(1)图 1 中,电解一段时间后,气球 b 中的气体是________________(填化学式),U 形管
________(填“左”或“右”)边的溶液变红。
(2)利用图2制作一种环保型消毒液发生器,可制备 84消毒液的有效成分,则 c为电源的
________极;该发生器中反应的总离子反应式为_______________________________。
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。
该工艺的相关物质运输与转化关系如图3所示(其中的电极未标出,所用的离子膜都只允许阳
离子通过)。
①燃料电池B中的电极反应式分别为
负极:__________________________________________________________________,
正极:___________________________________________________________________。
②分析图3可知,氢氧化钠的质量分数为a%、b%、c%,由大到小的顺序为________________。
7
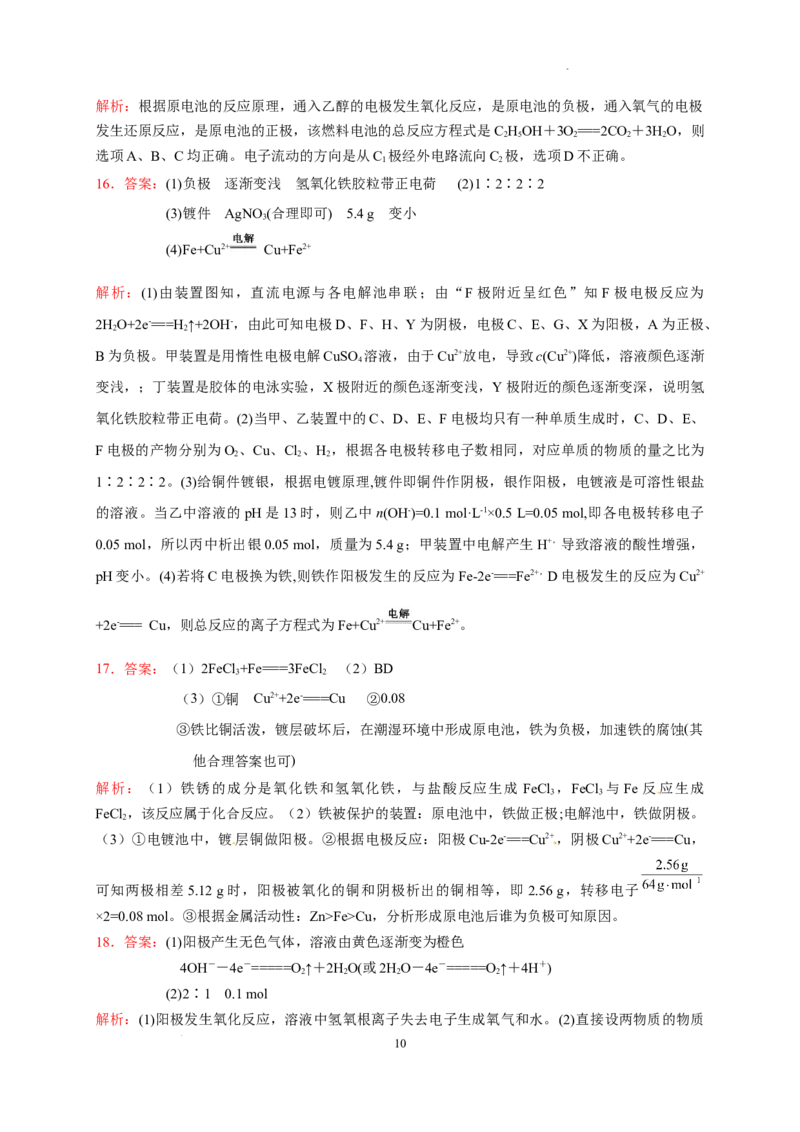
学科网(北京)股份有限公司1.答案:B
解析:电解质溶于水即可发生电离,不需要通电;电化学腐蚀的实质是发生原电池反应,是化学能
转变为电能的自发反应,也不需要通电。
2.答案:B
解析:①、②正好相反了,③、④正确,⑤中电镀是特殊形式的电解,仍然是化学变化。
3.答案:C
解析:只有电解装置,银做阳极,盐酸做电解质溶液可以实现。
4.答案:D
解析:电解质溶液通过离子移动导电,电解质溶液中没有电子移动,故A错误;若B为粗铜,A为
精铜,电解质溶液是硫酸铜溶液,该装置为电解精炼铜装置,溶液中c(Cu2+)略减小,故B错误;
若A、B均为石墨电极,电解总反应式为2CuSO +2HO=====2Cu+O↑+2HSO ,则通电一段时
4 2 2 2 4
间后,溶液pH减小,故C错误;根据电子守恒,阴极、阳极转移电子数一定相等,若B为粗铜,
A为精铜,则A、B两极转移的电子数相等,故D正确。
5.答案:C
解析:图a中,生铁棒中含有铁和碳,铁、碳和海水构成原电池,在海水与空气交接处氧气的浓度
较大,铁最容易被腐蚀,A正确;图b中,开关由M改置于N时,合金作正极,锌作负极,所以
合金的腐蚀速率减慢,B正确;图c中,接通开关时,Zn作负极,腐蚀速率增大,但氢离子在铂丝
上放电生成氢气,C错误;图d中,Fe、Mg构成原电池时,Mg的活泼性比Fe强,Mg作负极,可用
牺牲镁块的方法来防止地下钢铁输水管的腐蚀,D正确。
6.答案:C
解析:该电化学装置是利用电能转化为化学能,符合电解池原理,所以上述电化学装置相当于电解
池,故A正确;该电池中,阴极电极反应式为2CO +4e-+2HO===2CO+4OH-,阳极上氢氧根
2 2
离子失电子生成氧气,得失电子相同条件下将两个电极反应式相加即得电池总反应式为
2CO===2CO+O ,故 B 正确;阴极反应生成的 OH-在阳极完全反应,电池总反应式为
2 2
2CO===2CO+O ,所以反应结束后该电化学装置中的电解质溶液碱性不变,故C错误;阳极上氢
2 2
氧根离子失电子生成氧气供给呼吸,电极反应式为4OH--4e-===2H O+O↑,故D正确。
2 2
7.答案:C
解析:甲池为原电池,乙池为电解池。通入NH 的电极为负极,银电极为阴极,银电极上铜离子
2 4
得电子生成铜单质,A错误;甲池中负极反应为NH-4e-+4OH-===N +4H O,B错误;甲池中有水
2 4 2 2
生成,导致溶液中KOH浓度降低,则溶液pH减小,乙池中水电离出的氢氧根离子放电,导致溶液
pH减小,C正确;N H-4e-+4OH-===N +4H O,甲池消耗0.1 mol N H 时,转移0.4 mol电子,Cu2+
2 4 2 2 2 4
+2e- ===Cu,因此可产生0.2 mol铜,即12.8 g固体,D错误。
8
学科网(北京)股份有限公司8.答案:A
解析:此装置为电解池,总反应是N +3H2NH ,Pd电极b上发生的反应是氢气失去电子,氢
2 2 3
元素的化合价升高,Pd电极b为阳极,故A说法错误;根据A选项分析,Pd电极a为阴极,反应
式为N +6H++6e-===2NH ,故B说法正确;H+在阴极上与N 反应,则H+由阳极移向阴极,故
2 3 2
C说法正确;根据装置图,陶瓷可以隔离N 和H,故D说法正确。
2 2
9.答案:D
解析:放电时为原电池,质子向正极移动,Pt1电极为负极,则该电池放电时质子从 Pt1电极移向
Pt2电极,A错误;Pt1电极为负极,发生氧化反应,SO 被氧化为硫酸,电极反应式为SO +2HO
2 2 2
-2e-===SO+4H+,硫酸应当拆写成离子形式,B错误;酸性条件下,氧气得电子生成水, C错
误;相同条件下,放电过程中:负极发生氧化反应:2SO +4HO-4e-===2SO+8H+,正极发生还
2 2
原反应:O +4e-+4H+===2H O,根据转移电子数相等可知,放电过程中消耗的 SO 和O 的体积
2 2 2 2
比为2∶1,D正确。
10.答案:D
解析:A选项,CH 中C元素的化合价为-4价,CO中C元素的化合价为+2价,每个碳原子失去
4
6个电子,因此每消耗 1 mol CH 转移6 mol电子,错误;B选项,熔融盐中没有OH-,因此OH-
4
不能参与电极反应,错误;C选项,CO应向负极移动,即向电极A移动,错误;D选项,电极B
上O 得电子和CO 结合生成CO,正确。
2 2
11.答案:C
解析:电解过程中Zn被氧化,作阳极,所以Zn与电源的正极相连,A错误;Zn2+透过阳离子交换
膜到达左侧与生成的C O形成ZnC O ,B错误;没有给出气体所处的温度和压强,无法计算转移
2 2 4
电子的物质的量,D错误。
解析:由题意知,以盐酸作电解质溶液,Ag作阳极,设计成电解池可实现该反应。
12.答案:C
解析:酸性燃料电池工作时,正极反应:O +4H++4e-===2H O,A错误;a极是铁,b极是铜时,
2 2
a极上铁发生氧化反应逐渐溶解,b极上Cu2+发生还原反应有铜析出,B错误;a极是粗铜,b极是
纯铜时,a极上发生氧化反应,粗铜溶解,b极上Cu2+发生还原反应,有铜析出,C正确;a、b两
极均是石墨时,根据电子守恒,a极上产生的O 与电池中消耗的H 的体积比为1∶2,D错误。
2 2
13.答案:A
解析:原电池中离子的移动方向由静电作用决定,铁失去电子形成Fe2+进入FeCl 溶液中,使其带
2
正电,吸引盐桥中的Cl-,故c(Cl-)增大,A项正确;太阳能电池是太阳能转化为电能的装置,原
电池是化学能转化为电能的装置,B项错误;铁作负极,石墨作正极;C项错误;金属导线不能传
递离子,所以盐桥不能用导线代替,D项错误。
14.答案:B
解析:负极反应式为Fe-2e-===Fe2+,B不正确;阴离子移向负极(左池),C项正确;电流由正极
流向负极,D项正确。
15.答案:D
9
学科网(北京)股份有限公司解析:根据原电池的反应原理,通入乙醇的电极发生氧化反应,是原电池的负极,通入氧气的电极
发生还原反应,是原电池的正极,该燃料电池的总反应方程式是C HOH+3O===2CO +3HO,则
2 5 2 2 2
选项A、B、C均正确。电子流动的方向是从C 极经外电路流向C 极,选项D不正确。
1 2
16.答案:(1)负极 逐渐变浅 氢氧化铁胶粒带正电荷 (2)1∶2∶2∶2
(3)镀件 AgNO(合理即可) 5.4 g 变小
3
(4)Fe+Cu2+ Cu+Fe2+
解析:(1)由装置图知,直流电源与各电解池串联;由“F极附近呈红色”知F极电极反应为
2HO+2e-===H↑+2OH-,由此可知电极D、F、H、Y为阴极,电极C、E、G、X为阳极,A为正极、
2 2
B为负极。甲装置是用惰性电极电解CuSO 溶液,由于Cu2+放电,导致c(Cu2+)降低,溶液颜色逐渐
4
变浅,;丁装置是胶体的电泳实验,X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,说明氢
氧化铁胶粒带正电荷。(2)当甲、乙装置中的C、D、E、F电极均只有一种单质生成时,C、D、E、
F电极的产物分别为O 、Cu、Cl 、H ,根据各电极转移电子数相同,对应单质的物质的量之比为
2 2 2
1∶2∶2∶2。(3)给铜件镀银,根据电镀原理,镀件即铜件作阴极,银作阳极,电镀液是可溶性银盐
的溶液。当乙中溶液的 pH是13时,则乙中n(OH-)=0.1 mol·L-1×0.5 L=0.05 mol,即各电极转移电子
0.05 mol,所以丙中析出银0.05 mol,质量为5.4 g;甲装置中电解产生H+,导致溶液的酸性增强,
pH变小。(4)若将C电极换为铁,则铁作阳极发生的反应为Fe-2e-===Fe2+,D电极发生的反应为Cu2+
+2e-=== Cu,则总反应的离子方程式为Fe+Cu2+ Cu+Fe2+。
17.答案:(1)2FeCl +Fe===3FeCl (2)BD
3 2
(3)①铜 Cu2++2e-===Cu ②0.08
③铁比铜活泼,镀层破坏后,在潮湿环境中形成原电池,铁为负极,加速铁的腐蚀(其
他合理答案也可)
解析:(1)铁锈的成分是氧化铁和氢氧化铁,与盐酸反应生成 FeCl ,FeCl 与 Fe 反应生成
3 3
FeCl ,该反应属于化合反应。(2)铁被保护的装置:原电池中,铁做正极;电解池中,铁做阴极。
2
(3)①电镀池中,镀层铜做阳极。②根据电极反应:阳极Cu-2e-===Cu2+,阴极Cu2++2e-===Cu,
可知两极相差5.12 g时,阳极被氧化的铜和阴极析出的铜相等,即 2.56 g,转移电子
×2=0.08 mol。③根据金属活动性:Zn>Fe>Cu,分析形成原电池后谁为负极可知原因。
18.答案:(1)阳极产生无色气体,溶液由黄色逐渐变为橙色
4OH--4e-=====O↑+2HO(或2HO-4e-=====O↑+4H+)
2 2 2 2
(2)2∶1 0.1 mol
解析:(1)阳极发生氧化反应,溶液中氢氧根离子失去电子生成氧气和水。(2)直接设两物质的物质
10
学科网(北京)股份有限公司的量分别为x、y,则钾原子的物质的量为2x+2y,铬原子物质的量为x+2y,依据两原子个数比为
3∶2,可求出两物质的物质的量之比为2∶1;根据铬酸钾的质量可求出铬原子总物质的量为 0.2
mol,又t min后两物质的物质的量之比为2∶1,则铬酸钾为0.1 mol,重铬酸钾为0.05 mol,根据
化学方程式可知,生成0.05 mol的重铬酸钾的反应中转移电子为0.05×2 mol。
19.答案:(1)2HSO+2e-+2H+===S O+2HO 2NO+2SO+2HO===N +4HSO
2 2 2 2 2
(2)①Cl--5e-+2HO===ClO ↑+4H+
2 2
②0.01 在阴极发生反应:2H++2e-===H ↑,H+浓度减小,使得HOOH-+H+
2 2
的平衡向右移动,OH-浓度增大,阴极区溶液pH增大
解析:(1)阴极发生还原反应,是亚硫酸氢根离子得电子生成SO,电极反应式为2HSO+2e-+2H+
2
===S O+2HO; S O与一氧化氮发生氧化还原反应,生成氮气和亚硫酸氢根离子,离子反应方程式
2 2 2
为2NO+2SO+2HO===N +4HSO。(2)①由题意可知,氯离子放电生成ClO ,由元素守恒可知,
2 2 2 2
有水参加反应,同时生成氢离子,电极反应式为 Cl--5e-+2HO===ClO ↑+4H+。②在阴极发生
2 2
2H++2e-===H ↑,当阴极产生的气体体积为112 mL(标准状况)时,即产生氢气的物质的量为0.005
2
mol,外电路中转移的电子数为0.01 mol,因通过阳离子交换膜的阳离子为+1价离子,则通过阳离
子交换膜的阳离子的物质的量为 0.005 mol×2=0.01 mol,电解时阴极 H+浓度减小,使得
HOOH-+H+的平衡向右移动,OH-浓度增大,溶液的pH增大。
2
20.答案:(1)H 右 (2)负 Cl-+HO=====ClO-+H↑
2 2 2
(3)①2H-4e-+4OH-===4H O O+4e-+2HO===4OH- ②b%>a%>c%
2 2 2 2
解析:(1)图1中,根据电子流向知,左边电极是电解池阳极,右边电极是电解池阴极,阳极上氯离
子放电生成氯气,阴极上氢离子放电生成氢气,所以气球a中的气体是氯气,气球b中的气体是氢
气,同时阴极附近有NaOH生成,溶液呈碱性,无色酚酞遇碱变红色,所以U形管右边溶液变红色。
(2)利用图2制作一种环保型消毒液发生器,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢
气,同时阴极有NaOH生成,氯气和氢氧化钠反应生成NaClO,次氯酸钠具有漂白性,为了使反应
更充分,则下边电极生成氯气,上边电极附近有NaOH生成,上边电极生成氢气,为阴极,则c为
负极,d为正极,总反应式为Cl-+HO=====ClO-+H↑。(3)①B是燃料电池,右边电池中通入空
2 2
气,左边原电池中通入气体Y,则Y是氢气,则电解池中左边电极是阳极,右边电极是阴极,阳极
上氯离子放电,阴极上氢离子放电;燃料电池中通入空气的电极是正极,通入氢气的电极是负极,
正极上氧气得电子和水反应生成氢氧根离子,负极上氢气失电子和氢氧根离子反应生成水,负极、
正极反应式分别为 2H -4e-+4OH-===4H O、O +4e-+2HO===4OH-。②图3电解池中加入
2 2 2 2
NaOH的目的是增大溶液导电性,通入电解池后生成氢氧化钠,所以加入的NaOH浓度小于出来的
NaOH浓度,即a%>c%;原电池中,正极上生成氢氧化钠,且其浓度大于加入的氢氧化钠,即b%
>a%,所以氢氧化钠的质量分数大小顺序是b%>a%>c%。
11
学科网(北京)股份有限公司12
学科网(北京)股份有限公司