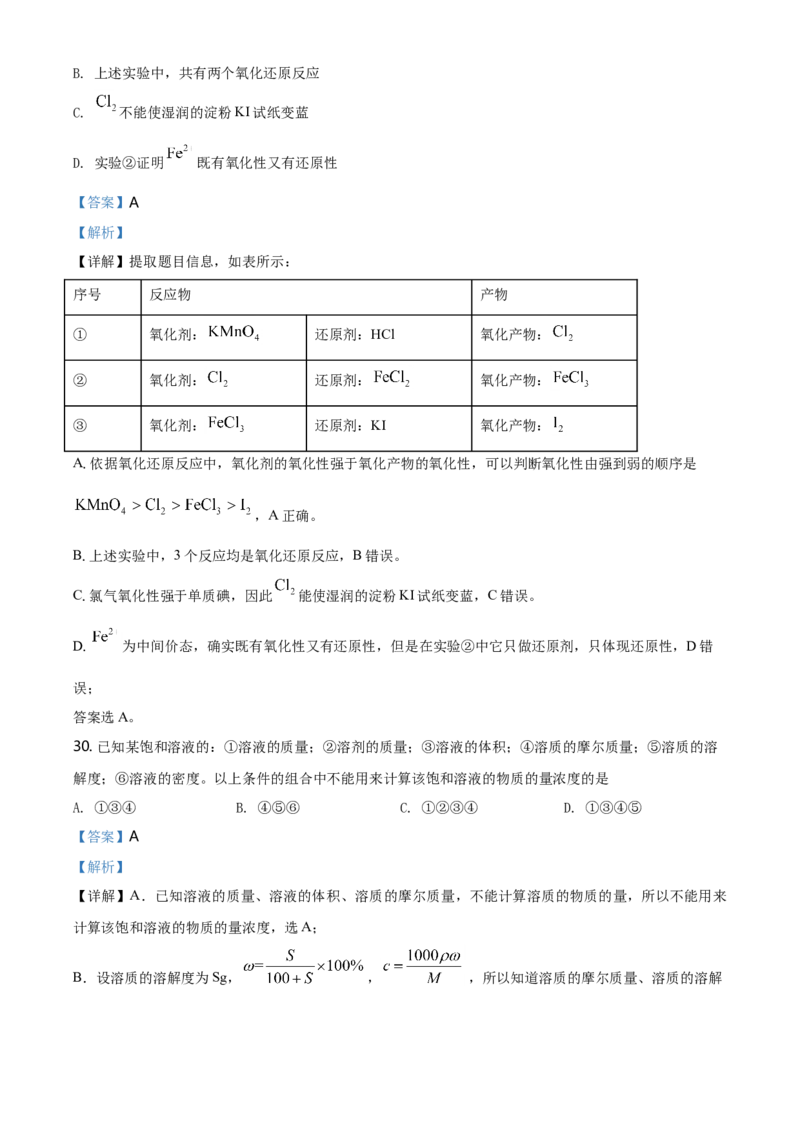文档内容
清华附中高一第一学期期中试卷
化学
可能用到的相对原子质量:H1 C12 N14 O16 Na23 Mg24 S32 Cl35.5 Mn55
一、选择题
1. 下列常用食品添加剂不属于电解质的是
A. NaCl B. C H OH C. CH COOH D. NaHCO
2 5 3 3
【答案】B
【解析】
【分析】
试题分析:在水溶液或熔化状态下能够导电的化合物,叫做电解质,包括酸、碱、盐、水和活泼金属氧化
物等。
【详解】A.NaCl为盐类,属于电解质,错误;
B.C H OH为非电解质,正确;
2 5
C.CH COOH为酸,属于电解质,错误;
3
D、NaHCO 为盐类,属于电解质,错误;
3
故选择B。
2. 下列分散系中,容易产生丁达尔效应的是
A. 黄山云雾 B. 氢氧化铁沉淀 C. 食盐水 D. 硫酸铜溶液
【答案】A
【解析】
【详解】A. 黄山云雾属于胶体分散系,当光束通过时,可能产生丁达尔效应,故A正确;
B. 氢氧化铁沉淀属于浊液分散系,当光束通过时,不可能产生丁达尔效应,故B错误;
C. 食盐水属于溶液分散系,当光束通过时,不可能产生丁达尔效应,故C错误;
D. 硫酸铜溶液属于溶液分散系,当光束通过时,不可能产生丁达尔效应,故D错误;
故选:A。
3. 下列事例不属于氧化还原反应的是
A. 金属冶炼 B. 石灰水粉刷墙壁 C. 食物腐败 D. 燃放鞭炮
【答案】B
【解析】
【详解】A.金属冶炼是把金属从化合态变为游离态的过程,有元素化合价变化,属于氧化还原反应,故
不选A;B.石灰水粉刷墙壁发生反应 ,没有元素化合价变化,不属于氧化还原
反应,故选B;
C.食物腐败是食物被氧气氧化的过程,属于氧化还原反应,故不选C;
D.燃放鞭炮时,黑火药发生爆炸,反应方程式是2KNO+ S + 3C K S + N ↑+ 3CO ↑,有元素化合价
3 2 2 2
变化,属于氧化还原反应,故不选D;
选B。
4. 下列电离方程式中,正确的是
A. NaSO =2Na + B. Ba(OH) =Ba2++
2 4 + 2
C. Al (SO )=2Al3++3 D. Ca(NO )=Ca2++2
2 4 3 3 2
【答案】C
【解析】
【详解】A.硫酸钠属于盐,在溶液中完全电离出钠离子和硫酸根离子,电离方程式为 NaSO =2Na++
2 4
,故A错误;
B.氢氧化钡是强碱,在溶液中完全电离出钡离子和氢氧根离子,电离方程式为Ba(OH) =Ba2++2OH—,故B
2
错误;
C.硫酸铝属于盐,在溶液中完全电离出铝离子和硫酸根离子,电离方程式为Al (SO )=2Al3++3 ,故C
2 4 3
正确;
D.硝酸钙属于盐,在溶液中完全电离出钙离子和硝酸根离子,电离方程式为Ca(NO )=Ca2++2NO ,故D
3 2
错误;
故选C。
5. 下列反应中,不属于离子反应的是
A. NaCO+CaCl =CaCO +2NaCl B. H+Cl 2HCl
2 3 2 3 2 2
C. Fe+CuSO=FeSO+Cu D. CaCO +2HCl=CaCl +H O+CO↑
4 4 3 2 2 2
【答案】B
【解析】【详解】有离子参与的反应为离子反应,H+Cl 2HCl为气体间的反应,无离子参加也没有离子生成,
2 2
故不属于离子反应;
答案选B。
6. 下列微粒中,只有氧化性的是
①Fe2+ ②SO ③H+ ④Cl- ⑤Na+ ⑥Al
2
A. ③ B. ③⑤ C. ①② D. ④⑥
【答案】B
【解析】
【详解】①Fe2+的化合价为+2价,既可以升高为+3价,又可以降低为0价,既有氧化性,又有还原性,①
与题意不符;
②SO 中的S的化合价为+4价,既可以升高为+6价,又可以降低为0价,既有氧化性,又有还原性,②与
2
题意不符;
③H+的化合价为+1价,只能降低,只有氧化性,③符合题意;
④Cl-的化合价为-1价,只能升高,只有还原性,④与题意不符;
⑤Na+的化合价为+1价,只能降低,只有氧化性,⑤符合题意;
⑥Al的化合价为0价,只能升高,只有还原性,⑥与题意不符;
综上所述,③⑤符合题意,答案 为B。
7. 在1 mol Na SO 中含有Na+的数目是
2 4
A. 6.02×1023 B. 1.204×1024 C. 1 D. 2
【答案】B
【解析】
【详解】1 mol Na SO 中,Na+的物质的量为1mol×2=2mol,由N=nN 可知,Na+个数为2×6.02×1023个,故
2 4 A
选B。
8. 下列离子可以在溶液中大量共存的是
A. Ba2+、Cl-、 、 B. Ca2+、Cl-、 、
C. H+、Cl-、 、 D. Ag+、 、Cl-、Fe3+
【答案】C
【解析】
【详解】A. Ba2+与 反应生成硫酸钡沉淀,不能共存,A错误;B. Ca2+与 反应生成碳酸钙沉淀,不能共存,B错误;
C. H+、Cl-、 、 四种离子不发生反应,能共存,C正确;
D. Ag+与Cl-反应生成氯化银沉淀,不能共存,D错误;
答案选C。
9. 加入NaOH溶液后,溶液中离子数目不会减少的是
A. B. Cu2+ C. D. Fe3+
【答案】C
【解析】
【详解】A.加入氢氧化钠后,碳酸氢根离子与氢氧根离子反应生成碳酸根离子,数目减少,A错误;
B.加入氢氧化钠后,铜离子与氢氧根离子反应生成氢氧化铜沉淀,数目减少,B错误;
C.加入氢氧化钠后,硫酸根离子不反应,数目不减少,C正确;
D.加入氢氧化钠后,铁离子与氢氧根离子反应生成氢氧化铁沉淀,数目减少,D错误;
答案选C。
10. 在下图表示的一些物质或概念间的从属关系中正确的是
X Y Z
A 酸 含氧酸 纯净物
B 电解质 盐 化合物
C 胶体 分散系 物质
D 碱性氧化物 氧化物 化合物
A. A B. B C. C D. D
【答案】CD
【解析】
【详解】A.含氧酸属于酸,酸属于纯净物,A错误;
B.电解质不一定是盐如NaOH等,B错误;
C.胶体属于分散系,分散系属于混合物,混合物属于物质,C正确;D.碱性氧化物属于氧化物,氧化物属于化合物,D正确;
答案选CD。
11. 下列反应中必须加入还原剂才能进行的是
A. Na →Na O B. Cl→HCl C. CaO→Ca(OH) D. Fe O→Fe
2 2 2 2 2 3
【答案】D
【解析】
【详解】A.Na →Na O 中,Na元素化合价升高,需加氧化剂发生反应,A错误;
2 2
B.Cl→HCl中,虽然Cl元素的化合价降低,但可与水反应发生自身氧化还原反应,B错误;
2
C.CaO→Ca(OH) 中,元素的化合价不变,不发生氧化还原反应,C错误;
2
D.Fe O→Fe中,Fe元素的化合价降低,需加还原剂发生反应,D正确;
2 3
答案选D。
12. 已知NaO属于碱性氧化物,推测它不可能发生的反应是
2
A. 与二氧化碳反应生成碳酸钠 B. 与水反应生成氢氧化钠
C. 与硫酸反应生成硫酸钠 D. 与酸性氧化物SO 反应生成硫酸钠
2
【答案】D
【解析】
【详解】A.碱性氧化物能与酸性氧化物反应生成盐,则氧化钠与二氧化碳反应生成碳酸钠,A与题意不
符;
B.碱性氧化物能与水反应生成碱,则氧化钠与水反应生成氢氧化钠,B与题意不符;
C.碱性氧化物能与酸反应生成盐和水,则氧化钠与硫酸反应生成硫酸钠和水,C与题意不符;
D.氧化钠无强氧化性,则氧化钠与酸性氧化物SO 反应生成亚硫酸钠,而不能生成硫酸钠,D说法错误;
2
答案为D。
13. 能够用来一次性鉴别BaCl 、NaCl、NaCO 三种溶液的试剂是( )
2 2 3
A. AgNO 溶液 B. 稀硫酸 C. 稀盐酸 D. 稀硝酸
3
【答案】B
【解析】
【分析】
BaCl 、NaCl、NaCO 三种溶液分别与稀硫酸反应的现象为:白色沉淀、无现象、气体生成,以此来解答。
2 2 3
【详解】A. 均与硝酸银反应生成白色沉淀,现象相同,不能鉴别,A不符合题意;
B. BaCl 、NaCl、NaCO 三种溶液分别与稀硫酸反应的现象为:白色沉淀、无现象、气体生成,现象不同,
2 2 3
可鉴别,B符合题意;
C. 稀盐酸与BaCl 、NaCl不反应,无法鉴别BaCl 、NaCl,C不符合题意;
2 2
D. 稀硝酸与BaCl 、NaCl不反应,无法鉴别BaCl 、NaCl,D不符合题意;故答案为:B。
2 214. 下列说法不正确的是
A. 化合物中除了电解质就是非电解质
B. 硫酸铜溶于水通电后产生Cu2+和
C. 胶粒带同种电荷是胶体稳定最主要 的原因
D. 分散质粒子大小不同是溶液、胶体和浊液的本质区别
【答案】B
【解析】
【详解】A.化合物依据水溶液或者熔融状态下是否能够导电,分为电解质和非电解质,故A不选;
B.电解质溶于水后,在水分子的作用下发生电离,不需要通电,故B选;
C.胶体粒子带同种电荷,相互排斥,比较稳定,是胶体稳定的最主要原因,故C不选;
D.分散系的本质区别是分散质粒子的大小不同,故D不选;
故选:B。
15. 下列物质的性质与用途(或储存方法)都正确且有逻辑关系的是
A. 钠有较强的还原性,可用于钛、锆、铌等金属的冶炼
B. 氯气具有强氧化性,可用干燥的氯气漂白红纸条
C. 过氧化钠为碱性氧化物,可用于呼吸面具中吸收二氧化碳
D. 次氯酸见光易分解,所以氯水应保存在钢瓶中
【答案】A
【解析】
【详解】A.金属钠的还原性强于金属钛等,可以将金属钛、铌、锆等从其熔融态的盐中置换出来,所以
可以用来冶炼金属钛、铌、锆等,故A正确;
B.氯气不具有漂白性,有漂白性的是次氯酸,干燥的氯气不能漂白红纸条,故B错误;
C.过氧化钠与酸反应生成盐、水和氧气,不属于碱性氧化物,故C错误;
D.次氯酸具有不稳定性,见光易分解,所以氯水(含有次氯酸)应保存在棕色试剂瓶中,氯水中有盐酸,
铁与盐酸反应,氯水不能保存在钢瓶中,故D错误;
故选A。
16. 下列各组物质相互反应,生成物不随反应条件或反应物 的用量变化而变化的是
A. Na和O B. NaOH和CO C. C和CO D. NaCO 和HCl
2 2 2 2 3
【答案】C
【解析】
【详解】A.钠和氧气在常温下反应生成氧化钠,加热条件下反应生成过氧化钠,A错误;
B.氢氧化钠和二氧化碳反应时,当氢氧化钠过量时反应生成碳酸钠,当二氧化碳过量时反应生成碳酸氢钠,B错误;
C.碳与二氧化碳反应生成一氧化碳,不随反应条件或反应物的用量变化而变化,C正确;
D.碳酸钠和盐酸反应时,当碳酸钠过量时反应生成碳酸氢钠,当盐酸过量时反应生成氯化钠、水和二氧化
碳,D错误;
答案选C。
17. 下列各组物质中,所含分子数相同的是
A. 10g H 和10g O B. 标况下5.6L N 和11g CO
2 2 2 2
C. 9g H O和1mol O D. 标况下224mL N 和0.1mol N
2 2 2 2
【答案】B
【解析】
【详解】A.10g H 含分子数 ,10g O 含分子数 ,故不选
2 2
A;
B.标况下5.6L N 含分子数 ,11g CO 含分子数 ,故
2 2
选B;
C.9g H O含分子数 、1mol O 含分子数N ,故不选C;
2 2 A
D.标况下224mL N 含分子数 ,0.1mol N 含分子数0.1N ,故不选D;
2 2 A
选B。
18. 用N 表示阿伏伽德罗常数,下列说法正确的是
A
A. 12g金刚石与石墨所含的碳原子数均为N
A
B. 1mol HCl气体溶于水,该盐酸中含N 个氯化氢分子
A
C. 4.48L N 含有的原子数为0.4N
2 A
D. 标准状况下,2.24L稀有气体所含原子数为0.2 N
A
【答案】A
【解析】
【详解】A.12g金刚石与石墨所含的碳原子为 =1mol,碳原子数为N ,故A正确;
AB.盐酸中不存在氯化氢分子,故B错误;
C.未告知温度和压强,无法计算4.48L N 的物质的量,故C错误;
2
D.标准状况下,2.24L稀有气体的物质的量为 =0.1mol,稀有气体为单原子分子,所含原子
数为0.1 N ,故D错误;
A
故选A。
19. 氯气是一种重要的工业原料。工业上利用反应在3Cl+2NH=N +6HCl检查氯气管道是否漏气。下列说
2 3 2
法错误的是
A. 该反应属于氧化还原反应 B. 该反应利用了Cl 的氧化性
2
C. 该反应属于复分解反应 D. 生成1mol N 有6mol电子转移
2
【答案】C
【解析】
【详解】A.该反应中氯气中的Cl原子化合价由0价变为-1价,属于氧化还原反应,A说法正确;
B.该反应中氯气中的Cl原子化合价由0价变为-1价,具有氧化性,则反应利用了Cl 的氧化性,B说法正
2
确;
C.该反应中部分元素的化合价发生变化,属于氧化还原反应,C说法错误;
D.N 中N原子的化合价由-3价变为0价,生成1个氮气转移6个电子,则生成1mol N 有6mol电子转移,
2 2
D说法正确;
答案为C。
20. 将60mL 0.25mol/L NaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为
A. 0.3mol/L B. 0.03mol/L C. 0.05mol/L D. 0.04mol/L
【答案】B
【解析】
【详解】根据溶液稀释时溶质的物质的量不变,c= =0.03mol/L,答案为B。
21. 下列物质所含分子数最多的是
A. 10000亿个水分子 B. 3.6g水
C. 标况下6.72L CO D. 500mL 1mol/L蔗糖溶液
【答案】D
【解析】
【详解】A.10000亿个水分子中水分子个数用科学计数法表示为1012;
B.3.6g水的物质的量为0.2mol,水分子个数为1.204×1023;C.标况下6.72L CO的物质的量为0.3mol,CO分子个数为1.806×1023;
D.500mL 1mol/L蔗糖溶液中水约有500g,水的物质的量约为27.8mol,含蔗糖分子物质的量为0.5mol
;
综上所述,含有分子数目最多的为500mL 1mol/L蔗糖溶液,答案选D。
22. NaCO 和NaHCO 可用作食用碱。下列用来解释事实的方程式中,不合理的是
2 3 3
A. NaCO 与食醋混用产生CO 气体: +2H+=CO +H O
2 3 2 2 2
B. NaCO 可用NaOH溶液吸收CO 制备:2OH-+CO = +H O
2 3 2 2 2
C. NaHCO 可用治疗胃酸过多: +H+=CO +H O
3 2 2
D. NaHCO 可作发酵粉:2NaHCO NaCO+CO +H O
3 3 2 3 2 2
【答案】A
【解析】
【详解】A.NaCO 与食醋混用,产生CO 气体: +2CH COOH═CO ↑+H O+2CHCOO-,故A选;
2 3 2 3 2 2 3
B.二氧化碳为酸性氧化物,二氧化碳与过量氢氧化钠反应生成碳酸钠,离子方程式:2OH-+CO ═CO 2-
2 3
+H O,故B不选;
2
C.NaHCO 可用治疗胃酸过多,碳酸氢钠与强酸反应,离子方程式 +H+=CO +H O,故C不选;
3 2 2
D.碳酸氢钠不稳定,受热分解生成碳酸钠和水、二氧化碳:2NaHCO NaCO+CO ↑+H O,所以可以做
3 2 3 2 2
发酵粉,故D不选;
故选:A。
23. 下列离子方程式可能不正确的是
A. 钠与水反应:2Na+2HO=2Na++2OH-+H ↑
2 2
B. 硫酸与氢氧化钡溶液反应:Ba2++2OH-+ +2H+=2H O+BaSO↓
2 4
C. 酸碱中和反应:OH-+H+=H O
2
D. 盐酸清除铁锈:Fe O+6H+=2Fe3++3H O
2 3 2
【答案】C
【解析】【详解】A.钠与水反应生成氢氧化钠和氢气,氢氧化钠可拆,则离子方程式为 2Na+2HO=2Na++2OH-
2
+H ↑,A正确;
2
B.硫酸与氢氧化钡溶液反应生成硫酸钡沉淀和水,离子方程式为Ba2++2OH-+ +2H+=2H O+BaSO↓,B
2 4
正确;
C.强酸和强碱的中和反应可用离子方程式OH-+H+=H O表示,弱酸或弱碱的中和反应不能用方程式表示,
2
C错误;
D.盐酸清除铁锈实质是氧化铁与氢离子反应,离子方程式为Fe O+6H+=2Fe3++3H O,D正确;
2 3 2
答案选C。
24. 电离概念是英国物理学家法拉第首先提出的,关于电离的说法正确的是
A. 电离是在电流作用下化合物解离成离子
B. 在水溶液中和熔化状态下都能发生电离的化合物称为电解质
C. 氯化氢溶于水能电离产生H+和Cl-,证明了氯化氢是由离子构成的
D. 使氯化钠中的Na+和Cl-能够自由移动的过程就是氯化钠的电离过程
【答案】D
【解析】
【详解】A.电离是在熔融状态或水分子用下化合物解离成离子,电离不需要通电,故A错误;
B.在水溶液中或熔化状态下能发生电离的化合物称为电解质,故B错误;
C.氯化氢溶于水能电离产生H+和Cl-,氯化氢是共价化合物,氯化氢由氯化氢分子构成,故C错误;
D.氯化钠电离是氯化钠在水溶液中或熔融状态下离解成自由移动Na+和Cl-的过程,故D正确;
选D。
25. 某溶液中含有较大量的Cl-、 、 OH-三种阴离子,如果只取一次该溶液就能够分别将三种阴离子
依次检验出来,下列实验操作顺序正确的是
①滴加足量的Mg(NO) 溶液;②过滤;③滴加适量的AgNO 溶液;④滴加足量的Ba(NO ) 溶液
3 2 3 3 2
A. ①②④②③ B. ④②①②③ C. ①②③②④ D. ④②③②①
【答案】B
【解析】
【详解】Ag+能与Cl-、 、 OH-三种结合,Mg2+能与 、 OH-结合,Ba2+只能与 结合,故先
加入Ba(NO ) 溶液溶液,检验出 离子,过滤除去生成的BaCO 沉淀;然后加入Mg(NO) 溶液,检验
3 2 3 3 2
出 OH-,过滤除去生成的 Mg(OH) 沉淀;最后加入 AgNO 溶液,检验出 Cl-,故正确的操作顺序是
2 3④②①②③,故合理选项是B。
26. 检验司机是否酒后驾车利用了下列反应:2KCr O + 2C HOH + 8H SO = 2K SO + 2Cr (SO ) +
2 2 7 2 5 2 4 2 4 2 4 3
3CHCOOH + 11H O( 和Cr3+在溶液中的颜色分别为橙色和绿色),下列说法错误的是
3 2
A. 该反应是氧化还原反应
B. 该反应不是离子反应
C. KCr O 和Cr (SO ) 都是电解质
2 2 7 2 4 3
D. 若司机醉酒驾车,则检测器中物质由橙色变为绿色
【答案】B
【解析】
【详解】A.由反应的化学方程式可知,反应中铬元素化合价降低,碳元素化合价升高,该反应属于氧化还
原反应,故A正确;
B.该反应是在水溶液中进行的反应,有离子参加反应,也有离子生成,属于离子反应,故B错误;
C.KCr O 和Cr (SO ) 都属于盐,在溶液中都能发生电离,都是电解质,故C正确;
2 2 7 2 4 3
D.由反应的化学方程式可知,若司机醉酒驾车,检测器中 被乙醇还原为Cr3+,溶液的颜色橙色变为
绿色,故D正确;
故选B。
27. 病人输液用的葡萄糖注射液是葡萄糖(C H O)的水溶液,其标签上的部分内容如图所示。
6 12 6
根据标签所提供的信息,判断下列说法不正确的是
A. 该注射液属于一种分散系
B. 该注射液中葡萄糖的质量分数为5%
C. 500mL该注射液质量为25g
D. 该注射液中葡萄糖的物质的量浓度约为0.28mol/L
【答案】C
【解析】【详解】A.注射液是一种混合物,属于一种分散系,A正确;
B.由标签所提供的信息,可知该注射液中葡萄糖的质量分数为5%,B正确;
C.500mL该注射液中葡萄糖的质量为25g,C错误;
D.葡萄糖的质量为25g,其物质的量n= = ,物质的量浓度约为c= =
=0.28mol·L-1,D正确;
答案选C。
28. 十八世纪末,瑞典化学家舍勒用软锰矿(主要成分MnO )和浓盐酸首先制出了黄绿色有毒气体Cl,反应
2 2
方程式为4HCl(浓) + MnO MnCl + Cl +2H O。经测定,常温常压下,1体积水可溶解约2体积Cl。则
2 2 2 2 2
下列说法正确的是
A. 该反应中盐酸是氧化剂
B. 该反应中盐酸部分被氧化
C. 该反应中每转移2mol e-,就有2mol HCl参加反应
D. 当8.7g MnO 被消耗时,用排水法可收集到标况下约2.24L Cl
2 2
【答案】B
【解析】
【详解】A.该反应中氯元素化合价由-1升高为0,盐酸是还原剂,故A错误;
B.盐酸中部分氯元素化合价化合价由-1升高为0,,所以盐酸部分被氧化,故B正确;
C.该反应中每转移2mol e-,有4mol HCl参加反应,只有2mol HCl被氧化,故C错误;
D.当8.7g MnO 被消耗时,生成0.1mol氯气,氯气能溶于水,用排水法收集到标况下氯气的体积小于
2
2.24L ,故D错误;
选B。
29. 某化学兴趣小组进行如下实验:
实验① 向 晶体中滴加浓盐酸,产生黄绿色气体 ;
实验② 向 溶液中通入少量实验①中产生的 ,溶液变为黄色;
实验③ 取实验②中生成的溶液滴在淀粉KI试纸上,试纸变为蓝色。
下列判断正确的是( )
A. 上述实验证明氧化性:B. 上述实验中,共有两个氧化还原反应
C. 不能使湿润的淀粉KI试纸变蓝
D. 实验②证明 既有氧化性又有还原性
【答案】A
【解析】
【详解】提取题目信息,如表所示:
序号 反应物 产物
① 氧化剂: 还原剂:HCl 氧化产物:
② 氧化剂: 还原剂: 氧化产物:
③ 氧化剂: 还原剂:KI 氧化产物:
A.依据氧化还原反应中,氧化剂的氧化性强于氧化产物的氧化性,可以判断氧化性由强到弱的顺序是
,A正确。
B.上述实验中,3个反应均是氧化还原反应,B错误。
C.氯气氧化性强于单质碘,因此 能使湿润的淀粉KI试纸变蓝,C错误。
D. 为中间价态,确实既有氧化性又有还原性,但是在实验②中它只做还原剂,只体现还原性,D错
误;
答案选A。
30. 已知某饱和溶液的:①溶液的质量;②溶剂的质量;③溶液的体积;④溶质的摩尔质量;⑤溶质的溶
解度;⑥溶液的密度。以上条件的组合中不能用来计算该饱和溶液的物质的量浓度的是
A. ①③④ B. ④⑤⑥ C. ①②③④ D. ①③④⑤
【答案】A
【解析】
【详解】A.已知溶液的质量、溶液的体积、溶质的摩尔质量,不能计算溶质的物质的量,所以不能用来
计算该饱和溶液的物质的量浓度,选A;
B.设溶质的溶解度为Sg, , ,所以知道溶质的摩尔质量、溶质的溶解度、溶液的密度,可计算物质的量浓度,故不选B;
C.m(质)= m(液)- m(剂),n(质)= , ,所以知道溶液的质量、溶剂的质量、溶液的体积、溶
质的摩尔质量,可计算物质的量浓度,故不选C;
D.溶质的溶解度为Sg, ,m(质)= m(液) ,n(质)= , ,所以知道溶液
的质量、溶液的体积、溶质的摩尔质量、溶质的溶解度,可计算物质的量浓度,故不选D;
选A。
二、填空题
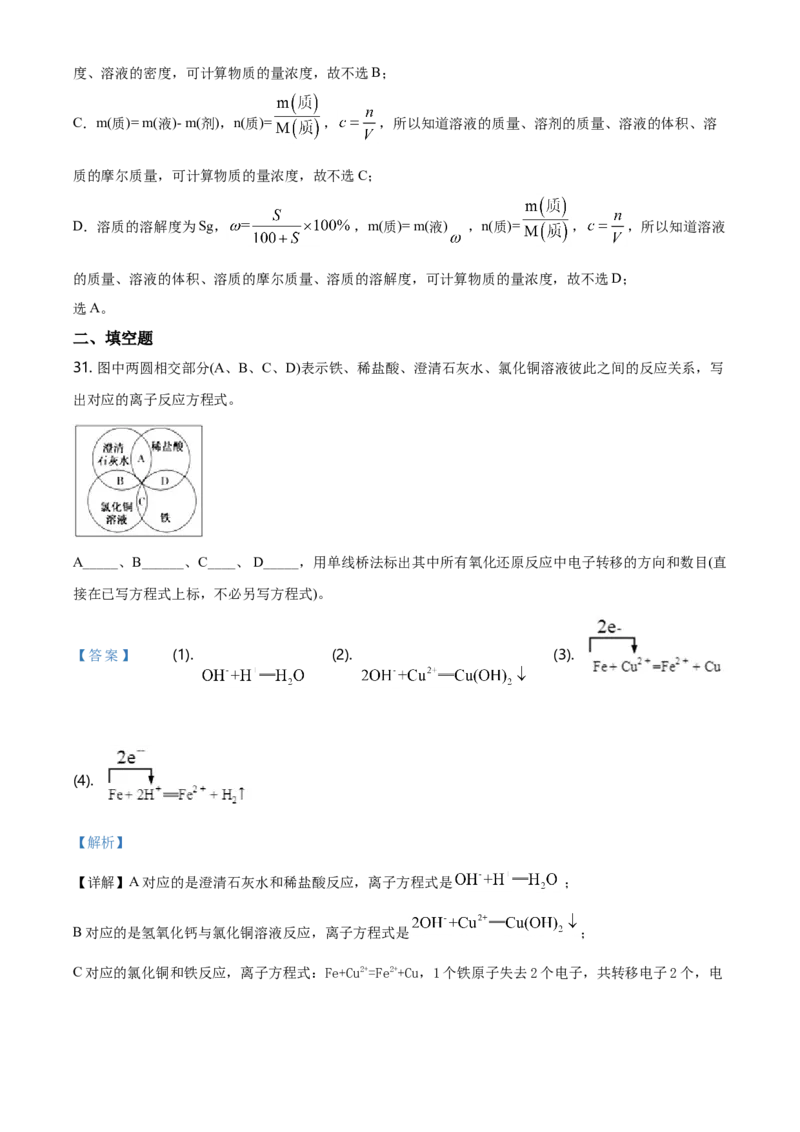
31. 图中两圆相交部分(A、B、C、D)表示铁、稀盐酸、澄清石灰水、氯化铜溶液彼此之间的反应关系,写
出对应的离子反应方程式。
A_____、B______、C____、 D_____,用单线桥法标出其中所有氧化还原反应中电子转移的方向和数目(直
接在已写方程式上标,不必另写方程式)。
【答案】 (1). (2). (3).
(4).
【解析】
【详解】A对应的是澄清石灰水和稀盐酸反应,离子方程式是 ;
B对应的是氢氧化钙与氯化铜溶液反应,离子方程式是 ;
C对应的氯化铜和铁反应,离子方程式:Fe+Cu2+=Fe2++Cu,1个铁原子失去2个电子,共转移电子2个,电子转移单线桥表示是: ;
D对应的是铁与盐酸反应生成氯化亚铁和氢气,离子方程式:Fe+2H+=Fe2++H 1个铁原子失去2个电子,共
2,
转移电子2个,电子转移单线桥表示是: 。
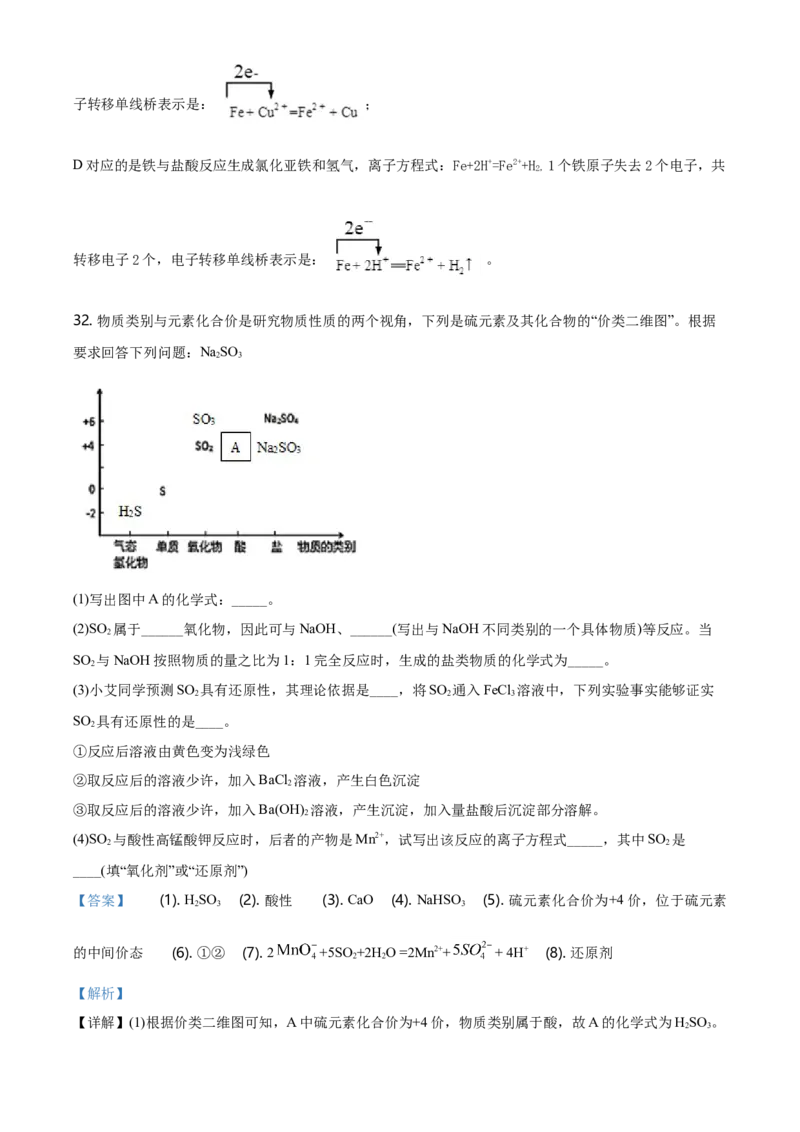
32. 物质类别与元素化合价是研究物质性质的两个视角,下列是硫元素及其化合物的“价类二维图”。根据
要求回答下列问题:NaSO
2 3
(1)写出图中A的化学式:_____。
(2)SO 属于______氧化物,因此可与NaOH、______(写出与NaOH不同类别的一个具体物质)等反应。当
2
SO 与NaOH按照物质的量之比为1:1完全反应时,生成的盐类物质的化学式为_____。
2
(3)小艾同学预测SO 具有还原性,其理论依据是____,将SO 通入FeCl 溶液中,下列实验事实能够证实
2 2 3
SO 具有还原性的是____。
2
①反应后溶液由黄色变为浅绿色
②取反应后的溶液少许,加入BaCl 溶液,产生白色沉淀
2
③取反应后的溶液少许,加入Ba(OH) 溶液,产生沉淀,加入量盐酸后沉淀部分溶解。
2
(4)SO 与酸性高锰酸钾反应时,后者的产物是Mn2+,试写出该反应的离子方程式_____,其中SO 是
2 2
____(填“氧化剂”或“还原剂”)
【答案】 (1). HSO (2). 酸性 (3). CaO (4). NaHSO (5). 硫元素化合价为+4价,位于硫元素
2 3 3
的中间价态 (6). ①② (7). 2 +5SO+2H O =2Mn2++ + 4H+ (8). 还原剂
2 2
【解析】
【详解】(1)根据价类二维图可知,A中硫元素化合价为+4价,物质类别属于酸,故A的化学式为HSO 。
2 3(2)二氧化硫能碱反应生成盐和水,故SO 属于酸性氧化物,可与NaOH、碱性氧化物,如CaO等反应。当
2
SO 与NaOH按照物质的量之比为1:1完全反应时,生成亚硫酸氢钠,化学式为NaHSO。
2 3
(3) SO 中硫元素化合价为+4价,位于硫元素的中间价态,故具有还原性,若二氧化硫具有还原性,将SO
2 2
通入FeCl 溶液中,会发生氧化还原反应生成氯化亚铁、硫酸和氯化氢,可以观察到反应后溶液由黄色变
3
为浅绿色,取反应后的溶液少许,加入BaCl 溶液,产生白色沉淀。
2
(4)SO 与酸性高锰酸钾反应发生氧化还原反应,后者的产物是Mn2+,离子方程式为2 +5SO+2H O
2 2 2
=2Mn2++5 + 4H+,其中SO 中硫元素化合升高,故二氧化硫作还原剂。
2
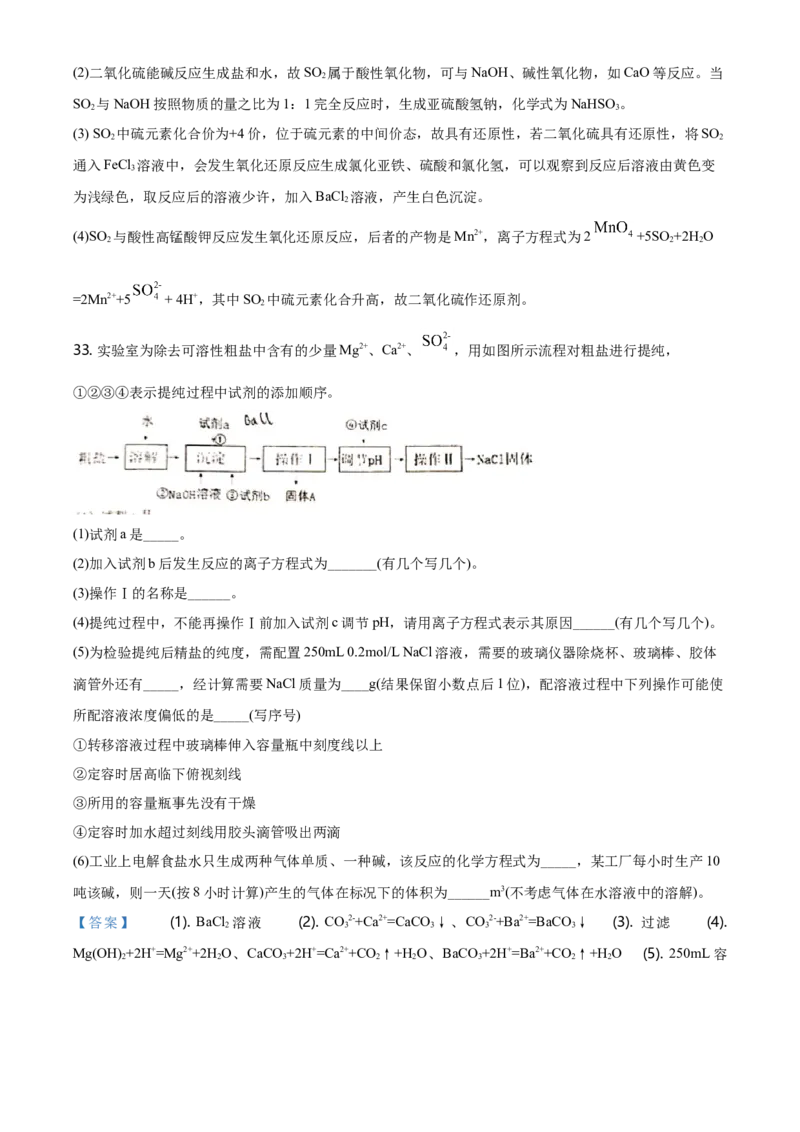
33. 实验室为除去可溶性粗盐中含有的少量Mg2+、Ca2+、 ,用如图所示流程对粗盐进行提纯,
①②③④表示提纯过程中试剂的添加顺序。
(1)试剂a是_____。
(2)加入试剂b后发生反应的离子方程式为_______(有几个写几个)。
(3)操作Ⅰ的名称是______。
(4)提纯过程中,不能再操作Ⅰ前加入试剂c调节pH,请用离子方程式表示其原因______(有几个写几个)。
(5)为检验提纯后精盐的纯度,需配置250mL 0.2mol/L NaCl溶液,需要的玻璃仪器除烧杯、玻璃棒、胶体
滴管外还有_____,经计算需要NaCl质量为____g(结果保留小数点后1位),配溶液过程中下列操作可能使
所配溶液浓度偏低的是_____(写序号)
①转移溶液过程中玻璃棒伸入容量瓶中刻度线以上
②定容时居高临下俯视刻线
③所用的容量瓶事先没有干燥
④定容时加水超过刻线用胶头滴管吸出两滴
(6)工业上电解食盐水只生成两种气体单质、一种碱,该反应的化学方程式为_____,某工厂每小时生产10
吨该碱,则一天(按8小时计算)产生的气体在标况下的体积为______m3(不考虑气体在水溶液中的溶解)。
【答案】 (1). BaCl 溶液 (2). CO2-+Ca2+=CaCO ↓、CO2-+Ba2+=BaCO ↓ (3). 过滤 (4).
2 3 3 3 3
Mg(OH) +2H+=Mg2++2H O、CaCO +2H+=Ca2++CO ↑+H O、BaCO +2H+=Ba2++CO ↑+H O (5). 250mL容
2 2 3 2 2 3 2 2量瓶 (6). 2.9g (7). ①、④ (8). 2NaCl+2H O H↑+Cl↑+2NaOH (9). 2.24×104
2 2 2
【解析】
【分析】
根据流程图分析知,将粗盐溶于水后,先加入氢氧化钠溶液,生成氢氧化镁沉淀,再加入氯化钡溶液,生
成硫酸钡沉淀,再加入碳酸钠溶液,生成碳酸钙沉淀和碳酸钡沉淀,经操作I过滤后得到固体A,则A为
氢氧化镁、碳酸钙和碳酸钡;滤液中加入盐酸调节pH,除去过量的碳酸根离子,操作II为蒸发结晶,得
到氯化钠固体,据此分析解答。
【详解】(1) 根据上述分析,试剂a的目的是除去硫酸根离子,则试剂a是BaCl 溶液,故答案为:BaCl 溶
2 2
液;
(2) 加入试剂碳酸钠溶液的目的是除去钙离子和钡离子,反应的离子方程式为CO2-+Ca2+=CaCO ↓、CO2-
3 3 3
+Ba2+=BaCO ↓,故答案为:CO2-+Ca2+=CaCO ↓、CO2-+Ba2+=BaCO ↓;
3 3 3 3 3
(3) 根据操作I可以得到固体A,则操作Ⅰ是过滤,故答案为:过滤;
(4) 若过滤前加入盐酸,则沉淀氢氧化镁、碳酸钙和碳酸钡都与盐酸反应溶解,离子方程式为:
Mg(OH) +2H+=Mg2++2H O、CaCO +2H+=Ca2++CO ↑+H O、BaCO +2H+=Ba2++CO ↑+H O;故答案为:
2 2 3 2 2 3 2 2
Mg(OH) +2H+=Mg2++2H O、CaCO +2H+=Ca2++CO ↑+H O、BaCO +2H+=Ba2++CO ↑+H O;
2 2 3 2 2 3 2 2
(5) 配制溶液过程中需要将溶液转移至250mL容量瓶中;经计算NaCl质量为
0.250L×0.2mol/L×58.5g/mol≈2.9g;
①转移溶液过程中玻璃棒伸入容量瓶中刻度线以上,导致溶液的体积偏大,浓度偏低,故①选;
②定容时居高临下俯视刻线,导致溶液体积偏小,浓度偏大,故②不选;
③所用的容量瓶事先没有干燥,对配制结果无影响,故③不选;
④定容时加水超过刻线用胶头滴管吸出两滴,导致溶质偏小,浓度偏低,故④选;
故答案为:250mL容量瓶;2.9g;①④;
(6) 电解食盐水生成氢气、氯气和氢氧化钠,化学方程式为:2NaCl+2H O H↑+Cl↑+2NaOH;根据
2 2 2
方程式计算得:n(Cl )= =1×106mol,则产生的气体在标况下的体积为1×106mol×22.4L/
2
mol=2.24×104 m3,故答案为:2NaCl+2H O H↑+Cl↑+2NaOH;2.24×104。
2 2 234. I.在2020年全国抗击新冠肺炎的战役中使用了大量的84消毒液,它是一种以次氯酸钠(NaClO)为有效
成分的高效消毒剂,其水溶液具有强氧化性,可以使病毒的核酸物质被氧化从而杀灭病毒。使用时需注意:
勿与洁厕灵(主要成分为浓盐酸)混用:宜储存在避光、阴凉处······
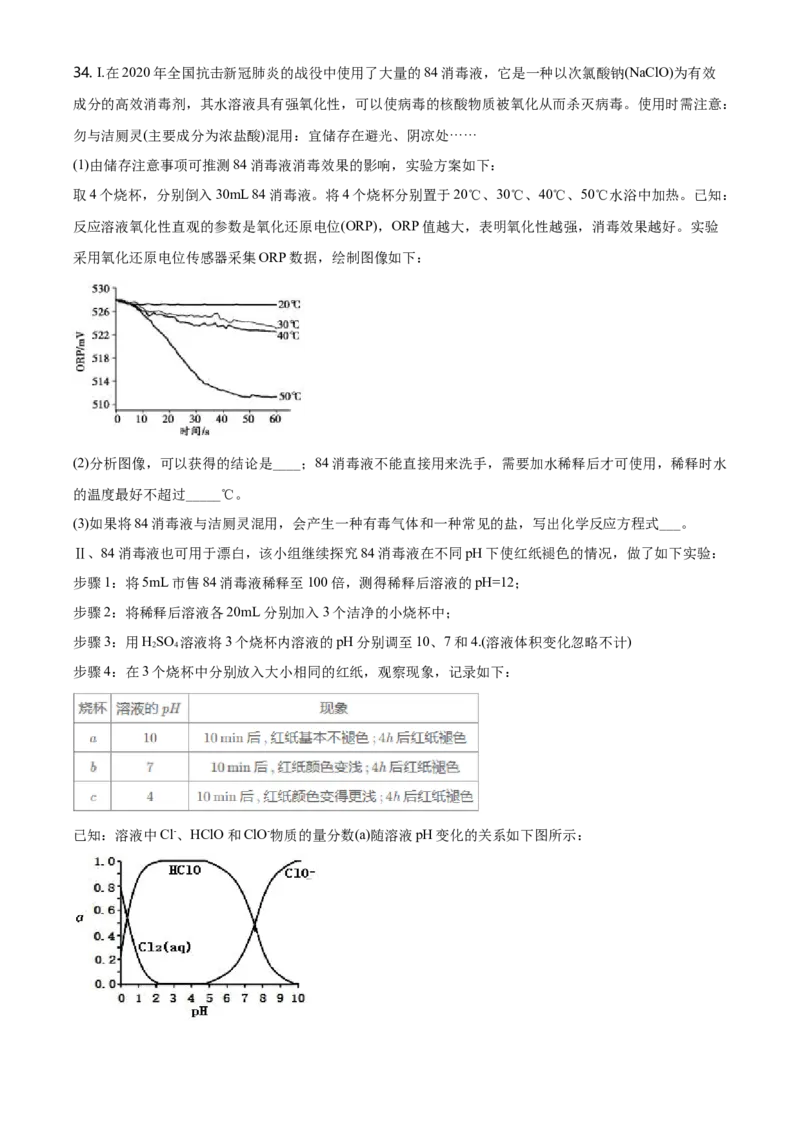
(1)由储存注意事项可推测84消毒液消毒效果的影响,实验方案如下:
取4个烧杯,分别倒入30mL 84消毒液。将4个烧杯分别置于20℃、30℃、40℃、50℃水浴中加热。已知:
反应溶液氧化性直观的参数是氧化还原电位(ORP),ORP值越大,表明氧化性越强,消毒效果越好。实验
采用氧化还原电位传感器采集ORP数据,绘制图像如下:
(2)分析图像,可以获得的结论是____;84消毒液不能直接用来洗手,需要加水稀释后才可使用,稀释时水
的温度最好不超过_____℃。
(3)如果将84消毒液与洁厕灵混用,会产生一种有毒气体和一种常见的盐,写出化学反应方程式___。
Ⅱ、84消毒液也可用于漂白,该小组继续探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售84消毒液稀释至100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用HSO 溶液将3个烧杯内溶液的pH分别调至10、7和4.(溶液体积变化忽略不计)
2 4
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
已知:溶液中Cl-、HClO和ClO-物质的量分数(a)随溶液pH变化的关系如下图所示:(4)①由实验现象可获得一下结论:溶液的pH再4~10范围内,pH越大,红纸褪色_____。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是_______。
③图像表明,当调至pH=4时,84消毒液中的有效成分几乎变成HClO,由上述实验可知,其他条件相同
时,氧化性HClO_____NaClO(填“>”或“<”),消毒液之所以为次氯酸盐而不是此路算是由于此路算不稳定,
写出HClO见光分解的化学反应方程式______,每有10.5gHClO分解,转移电子的物质的量为______。
【答案】 (1). 低于 40℃时,NaClO 能稳定存在;高于 40℃时,NaClO 易分解 (2). 40 (3).
NaClO+2HCl=NaCl+Cl +H O (4). 越慢 (5). b烧杯中溶液的pH大于c烧杯中溶液的pH,HClO的浓度
2 2
较小,反应速率较慢,褪色较慢 (6). > (7). 2HClO=2HCl+O ↑ (8). 0.4
2
【解析】
【分析】
I.根据图像可知,20℃、30℃、40℃时,ORP数据变化不大,氧化性基本保持不变;50℃水浴中加热,
ORP数据减小,氧化性减弱;
II.根据溶液中 的pH及氯原子的存在形式及实验现象可知,溶液的碱性越强,次氯酸的浓度越小,氧化性
越弱。
【详解】(2)分析图像,NaClO溶液低于40℃时,能稳定存在;高于40℃时,易分解;稀释时水的温度最
好不超过40℃;
(3)已知NaClO与洁厕灵(HCl)混用,会产生一种有毒气体和一种常见的盐,毒气为氯气,盐为氯化钠,化
学方程式为NaClO+2HCl=NaCl+Cl +H O;
2 2
(4)①由实验现象可获得一下结论,溶液的pH再4~10范围内,pH越大,次氯酸的浓度越小,红纸褪色越
慢;
②b、c两烧杯中,b烧杯中溶液的pH大于c烧杯中溶液的pH,HClO的浓度较小,反应速率较慢,褪色较
慢;
③pH越大,HClO的浓度越小,褪色越慢,则氧化性HClO>NaClO;HClO见光分解为HCl和氧气,化学
反应方程式为2HClO=2HCl+O ↑;2molHClO分解时,转移4mol电子,10.5gHClO即0.2mol分解,转移
2
0.4mol电子。