文档内容
绝密★启用前|考试研究中心命制
B Cl 浓盐酸与二氧化锰 饱和NaCl溶液 NaOH溶液
2
下学期期中测试卷 02
C HI 浓硫酸与KI 浓硫酸 水
高一化学
D HS FeS与稀盐酸 浓硫酸 酸性KMnO 溶液
2 4
4.(本题3分)下列离子组因发生氧化还原反应而不能大量共存的是
(考试时间:90分钟 试卷满分:100分)
A.H+、Fe2+、SO 、NO B.NH 、SO 、Fe3+、SCN-
测试范围:人教版2019必修第二册:第五章、第六章
第Ⅰ卷(选择题 共 48 分) C.Ba2+、CO 、Na+、ClO- D.K+、Na+、HCO 、OH-
5.(本题3分)无色的混合气体甲。可能含有NO、CO、 NO 、NH 、N 中的某几种。将100mL气体经过如
2 2 3 2
一、选择题:本题共16个小题,每小题3分。在每小题给出的四个选项中,只有一项是符合题目要求的。
下图的实验处理,结果得到酸性溶液,而几乎无气体剩余。则甲气体的组成为
1.(本题3分)下列关于硫及其化合物的说法正确的是( )
A.单质硫易溶于CS,实验室常用CS 清洗沾有硫单质的试管
2 2
B.二氧化硫使酸性高锰酸钾溶液褪色,体现了其漂白性
C.浓硫酸具有吸水性,可用于干燥HCl、NH 、Cl 等气体
3 2
D.常温下将铜片插入浓硫酸时无明显现象,说明浓硫酸可使铜钝化
A.NH 、NO 、N B.NH 、NO 、CO
3 2 2 3 2 2
2.(本题3分)下列实验中的颜色变化,与氧化还原反应无关的是( )
C.NH 、NO、CO D.NO、CO、N
3 2 2 2
① ② ③ ④ ⑤ 6.(本题3分)下列离子方程式能用来解释相应实验现象的是
实 NaOH溶液滴入 石蕊溶液滴入 SO 2 通入品红 Na 2 S溶液滴入 H 2 O 2 滴入含有酚 A.氢氧化钠腐蚀磨口玻璃塞:SiO 2 +2OH-=SiO +H 2 O
验 FeSO 4 溶液中 氯水中 溶液中 CuCl 2 溶液中 酞的氨水中 B.氯化铝液中滴加氨水,生成沉淀:Al3++3OH-=Al(OH) 3 ↓
现 产生白色沉淀,随 溶液变红,随 溶液由红色逐 蓝绿色溶液产生 溶液由红色逐渐 C.铜溶于浓硝酸:Cu+4HNO =Cu2++2NO +2H O+2NO ↑
3 2 2
象 后变为红褐色 后迅速褪色 渐变无色 黑色浑浊 变无色
D.84消毒液与洁厕灵混用产生有毒气体:ClO-+Cl-+H+=Cl↑+OH-
2
A.①② B.①③ C.②⑤ D.③④ 7.(本题3分)下列叙述不正确的是
3.(本题3分)用如图装置制取并收集气体,对应的装置和试剂均正确的是( ) A.水玻璃可用作制备木材防火剂的原料
B.SiO 是酸性氧化物,所以不与任何酸反应
2
C.SiC俗称金刚砂,其中碳原子和硅原子通过共价键连接
D.NaOH溶液不能盛装在带玻璃塞的磨口试剂瓶中
8.(本题3分)我国成功地发射了“嫦娥一号”探测卫星,对月球土壤中14种元素的分布及含量进行探测等。
月球的矿产资源极为丰富,仅月球表层5cm厚的沙土就含铁单质有上亿吨,月球上的主要矿物有辉石
选项 Ⅲ中收集气体 Ⅰ中试剂a、b Ⅱ中试剂c Ⅳ中试剂d (CaMgSi O)、钾长石(KAlSi O)和橄榄石(Mg Fe SiO)等,下列说法或分析不正确的是
2 6 3 8 x 2-x 4
A.辉石、钾长石及橄榄石均属于硅酸盐矿
A SO 稀硫酸与铜片 浓硫酸 NaOH溶液
2
B.钾长石的氧化物形式可表示为:KO•Al O•6SiO
2 2 3 2C.橄榄石中铁为+2价 有关这种燃料电池的下列说法中,不正确的是
D.月球上有游离态铁是因为月球上铁的活动性比地球上铁的活动性弱
9.(本题3分)为提纯下列物质(括号内的物质为少量杂质),所选用的除杂试剂和纯化方法正确的是
选项 ① ② ③ ④
被提纯物 I(水) SiO(AlO) HCl (Cl ) Fe(Al)
2 2 2 3 2
FeCl 溶液、浓硫
2
除杂试剂 CCl 稀盐酸 NaOH溶液
4
酸
过滤、洗涤、烘
纯化方法 萃取 洗气 过滤、洗涤、烘干 A.供电时的总反应为2H+O =2H O
2 2 2
干
B.该装置中发生化学反应,实现了电能到化学能的转化
A.①② B.③④ C.② D.①③
C.正极上反应的电极反应式为:O+4H++4e-=2H O
2 2
10.(本题3分)下列物质性质与应用对应关系正确的是
D.氢氧燃料电池不仅能量转化率高,而且产物是水,属于环境友好电池
A.晶体硅熔点高硬度大,可用于制作半导体材料
13.(本题3分)利用生物燃料电池原理研究室温下氨的合成,电池工作时 在电极与酶之间传递
B.硅胶疏松多孔接触面积大吸水性强,可用作食品干燥剂
电子,示意图如图所示。下列说法不正确的是
C.漂白粉氧化性强,可用于泳池消毒、灭活病毒和漂白食物、纸张
D.SO 还原性强,可用于葡萄酒的抗菌消毒和防腐
2
11.(本题3分)最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。
反应过程的示意图如下:
A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
B.H 在氢化酶作用下发生反应
2
C.正极区,固氮酶为催化剂, 发生还原反应生成
D.电池工作时H+通过交换膜由负极区向正极区移动
下列说法正确的是 14.(本题3分)将 4 mol A 和 2 mol B 在 2 L 的容器中混合并在一定条件下发生如下反应:2A +B 2C 若
(s) (g) (g)
A.CO和O生成CO 是放热反应 经2s(秒)后测得 C 的浓度为0.6 mol·L-1 ,现有下列几种说法: ⇌
2
B.在该过程中,CO断键形成C和O ① 用物质 A 表示的反应的平均速率为 0.3 mol·(L·s)-1
C.CO和O生成了具有极性共价键的CO ② 用物质 B 表示的反应的平均速率为 0.6 mol·(L·s)-1
2
D.状态Ⅰ→状态Ⅲ表示CO与O 反应的过程 ③ 2 s 时物质 A 的转化率为30%
2
12.(本题3分)某种氢氧燃料电池已经成功应用在城市公交汽车上,该电池用30%H SO 溶液作电解质溶液。 ④ 2 s 时物质 B 的浓度为0.7 mol·L-1
2 4其中正确的是 A.①② B.②④ C.③ D.①⑥
A.①③④ B.①④ C.②③ D.③④ (2)断开1molH-H键、1molN-H键、1molN≡N键分别需要吸收的能量为436kJ、391kJ、946kJ,则1mol N 2 生
15.(本题3分)将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度 成NH 3 理论上能___________(填“吸收”或“放出”)能量___________kJ。
下使其达到分解平衡:NH COONH(s) 2NH (g)+CO (g) ∆H=akJ/mol(a>0)。下列分析正确的是 (3)某学习小组研究影响锌与稀硫酸反应速率的外界条件,设计实验的数据如下:
2 4 3 2
A.反应开始后至到平衡,密闭容器中⇌氨气的体积分数不变 反应前溶液的
序号 锌的质量/g 锌的状态 c(H SO )/mol·L-1 V(H SO )/mL 其他试剂
2 4 2 4
B.平衡时的CO 的浓度是NH 浓度的二倍 温度/℃
2 3
C.若2v(NH )=v(CO ),则该反应达到平衡状态
3 2
1 0.65 粒状 0.5 50 20 无
D.若开始时向容器中加入2molNH 和1molCO ,达到平衡时放出akJ热量
3 2
2 0.65 粉末 0.5 50 20 无
16.(本题3分)把在空气中久置的铝片5.0g投入盛有50mL0.5mol/L硫酸溶液的烧杯中,该铝片与硫酸反应
产生氢气的速率v与反应时间t可用如图所示的坐标曲线来表示。下列推论错误的是 3 0.65 粒状 0.5 50 20 2滴CuSO 溶液
4
4 0.65 粉末 0.8 50 20 无
5 0.65 粉末 0.8 50 35 2滴CuSO 溶液
4
在此5组实验中,速率最快的是___________(填实验序号);
实验1和2表明___________对反应速率有影响;
实验1和3表明___________对反应速率有影响。
(4)用CH 和O 组合形成的质子交换膜燃料电池的结构如图丙:
4 2
A.O→a段不产生氢气是因为表面的氧化物隔离了铝和硫酸溶液
B.b→c段产生氢气的速率增加较快的主要原因之一是温度升高
C.t=c时反应处于平衡状态
D.t>c时,产生氢气的速率降低主要是因为溶液中c(H+)降低
第 II 卷(非选择题 共 52 分)
二、非选择题:包括第17题~第21题5个大题,共52分。
17.(本题12分)化学反应中伴随着能量的变化。
(1)下列变化中属于吸热反应的是___________(填字母)
①液态水汽化②将胆矾加热变为白色粉末③苛性钠固体溶于水④氯酸钾分解制氧气⑤生石灰跟水反应生成
熟石灰⑥干冰升华①则电极d是___________(填“正极”或“负极”),电极c的电极反应式为___________。
②若线路中转移2mol电子,则该燃料电池理论上消耗的O 在标准状况下的体积为___________L。
2
18.(本题7分)(1)已知2H→H 放出437.6 kJ的热量,下列说法正确的是_______
2
A.氢气分子内每个氢原子都达到稳定结构
B.氢气分子的能量比两个氢原子的能量低
C.1 mol H 离解成2 mol H 要放出437.6 kJ热量
2
D.氢原子比氢气分子稳定
(1)装置A中发生反应的化学方程式为___________
(2)科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO)表面作用使海水分解得到氢气的新技术
2
(2)装置D中试管口放置的棉花应浸一种溶液,这种溶液是___________其作用是___________
2HO 2H↑+O ↑.制得的氢气可用于制作燃料电池。试回答下列问题:
2 2 2 (3)装置B的作用是___________当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A
①分解海水时,实现了光能转化为_______能;生成的氢气用于制作燃料电池时,实现了化学能转化为 处仍有气体产生,此时B中现象是___________B中应放置的液体是___________(填字母)
_______能;分解海水的反应属于_______反应(填“放热”或“吸热”) A.水 B.酸性高锰酸钾 C.浓溴水 D.饱和NaHSO
3
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应为:2H+2O2--4e-=2H O, (4)实验中,取一定质量的铜片和一定体积18 mol•L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶
2 2
则B极的电极反应式为:_______ 中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,下列药品能用来证明反应
19.(本题9分)已知有如图所示转化关系(反应条件略)。 结束后的烧瓶中有余酸的是___________(填字母)。
a.铁粉 b.BaCl 溶液 c.银粉 d.NaCO 溶液
2 2 3
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色。为了证明
蓝色只与Cu2+有关,而与其他离子无关,某同学设计了下列实验,其中对实验目的没有意义的是
___________。(填序号)
①观察稀硫酸溶液呈无色;②观察CuSO 粉末呈白色;③稀释CuSO 溶液,溶液蓝色变浅;④往CuSO 溶
4 4 4
已知:①X、Y、Z、W均为氧化物。常温下,X是红棕色气体;Y能使澄清石灰水变浑浊但不能使品红溶
液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色;⑤往CuSO 溶液中加入足量BaCl 的溶液,
4 2
液褪色。②相对分子质量:甲<乙。③将甲的浓溶液露置在空气中一段时间,质量减小浓度降低;将乙的
生成白色沉淀,过滤,滤液仍呈蓝色。
浓溶液露置在空气中一段时间,质量增加浓度降低。请完成下列空白:
21.(本题12分)某研究性学习小组对实验室中NH 制取、收集、吸收,以及NH 的还原性探究进行了如下
3 3
(1)Z是(写化学式):___________。
实验设计。
(2)将乙的浓溶液露置在空气中一段时间,质量增加浓度降低,表明乙的浓溶液具有___________性。利用这
Ⅰ.NH 的收集和吸收
3
种性质可以进行___________项(填字母)实验操作
(1)若用图甲装置,排空气法收集NH ,气体应从___________口进入(选填“m”或“n”)。
3
A.钝化铁片 B.检验Ba2+ C.干燥氨气 D.干燥氯气
(2)已知NH 难溶于CCl 图乙、丙、丁、戊四种装置中,不能用来吸收NH 的是___________。
3 4. 3
(3)在X与Z的反应中,被氧化的X与被还原的X的物质的量之比是___________
(4)W可用于工业制溴过程中吸收潮湿空气中的Br ,写出该反应的化学方程式:___________
2
(5)写出M与甲的浓溶液在加热条件下反应的化学方程式:___________
20.(本题12分)某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验。
Ⅱ.NH 的还原性探究:
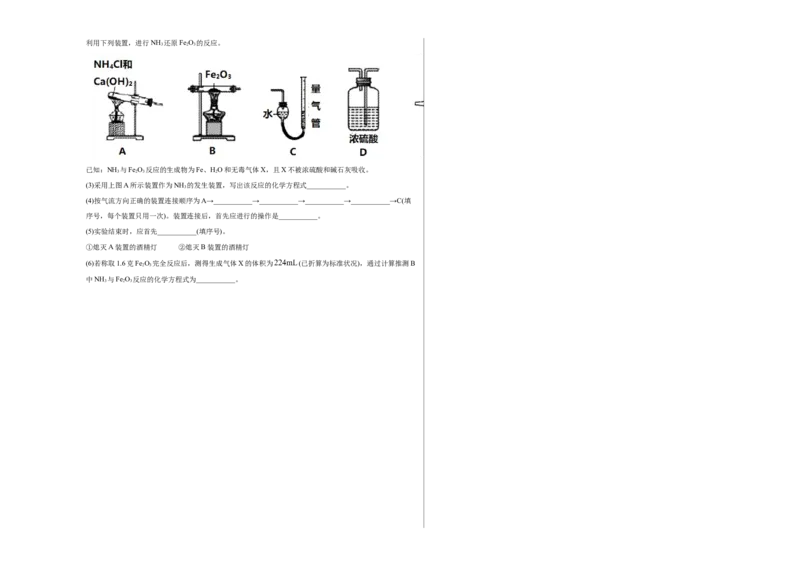
3利用下列装置,进行NH 还原Fe O 的反应。
3 2 3
已知:NH 与Fe O 反应的生成物为Fe、HO和无毒气体X,且X不被浓硫酸和碱石灰吸收。
3 2 3 2
(3)采用上图A所示装置作为NH 的发生装置,写出该反应的化学方程式___________。
3
(4)按气流方向正确的装置连接顺序为A→___________→___________→___________→___________→C(填
序号,每个装置只用一次)。装置连接后,首先应进行的操作是___________。
(5)实验结束时,应首先___________(填序号)。
①熄灭A装置的酒精灯 ②熄灭B装置的酒精灯
(6)若称取1.6克Fe O 完全反应后,测得生成气体X的体积为 (已折算为标准状况),通过计算推测B
2 3
中NH 与Fe O 反应的化学方程式为___________。
3 2 3