文档内容
决胜新高考——2024 届高三年级大联考
化 学
注意事项:
考生在答题前请认真阅读本注意事项及各题答题要求
1.本试卷共6页。满分为100分,考试时间为75分钟。考试结束后,请将答题卡交回。
2.答题前,请您务必将自己的姓名、学校、考试号等用书写黑色字迹的 0.5毫米签字笔填写在
答题卡.上规定的位置。
3.请认真核对监考员在答题卡上所粘贴的条形码上的姓名、准考证号与本人是否相符。
4.作答选择题,必须用2B铅笔将答题卡上对应选项的方框涂满、涂黑;如需改动,请用橡皮
擦干净后,再选涂其他答案。作答非选择题,必须用 0.5毫米黑色墨水的签字笔在答题卡上的
指定位置作答,在其他位置作答一律无效。
5.如需作图,必须用2B铅笔绘、写清楚,线条、符号等须加黑、加粗。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 V 51 Fe 56 Zn 65
一、单项选择题:共13题,每题3分,共39分。每题只有一个选项最符合题意。
1.我国早在“十二五”期间就增加了“脱硝”这一节能减排约束性硬指标。“脱硝”中的“硝”是指
( )
A. B. C. D.
2.反应 可用于制备脱氧清洗剂。下列说法正确的是( )
A.NaClO的电子式为 B. 与 具有相同的电子层结构
C. 分子中存在 D. 为非极性分子
3.下列利用氨碱法制纯碱的实验原理与装置不能达到实验目的的是( )
A.用装置甲制取氨气 B.用装置乙制取碳酸氢钠
C.用装置丙过滤得到碳酸氢钠固体 D.用装置丁加热分解碳酸氢钠得到纯碱
4.元素B、Al、Ga位于周期表中IIA族。下列说法正确的是( )
A.原子半径: B.第一电离能:
学科网(北京)股份有限公司C.BN、 、 均为共价晶体 D.可在周期表中元素Al附近寻找半导体材料
阅读下列资料,完成5~7题:
氯、溴、碘及其化合物在自然界广泛存在且具有重要应用。氯、溴主要存在于海水中,工业常通,过电
解NaCl饱和溶液制备 , 可用于制取漂白粉、氯化氢( 、 、 的键能分别为436
、243 、432)。卤水中 可通过 氧化、 溶液吸收,BrCl能发生水解反应。
锂碘电池可供电心脏起搏器,一种 二次电池正极界面反应机理如题6图所示。
5.下列有关说法正确的是( )
题5图
A. 是非极性分子
B.二氯化二硫( )分子结构和 类似
C. 和 的中心原子杂化轨道类型均为
D.NaCl晶胞(如题5图)中钠离子周围最近且等距离的钠离子数为4
6.下列化学反应表示正确的是( )
题6图
A. 电池正极放电时的电极反应有:
学科网(北京)股份有限公司B. 用 溶液吸收:
C.BrCl与 反应:
D.氯气制氯化氢:
7.下列物质结构与性质或物质性质与用途具有对应关系的是( )
A.漂白粉在空气中不稳定,可用于漂白纸张
B. 溶液具有酸性,可用于腐蚀印刷电路板上的Cu
C.BrCl和IBr中Br所带的电性不同,BrCl和IBr与水反应的产物不同
D. 易升华,可用于检验淀粉的存在
8.在给定条件下,下列选项所示的物质间转化能实现的是( )
A.
B.
C.
D.
9.化合物Z是一种治疗糖尿病药物的重要中间体,可由下列反应制得。
下列有关X、Y、Z的说法正确的是( )
A.X中所有碳原子的杂化方式均为 杂化
B.Y在水中的溶解度比X在水中的溶解度小
C.Z与足量 反应生成的有机化合物中含2个手性碳原子
D.X、Y、Z分别与足量酸性 溶液反应所得芳香族化合物相同
10.反应 是汽车尾气无害化处理中的反应之一。下列说法正确的
学科网(北京)股份有限公司是( )
题10图
A.该反应的 ,
B.该反应的平衡常数
C.题10图所示的反应机理中,步骤Ⅰ可理解为 和CO仅在一定方向上才发生有效碰撞
D.反应中每消耗22.24L ,转移电子的数目为
11.室温下,下列实验探究方案能达到探究目的的是( )
选项 探究方案 探究目的
向5mL浓度均为0.05 的NaI、NaCl混合溶液中滴加2
A
滴0.05 溶液,观察现象
B
向2mL 5% 溶液中滴加几滴 溶液,观察气泡产生 能否催化 分解
C 用pH计测量醋酸、盐酸的pH,比较溶液pH大小
是弱电解质
D
取少量久置的 溶液向其中滴加 溶液,观察现象 溶液是否变质
12 . 室 温 下 : 、 、 、
实验室进行多组实验测定某些酸、碱、盐性质,相关实验记录如下:
实验 实验操作和现象
1
测定0.10 溶液的pH约为8
2 测定0.10 HCN与0.05 NaOH溶液等体积混合,测得混合溶液的pH>7
3
向NaClO溶液中通入少量的 ,测得pH降低
4
向0.01 溶液中加入等体积0.03 溶液,产生白色沉淀
下列所得结论正确的是( )
A.实验1溶液中存在:
B.由实验2可得
学科网(北京)股份有限公司C.实验3反应的离子方程式:
D.实验4所得上层清液中的
13. 催化加氢过程中主要发生下列反应:
反应Ⅰ:
反应Ⅱ:
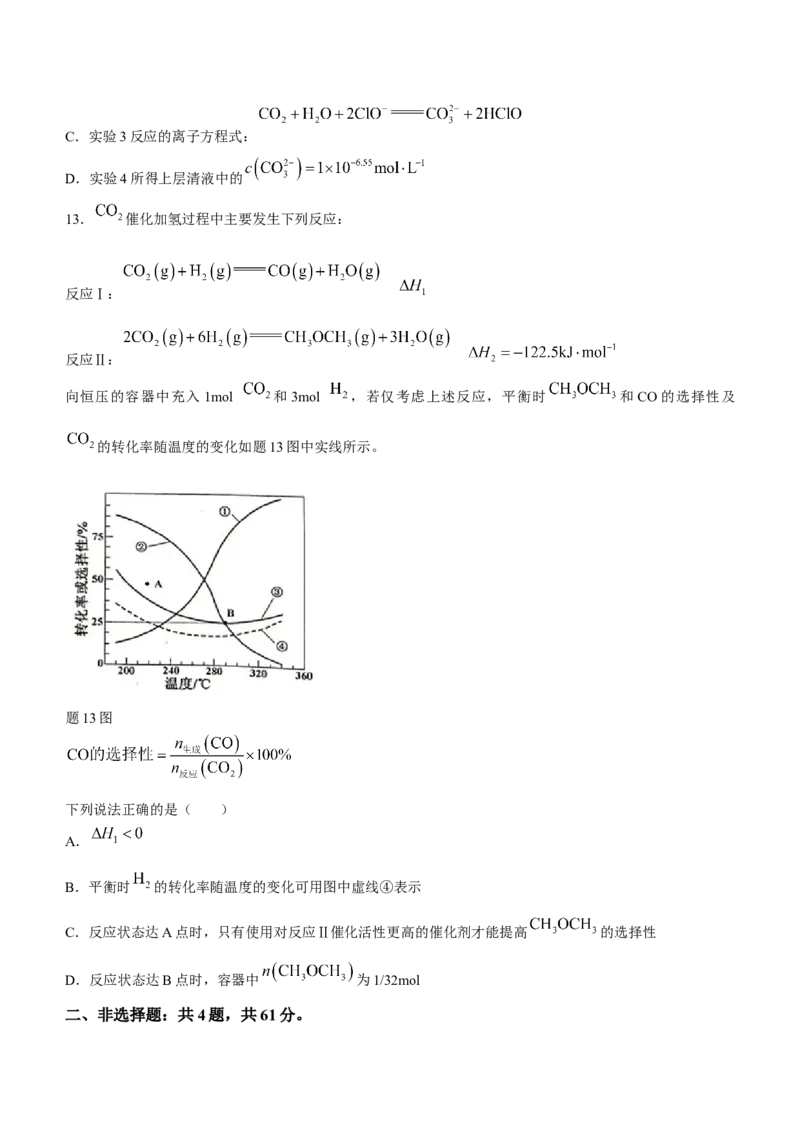
向恒压的容器中充入1mol 和3mol ,若仅考虑上述反应,平衡时 和CO的选择性及
的转化率随温度的变化如题13图中实线所示。
题13图
下列说法正确的是( )
A.
B.平衡时 的转化率随温度的变化可用图中虛线④表示
C.反应状态达A点时,只有使用对反应Ⅱ催化活性更高的催化剂才能提高 的选择性
D.反应状态达B点时,容器中 为1/32mol
二、非选择题:共4题,共61分。
学科网(北京)股份有限公司14.(15分)钴( )的常见化合价有+2、+3等,对应的化合物性质也各有差异。
(1)利用钴渣(主要含金属钴,还含有铜、铁等金属)可富集钴,流程如下:
①“氧化除铁”的化学反应方程式为______。
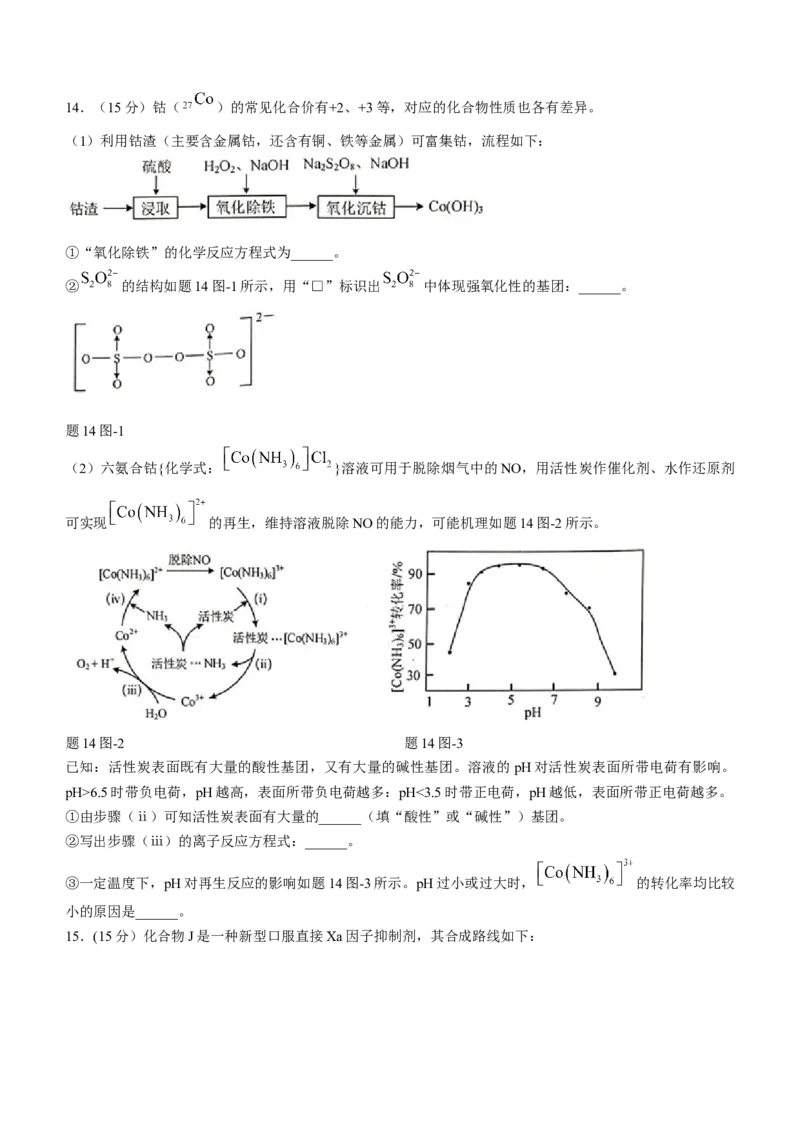
② 的结构如题14图-1所示,用“□”标识出 中体现强氧化性的基团:______。
题14图-1
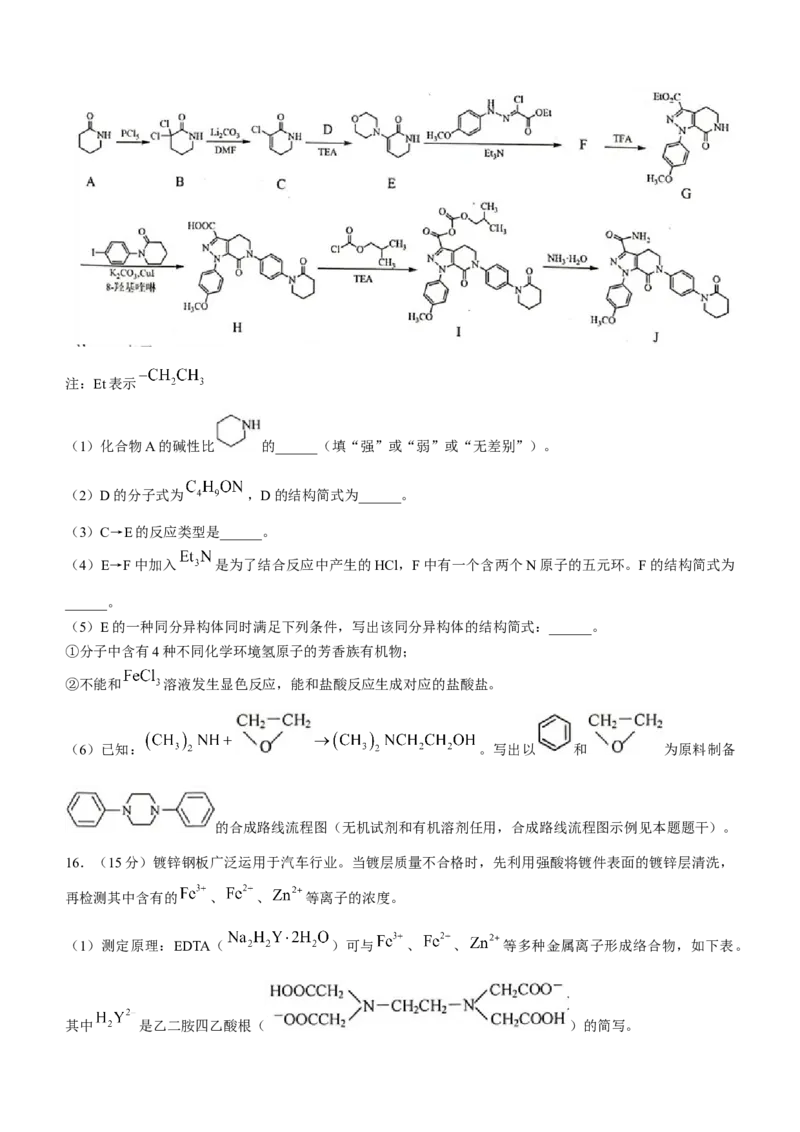
(2)六氨合钴{化学式: }溶液可用于脱除烟气中的NO,用活性炭作催化剂、水作还原剂
可实现 的再生,维持溶液脱除NO的能力,可能机理如题14图-2所示。
题14图-2 题14图-3
已知:活性炭表面既有大量的酸性基团,又有大量的碱性基团。溶液的pH对活性炭表面所带电荷有影响。
pH>6.5时带负电荷,pH越高,表面所带负电荷越多:pH<3.5时带正电荷,pH越低,表面所带正电荷越多。
①由步骤(ⅱ)可知活性炭表面有大量的______(填“酸性”或“碱性”)基团。
②写出步骤(ⅲ)的离子反应方程式:______。
③一定温度下,pH对再生反应的影响如题14图-3所示。pH过小或过大时, 的转化率均比较
小的原因是______。
15.(15分)化合物J是一种新型口服直接Xa因子抑制剂,其合成路线如下:
学科网(北京)股份有限公司注:Et表示
(1)化合物A的碱性比 的______(填“强”或“弱”或“无差别”)。
(2)D的分子式为 ,D的结构简式为______。
(3)C→E的反应类型是______。
(4)E→F中加入 是为了结合反应中产生的HCl,F中有一个含两个N原子的五元环。F的结构简式为
______。
(5)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:______。
①分子中含有4种不同化学环境氢原子的芳香族有机物;
②不能和 溶液发生显色反应,能和盐酸反应生成对应的盐酸盐。
(6)已知: 。写出以 和 为原料制备
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
16.(15分)镀锌钢板广泛运用于汽车行业。当镀层质量不合格时,先利用强酸将镀件表面的镀锌层清洗,
再检测其中含有的 、 、 等离子的浓度。
(1)测定原理:EDTA( )可与 、 、 等多种金属离子形成络合物,如下表。
其中 是乙二胺四乙酸根( )的简写。
学科网(北京)股份有限公司络合反应
(K为平衡常数)
14.3
16.5
25.1
①EDTA在水溶液中可看作“六元酸”的一种微粒可表示为______(用H、Y表示)。
②表中最稳定的金属络合物是______(填化学式)。
(2)测定过程:已知EDTA标准溶液滴定 的相关信息如下表:
滴定对象
滴定时溶液pH范围 1.5~2.0
指示剂 磺基水杨酸
滴定终点现象 紫红色→亮黄色
可采用连续滴定法测定 、 、 的浓度,具体步骤如下:
Ⅰ 先测定 ( 、 不影响Fe3+的滴定):
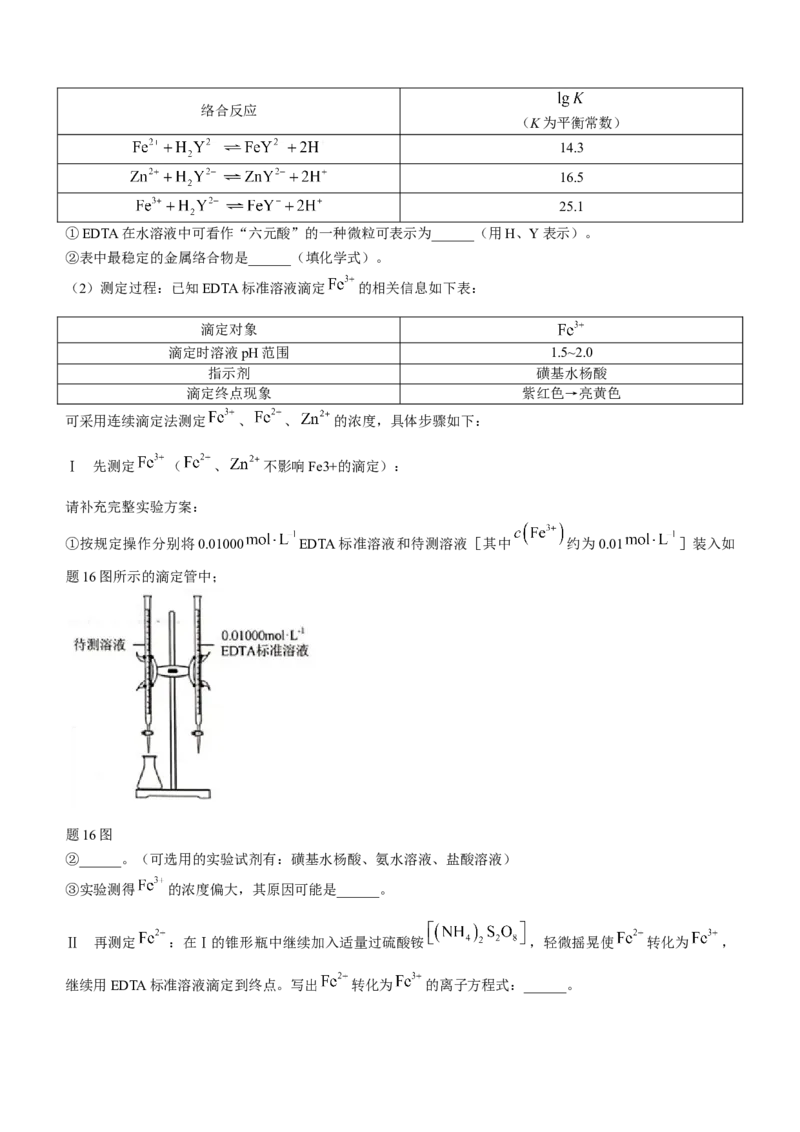
请补充完整实验方案:
①按规定操作分别将0.01000 EDTA标准溶液和待测溶液[其中 约为0.01 ]装入如
题16图所示的滴定管中;
题16图
②______。(可选用的实验试剂有:磺基水杨酸、氨水溶液、盐酸溶液)
③实验测得 的浓度偏大,其原因可能是______。
Ⅱ 再测定 :在Ⅰ的锥形瓶中继续加入适量过硫酸铵 ,轻微摇晃使 转化为 ,
继续用EDTA标准溶液滴定到终点。写出 转化为 的离子方程式:______。
学科网(北京)股份有限公司Ⅲ 最后测定 :在Ⅱ的锥形瓶中继续加入一定量过量的EDTA标准溶液,调节溶液pH至5.0~6.0,再用
标准溶液滴定到终点。 不影响 滴定的原因是______。
17.(16分) 的捕集和利用具有重要意义。
Ⅰ 的催化氧化
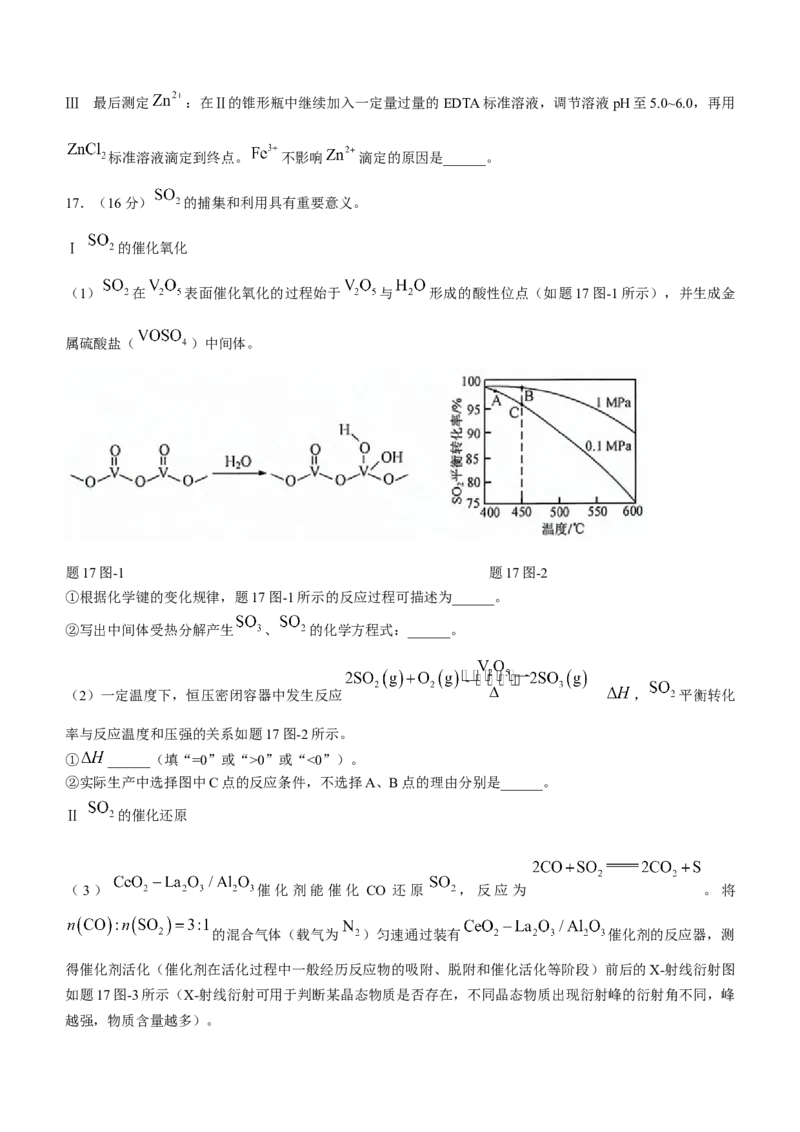
(1) 在 表面催化氧化的过程始于 与 形成的酸性位点(如题17图-1所示),并生成金
属硫酸盐( )中间体。
题17图-1 题17图-2
①根据化学键的变化规律,题17图-1所示的反应过程可描述为______。
②写出中间体受热分解产生 、 的化学方程式:______。
(2)一定温度下,恒压密闭容器中发生反应 , 平衡转化
率与反应温度和压强的关系如题17图-2所示。
① ______(填“=0”或“>0”或“<0”)。
②实际生产中选择图中C点的反应条件,不选择A、B点的理由分别是______。
Ⅱ 的催化还原
(3) 催化剂能催化 CO 还原 ,反应为 。将
的混合气体(载气为 )匀速通过装有 催化剂的反应器,测
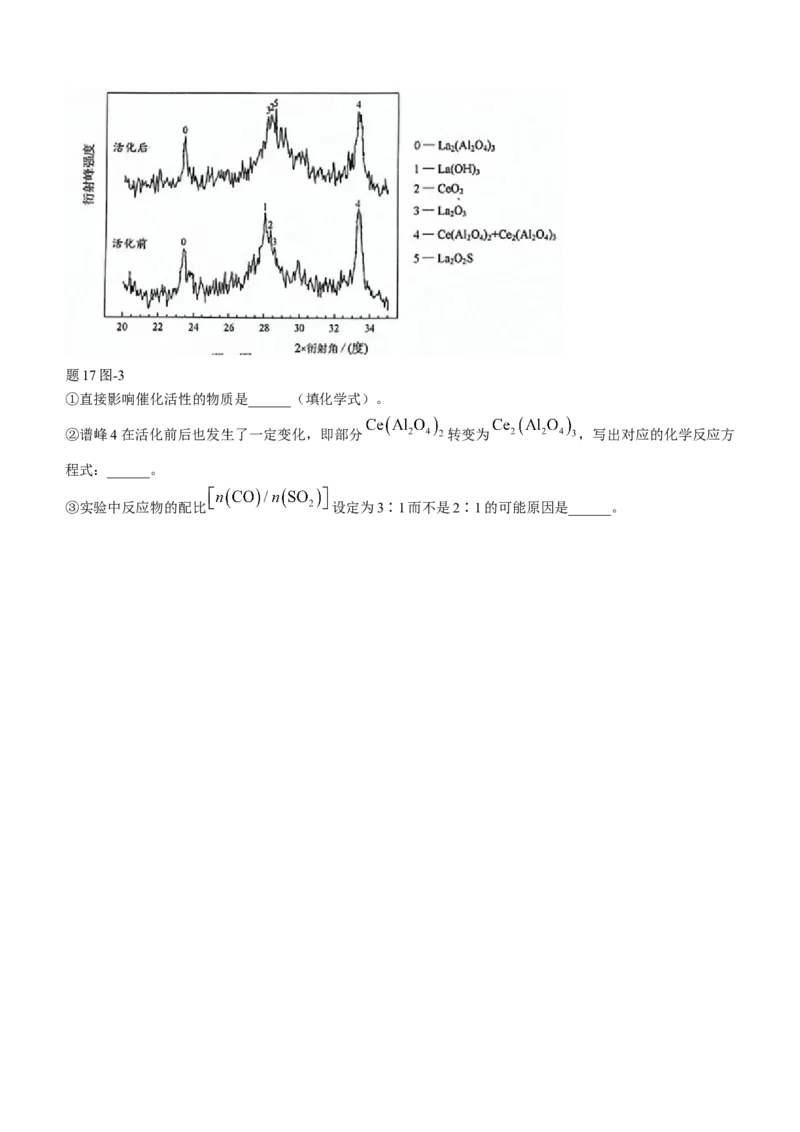
得催化剂活化(催化剂在活化过程中一般经历反应物的吸附、脱附和催化活化等阶段)前后的X-射线衍射图
如题17图-3所示(X-射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同,峰
越强,物质含量越多)。
学科网(北京)股份有限公司题17图-3
①直接影响催化活性的物质是______(填化学式)。
②谱峰4在活化前后也发生了一定变化,即部分 转变为 ,写出对应的化学反应方
程式:______。
③实验中反应物的配比 设定为3∶1而不是2∶1的可能原因是______。
学科网(北京)股份有限公司