文档内容
2024--2025 学年第一学期高二月考化学试题 B. 既可被氧化,也可被还原
8.27
相对原子质量:H:1 C:12 N:14 O:16 Na:23 Al:27 S:32 Cl:35.5 Zn:65 C. 可与 反应生成
一、单选题(每小题只有一个正确答案,每小题2分,共44分)
D. 可存在 的循环转化关系
1. 化学与生活息息相关,下列说法不正确的
A. 添加小苏打蒸制“粵菜"糕点,小苏打的化学式为NaHCO
3
B. 广府文化代表之一“镬耳屋”是使用青砖建造,青砖的青色来自Fe 2 O 3 7. 下列实验能达到实验目的的是
C. 不锈钢中常添加镍和铬元素,从而使其具有特殊性能
D. 铝制餐具不适宜长时间存放酸性或碱性食物
2. 下列叙述或化学用语正确的是
A. 乙烯的结构式为CH =CH B. 的电子式:
2 2
C. HClO的结构式: D. 中子数为18的氯原子:
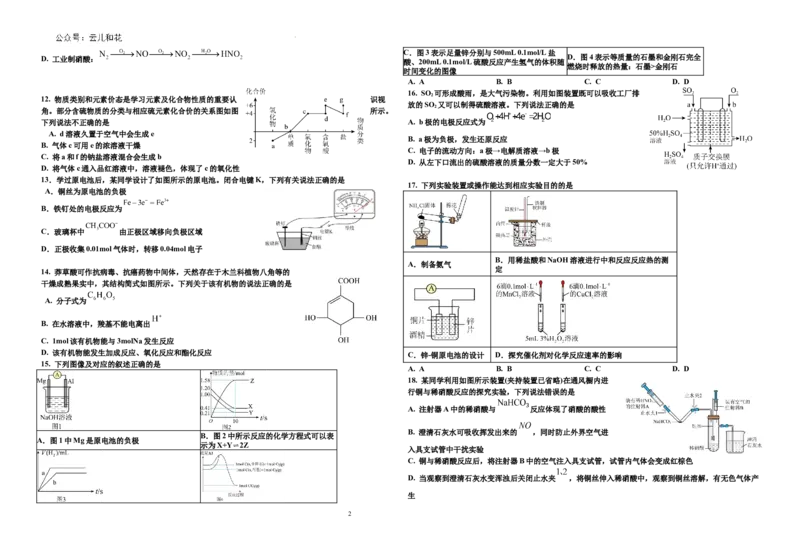
3. 用 表示阿伏加德罗常数的值,下列说法正确的是 A.配制 C.验证某NaCl固
100.00mL0.100mol/ B.净化 体样品中混有 D.鉴别纯碱与小苏打
A. 13gZn与足量稀 完全反应,生成的 所含原子数目为
LNaCl溶液 KCI
B. 0.5mol/L 溶液中含有 和 总物质的量为1mol
A. A B. B C. C D. D
C. 气体溶于水,所得溶液中含有的氯化氢分子为 8.下列反应中前者属于取代反应,后者属于加成反应的是
A.丙烯和氢气反应生成丙烷;甲醇和甲酸反应生成甲酸甲酯
D. 的铁与足量 反应失去电子数为
B.乙烯使酸性高锰酸钾溶液褪色;乙烯在催化剂作用下生成聚乙烯
4. 短周期主族元素X、Y、Z、W的原子序数依次增大, 在短周期中原子半径最大, 是地壳中含量最
C.乙醇和氧气反应生成乙醛;乙烯与水蒸气在一定条件下反应生成乙醇
高的金属元素, 和 同主族, 的最高正化合价与最低负化合价的代数和为4。下列说法不正确的是 D.光照条件下甲烷与氯气的反应;乙烯使溴的四氯化碳溶液褪色
9.劳动创造美好生活。下列劳动项目所涉及的化学知识不正确的是
A. 简单气态氢化物的稳定性:
B. 离子半径由小到大的顺序: 选项 劳动项目 化学知识
C. 的最高价氧化物的水化物能与强碱反应 A 用干燥的模具盛装熔融钢水 铁与H₂O高温下会反应
B 通过煤的干馏获得煤焦油、焦炭等物质 煤的干馏属于物理变化
D. 与 形成的化合物中可能既含有离子键,又含有共价键
C 制作水果罐头时加入少量维生素C 维生素C是抗氧化剂
5. 以不同类别物质间的转化为线索,认识钠及其化合物。下列分析不正确的是
D 用铁罐车运输浓硫酸 常温下浓硫酸遇铁钝化
10. 在指定条件下,下列选项所示的物质间转化均能实现的是
A. B.
C. (浓) D.
A. 反应③表明CO 具有酸性氧化物的性质
2 11. 工业上制备下列物质的生产流程合理的是
B. B. 反应⑤、⑥可用于潜水艇中氧气的供给
C. 反应④说明NaHCO 的热稳定性强于Na CO A. 由铝土矿冶炼铝:铝土矿
3 2 3
D. 上述转化中发生的反应有分解反应、化合反应、置换反应
6. 部分含铁物质的分类与相应化合价关系如图所示。下列推断 B. 由石英砂制高纯硅:石英砂 粗硅 高纯硅
不合理的是
C. 从海水中提取镁:海水
A. 可将 加入浓碱液中制得 的胶体
1
学科网(北京)股份有限公司C.图3表示足量锌分别与500mL 0.1mol/L盐
D. 工业制硝酸: D.图4表示等质量的石墨和金刚石完全
酸、200mL 0.1mol/L硫酸反应产生氢气的体积随
燃烧时释放的热量:石墨>金刚石
时间变化的图像
A. A B. B C. C D. D
16. SO 可形成酸雨,是大气污染物。利用如图装置既可以吸收工厂排
2
12. 物质类别和元素价态是学习元素及化合物性质的重要认 识视
放的SO 又可以制得硫酸溶液。下列说法正确的是
2
角。部分含硫物质的分类与相应硫元素化合价的关系图如图 所示。
下列说法不正确的是 A. b极的电极反应式为
A. d溶液久置于空气中会生成e
B. a极为负极,发生还原反应
B. 气体c可用e的浓溶液干燥
C. 电子的流动方向:a极→电解质溶液→b极
C. 将a和f的钠盐溶液混合会生成b
D. 从左下口流出的硫酸溶液的质量分数一定大于50%
D. 将气体c通入品红溶液中,溶液褪色,体现了c的氧化性
13.学过原电池后,某同学设计了如图所示的原电池。闭合电键K,下列有关说法正确的是
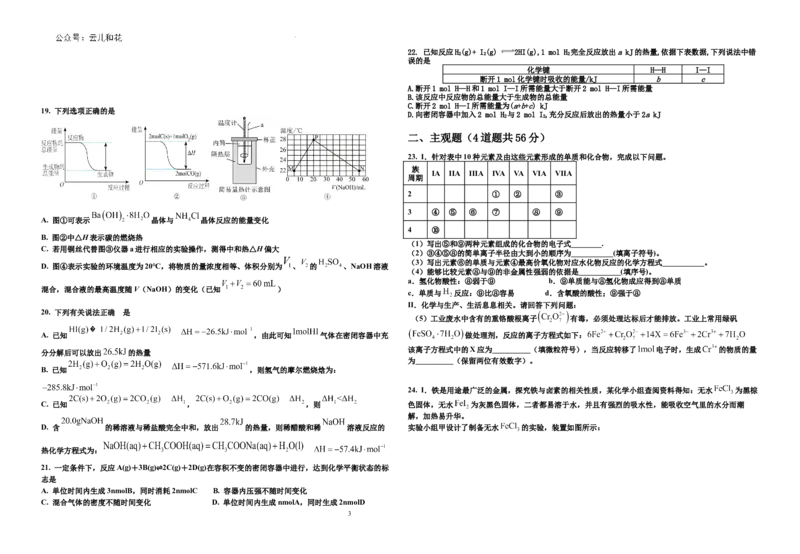
17. 下列实验装置或操作能达到相应实验目的的是
A.铜丝为原电池的负极
B.铁钉处的电极反应为
C.玻璃杯中 由正极区域移向负极区域
D.正极收集0.01mol气体时,转移0.04mol电子
B.用稀盐酸和NaOH溶液进行中和反应反应热的测
A.制备氨气
定
14. 莽草酸可作抗病毒、抗癌药物中间体,天然存在于木兰科植物八角等的
干燥成熟果实中,其结构简式如图所示。下列关于该有机物的说法正确的是
A. 分子式为
B. 在水溶液中,羧基不能电离出
C. 1mol该有机物能与3molNa发生反应
D. 该有机物能发生加成反应、氧化反应和酯化反应
C.锌-铜原电池的设计 D.探究催化剂对化学反应速率的影响
15. 下列图像及对应的叙述正确的是
A. A B. B C. C D. D
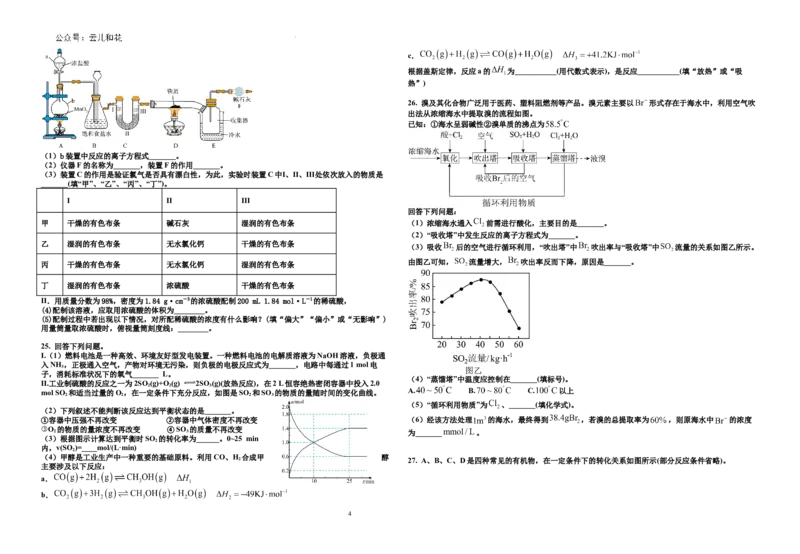
18. 某同学利用如图所示装置(夹持装置已省略)在通风橱内进
行铜与稀硝酸反应的探究实验,下列说法错误的是
A. 注射器A中的稀硝酸与 反应体现了硝酸的酸性
B. 澄清石灰水可吸收挥发出来的 ,同时防止外界空气进
B.图2中所示反应的化学方程式可以表
A.图1中Mg是原电池的负极
示为X+Y⇌2Z
入具支试管中干扰实验
C. 铜与稀硝酸反应后,将注射器B中的空气注入具支试管,试管内气体会变成红棕色
D. 当观察到澄清石灰水变浑浊后关闭止水夹 ,将铜丝伸入稀硝酸中,观察到铜丝溶解,有无色气体产
生
2
学科网(北京)股份有限公司22. 已知反应H(g)+ I(g) 2HI(g),1 mol H 完全反应放出a kJ的热量,依据下表数据,下列说法中错
2 2 2
误的是
化学键 H—H I—I
断开1 mol化学键时吸收的能量/kJ b c
A.断开1 mol H—H和1 mol I—I所需能量大于断开2 mol H—I所需能量
B.该反应中反应物的总能量大于生成物的总能量
C.断开2 mol H—I所需能量为(a+b+c) kJ
19. 下列选项正确的是
D.向密闭容器中加入2 mol H 与2 mol I,充分反应后放出的热量小于2a kJ
2 2
二、主观题(4道题共56分)
23. Ⅰ.针对表中10种元素及由这些元素形成的单质和化合物,完成以下问题。
族
IA IIA IIIA IVA VA VIA VIIA
周期
2 ① ② ③
3 ④ ⑤ ⑥ ⑦ ⑧ ⑨
A. 图①可表示 晶体与 晶体反应的能量变化
4 ⑩
B. 图②中△H表示碳的燃烧热
(1)写出⑤和⑨两种元素组成的化合物的电子式________.
C. 若用铜丝代替图③仪器a进行相应的实验操作,测得中和热△H偏大
(2)③④⑤⑧的简单离子半径由大到小的顺序为___________(填离子符号)。
(3)写出元素⑥的单质与元素④最高价氧化物对应水化物反应的化学方程式___________。
D. 图④表示实验的环境温度为20℃,将物质的量浓度相等、体积分别为 、 的 、NaOH溶液
(4)能够比较元素⑧与⑨的非金属性强弱的依据是___________(填序号)。
a.氢化物酸性:⑧弱于⑨ b.⑨单质能与⑧氢化物成应得到⑧单质
混合,混合液的最高温度随V(NaOH)的变化(已知 )
c.单质与 反应:⑨比⑧容易 d.含氧酸的酸性;⑨强于⑧
的 Ⅱ.化学与生产、生活息息相关。请回答下列问题:
20. 下列有关说法正确 是
(5)工业废水中含有的重铬酸根离子 有毒,必须处理达标后才能排放。工业上常用绿矾
A. 已知 ,由此可知 气体在密闭容器中充 做处理剂,反应的离子方程式如下:
该离子方程式中的X应为__________(填微粒符号),当反应转移了 电子时,生成 的物质的量
分分解后可以放出 的热量
为__________(保留两位有效数字)。
B. 已知 ,则氢气的摩尔燃烧焓为:
24. Ⅰ.铁是用途最广泛的金属,探究铁与卤素的相关性质,某化学小组查阅资料得知:无水 为黑棕
C. 已知 , ,则 色固体,无水 为灰黑色固体,二者都易溶于水,并且有强烈的吸水性,能吸收空气里的水分而潮
解,加热易升华。
D. 含 的稀溶液与稀盐酸完全中和,放出 的热量,则稀醋酸和稀 溶液反应的 实验小组甲设计了制备无水 的实验,装置如图所示:
热化学方程式为:
21. 一定条件下,反应A(g)+3B(g) 2C(g)+2D(g)在容积不变的密闭容器中进行,达到化学平衡状态的标
志是
⇌
A. 单位时间内生成3nmolB,同时消耗2nmolC B. 容器内压强不随时间变化
C. 混合气体的密度不随时间变化 D. 单位时间内生成nmolA,同时生成2nmolD
3
学科网(北京)股份有限公司c.
根据盖斯定律,反应a的 为___________(用代数式表示),是反应___________(填“放热”或“吸
热”)
26. 溴及其化合物广泛用于医药、塑料阻燃剂等产品。溴元素主要以 形式存在于海水中,利用空气吹
出法从浓缩海水中提取溴的流程如图。
已知:①海水呈弱碱性②溴单质的沸点为
(1)b装置中反应的离子方程式_______。
(2)仪器F的名称为_______,装置F的作用_______。
(3)装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C中Ⅰ、Ⅱ、Ⅲ处依次放入的物质是
_______(填“甲”、“乙”、“丙”、“丁”)。
Ⅰ Ⅱ Ⅲ
回答下列问题:
甲 干燥的有色布条 碱石灰 湿润的有色布条 (1)浓缩海水通入 前需进行酸化,主要目的是_______。
(2)“吸收塔”中发生反应的离子方程式为_______。
乙 湿润的有色布条 无水氯化钙 干燥的有色布条
(3)吸收 后的空气进行循环利用,“吹出塔”中 吹出率与“吸收塔”中 流量的关系如图乙所示。
由图乙可知, 流量增大, 吹出率反而下降,原因是_______。
丙 干燥的有色布条 无水氯化钙 湿润的有色布条
丁 湿润的有色布条 浓硫酸 干燥的有色布条
Ⅱ.用质量分数为98%,密度为1.84 g·cm-3的浓硫酸配制200 mL 1.84 mol·L-1的稀硫酸,
(4)配制该溶液,应取用浓硫酸的体积为________。
(5)配制过程中若出现以下情况,对所配稀硫酸的浓度有什么影响?(填“偏大”“偏小”或“无影响”)
用量筒量取浓硫酸时,俯视量筒刻度线:________。
25. 回答下列问题。
I.(1)燃料电池是一种高效、环境友好型发电装置。一种燃料电池的电解质溶液为NaOH溶液,负极通
入NH ,正极通入空气,产物对环境无污染,则负极的电极反应式为_______,电路中每通过1 mol电
3
子,消耗标准状况下的氧气_______ L。
(4)“蒸馏塔”中温度应控制在_______(填标号)。
Ⅱ.工业制硫酸的反应之一为2SO (g)+O (g) 2SO (g)(放热反应),在2 L恒容绝热密闭容器中投入2.0
2 2 3
mol SO 和适当过量的O,在一定条件下充分反应,如图是SO 和SO 的物质的量随时间的变化曲线。 A. B. C. 以上
2 2 2 3
(5)“循环利用物质”为 、_______(填化学式)。
(2)下列叙述不能判断该反应达到平衡状态的是_______。
①容器中压强不再改变 ②容器中气体密度不再改变 (6)经该方法处理 的海水,最终得到 ,若溴的总提取率为 ,则原海水中 的浓度
③O 的物质的量浓度不再改变 ④SO 的质量不再改变
2 3 为_______ 。
(3)根据图示计算达到平衡时SO 的转化率为______。0~25 min
2
内,v(SO )=____mol/(L·min)
2
(4)甲醇是工业生产中一种重要的基础原料。利用CO、H 合成甲 醇
2 27. A、B、C、D是四种常见的有机物,在一定条件下的转化关系如图所示(部分反应条件省略)。
主要涉及以下反应:
a.
b.
4
学科网(北京)股份有限公司回答下列问题:
(1)反应①的反应类型为_______。 (2)丙烯酸中含有官能团的名称为_______。
(3)聚丙烯酸的结构简式为_______。 (4)反应③的化学方程式为_______。
(5)下列说法正确的是_______(填标号)。
a.若 中含有 杂质,可依次通过溴水、浓硫酸除杂
b.可用饱和碳酸钠溶液鉴别B、C、D
c.丙烯酸分子中所有原子可能共平面
d.丙烯酸乙酯可以发生取代、加聚、氧化、中和反应
(6)符合下列条件的有机物的同分异构体有_______种(不考虑立体异构),其中一氯代物有两种的同分异
构体的结构简式为_______。
a.分子式为 b.与D具有相同官能团
5
学科网(北京)股份有限公司