文档内容
高三化学试题参考答案(详解)
【答案】1.D
【解析】
A.晶体硅是良好的半导体材料,太阳能电池板的半导体材料主要成分是晶体硅,A正确;
B.石墨烯与足球烯(C )是由碳元素形成的不同单质,互为同素异形体,B正确;
60
C. 葡萄酒中通常含有微量的 , 可以起到杀菌的作用, 又是一种抗氧化剂,能
防止葡萄酒中的营养成分被氧化,起到保质作用,并有助于保持葡萄酒的天然果香味,C
正确;
D.深埋于地下生锈主要是发生的吸氧腐蚀,D错误。
【答案】2.C
【解析】
A.Na N与盐酸反应能够生成NH Cl和NaCl两种盐,A正确;
3 4
B.Na N和NaN 属于电解质,氨气属于非电解质,氢气是单质,不是化合物,B正确;
3 3
C.Na N和NaN 的电子式分别为: 和 ,故它们的阴
3 3
离子和阳离子的个数比分别为1:3和1:1,C错误;
D.由化学方程式可知,每生成1molNa N和8molNH 转移24mol ,所以标况下体积为
3 3
89.6L的NH 物质的量为4mol ,转移电子为12mol, D正确。
3
【答案】3.A
【解析】
A.25℃,101KPa下,气体摩尔体积大于22.4L/mol,11.2LSO 的物质的量小于0.5mol,所
2
含氧原子个数小于N ,A正确;
A
B. 常温下,pH=1的H SO 溶液中氢离子浓度是0.1mol/L,1L pH=1的H SO 溶液中的H+数目
2 4 2 4
为0.1N ,B错误;
A
C. NaHSO 溶液的体积未知,故无法计算其物质的量,也就无法求微粒数目,C错误;
4
D. 二氧化锰固体和浓盐酸在加热条件下生成氯气,制备Cl 的离子方程式为MnO +4H+
2 2
+2Cl- Mn2++Cl ↑+2H O,若用含有0.2molHCl的浓盐酸与足量MnO 反应制取Cl ,制得Cl
2 2 2 2 2
的个数小于0.1N ,原因是HCl挥发以及随着反应进行,盐酸浓度降低,MnO 与稀盐酸不
A 2
学科网(北京)股份有限公司反应,D错误。
【答案】4.B
【解析】
A. 向Ca(ClO) 溶液中通入少量SO ,二氧化硫具有还原性,会被次氯酸根离子氧化为硫酸
2 2
根,不能生成CaSO ,A错误;
3
B. 根据以少定多原则,NaHCO 溶液中加过量Ba(OH) 溶液生成碳酸钡、氢氧化钠和水,其
3 2
反应为 ,故B正确;
C.H S的摩尔燃烧焓为 ,利用已知条件中的数据进行计算,要注意H O应为
2 2
液态,H S燃烧的热化学方程式为:
2
,故C错误;
D.用铜电极电解氯化镁溶液,阳极Cu放电生成Cu2+,阴极氢离子得电子生成氢气,故D
错误。
【答案】5.A
【解析】
A.上述装置中先闭合K ,打开K 构成电解池装置,左侧石墨电极为阳极,溶液中的水发
1 2
生失电子的氧化反应生成氧气,右侧石墨电极作阴极,放出氢气;再闭合K ,打开K ,形
2 1
成原电池,右侧石墨电极为负极,氢气放电,左侧石墨电极为正极,氧气得电子,能达到
实验目的,A正确;
B.浓氨水滴到生石灰上可快速产生氨气,氨气密度比空气小,应采用向下排空气法收集,
但收集装置不能密闭,否则可能发生爆炸,B错误;
C.除去Na CO 固体中的NaHCO ,用加热的方法,但应在坩埚中进行灼烧,不能在蒸发皿
2 3 3
中灼烧固体,C错误;
D. 碳酸氢钠受热分解时生成碳酸钠、二氧化碳和水,试管口若向上倾斜,水蒸气冷凝回流
会导致试管炸裂,D错误。
【答案】 6.B
【解析】
A. 不溶于酸的白色沉淀有氯化银和硫酸钡,向某溶液中加入硝酸钡溶液有白色沉淀产生,
再加稀盐酸,沉淀不消失,由于硝酸根在酸性条件下有强氧化性,则原溶液中可能SO 2-、
3
学科网(北京)股份有限公司SO 2-或Ag+,A错误;
4
B.某溶液中加入硝酸酸化的硝酸钡溶液,没有白色沉淀产生,说明该溶液中不存在SO
、SO ,再滴加硝酸银溶液,有白色沉淀产生,该沉淀应不溶于硝酸,即该白色沉淀为
AgCl,原溶液中一定存在Cl-,B正确;
C.若原溶液中含有铁离子,实验现象相同。应该先加KSCN溶液,如果没有产生血红色,
然后再加入双氧水后产生血红色,说明原溶液中含有亚铁离子,C错误;
D.向某溶液中加入稀NaOH溶液,氨气极易溶于水,由于没有加热,导致氨气没有逸出,
则试纸不变蓝,不能判断原溶液中是否含有 ,D错误。
【答案】7.C
【解析】
A.装置①为简易气体发生装置,要求反应物之一必须为块状固体,而KMnO 为粉末状固
4
体,且能溶于水,达不到控制反应的发生与停止的目的,且生成的Cl 能被碱石灰吸收,所
2
以①中制取的气体是NO,A错误;
B. 装置内可能含有O ,NO可与O 反应产生NO ,若将Y装置中的药品换成浓硫酸,则无法
2 2 2
除去X中可能混有的NO 等气体杂质,且一般情况下,用U形管装置盛装的干燥剂应该为
2
固体,浓硫酸应该用洗气瓶洗气干燥,B错误;
C. 冰盐水的温度低,能将氧氯化氮冷却,并由气体转变为液体,以便收集于三颈烧瓶中,
C正确;
D. 实验时先通入氯气,把装置中的空气排出来,防止NO被氧气氧化,D错误。
【答案】8.B
【解析】A. 由题图可知Nafion膜的左边水失电子生成氧气,发生氧化反应,则铁元素发生
还原反应,Nafion膜的右边二氧化碳得电子生成甲酸,发生了还原反应,则铁元素发生氧
化反应,图中a、b分别代表 ,A正确;
B.甲酸与氧气燃烧生成二氧化碳和水为放热反应,根据盖斯定律,逆向为该人工光合作用
体系的总反应 为吸热反应,焓变大于0,ΔH=正反应
学科网(北京)股份有限公司活化能-逆反应活化能,所以E >E ,B错误;
a正 a逆
C.左侧 发生氧化反应失去电子生成O , 发生还原反应得到电子生成 。右侧
2
发生氧化反应失去电子生成 , 发生还原反应得到电子生成HCOOH的过程中,
催化剂表面反应的机理,一定有e-或h+参与,C正确;
D.该人工光合作用体系的总反应为 ,可知氧化产物
为O ,还原产物为HCOOH,根据方程式系数两者比为1:2,D正确。
2
【答案】9.D
【解析】
A.分解水总反应为吸热反应,在此过程中,水的分解分两步,根据盖斯定律,若反应Ⅱ
是放热反应,则反应Ⅰ一定是吸热反应,A正确;
B.焓变的大小取决于反应物和生成物能量的大小,催化剂不影响焓变,B正确;
C.该过程中碳纳米点是碳单质、但碳原子之间存在共价键。氮化碳是化合物、存在共价键。
H O、H O 、H 、O 等均只含共价键,所以图中物质构成中均只由共价键构成,C正确;
2 2 2 2 2
D. 碳量子点是一类具有显著荧光性能的零维碳纳米材料只含碳原子,属于碳单质,与胶粒
直径吻合,但是需要分散到分散剂才能形成胶体, D错误。
【答案】10.答案C
【解析】A.根据产品室要得到 ,可以确定Co2+需要通过A膜到达产品室,同
理HPO -也需要通过C膜到达产品室。所以A正确
2 2
B. 根据得失电子守恒可知1molC 对应1molH ,所以B正确
O 2
C. 增加2mol产品对应转移4mol电子,根据正极反应PbO +2e-+SO 2-
2 4
+4H+=PbSO +2H O,消耗8molH+,C错误
4 2
D.考虑到HPO 为二元弱酸,HPO 为一元弱酸。碱性条件下其离子方程式为Co2++
3 3 3 2
+3OH-=Co+ +2H O 正确
2
【答案】11.A
【解析】
学科网(北京)股份有限公司A.溴蒸气与水反应可生成 和 , 与 溶液反应生成淡黄色 沉淀,
与水反应生成 , 与 溶液不反应,现象不同,能鉴别,A正确;
B.反应后,浓硫酸有剩余,浓硫酸的稀释应该是酸入水,因此应该将试管中的溶液加入到
水中,如果溶液呈蓝色,说明Cu被氧化成Cu2+,B错误;
C.盐酸易挥发, 中混有 , 与 溶液反应也会产生白色沉淀,故无法确
定酸性 ,无法证明非金属性 ,故C错误;
D.向浓 中插入红热的炭,产生红棕色气体,也可能是浓 受热分解产生的 ,
无法证明是炭与浓 反应生成的 ,D错误。
【答案】12. C D
【解析】
A. 焙烧后的酸性气体为HF,不可以使用陶瓷容器,A错误
B. 滤渣1的成分主要有二氧化硅、磷酸铁、磷酸钙(硫酸钙),至少三种 B错误
C. 硅酸胶体胶粒带负电,可以使氢氧化铝胶体聚沉。C正确
D. ↑ D正确
【答案】13. A D
【解析】
A. 转移2mol电子时,Cu(1)极析出64g铜,同时有96g硫酸根从乙室到甲室,共减少
160g,A错误
B. 正确
C. 停止工作时已有2mol硫酸根发生了转移,整个电路中转移2mol电子,根据电荷守恒有
4molOH-从N→M,C正确
D. 恢复原浓差Cu(2)电极需发生还原反应,Cu2+放电析出铜单质,所以和电源负极相连,
D错误。
【答案】14. C D
【解析】A. 根据题目信息,“熔融煅烧”出来的产物显墨绿色可得KMnO ,A正确
2 4
学科网(北京)股份有限公司B.通入CO 可将可溶性铝盐转化为氢氧化铝,将硅酸盐转化为硅酸沉淀,所以B正确,C
2
错误。
D.盐酸中氯离子可还原高锰酸根,影响目标产物的产量,D错误。
【答案】15. B D
A. 根据化合价代数和为0可得出该关系式,A正确
B. 根据题目信息可得M为Fe3+,N为Fe2+,Fe3+遇亚铁氰化钾产生蓝色沉淀,B错误。
C. 加少量CuO通过调节PH除去Fe3+,C正确。
D. 根据得实电子守恒,理论上消耗标准状况下约11.2L的氧气,D错误。
三、非选择题:本题共5小题,共60分
16.(12分)
Ⅰ.CO (g)+3H(g)=CH OH(g)+HO(g) ΔH=-46 kJ·mol-1(2分))
2 2 3 2
Ⅱ.-90 (1分)
Ⅲ.(1) ①2CO + 10H+ + 10e— = CHCHO + 3H O (1分) 7.2 (2分)
2 3 2
② 此时阴极主要为氢离子放电(1分)
(2)CO2— + 4e— = C + 3O2— (1分) 4N (2分)
3 A
(3)Cu (1分) *COOH + H+ +e— = *CO + H O(1分)
2
【解析】
Ⅰ.焓变等于反应物的总键能减去生成物的总键能。
Ⅱ.根据题干信息可知,
= +2 - -2 。
=0KJ/mol-2×242KJ/mol+394KJ/mol-0KJ/mol=-90KJ/mol;
Ⅲ.(1)①铜电极为阴极,铜电极上产生CHCHO的电极反应式为
3
2CO + 10H+ + 10e— = CHCHO + 3H O
2 3 2
若铜电极上只产生3.2gCH ,则说明转移了1.6mol电子,发生反应CO + 8H+ + 8e— = CH +
4 2 4
2HO,铜极区溶液质量变化了7.2g
2
②当PH过低时,阴极主要为氢离子放电,导致有机物产率降低。
(2)由图可知, 电极CH→CO ,C元素化合价升高,则为阳极;Ni电极碳元素
4 2
价态降低得电子,故Ni电极为阴极,电极反应式为CO2— + 4e— = C + 3O2— ;
3
②Ni-YSZ电极为阳极,电极反应式为CH+2O2--4e-═CO +2H ,生成的CO 与氧离子结合生
4 2 2 2
学科网(北京)股份有限公司成CO2—,故理论上,生成1mol二氧化碳转移电子数为4N ;
3 A
(3)若还原产物主要为CH 时,应选择Cu作催化剂,因为Cu对CO的吸附能力远大于
4
Au,且Cu吸附CO后不易脱离,第1步是C与催化剂活性位点相连,排除Sn;Au对CO
的吸附能力较小,易脱离;Cu对CO的吸附能力强,不易从催化剂表面脱离。
根据图中信息可知,电极反应式为 *COOH + H+ +e— = *CO + H O
2
17.(12分)
(1)赶尽反应装置中的空气,将四氯化碳吹入管式炉中(2分)(解释合理即可)
(2)Cr O
2 3
(3)还原Cr3+为Cr2+,加快反应的进行(1分)
(4) c(1分)
(5)①作反应物②作萃取剂(2分,各1分)
(6)溶剂可循环使用,使用量减少;生成物溶于 被分离,可提高转化率(2分)
(7)61.42(2分)
【解析】
(1)本实验持续通入 的目的是赶走体系中原有的空气和将四氯化碳吹入到管式炉中。
(2)反应管的温度升到660℃时发生反应,生成 和 (光气),根据原子守恒配平
其化学方程式为 。
(3) 是反应的催化剂,Zn具有还原性,与 反应生成 ,加快反应的进行
(5) 易溶于四氢呋喃,故双颈烧瓶中四氢呋喃除作为反应物外还有一个用途
是萃取剂;
(6)本实验使用索氏提取器的优点是:溶剂可循环使用,使用量减少;生成物溶于
被分离,可提高转化率。
(7)根据铬元素守恒可知, 的物质的量为0.01mol,理论上可制得
学科网(北京)股份有限公司,即 ,所以本实验的产率为 。
18.【答案】(1) CaSO Fe(OH) (2分,各1分) 过量的CaCO 会使Al3+水解彻底,
4 3 3
形成Al(OH) 沉淀,而失去吸收SO 的能力(2分)
3 2
(2)SO 被循环液吸收生成的SO 2—易被氧化为SO 2—,使循环液失去吸收SO 作用(2
2 3 4 2
分)
(3)0.59(2分)。
(4)① NaHCO 、 NaSO (2分,各1分) 环节II (1分)
3 2 3
②b(1分)
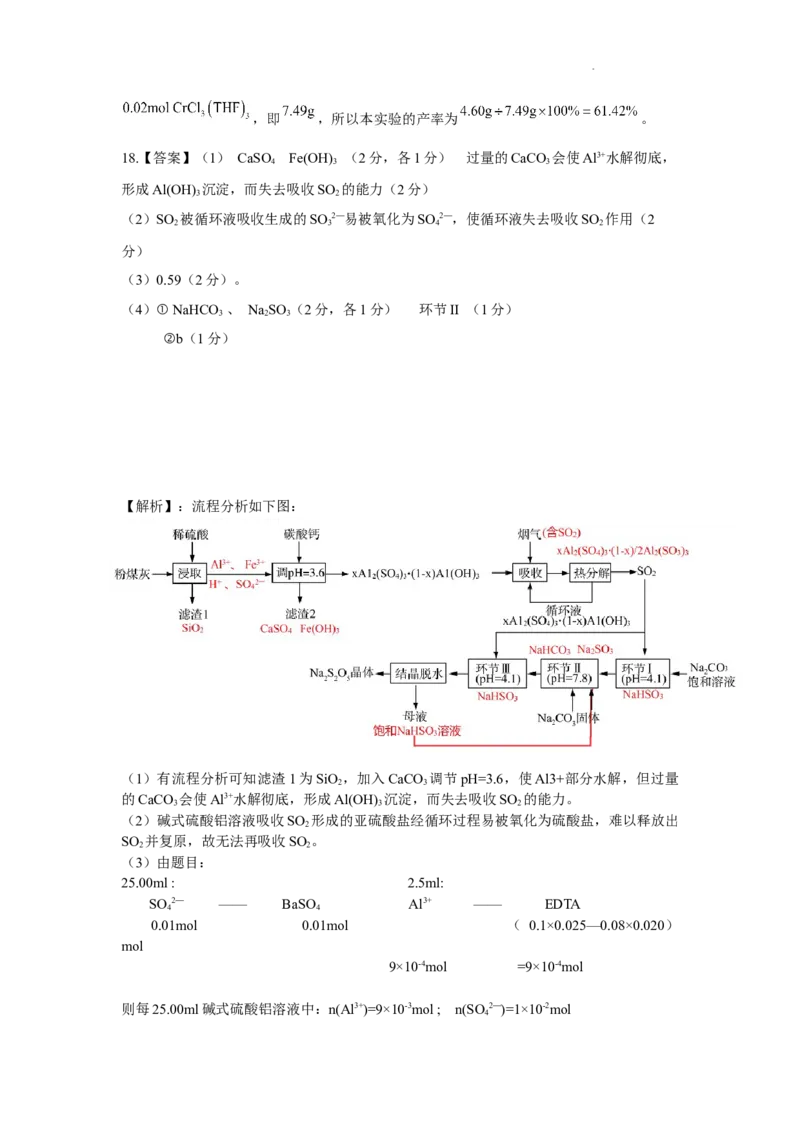
【解析】:流程分析如下图:
(1)有流程分析可知滤渣1为SiO ,加入CaCO 调节pH=3.6,使Al3+部分水解,但过量
2 3
的CaCO 会使Al3+水解彻底,形成Al(OH) 沉淀,而失去吸收SO 的能力。
3 3 2
(2)碱式硫酸铝溶液吸收SO 形成的亚硫酸盐经循环过程易被氧化为硫酸盐,难以释放出
2
SO 并复原,故无法再吸收SO 。
2 2
(3)由题目:
25.00ml : 2.5ml:
SO 2— —— BaSO Al3+ —— EDTA
4 4
0.01mol 0.01mol ( 0.1×0.025—0.08×0.020)
mol
9×10-4mol =9×10-4mol
则每25.00ml碱式硫酸铝溶液中:n(Al3+)=9×10-3mol ; n(SO 2—)=1×10-2mol
4
学科网(北京)股份有限公司由化学式xAl (SO )·(1-x)Al(OH) 可得:
2 4 3 3
n(Al3+) : n(SO 2—)=(2x + 1-x):3x = 9:10 解得:x=0.59
4
(4)①由溶液的pH,环节I、II、III的反应过程依次为:
环节I:SO + CO2— + H O = 2HSO — + CO
2 3 2 3 2
环节II:2HSO — + CO2— = SO 2— + CO2—
3 3 3 3
环节III:SO + SO 2— + H O = 2HSO — ; SO + CO2— + H O = 2HSO — + CO
2 3 2 3 2 3 2 3 2
经过3个环节得到过饱和NaHSO 溶液,经脱水结晶得焦亚硫酸钠溶液。母液为饱和的亚
3
硫酸氢钠溶液,可回到环节II继续反应,提高S元素的利用率。
②焦亚硫酸钠含+4价S,易被氧化,所以不可过分搅拌。且用浓硫酸脱水工序复杂,
污染、腐蚀严重。而真空干燥既可以加快水的蒸发速度,又不会使产品变质。b为最佳答
案。
19.(12分)
(1)hcdabg(1分)
(2) 恒压滴液漏斗(1分)
(3)液面上方有黄绿色气体 (1分)
使生成的 NaOH 转化为 NaClO 继续参与反应,以提高原料利用率(1分)
C HNO+9Cl+3H O 3NCl +3CO +9HCl(2分)
3 3 3 3 2 2 3 2
(4)①250mL容量瓶、胶头滴管(2分)
②淀粉溶液(1分) 95.1 (2分)
③ac (1分)
【解析】
装置E为制取氯气,装置B为饱和食盐水,可以吸收氯气中的HCl,将生成的氯气通入A
装置中,与X反应制备NaClO,A装置中生成的NaClO与氰尿酸C HNO 制得二氯异氰
3 3 3 3
尿酸钠,最后用D装置中NaOH溶液吸收尾气中的氯气。
(1) 根据以上分析,按气流从左至右方向组装,则导管连接顺序为hcdabg
(2) 恒压滴液漏斗可以平衡气压,使液体能够顺利滴下
(3) 待装置A液面上方有黄绿色气体时,说明NaOH溶液与Cl 已经完全反应,再由三颈烧
2
瓶上口加入C HNO 固体;由已知信息可知,加入 C HNO 固体后反应为:2NaClO+
3 3 3 3 3 3 3 3
C HNO=C NOClNa+NaOH+HO,该反应过程中生成了NaOH,故仍需不断通入Cl
3 3 3 3 3 3 3 2 2 2
以增大NaOH的利用率,使反应生成的NaOH再次生成NaClO,提高原料的利用率;
副反应 C HNO 为与氯气发生反应生成 NCl 和 CO 该副反应的化学方程式:
3 3 3 3 3 2
学科网(北京)股份有限公司;
(4)①需要的玻璃仪器还有250mL容量瓶、胶头滴管,
②根据题目信息可知,淀粉溶液作为指示剂;
由已知反应不难找出关系式为: ,n(HClO)= n( )
③a.碘量瓶中加入的稀硫酸偏少不能将所有的碘离子进行转化,导致消耗NaSO 的量减小,
2 2 3
导致测定值偏低;
b.滴定管在滴定前未排气泡,滴定后气泡消失,说明读出的数据偏大,导致测定值偏高;
c.读数时,滴定前仰视、滴定后俯视,将使V偏低,故将导致样品有效氯测定值偏低。
故选答案ac;
20. 【答案】(12分)
(1)2MoS + 7O 2MoO + 4SO (2分)
2 2 3 2
(2)可使Mo元素被进一步充分氧化(1分)
(3)SiO (1分) 防止SiO 溶解生成SiO2—使产品不纯(1分)
2 2 3
(4)浓氨水(1分)
(5)降温至10℃之下结晶 (1分)
(6)1.8N (1分)
A
(7)KI(1分)当滴入最后半滴Pb(NO3)2溶液时,锥形瓶内生成亮黄色沉淀,且半分
钟内不恢复原色。(1分)
(2分)
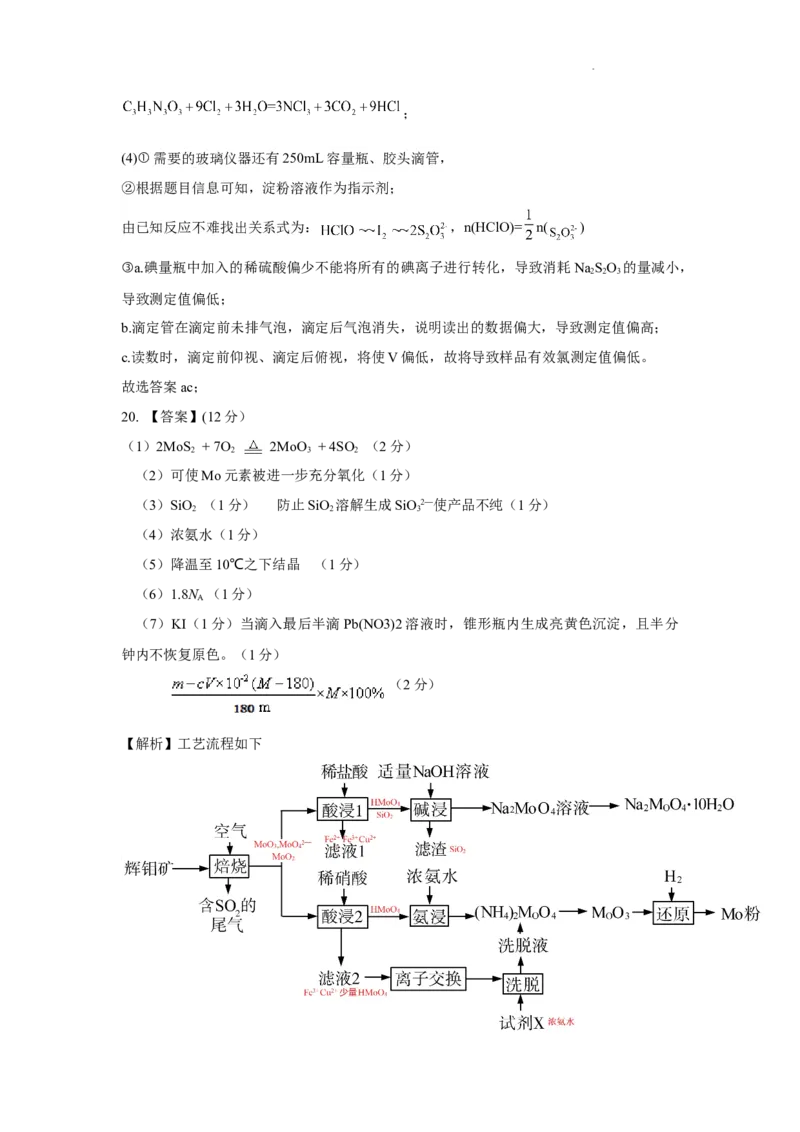
【解析】工艺流程如下
学科网(北京)股份有限公司(1)由氧化还原反应的配平可得:2MoS + 7O = 2MoO + 4SO
2 2 3 2
(2)由已知焙烧产物中还会存在MoO ,稀硝酸具有强氧化性,可使Mo元素被进一步充
2
分氧化,提高利用率。
(3)由流程可知滤渣为SiO,且为避免SiO 溶于NaOH溶于引入SiO2—杂质,需加入适
2 2 3
量NaOH。
(4)滤液2中含有少量的HMoO ,为提高产率,用阴离子交换树脂提取MoO 2— , 由
2 4 4
萃取反应2R—OH+MeMoO →R MoO +Me(OH) 可知,反萃取时需要使反应逆向移动,需
4 2 4 2
要较大浓度的OH—,且由流程可知洗脱液为(NH )MoO ,故试剂X为浓氨水。
4 2 4
(5)由溶解度曲线可知,应降温至10℃以下可结晶析出NaMoO ▪10H O。
2 4 2
(6)由图可知:
阳极反应:2Cl— —2e— = Cl
2
阴极反应:2HO + 2e— = H + 2OH—
2 2
Cl + 2OH— = Cl— + ClO— + 2H O
2 2
9ClO— + MoS + 6OH— = MoO 2— + 9Cl— + 2SO 2— + 3H O
2 4 4 2
可得对应关系: MoS —— 9ClO——— 18OH—
2
0.1mol 1.8mol
(7)沉淀滴定,指示剂生成的沉淀应颜色明显,且与滴定主要反应产物相比Ksp更大,应
选KI溶液为指示剂,当最后半滴指示剂加入时,锥形瓶内产生亮黄色沉淀,且30秒内不
消失。
计算过程如下:
学科网(北京)股份有限公司