文档内容
余姚中学 2024 学年第二学期质量检测
高二化学试卷
命题教师:周浩楠 审题教师:陆军苗
本试题卷分选择题和非选择题两部分,满分 100分,考试时间 90分钟。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5
K-39 Ca-40 Fe-56 Ni-59 Cu-64 Ag-108 I-127 Ba-137
一、选择题(本大题共 20 小题,每题 2分,总共 40 分。每个小题列出的四个备选项中只有一
个是符合题目要求的,不选、多选、错选均不得分)
1.下列物质属于强电解质的是
A.NaCl溶液 B.CuSO ·5H O C.冰醋酸 D.葡萄糖
4 2
2.下列事实不能用勒夏特列原理解释的是
A.工业合成氨采用400 ℃的高温 B.夏天打开啤酒瓶,有许多气泡冒出
C.可用浓氨水和氢氧化钠固体快速制取氨气 D.对CO中毒病人给予高压氧舱治疗
3.常温常压下,下列指定条件的各组离子一定能大量共存的是
A.透明的溶液中:
试卷第1页,共8页
M g 2 + 、H+、Cl−、 M n O −4
B.在酒精中:CrO2−、
2 7
S O 24 − 、H+、 N a +
C.加入苯酚显紫色的溶液: K + 、 B a 2 + 、 C l − 、 I −
D.0.1mol·L-1 FeCl 溶液中:NH +、Mg2+、SO 2-、NO -
3 4 4 3
4.下列化学反应的方程式正确的是
A.向CuSO 溶液中加入少量NaHS溶液:Cu2+ + S2- = CuS↓
4
B.铅酸蓄电池充电时的阳极反应:Pb2+ + 2H O - 2e- = PbO + 4H+
2 2
C.K [Fe(CN) ]溶液滴入FeCl 溶液中:K+ + Fe2+ + [Fe(CN) ]3- = KFe[Fe(CN) ]↓
3 6 2 6 6
D.水杨酸溶液中加入少量碳酸钠:
5.化合物H是一种低能量的甜味剂,其结构简式如图所示。其中X、Y、Z、W、M和Q是原子序数依次
增大的前20号元素,W和M位于同一主族。下列说法正确的是
A.简单离子半径: M Q
B.键角: M W
2
Y W
2
C.第一电离能:W > Z
D.Y和Z均能与X形成2种以上的化合物
6.SOCl 是一种无色易挥发的液体,可以用作锂电池的正极活性物质。研究表明在含Li+的
2
S O C l
2
溶液中加
入I ,可提高Li−SOCl 电池的性能,该电池放电时,正极的物质转变步骤如图所示。下列说法错误的是
2 2A.I 是该反应的催化剂
2
B.正极的电极反应式为
试卷第2页,共8页
2 S O C l
2
+ 4 L i + + 4 e −
I
2 S + S O
2
+ 4 L iC l
C.S、O、 C l 三种元素的电负性为 O C l S
D. S O
2
分子的 V S E P R 模型名称为V形
7.柠檬酸钙Ca (C H O ) 是一种常见的食品补钙剂。柠檬酸钙微溶于水,难溶于乙醇,在常温常压下稳
3 6 5 7 2
定,但在高温、潮湿或与强氧化剂接触时可能会发生分解反应。某学习小组以蛋壳为主要原料制备柠檬酸
钙的流程如下图:
下列说法正确的是
A.上述实验流程中可循环使用的物质是醋酸
B.上述实验流程中干燥柠檬酸钙时,高温干燥效果更好
C.上述实验流程中生成醋酸钙的离子方程式为 C a C O
3
+ 2 H + = C a 2 + + H
2
O + C O
2
D.与金属反应时,同浓度的柠檬酸的反应速率比醋酸慢
8.M是一种香料,其合成路线之一如图,下列说法正确的是
A.Y分子中所有原子共平面
B.M中碳原子的杂化类型均为sp3
C.X→Y的条件是NaOH水溶液、加热
D.Z的结构简式为CH CH=CHCOOCH
3 3
9.某苯的同系物分子式为C H ,经分析分子中除苯环结构外,不再含有其他环状结构,还有两个-CH ,
11 16 3
两个-CH -和一个 ,它可能的结构数目是
2
A.4 B.5 C.6 D.7
10.硅烷法制备多晶硅的核心反应 2 S iH C l
3
( g ) = S iH
2
C l
2
( g ) + S iC l
4
( g ) H 0 。已知v =
正
k
正
x 2 ( S iH C l
3
) ,
v =k x(SiH Cl )x(SiCl ),k 、k 分别为正、逆反应速率常数且只与温度有关,x为各组分的物质的
逆 逆 2 2 4 正 逆
量分数。在一恒容密闭容器中加入一定量的SiHCl (g),不同温度下反应,测得反应体系中SiHCl (g)的物
3 3
质的量分数随时间变化的关系如图所示,下列说法错误的是
A.当 v
正
( S iH C l
3
) = 2 v
逆
( S iH
2
C l
2
) 时可判断该反应已达平衡
B.平衡后温度由T 变为T ,
1 2
k
正
增大的倍数小于 k
逆
增大的倍数
C.平衡后恒温下再加入SiHCl (g),再达平衡时x(SiHCl )不变
3 3
k 1
D.T 温度下,平衡时 正 =
1 k 64
逆
11.磷的常见含氧酸化学式为H PO (x=2、3、4),其分子结构和亚磷酸与水形成的部分氢键如下图所示:
3 x下列说法不正确的是
...
A.
试卷第3页,共8页
H
3
P O
2
与足量NaOH溶液反应的离子方程式为: H
3
P O
2
+ O H -= H
2
P O -2 + H
2
O
B. H
3
P O
3
分子中P采取 s p 3 杂化
C.H PO 与水形成如图所示的环,使得羟基难以电离出H+
3 3
D.相同温度、相同浓度的稀溶液的酸性:H PO c(A-)>c(OH-)>c(HA)>c(H+)
C.P点溶液中由水电离产生的氢离子浓度为1.0×10-7 mol·L-1,溶液呈中性
D.当滴入NaOH溶液10 mL时,c(HA)+2c(H+)=c(A-)+2c(OH-)
13.25℃时,FeS、CuS和Ag S的沉淀溶解平衡曲线如图所示。已知:①相同条件下FeS溶解度大于CuS;
2
②25℃时,H S的电离平衡常数为 2 K a1 = 1 0 − 6 .9 7 、 K a 2 = 1 0 − 1 2 .9 0 。 p M = − lg c ( M ) / ( m o l L − 1 ) (M代表 F e 2 + 、 C u 2 +
或Ag+); p S = − lg c ( S 2 − ) / ( m o l L − 1 ) 。下列说法不正确的是
A.曲线③为Ag S的沉淀溶解平衡曲线
2
B.向含Cu2+的废水中加入FeS可除去Cu2+
C.若曲线②③所示物质的混合溶液中各离子浓度如J点所示,
c
( Cu2+)
加入Na S(s)后 变大
2
c
( Ag+)
D.FeS能溶于浓盐酸,CuS难溶于浓盐酸
14.恒温条件下,用图1所示装置研究铁的电化学腐蚀,测定结果如图2。下列说法错误的是A.AB段pH越大,析氢速率越大
B.AD段负极反应式为
试卷第4页,共8页
F e − 2 e = F e 2 +
C.BC段正极反应式主要为 O
2
+ 4 e − + 4 H + = 2 H
2
O
D.DE段溶液pH基本不变,可能的原因:相同时间内, 2 F e + O
2
+ 4 H + = 2 F e 2 + + 2 H
2
O 消耗 H + 的量与
4 F e 2 + + O
2
+ 1 0 H
2
O = 4 F e ( O H )
3
+ 8 H + 产生H+的量基本相同
15.灰锡与金刚石的晶体类型相同,其晶胞如图所示。下列有关说法不正确的是
A.一个灰锡晶胞中含有8个Sn原子
B.灰锡属于共价晶体,其熔点低于金刚石
C.若Sn−Sn键的键长为a pm,则晶胞参数为 2 a p m
D.灰锡中每个Sn原子周围与它距离最近的Sn原子有4个
16.在HY沸石催化下,萘与丙烯反应主要生成二异丙基萘M和N。下列说法正确的是
A.M和N互为同系物
B.M分子中最多有12个碳原子共平面
C.N的一溴代物有5种
D.萘的二溴代物有12种
17.鹰爪花根部含有的鹰爪甲素可用于治疗疟疾。结构如图所示,下列说法正确的是
A.含有4个手性碳原子
B.同分异构体的结构中可能含有苯环
C.能使酸性高锰酸钾溶液褪色
D.可在120C条件下烘干样品
18.有机物Z是合成抗病毒药物氧化白藜芦醇的中间体,其合成路线如图。下列叙述正确的是
A.鉴别X和Z可以用酸性高锰酸钾溶液
B.合成路线中反应①、反应②均属于取代反应
C.1molZ最多能与3molBr 发生加成反应
2
D.X、Y、Z三种物质中所有碳原子均一定共平面19.
试卷第5页,共8页
B r C l 、IF 、
5
B r F
3
等都属于卤素互化物,性质与卤素相似。液态 B r F
3
能类似于水发生微弱电离(2H O ⇌ H O+
2 3
+ OH-),产生阳离子M和一价阴离子N。下列说法不正确的是
...
A. I F
5
、 B r F
5
、 C lF
5
的沸点依次降低
B.一定条件下,苯( C
6
H
6
)与ClF发生反应的方程式为: C
6
H
6
+ C lF → C
6
H
5
F + H C l
C.ClF可使湿润的淀粉碘化钾试纸变蓝
D.阳离子M的空间结构与水分子类似
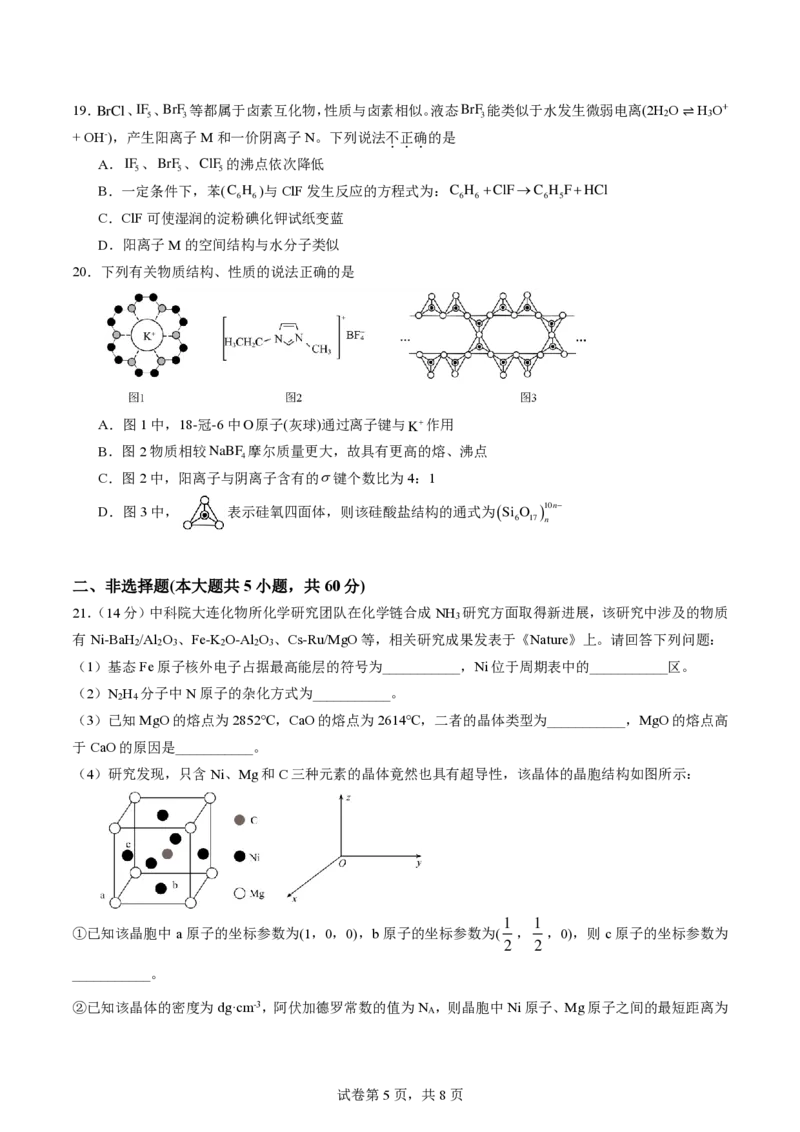
20.下列有关物质结构、性质的说法正确的是
A.图1中,18-冠-6中 O 原子(灰球)通过离子键与K+作用
B.图2物质相较 N a B F
4
摩尔质量更大,故具有更高的熔、沸点
C.图2中,阳离子与阴离子含有的键个数比为4:1
D.图3中, 表示硅氧四面体,则该硅酸盐结构的通式为 ( S i
6
O
1 7
) 1 0
n
n −
二、非选择题(本大题共 5小题,共 60分)
21.(14分)中科院大连化物所化学研究团队在化学链合成NH 研究方面取得新进展,该研究中涉及的物质
3
有Ni-BaH /Al O 、Fe-K O-Al O 、Cs-Ru/MgO等,相关研究成果发表于《Nature》上。请回答下列问题:
2 2 3 2 2 3
(1)基态Fe原子核外电子占据最高能层的符号为___________,Ni位于周期表中的___________区。
(2)N H 分子中N原子的杂化方式为___________。
2 4
(3)已知MgO的熔点为2852℃,CaO的熔点为2614℃,二者的晶体类型为___________,MgO的熔点高
于CaO的原因是___________。
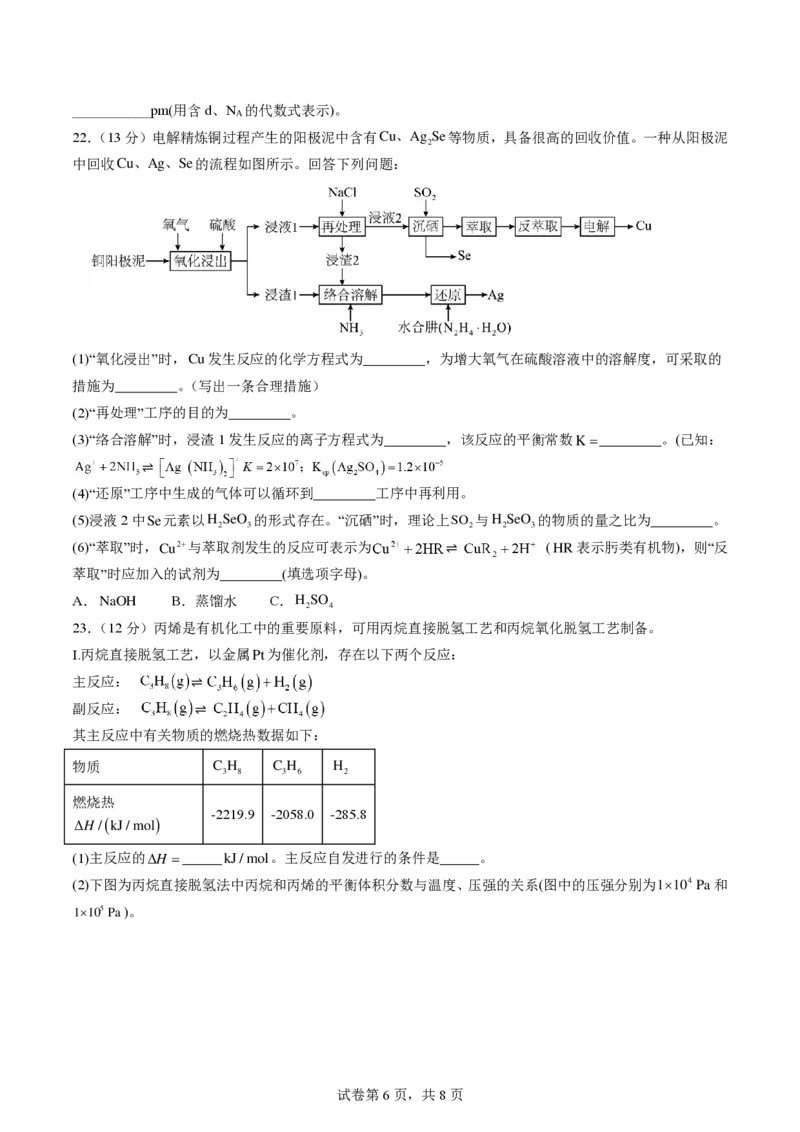
(4)研究发现,只含Ni、Mg和C三种元素的晶体竟然也具有超导性,该晶体的晶胞结构如图所示:
1 1
①已知该晶胞中 a原子的坐标参数为(1,0,0),b原子的坐标参数为( , ,0),则 c原子的坐标参数为
2 2
___________。
②已知该晶体的密度为dg·cm-3,阿伏加德罗常数的值为N ,则晶胞中Ni原子、Mg原子之间的最短距离为
A___________pm(用含d、N 的代数式表示)。
A
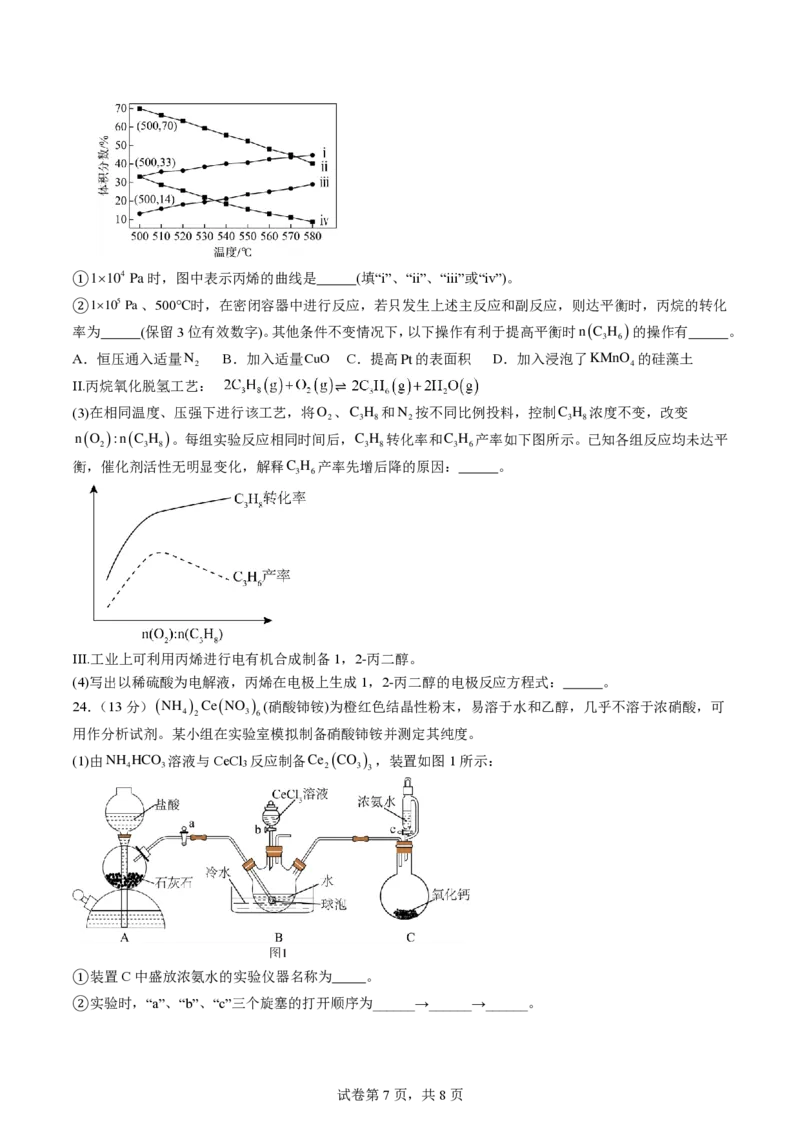
22.(13分)电解精炼铜过程产生的阳极泥中含有
试卷第6页,共8页
C u 、 A g
2
S e 等物质,具备很高的回收价值。一种从阳极泥
中回收 C u 、 A g 、 S e 的流程如图所示。回答下列问题:
(1)“氧化浸出”时, C u 发生反应的化学方程式为 ,为增大氧气在硫酸溶液中的溶解度,可采取的
措施为 。(写出一条合理措施)
(2)“再处理”工序的目的为 。
(3)“络合溶解”时,浸渣1发生反应的离子方程式为 ,该反应的平衡常数 K = 。(已知:
⇌
(4)“还原”工序中生成的气体可以循环到 工序中再利用。
(5)浸液2中Se元素以H SeO 的形式存在。“沉硒”时,理论上
2 3
S O
2
与 H
2
S e O
3
的物质的量之比为 。
(6)“萃取”时,Cu2+与萃取剂发生的反应可表示为 ⇌ ( H R 表示肟类有机物),则“反
萃取”时应加入的试剂为 (填选项字母)。
A. N a O H B.蒸馏水 C.H SO
2 4
23.(12分)丙烯是有机化工中的重要原料,可用丙烷直接脱氢工艺和丙烷氧化脱氢工艺制备。
I.丙烷直接脱氢工艺,以金属 P t 为催化剂,存在以下两个反应:
主反应: ⇌
副反应: ⇌
其主反应中有关物质的燃烧热数据如下:
物质 C H C H H
3 8 3 6 2
燃烧热
-2219.9 -2058.0 -285.8
ΔH /(kJ/mol)
(1)主反应的H = k J / m o l 。主反应自发进行的条件是 。
(2)下图为丙烷直接脱氢法中丙烷和丙烯的平衡体积分数与温度、压强的关系(图中的压强分别为1104 Pa和
1105Pa)。①1104 Pa时,图中表示丙烯的曲线是 (填“i”、“ii”、“iii”或“iv”)。
②
试卷第7页,共8页
1 1 0 5 P a 、500℃时,在密闭容器中进行反应,若只发生上述主反应和副反应,则达平衡时,丙烷的转化
率为 (保留3位有效数字)。其他条件不变情况下,以下操作有利于提高平衡时 n ( C
3
H
6
) 的操作有 。
A.恒压通入适量N B.加入适量CuO C.提高Pt的表面积 D.加入浸泡了KMnO 的硅藻土
2 4
II.丙烷氧化脱氢工艺: ⇌
(3)在相同温度、压强下进行该工艺,将 O
2
、 C
3
H
8
和 N
2
按不同比例投料,控制 C
3
H
8
浓度不变,改变
n ( O
2
) : n ( C
3
H
8
) 。每组实验反应相同时间后, C
3
H
8
转化率和 C
3
H
6
产率如下图所示。已知各组反应均未达平
衡,催化剂活性无明显变化,解释 C
3
H
6
产率先增后降的原因: 。
III.工业上可利用丙烯进行电有机合成制备1,2-丙二醇。
(4)写出以稀硫酸为电解液,丙烯在电极上生成1,2-丙二醇的电极反应方程式: 。
24.(13分) ( N H
4
)
2
C e ( N O
3
)
6
(硝酸铈铵)为橙红色结晶性粉末,易溶于水和乙醇,几乎不溶于浓硝酸,可
用作分析试剂。某小组在实验室模拟制备硝酸铈铵并测定其纯度。
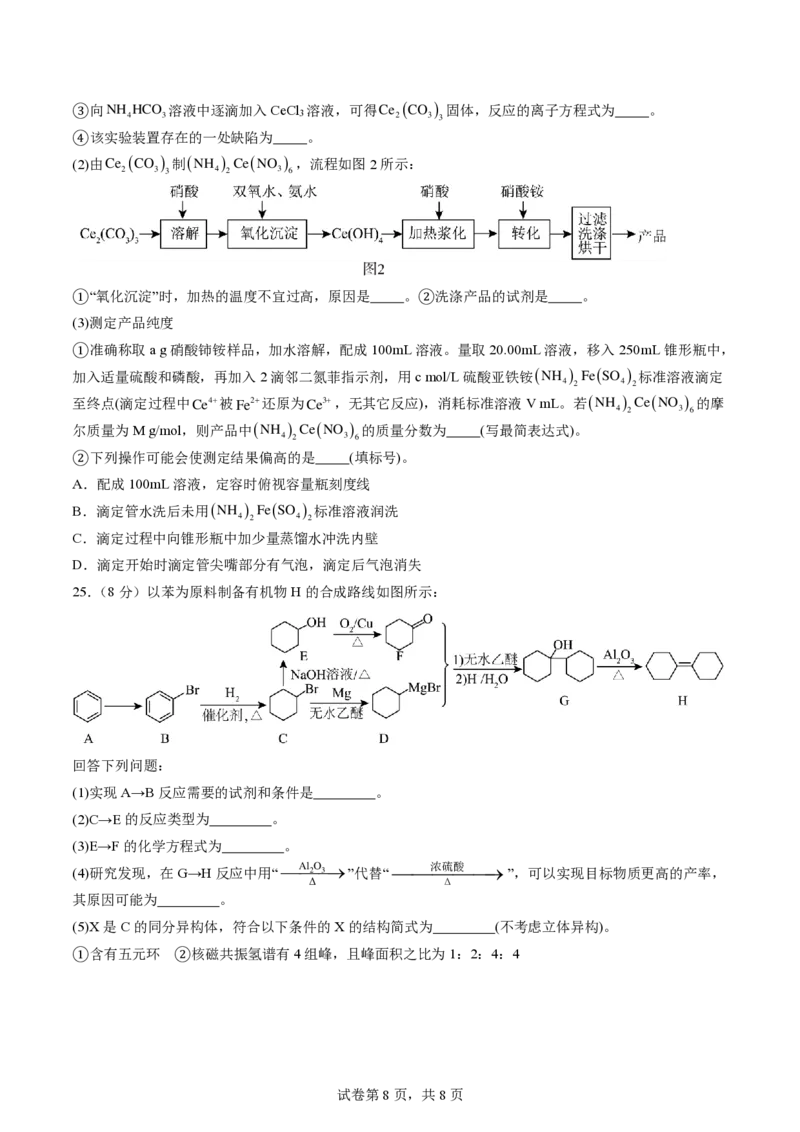
(1)由 N H
4
H C O
3
溶液与CeCl 反应制备Ce (CO ) ,装置如图1所示:
3 2 3 3
①装置C中盛放浓氨水的实验仪器名称为 。
②实验时,“a”、“b”、“c”三个旋塞的打开顺序为______→______→______。③向
试卷第8页,共8页
N H
4
H C O
3
溶液中逐滴加入CeCl 溶液,可得
3
C e
2
( C O
3
)
3
固体,反应的离子方程式为 。
④该实验装置存在的一处缺陷为 。
(2)由Ce (CO ) 制(NH ) Ce(NO ) ,流程如图2所示:
2 3 3 4 2 3 6
①“氧化沉淀”时,加热的温度不宜过高,原因是 。②洗涤产品的试剂是 。
(3)测定产品纯度
①准确称取a g硝酸铈铵样品,加水溶解,配成100mL溶液。量取20.00mL溶液,移入250mL锥形瓶中,
加入适量硫酸和磷酸,再加入2滴邻二氮菲指示剂,用c mol/L硫酸亚铁铵 ( N H
4
)
2
F e ( S O
4
)
2
标准溶液滴定
至终点(滴定过程中 C e 4 + 被Fe2+还原为 C e 3 + ,无其它反应),消耗标准溶液V mL。若 ( N H
4
)
2
C e ( N O
3
)
6
的摩
尔质量为M g/mol,则产品中(NH ) Ce(NO ) 的质量分数为 (写最简表达式)。
4 2 3 6
②下列操作可能会使测定结果偏高的是 (填标号)。
A.配成100mL溶液,定容时俯视容量瓶刻度线
B.滴定管水洗后未用 ( N H
4
)
2
F e ( S O
4
)
2
标准溶液润洗
C.滴定过程中向锥形瓶中加少量蒸馏水冲洗内壁
D.滴定开始时滴定管尖嘴部分有气泡,滴定后气泡消失
25.(8分)以苯为原料制备有机物H的合成路线如图所示:
回答下列问题:
(1)实现A→B反应需要的试剂和条件是 。
(2)C→E的反应类型为 。
(3)E→F的化学方程式为 。
(4)研究发现,在G→H反应中用“⎯A⎯l
2
O⎯3→”代替“⎯⎯浓⎯硫酸⎯⎯→”,可以实现目标物质更高的产率,
Δ Δ
其原因可能为 。
(5)X是C的同分异构体,符合以下条件的X的结构简式为 (不考虑立体异构)。
①含有五元环 ②核磁共振氢谱有4组峰,且峰面积之比为1:2:4:4