文档内容
湖南省常德市汉寿县第一中学2024-2025学年
高二下学期2月月考化学试卷
可能用到的相对原子质量:H-1 N-14 O-16 Na-23 V-51 Fe-56 Cu-64
一、单选题(每题 3 分,共 42 分)
1.下列事实不能用勒夏特列原理解释的是
A.浓氨水中加入氢氧化钠固体产生刺激性气味的气体
B.由 和 组成的平衡体系加压后颜色变深
C.实验室可用排饱和食盐水收集氯气
D.当我们打开可乐瓶盖时立即有气泡冒出
2.下列说法正确的是
A.2p、3p、4p能级的轨道数依次增多
B.基态氮原子核外电子空间运动状态有5种
C.焰色试验中可用无锈铁丝的原因是铁灼烧时不会产生发射光谱
D.K和Cu元素的最外层电子数均为1,故均位于周期表中的s区
3.下列有关阿伏加 德罗常数N 的说法正确的是
A
A.标准状况下,2.24 LSO 所含的原子总数为0.4N
3 A
B.将足量的CO 通入7.8 g Na O 中,充分反应后转移的电子数为0.2N
2 2 2 A
C.一定条件下,6.4g Cu与足量硫粉充分反应转移的电子数为0.1N
A
D.熔融状态下,8.4 g NaHCO 中所含离子总数为0.2N
3 A
4.下列说法错误的是
A. 不符合泡利原理
B.p能级能量一定比s能级的能量高
C.2p和3p轨道形状均为哑铃形,3p的半径比2p大
D.基态N原子的轨道表示式为 ,违背了洪特规则
5.下列叙述中,正确的是
A.各电子层含有的原子轨道数为2n B.各电子层的能级都是从s能级开始到f能
级结束
C.冰融化时,分子中氢氧键发生断裂 D.金属晶体中含有离子,但不存在离子键6.下列实验操作对应的现象与结论均正确的是
选
实验操作 现象 结论
项
含有酚酞的 溶液中加入
溶液红色
A 少量 固体,观察溶液颜色 证明 溶液中存在水解平衡
变浅
的变化
用广泛 试纸测定 测得溶液 溶液呈酸性,证明 在
B
溶液的酸碱性 水中的电离程度大于水解程度
烧瓶内气
将充有 的密闭烧瓶放入热
C 体颜色变
水中
深
缓慢加热 溶液pH 溶液中 逐渐增大, 逐渐
D
溶液至 逐渐减小 减小
A.A B.B C.C D.D
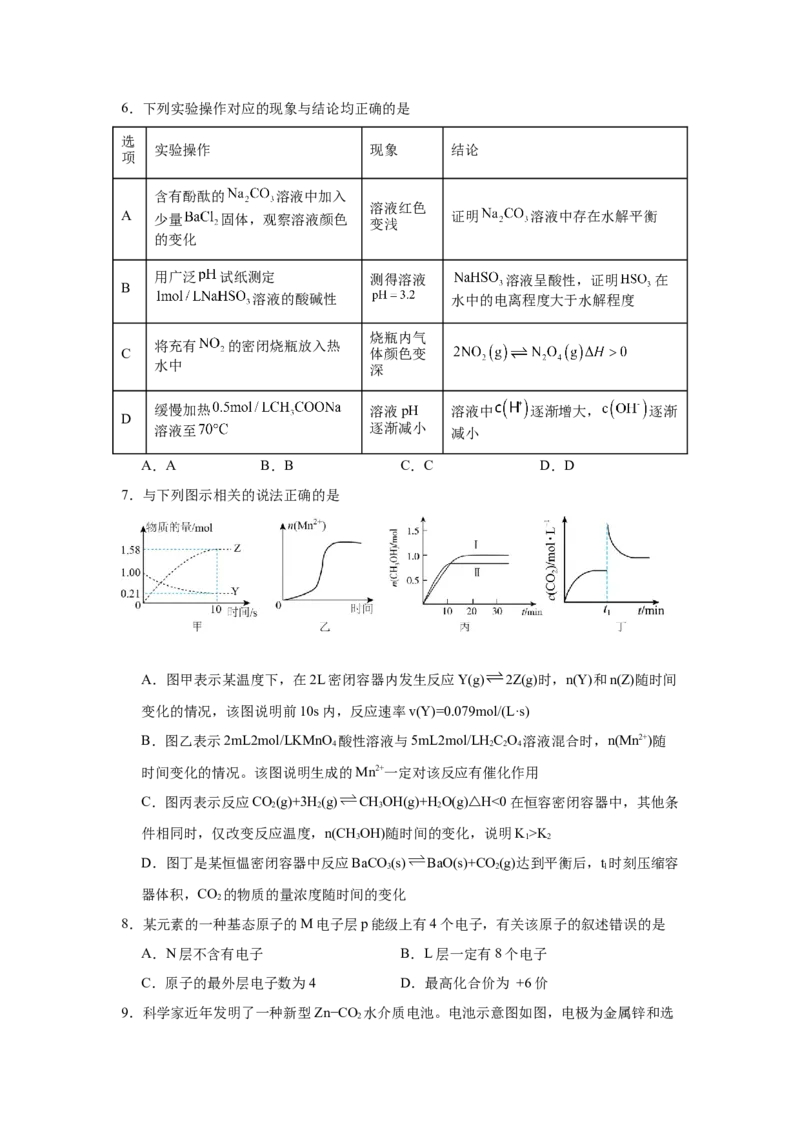
7.与下列图示相关的说法正确的是
A.图甲表示某温度下,在2L密闭容器内发生反应Y(g) 2Z(g)时,n(Y)和n(Z)随时间
变化的情况,该图说明前10s内,反应速率v(Y)=0.079mol/(L·s)
B.图乙表示2mL2mol/LKMnO 酸性溶液与5mL2mol/LH C O 溶液混合时,n(Mn2+)随
4 2 2 4
时间变化的情况。该图说明生成的Mn2+一定对该反应有催化作用
C.图丙表示反应CO(g)+3H(g) CHOH(g)+H O(g)△H<0在恒容密闭容器中,其他条
2 2 3 2
件相同时,仅改变反应温度,n(CHOH)随时间的变化,说明K>K
3 1 2
D.图丁是某恒愠密闭容器中反应BaCO (s) BaO(s)+CO (g)达到平衡后,t时刻压缩容
3 2 l
器体积,CO 的物质的量浓度随时间的变化
2
8.某元素的一种基态原子的M电子层p能级上有4个电子,有关该原子的叙述错误的是
A.N层不含有电子 B.L层一定有8个电子
C.原子的最外层电子数为4 D.最高化合价为 +6价
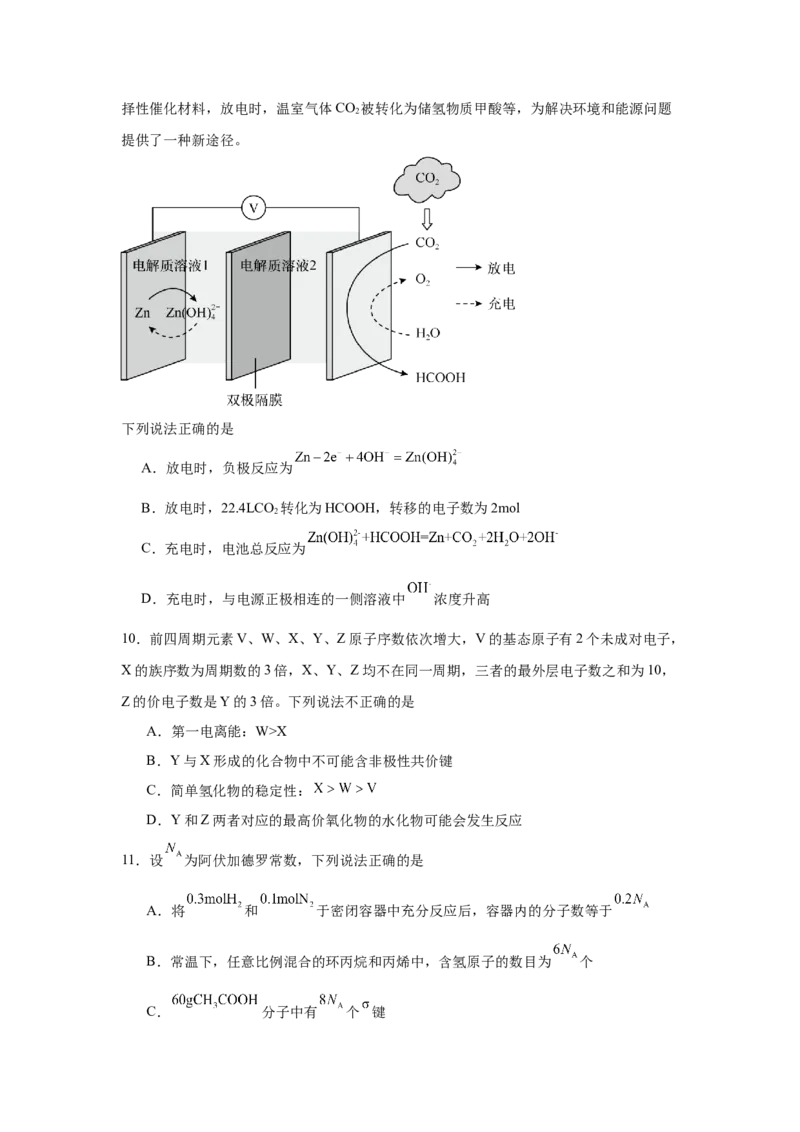
9.科学家近年发明了一种新型Zn−CO 水介质电池。电池示意图如图,电极为金属锌和选
2择性催化材料,放电时,温室气体CO 被转化为储氢物质甲酸等,为解决环境和能源问题
2
提供了一种新途径。
下列说法正确的是
A.放电时,负极反应为
B.放电时,22.4LCO 转化为HCOOH,转移的电子数为2mol
2
C.充电时,电池总反应为
D.充电时,与电源正极相连的一侧溶液中 浓度升高
10.前四周期元素V、W、X、Y、Z原子序数依次增大,V的基态原子有2个未成对电子,
X的族序数为周期数的3倍,X、Y、Z均不在同一周期,三者的最外层电子数之和为10,
Z的价电子数是Y的3倍。下列说法不正确的是
A.第一电离能:W>X
B.Y与X形成的化合物中不可能含非极性共价键
C.简单氢化物的稳定性:
D.Y和Z两者对应的最高价氧化物的水化物可能会发生反应
11.设 为阿伏加德罗常数,下列说法正确的是
A.将 和 于密闭容器中充分反应后,容器内的分子数等于
B.常温下,任意比例混合的环丙烷和丙烯中,含氢原子的数目为 个
C. 分子中有 个 键D.标况下, 溶于水得到的溶液中, 和 的总数小于
12.有些科学工作者认为反应物变到生成物,要经过一个中间过渡状态,即反应物分子首
先形成活化络合物,反应物→过渡态→生成物,如图所示是 [中间过渡态]
的能量变化示意图。下列说法错误的是
A.反应速率的快慢与形成活化络合物的浓度有关
B.反应速率的快慢与活化络合物解离的速率有关
C.中间过渡态可能形成了
D.加入催化剂会使反应的 和E的数值均变小
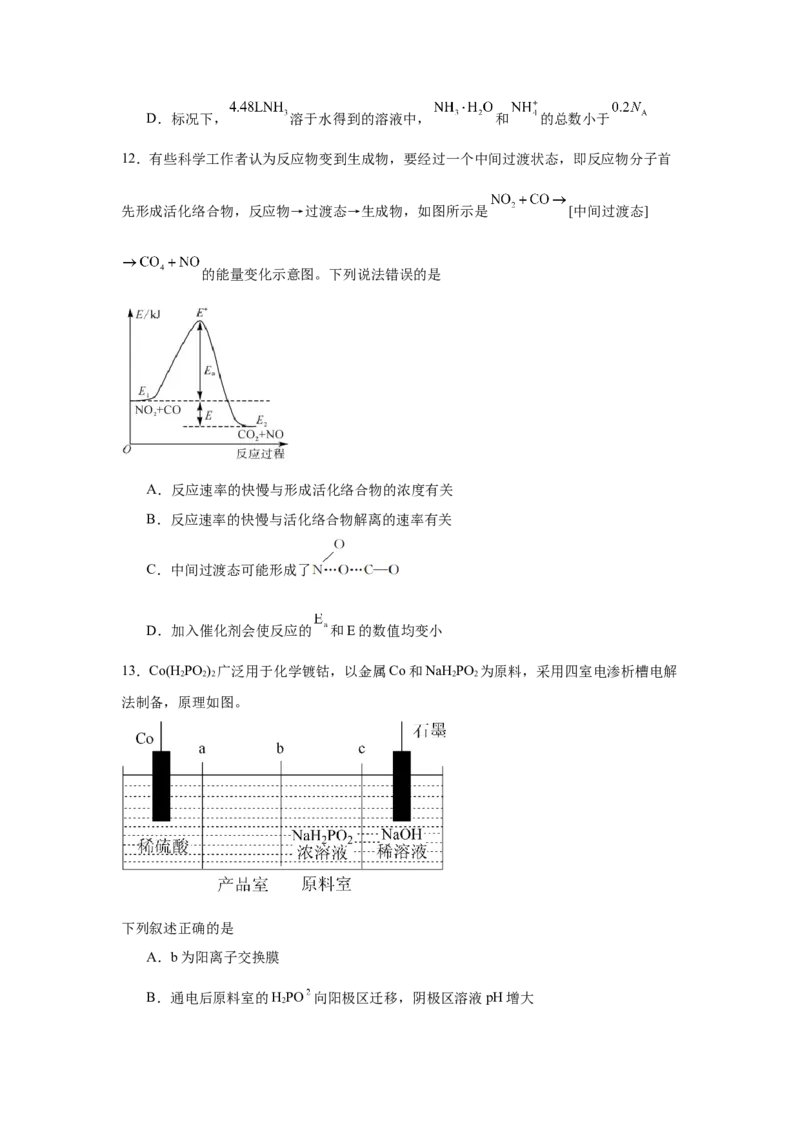
13.Co(HPO ) 广泛用于化学镀钴,以金属Co和NaH PO 为原料,采用四室电渗析槽电解
2 2 2 2 2
法制备,原理如图。
下列叙述正确的是
A.b为阳离子交换膜
B.通电后原料室的HPO 向阳极区迁移,阴极区溶液pH增大
2C.石墨电极反应为4OH--4e-=O ↑+2H O
2 2
D.当产生1molCo(H PO ) 时,产生标准状况下气体11.2L
2 2 2
14.常温下,用 溶液滴定 溶液所得滴定曲线
如图所示。下列说法正确的是
A.点①所示溶液溶质为 和 ,且
B.点②所示溶液中:
C.点①、②、③所示溶液中,水的电离程度最大的是③
D.滴定过程中可能出现:
二、非选择题(共 4 个大题,除标注外每空 2 分,共 58 分)
15.现有部分短周期元素的性质或原子结构如下表:
元素编号 元素性质或原子结构
A 有三个电子层,K、M层电子数之和等于L层电子数
B 短周期中金属性最强
C 常温下单质为双原子分子,氢化物的水溶液呈碱性
D 元素最高正价是+7价
(1)用化学用语回答下列问题:
①A元素在周期表中的位置 ;②C单质分子的电子式 ;
(2)元素D与元素A相比,非金属性较强的是 (用元素符号表示),下列表述中
能证明这一事实的是 (填选项序号)。
a.常温下D的单质和A的单质状态不同b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A最高价含氧酸的酸性弱于D最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
16.根据所学知识回答下列问题:
(1)将FeCl 溶液进行蒸干,得到的固体化学式为 。
3
(2)某温度下纯水的c(H+)=4×10-7mol•L-1,若温度不变,滴入稀醋酸,使c(H+)=2.0×10-
4mol•L-1,则此溶液中由水电离产生的c(H+)= mol•L-1。
(3)25℃时,在浓度均为1mol•L-1的(NH )SO 、(NH )CO、(NH )Fe(SO ) 三种溶液中,若
4 2 4 4 2 3 4 2 4 2
测得其中铵根离子浓度分别为a、b、c(单位为mol•L-1),由大到小顺序为 。
(4)在日常生活中经常用Al (SO ) 和NaHCO 混合溶液作灭火剂,其灭火原理为 (用
2 4 3 3
离子方程式表示)。
(5)某CuSO 溶液中含有Fe3+杂质,溶液中CuSO 的浓度为0.020mol•L-1,通常认为残留在溶
4 4
液中的离子浓度小于1×10-5mol•L-1时即沉淀完全(注:lg2=0.3),已知K [Cu(OH) ]=2×10-
sp 2
20,K [Fe(OH) ]=8×10-38,则除去Cu2+中的Fe3+选择的pH范围是 。
sp 3
(6)CH OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、
3
KOH(电解质溶液)构成,其中负极的电极反应式为: 。
17.某化学兴趣小组以废铁屑(含有碳、Fe O 杂质)为原料制备 晶体。具体的流
2 3
程如下:
试回答下列问题:
(1)请写出“酸溶”时发生反应的离子方程式: 、 。
(2)过滤时,需要用到的玻璃仪器有 。
(3)“氧化”过程中发生反应的化学方程式为 ,该反应中氧化剂是 ,
每消耗22.4LCl (标准状况下),转移的电子数为 。
2
(4)蒸发过程中需要用到玻璃棒,此时玻璃棒的作用是 。18.Ⅰ.研究水溶液中的粒子行为在研究中具有重要价值。
(1)常常用 溶液做焊接金属的除锈剂,又最大限度降低对设备的腐蚀,请结合化学用
语解释原因: 。
(2)根据表中所列三种溶液在25℃时的相关数据,按要求填空:
溶液 物质的量浓度 pH 用化学用语表示溶液显酸性/碱性的原因
(Ⅰ) 0.1 mol/L 3 ①
(Ⅱ) 0.1 mol/L 6 (不需要作答)
(Ⅲ) 0.1 mol/L 1 ②
(Ⅳ) 0.1 mol/L 11 ③
(3)比较溶液(Ⅱ)、(Ⅲ)、(Ⅳ)中 的大小关系是 。(填序号)
(4)溶液(Ⅰ)和(Ⅱ)中由水电离出的 之比是 。溶液(Ⅱ)中由水电离出的
mol ·L 。
(5)将相同体积的溶液(Ⅰ)与0.1 mol/L HCl溶液均稀释100倍,则溶液pH醋酸 盐酸
(填>、<、=下同),加等浓度的NaOH溶液至恰好完全反应,所需NaOH溶液的体积:醋酸
盐酸。
Ⅱ. 会对环境和人体健康带来极大的危害,工业上采取多种方法减少 的排放,将其
通入NaOH溶液中,得到 溶液。
(6) 溶液呈酸性,其原因是 。
(7)向 的 溶液中滴加一定浓度的 溶液,溶液中出现浑浊,pH降为2,
用平衡移动原理解释溶液pH降低的原因是 。
参考答案题号 1 2 3 4 5 6 7 8 9 10
答案 B B C B D A C C A B
题号 11 12 13 14
答案 D D B C
15. 第三周期第VIA族 Cl bde
16.(1)Fe(OH)
3
(2)8×10-10
(3)c>a>b
(4)Al3++3HCO =Al(OH) ↓+3CO ↑
3 2
(5)3.3≤pH<5
(6)CH OH-6e-+8OH-=CO +6H O
3 2
17.(1)
(2)玻璃棒、漏斗、烧杯
(3) Cl 2N (或 )
2 A
(4)搅拌,使液体受热均匀
18.(1)
(2)
(3)(Ⅲ) >(Ⅱ)>(Ⅳ)
(4)
(5) > =
(6)亚硫酸氢根离子电离大于水解
(7) ,加入 溶液,钙离子和亚硫酸根离子生成亚硫酸钙沉淀,导
致平衡正向移动,氢离子浓度变大,溶液pH值减小