文档内容
高三第一次大联考化学1
高三第一次大联考化学2
高三第一次大联考化学答案
1—5:DCBAC 6—10:BBADA 11—14:DCDC
部分解析:
11. D解析:基态S2-的核外电子排布式为1s22s22p63s23p6ꎬ
量子力学把电子在原子核外的一个空间运动状态成为
一个原子轨道ꎬ1s、2s、3s都有1个原子轨道ꎬ2p、3p都有
3个轨道ꎬ故基态S2-的核外电子共有9种空间运动状
态ꎬA错误ꎻ结合晶胞图ꎬFeS2晶体中ꎬ与Fe2+最近且等距
离相等的Fe2+有12个ꎬB错误ꎻ晶胞中ꎬFe2+位于S2-
2所
形成正八面体体心ꎬ该八面体的平面对角线为2apmꎬ则
八面体的边长为2
2apmꎬC错误ꎻ该晶胞中含有4个
Fe2+ꎬ4个S2-
2ꎬ令该晶体的密度为ρgcm
-3ꎬ则( a×
10
-10cm) 3(ρgcm
-3)NA=4×(56+32×2)gꎬρ=480
a3NA
×1030gcm
-3ꎬD正确ꎮ
12. C解析:根据惰性电极X极的反应物和生成物可知ꎬ惰
性电极X为阴极、惰性电极Y为阳极ꎬ电解时ꎬH
+由阳
极区通过质子交换膜进入阴极区ꎬA正确ꎻ根据电荷守
恒ꎬCH2CHCN+2H2O+2e
-C2H5CN+2OH
-ꎬB正
确ꎻM为电源的负极、N为正极ꎬN极的电势比M极电势
高ꎬC错误ꎻ制备己二腈的电极反应式为2CH2CHCN+
2H2O+2e
-NC(CH2) 4CN+2OH
-ꎬ故若制备己二腈
电解效率为85%ꎬ电路中通过4mole
-时ꎬ生成NC
(CH2) 4CN的质量为:4mol× 85%÷ 2× 108gmol
-1=
183.6gꎬD正确ꎮ
13. D解析:为制备(NH4) 2Fe(SO4) 26H2O产品ꎬ酸浸废
料ꎬ选用的酸应为硫酸ꎬ若为其他酸ꎬ则会引入杂质ꎬ试
剂Y为铁粉ꎬ将滤液1中的Fe3+还原为Fe2+ꎬA正确ꎻ
Fe2+具有强还原性ꎬ以及( NH4) 2SO4、Fe( SO47H2O、
(NH4) 2Fe(SO4) 26H2O的溶解度大小ꎬ从滤液②得到
(NH4) 2Fe(SO4) 26H2O产品过程中ꎬ需要控制好条件
和温度ꎬ同时还得防止(NH4) 2Fe(SO4) 26H2O其失去
部分结晶水ꎬB正确ꎻ电解熔融的Al2O3制备Alꎬ是在高
温下进行的ꎬ阳极生成的氧气可能会与石墨反应生成
CO或CO2ꎬC正确ꎻ要使溶液中Fe2+不沉淀ꎬ应满足
c(Fe2+)c2( OH
-) < Ksp[ Fe( OH) 2]ꎬ加入氨水后
c(Fe2+) =0.08molL
-1ꎬ即c(OH
-)<10
-7molL
-1ꎬKb
=
c(NH
+
4)c(OH
-)
c(NH3H2O)
=1. 8× 10
-5ꎬ此时溶液的中
c(NH
+
4)
c(NH3H2O)
>
180ꎬ
故
c(NH3H2O)
c(NH
+
4)
<
1
180ꎬ
n(NH3H2O)
n(NH
+
4)
< 1
180ꎬD错误ꎮ
14. C解析:随着盐酸的滴加ꎬ溶液中c(OH
-) 浓度逐渐减
小ꎬδ(ROH) 逐渐减小ꎬδ(R
+) 逐渐增加ꎬA正确ꎻ图中
ROH和R
+分布系数交点对应的溶液中ꎬc( ROH) =
c(R
+)ꎬ此时溶液的pH=4. 76ꎬKb=c(R
+)c(H
+)
c(ROH)
=
c(H
+)=10
-4.76ꎬ故ROH电离平衡常数的数量级为10
-5ꎬ
B正确ꎻ根据电荷守恒ꎬc( R
+) +c( Na
+) +c( H
+) =
c(OH
-) +c(Cl
-)ꎬc(Cl
-) =c(R
+) +c(Na
+) +c(H
+) -
c(OH
-)ꎬ当滴加盐酸的体积为20mL时ꎬc(Cl
-)=c(R
+)
+c(Na
+) +c( H
+) -c( OH
-) =0. 05molL
-1、c( R
+) <
c(ROH)ꎬ故当滴加盐酸的体积为20mL时ꎬc( ROH) +
c(Na
+)+c(H
+)-c(OH
-)>0.05molL
-1ꎬC错误ꎻ甲基橙
作指示剂时ꎬpH的变色范围为3.3~ 4.4ꎬ结合图像中的
信息ꎬ第二次滴定终点pOH的突跃范围为7.5~ 11.5ꎬpH
为6.5~2.5ꎬ故可以用甲基橙作指示剂ꎮD正确ꎮ
15. (14分)(1)6s26p3(2分)
(2)将含铋烧渣粉碎、搅拌或升温(其他答案合理也可给
分)(2分)
(3)SiO2(2分)
(4)温度升高ꎬ盐酸挥发ꎬ反应物浓度降低(2分)
(5)50∶1(2分)
(6)2.0~7.95(或2.0~8.0)(2分)
(7)5NaBiO3+2Mn2++14H
+5Na
++5Bi3++H2O+2Mn2+(2分)
16. (14分) (1) 4.3(1分)
胶头滴管、250mL容量瓶(2
分)
(2)①Ag2S(s) +4NH3H2O(aq)
2[Ag( NH3) 2]
+
( aq)
+
S2-
( aq)
+
4H2
O
( l)ꎬ
K
=
c2[Ag(NH3)
+
2]c(S2-)c2(Ag
+)
c4(NH3H2O)c2(Ag
+)
=Ksp( Ag2S) K2
稳
[Ag(NH3)
+
2] =6.3× 10
-50× (1.1×107) 2=7.6×10
-36<<
10
-5(2分)
②Ag2S+8HNO3(浓) =Ag2SO4+8NO2↑+4H2O(2
分)
B(1分)
生成白色沉淀(2分)
③加入浓氨水ꎬ过滤后ꎬ向滤液中滴加盐酸(答案合理给
分)(2分)
滴加盐酸后ꎬ出现白色沉淀(2分)
17. (15分)(1)ΔH1>ΔH3>ΔH2(2分)
(2)1.65(2分) 1.2(2分)
0.0083(1分) Ⅰ(1分)
(3)选择性膜吸附C2H4(g)ꎬ促进反应③平衡正向移动ꎬ
提高C2H4(g)的选择性(2分)
(4)①>(1分)
合成甲烷的反应是气体分子数减小的
反应ꎬ相同温度下ꎬ增大压强ꎬ平衡正向移动ꎬ甲烷的物
质的量分数增大(2分)
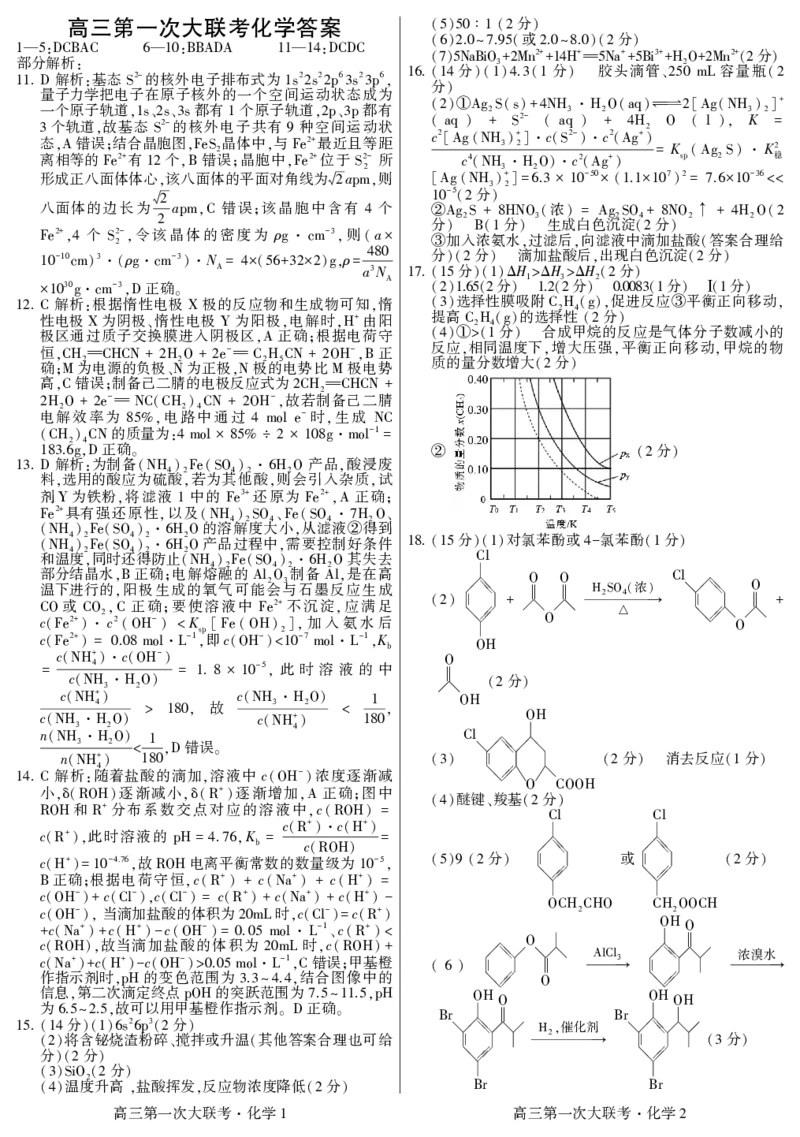
②
(2分)
18. (15分)(1)对氯苯酚或4-氯苯酚(1分)
(2)
OH
Cl
+
O
O
O
H2SO4(浓)
△
→
Cl
O
O
+
O
OH
(2分)
(3)
Cl
O
OH
COOH
(2分)
消去反应(1分)
(4)醚键、羧基(2分)
(5)9(2分)
OCH2CHO
Cl
或
CH2OOCH
Cl
(2分)
( 6)
O
O
AlCl3→
OHO
浓溴水→
Br
Br
OHO
H2ꎬ催化剂
→
Br
Br
OHOH
(3分)
{#{QQABBQAUgggAQBIAABhCEwUACgOQkhGAAQgOhAAIsAAASQNABAA=}#}