文档内容
济宁市第一中学
2024—2025 学年度第一学期质量检测(一)
高三化学
注意事项:
1.答题前,考生先将自己的姓名、考生号、座号填写在相应位置,认真核对条形码上的姓名、
考生号和座号,并将条形码粘贴在指定位置上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,
用橡皮擦干净后,再选涂其他答案标号。
3.回答非选择题时,必须使用 0.5 毫米黑色签字笔书写,按照题号在各题目的答题区域内作
答,超出答题区域书写的答案无效;在草稿纸,试题卷上答题无效。保持卡面清洁,不折叠,
不破损。
可能用到的相对原子质量: Li-7 C-12 N-14 O-16 Na-23 Cl-35.5 Ca-40 Fe-56 Cu-64
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.2024年7月第33届夏季奥林匹克运动会在法国巴黎举办。下列属于有机高分子材料的是
A.奥林匹克烯(五环标志)—C H B.举重运动员使用的“镁粉”—碳酸镁
19 12
C.篮球和排球运动鞋底—顺丁橡胶 D.跳高运动员使用的撑杆—碳纤维
2.在溶液中能大量共存的离子组是
A.H+、I-、Ba2+、NO- B.Fe3+、K+、CN-、Cl-
3
C.Na+、SiO2-、Br-、Ca2+ D.NH+、SO2-、CH COO-、HCO-
3 4 4 3 3
3.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.标准状况下,11.2 L Cl
2
溶于水,溶液中Cl-、ClO-和HClO的微粒数目之和为N
A
B.12 g石墨中含有的碳碳单键数目为2N
A
C.常温常压下,Na O 与足量H O反应,共生成0.2 mol O ,转移电子的数目为0.4N
2 2 2 2 A
D.0.1 mol/L的CH COONH 溶液显中性,1 L该溶液中含CH COO-的数目为0.1N
3 4 3 A
4.对于下列过程中发生的化学反应,相应离子方程式正确的是
A.向FeBr 溶液中通入足量的氯气:2Fe2++2Br⁻+2Cl =2Fe3++Br +4Cl⁻
2 2 2
B.泡沫灭火器的工作原理:Al3++3HCO-=Al(OH) ↓+3CO ↑
3 3 2
C.同浓度同体积NH HSO 溶液与NaOH溶液混合:NH+-+OH =×NH H O
4 4 4 3 2
D.将Cl 通入冷的石灰乳中制备漂白粉:Cl +2OH-=Cl-+ClO-+H O
2 2 2
5.对下列一些实验事实的理论解释,错误的是
高三化学试题 第1页(共8页)
{#{QQABaYAEogioAJIAABgCUwGICgAQkAAAASgGAEAEoAAAQQFABAA=}#}实验事实 理论解释
C原子处在4个F原子所组成的正方形中心,键的极性
A CF 是非极性分子
4
的向量和为零
B 一氟乙酸的K 大于一溴乙酸 F的电负性比Br的大
a
向加入过量氨水的硫酸铜溶液中加
C 乙醇的加入降低了[Cu(NH ) ]SO ·H O的溶解度
3 4 4 2
入乙醇,将析出深蓝色晶体
D P原子的第一电离能大于S原子 磷原子的电子排布是半充满的,比较稳定,电离能较高
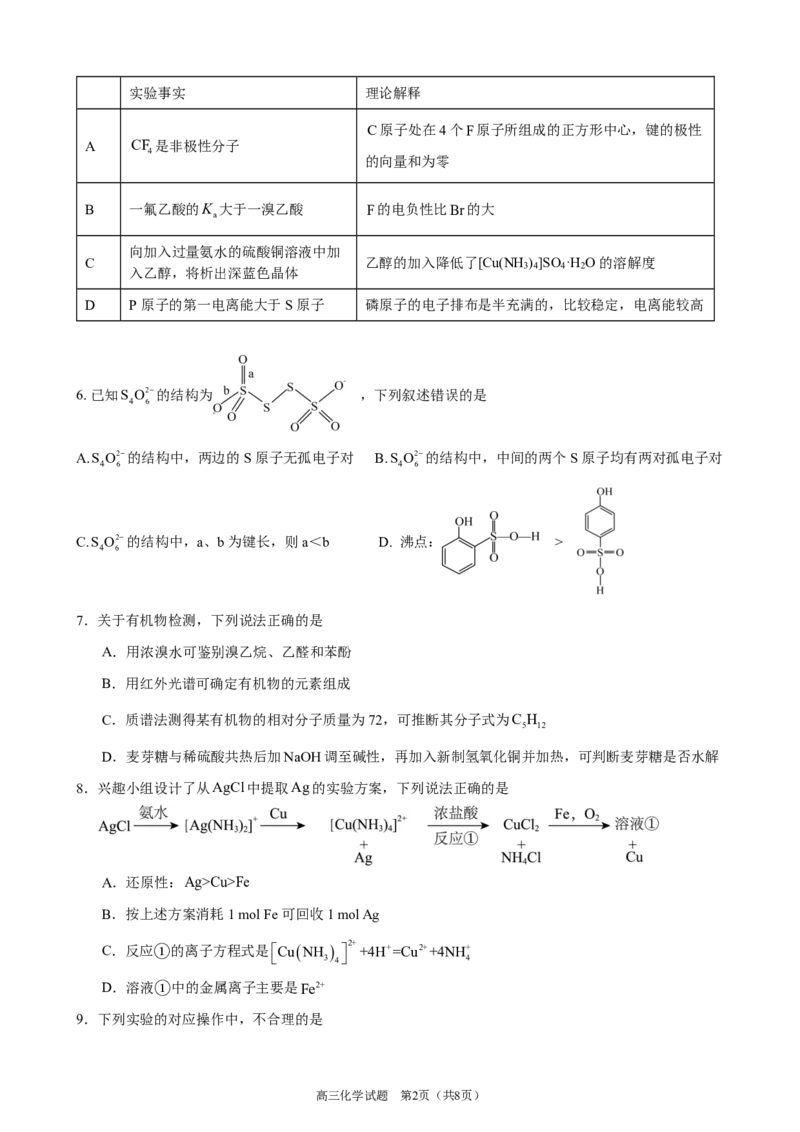
6. 已知S O2-的结构为 ,下列叙述错误的是
4 6
A.S O2-的结构中,两边的S原子无孤电子对 B.S O2-的结构中,中间的两个S原子均有两对孤电子对
4 6 4 6
C.S O2-的结构中,a、b为键长,则a<b D. 沸点: >
4 6
7.关于有机物检测,下列说法正确的是
A.用浓溴水可鉴别溴乙烷、乙醛和苯酚
B.用红外光谱可确定有机物的元素组成
C.质谱法测得某有机物的相对分子质量为72,可推断其分子式为C H
5 12
D.麦芽糖与稀硫酸共热后加NaOH调至碱性,再加入新制氢氧化铜并加热,可判断麦芽糖是否水解
8.兴趣小组设计了从AgCl中提取Ag的实验方案,下列说法正确的是
A.还原性:Ag>Cu>Fe
B.按上述方案消耗1 mol Fe可回收1 mol Ag
C.反应①的离子方程式是éCu(NH ) ù 2+ +4H+=Cu2++4NH+
ë 3 4 û 4
D.溶液①中的金属离子主要是Fe2+
9.下列实验的对应操作中,不合理的是
高三化学试题 第2页(共8页)
{#{QQABaYAEogioAJIAABgCUwGICgAQkAAAASgGAEAEoAAAQQFABAA=}#}眼睛注视锥形瓶中溶液
A.用HCl标准溶液滴定NaOH溶液 B.稀释浓硫酸
C.从提纯后的NaCl溶液获得NaCl晶体 D.配制一定物质的量浓度的KCl溶液
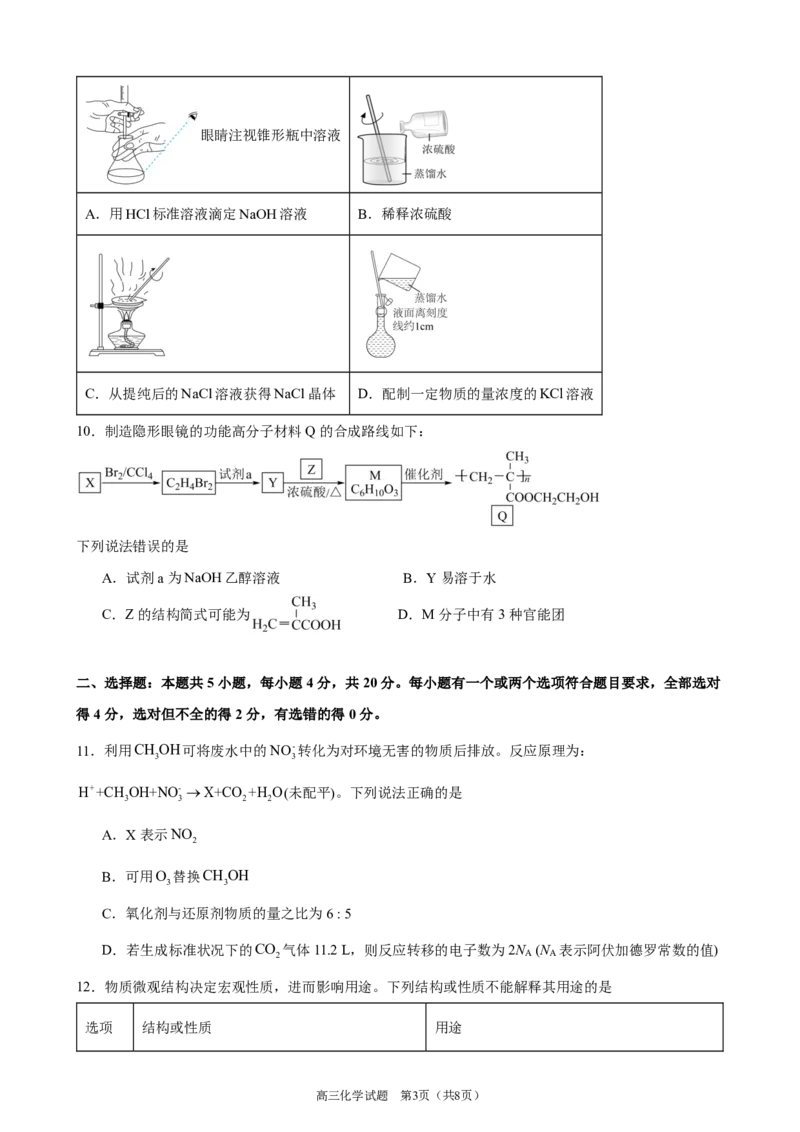
10.制造隐形眼镜的功能高分子材料Q的合成路线如下:
下列说法错误的是
A.试剂a为NaOH乙醇溶液 B.Y易溶于水
C.Z的结构简式可能为 D.M分子中有3种官能团
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对
得4分,选对但不全的得2分,有选错的得0分。
11.利用CH OH可将废水中的NO-转化为对环境无害的物质后排放。反应原理为:
3 3
H++CH OH+NO- ®X+CO +H O(未配平)。下列说法正确的是
3 3 2 2
A.X表示NO
2
B.可用O 替换CH OH
3 3
C.氧化剂与还原剂物质的量之比为6 : 5
D.若生成标准状况下的CO 气体11.2 L,则反应转移的电子数为2N (N 表示阿伏加德罗常数的值)
2 A A
12.物质微观结构决定宏观性质,进而影响用途。下列结构或性质不能解释其用途的是
选项 结构或性质 用途
高三化学试题 第3页(共8页)
{#{QQABaYAEogioAJIAABgCUwGICgAQkAAAASgGAEAEoAAAQQFABAA=}#}A 石墨呈层状结构,层间以范德华力结合 石墨可用作润滑剂
B SO 具有氧化性 SO 可用作漂白剂
2 2
C 聚丙烯酸钠( )中含有亲水基团 聚丙烯酸钠可用于制备高吸水性树脂
冠醚18-冠-6空腔直径(260~320 pm)与K+直 冠醚18-冠-6可识别K+,能增大KMnO 在有
D 4
径(276 pm)接近 机溶剂中的溶解度
13.氮化钙(Ca N )是一种重要的化学试剂。某化学兴趣小组用如图所示装置(部分夹持装置已略去)制备
3 2
Ca N (易与水反应),下列说法错误的是
3 2
A.Ca N 与水反应主要生成氢氧化钙和肼
3 2
B.实验开始前,首先应检查装置的气密性
C.实验中每消耗6 g Ca,同时消耗0.5 mol NO-
2
D.前后两处浓硫酸的作用分别是干燥N 及防止
2
空气中的水进入装置乙
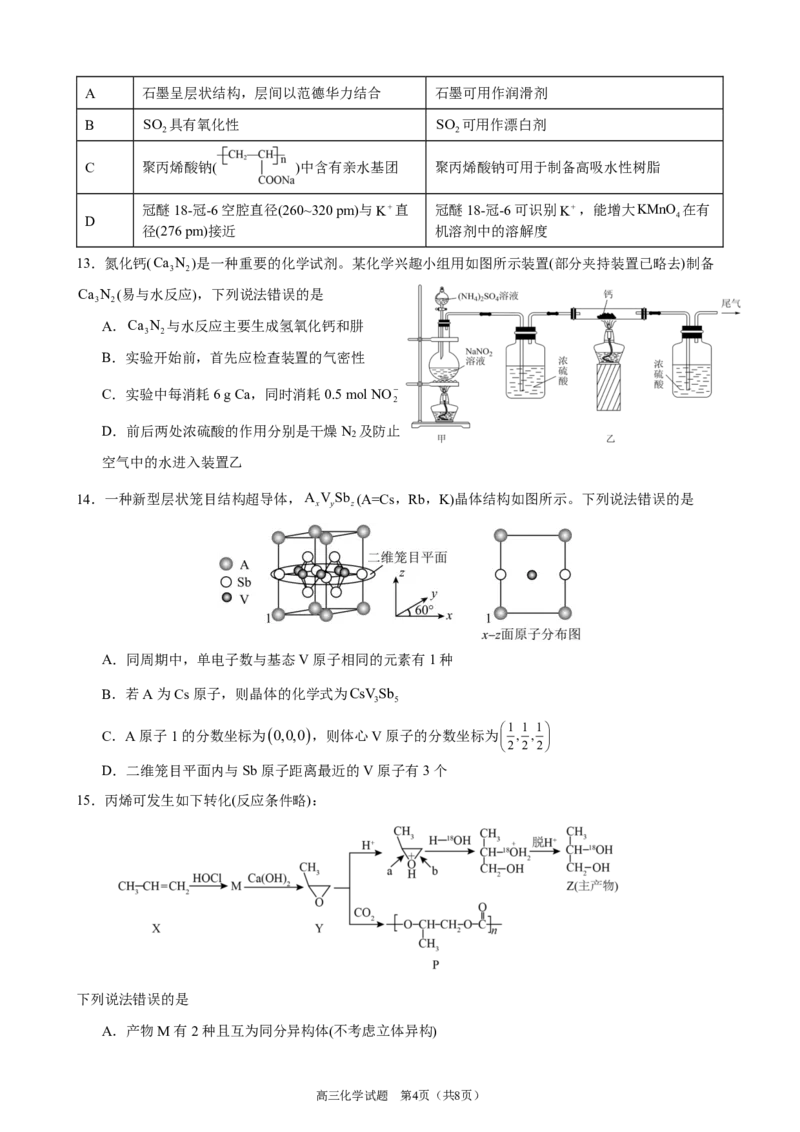
14.一种新型层状笼目结构超导体,A VSb (A=Cs,Rb,K)晶体结构如图所示。下列说法错误的是
x y z
A.同周期中,单电子数与基态V原子相同的元素有1种
B.若A为Cs原子,则晶体的化学式为CsVSb
3 5
C.A原子1的分数坐标为(0,0,0),则体心V原子的分数坐标为 æ ç 1 , 1 , 1ö ÷
è2 2 2ø
D.二维笼目平面内与Sb原子距离最近的V原子有3个
15.丙烯可发生如下转化(反应条件略):
下列说法错误的是
A.产物M有2种且互为同分异构体(不考虑立体异构)
高三化学试题 第4页(共8页)
{#{QQABaYAEogioAJIAABgCUwGICgAQkAAAASgGAEAEoAAAQQFABAA=}#}B.H+可提高Y→Z转化的反应速率
C.Y→Z过程中,a处碳氧键比b处更易断裂
D.Y→P是缩聚反应,该工艺有利于减轻温室效应
三、非选择题:本题共5小题,共60分。
16.(10分)研究化学物质有利于科技的发展和社会的进步。现有以下物质:
①CH CH OH ②Ba(OH) ③NaHSO ④SO ⑤AgCl ⑥超氧化钾(KO )⑦电石 ⑧FeCl ⑨盐酸,
3 2 2 4 2 2 3
回答下列有关问题。
(1)以上物质中不属于电解质的是____________,既含离子键又含共价键的是____________。
(2)向盛有0.01 mol/L Ba(OH) 溶液的烧杯中逐滴滴入0.5 mol/L的NaHSO 溶液(可忽略溶液体积变
2 4
化),混合溶液的导电能力最弱时溶液中大量存在的离子有_______________________________。
(3)酒精仪中酸性重铬酸钾(稀硫酸酸化)可将乙醇氧化成乙酸,本身被还原成Cr3+。请写出反应原理
(用离子方程式表示)_______________________________________________________。
(4)以电石为原料制得的气体,可与2-甲基-1,3-丁二烯合成六元环状化合物H,H的结构简式为____。
17.(12分)我国在新材料领域研究中取得一系列重大突破,为中华民族伟大复兴奠定了坚实的物质基
础。N、P、Sn、Ca等是新材料中常见的元素。回答下列问题:
(1)Sn在元素周期表中的位置是 ,SnCl 和SnCl 是锡的常见氯化物,SnCl 的分子构型
2 4 2
为 ,SnCl 的Sn—Cl键是由锡的 轨道与氯的3p轨道重叠形成的σ键。
4
(2)白磷晶胞属于面心立方最密堆积,每个P 周围距离最近的P 个数为___________;白磷隔绝空气加
4 4
热转化为红磷,红磷是巨型分子,无定型结构,能证明白磷是晶体的实验仪器为___________________。
(3)叠氮酸(HN )常用于引爆剂,可用联氨(H N-NH )制取。比较联氨与双氧水分子中键角大
3 2 2
小:ÐH-N-N______ÐH-O-O(填“>”、“=”或“<”,下同)。叠氮酸结构如图所示:
,*N为sp2杂化,已知参与形成π键的电子越多,键长越短,则键长:①______②。
(4)某含钙化合物的晶胞结构如图甲所示,沿x轴方向的投影为图乙,晶胞底面显示为图丙,晶胞参数
a¹°c,α=β=γ=90 。图丙中Ca与N的距离为 cm;化合物的化学式是 ,其摩尔质量为M g/mol,
阿伏加德罗常数的值是N ,则晶体的密度为 g×cm-3(列出计算表达式)。
A
高三化学试题 第5页(共8页)
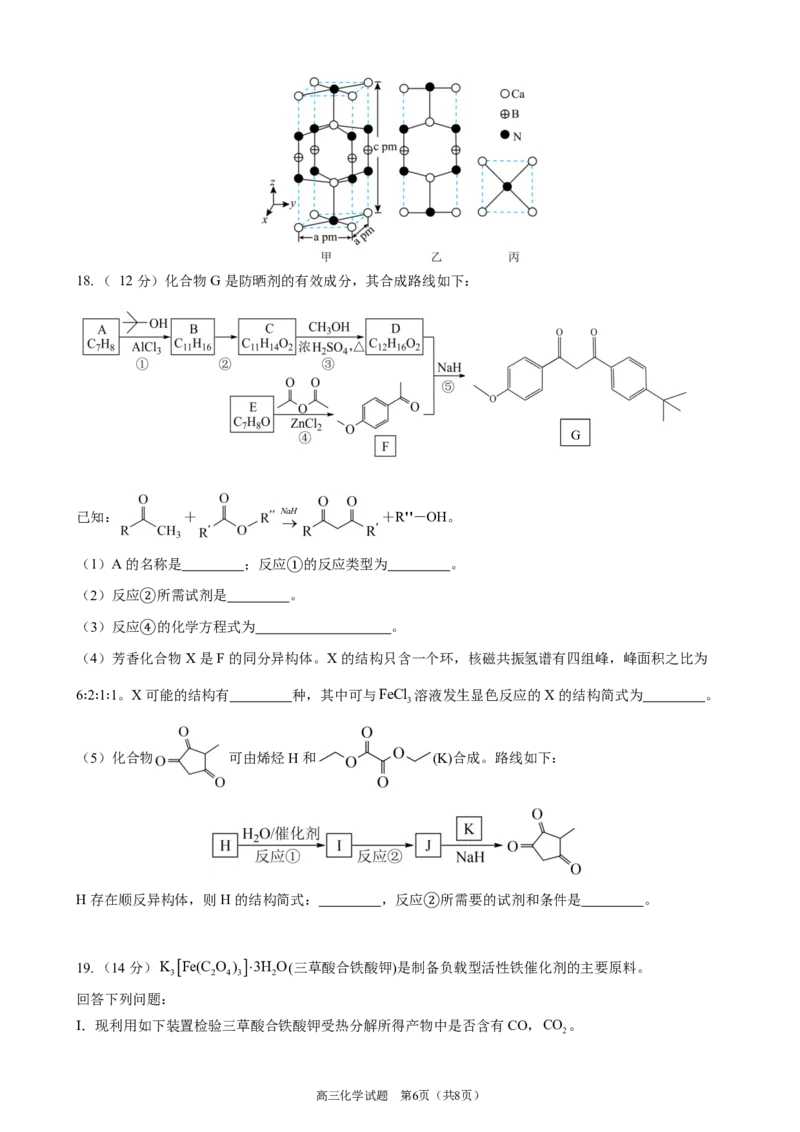
{#{QQABaYAEogioAJIAABgCUwGICgAQkAAAASgGAEAEoAAAQQFABAA=}#}18. ( 12分)化合物G是防晒剂的有效成分,其合成路线如下:
G
已知: + NaH +R''-OH。
®
(1)A的名称是 ;反应①的反应类型为 。
(2)反应②所需试剂是 。
(3)反应④的化学方程式为 。
(4)芳香化合物X是F的同分异构体。X的结构只含一个环,核磁共振氢谱有四组峰,峰面积之比为
6∶2∶1∶1。X可能的结构有 种,其中可与FeCl 溶液发生显色反应的X的结构简式为 。
3
(5)化合物 可由烯烃H和 (K)合成。路线如下:
H存在顺反异构体,则H的结构简式: ,反应②所需要的试剂和条件是 。
19. (14分)K [Fe(C O ) ]×3H O(三草酸合铁酸钾)是制备负载型活性铁催化剂的主要原料。
3 2 4 3 2
回答下列问题:
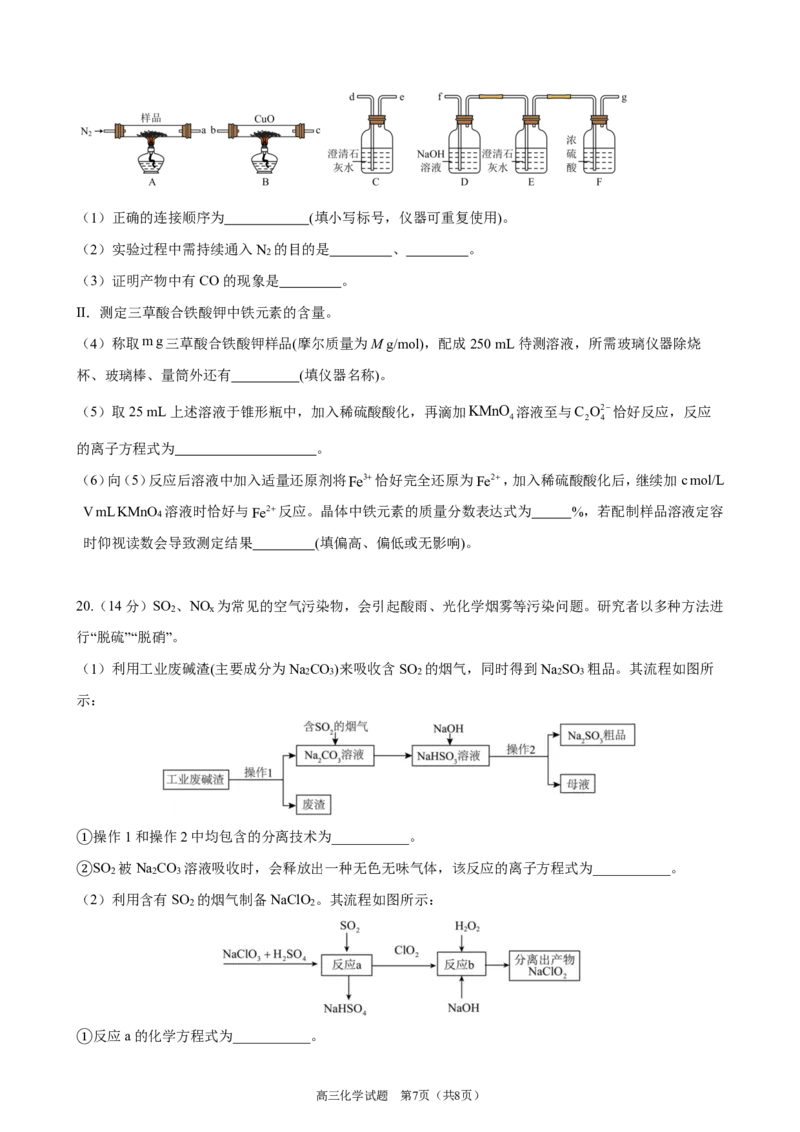
Ⅰ.现利用如下装置检验三草酸合铁酸钾受热分解所得产物中是否含有CO,CO 。
2
高三化学试题 第6页(共8页)
{#{QQABaYAEogioAJIAABgCUwGICgAQkAAAASgGAEAEoAAAQQFABAA=}#}(1)正确的连接顺序为 (填小写标号,仪器可重复使用)。
(2)实验过程中需持续通入N 的目的是 、 。
2
(3)证明产物中有CO的现象是 。
Ⅱ.测定三草酸合铁酸钾中铁元素的含量。
(4)称取m g三草酸合铁酸钾样品(摩尔质量为M g/mol),配成250 mL待测溶液,所需玻璃仪器除烧
杯、玻璃棒、量筒外还有 (填仪器名称)。
(5)取25 mL上述溶液于锥形瓶中,加入稀硫酸酸化,再滴加KMnO 溶液至与C O2-恰好反应,反应
4 2 4
的离子方程式为 。
(6)向(5)反应后溶液中加入适量还原剂将Fe3+恰好完全还原为Fe2+,加入稀硫酸酸化后,继续加c mol/L
V mL KMnO
4
溶液时恰好与Fe2+反应。晶体中铁元素的质量分数表达式为 %,若配制样品溶液定容
时仰视读数会导致测定结果 (填偏高、偏低或无影响)。
20.(14分)SO 、NO 为常见的空气污染物,会引起酸雨、光化学烟雾等污染问题。研究者以多种方法进
2 x
行“脱硫”“脱硝”。
(1)利用工业废碱渣(主要成分为Na CO )来吸收含SO 的烟气,同时得到Na SO 粗品。其流程如图所
2 3 2 2 3
示:
①操作1和操作2中均包含的分离技术为___________。
②SO 被Na CO 溶液吸收时,会释放出一种无色无味气体,该反应的离子方程式为___________。
2 2 3
(2)利用含有SO 的烟气制备NaClO 。其流程如图所示:
2 2
①反应a的化学方程式为___________。
高三化学试题 第7页(共8页)
{#{QQABaYAEogioAJIAABgCUwGICgAQkAAAASgGAEAEoAAAQQFABAA=}#}②反应b中的还原剂和氧化剂的物质的量之比为___________。
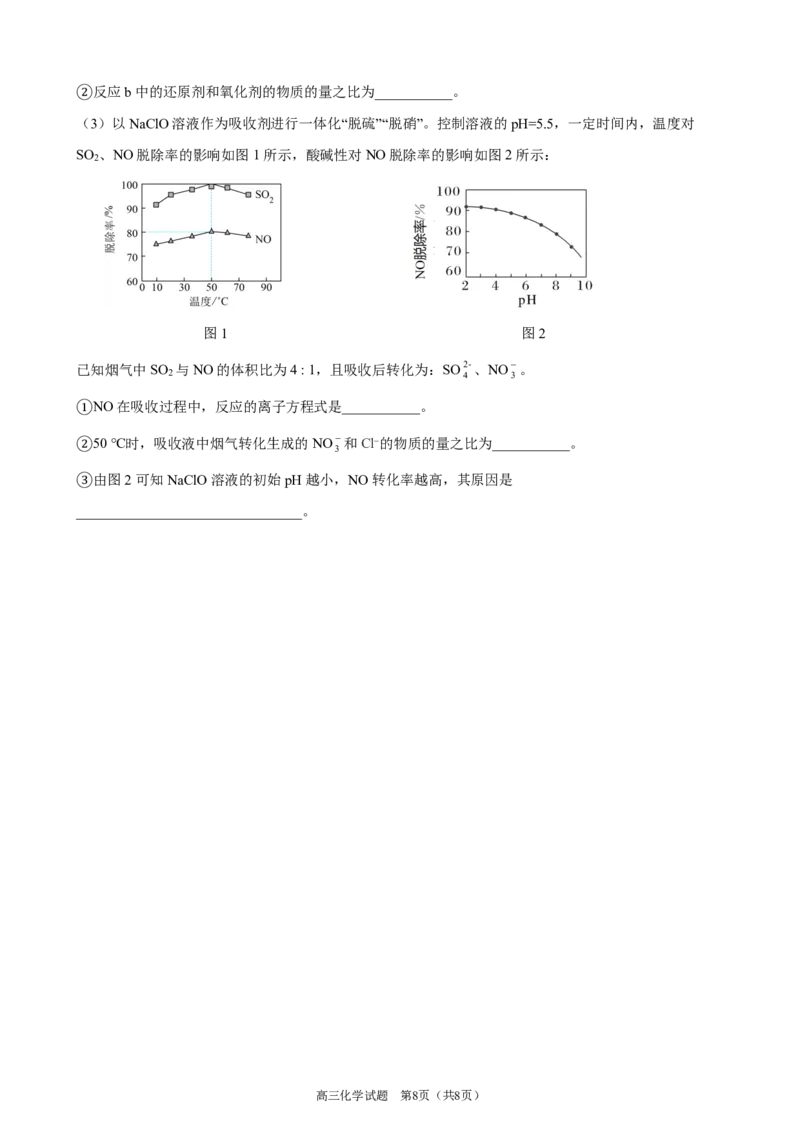
(3)以NaClO溶液作为吸收剂进行一体化“脱硫”“脱硝”。控制溶液的pH=5.5,一定时间内,温度对
SO 、NO脱除率的影响如图1所示,酸碱性对NO脱除率的影响如图2所示:
2
图1 图2
已知烟气中SO 与NO的体积比为4 : 1,且吸收后转化为:SO2-、NO-。
2 4 3
①NO在吸收过程中,反应的离子方程式是___________。
②50 ℃时,吸收液中烟气转化生成的NO-和Cl⁻的物质的量之比为___________。
3
③由图2可知NaClO溶液的初始pH越小,NO转化率越高,其原因是
________________________________。
高三化学试题 第8页(共8页)
{#{QQABaYAEogioAJIAABgCUwGICgAQkAAAASgGAEAEoAAAQQFABAA=}#}