文档内容
2024—2025 学年度上学期 2022 级
9 月月考化学试卷
时间:75分钟 满分:100分
命题人:蔡艳 审题人:吴志敏
考试时间:2024年9月25日
可能用到的相对原子质量:H 1 C 12 O 16 Cl 35.5 K 39 Mn 55 Zn 65
一、选择题(本题包括15个小题,每小3分,共45分,每小题只有1个选项符合题意)
1.在巴黎奥运会舞台上,科技与体育双向奔赴,释放更加迷人的魅力。下列说法不正确的是
A.比赛场馆 使用可再生能源供电,可减少碳排放量
B.中国队领奖服采用的环保再生纤维材料为有机高分子材料
C.乒乓球台可变灯光系统的控制芯片主要成分为SiO
2
D.生产橡胶弹性地板的原料天然橡胶是异戊二烯的聚合物
2.用NaCN溶液浸取矿粉中金的反应为4Au+2HO+8NaCN+O=4Na[Au(CN) ]+4NaOH。下列说
2 2 2
法正确的是
A.HO的空间结构为直线形 B.NaCN中含有离子键和共价键
2
C.1 mol [Au(CN) ]-中含有2 mol σ键 D.NaOH的电子式为
2
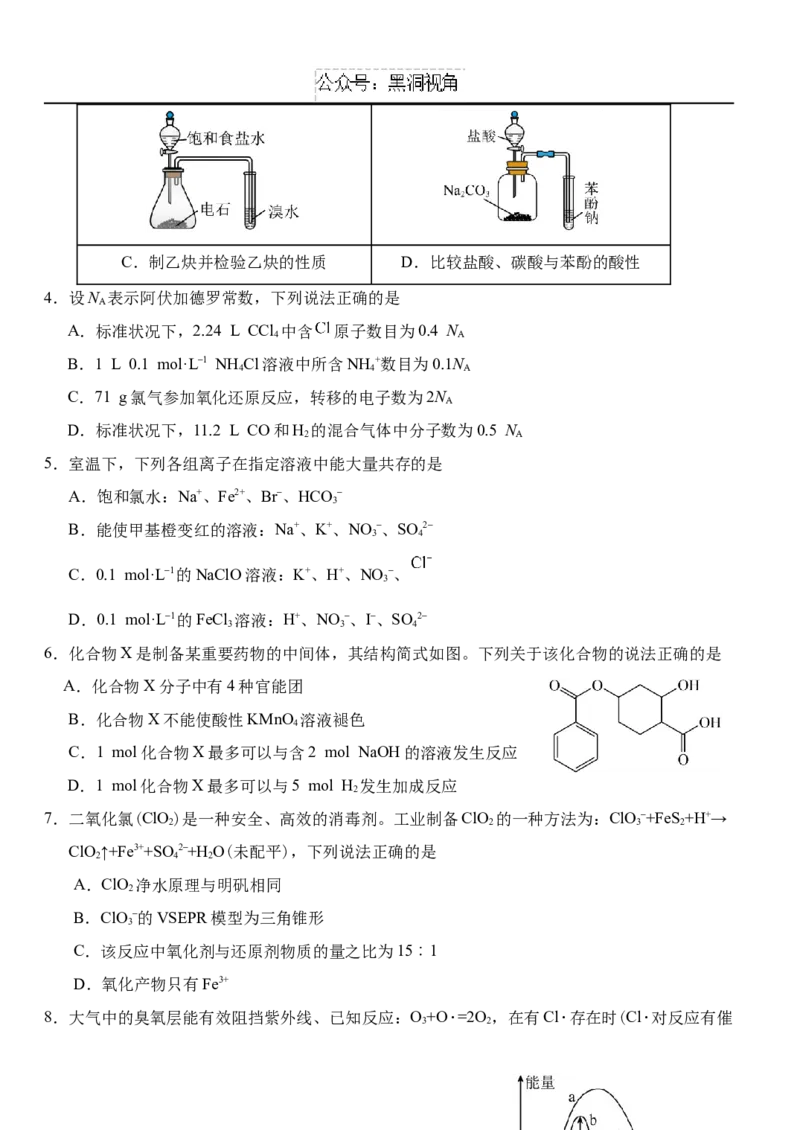
3.下列选用的仪器(部分夹持装置已略去)和药品能达到实验目的的是
A.比较碳酸钠和碳酸氢钠的稳定性 B.检验铜与浓硫酸反应产生的C.制乙炔并检验乙炔的性质 D.比较盐酸、碳酸与苯酚的酸性
4.设N 表示阿伏加德罗常数,下列说法正确的是
A
A.标准状况下,2.24 L CCl 中含 原子数目为0.4 N
4 A
B.1 L 0.1 mol·L–1 NH Cl溶液中所含NH +数目为0.1N
4 4 A
C.71 g氯气参加氧化还原反应,转移的电子数为2N
A
D.标准状况下,11.2 L CO和H 的混合气体中分子数为0.5 N
2 A
5.室温下,下列各组离子在指定溶液中能大量共存的是
A.饱和氯水:Na+、Fe2+、Br–、HCO –
3
B.能使甲基橙变红的溶液:Na+、K+、NO –、SO 2–
3 4
C.0.1 mol·L–1的NaClO溶液:K+、H+、NO –、
3
D.0.1 mol·L–1的FeCl 溶液:H+、NO –、I–、SO 2–
3 3 4
6.化合物X是制备某重要药物的中间体,其结构简式如图。下列关于该化合物的说法正确的是
A.化合物X分子中有4种官能团
B.化合物X不能使酸性KMnO 溶液褪色
4
C.1 mol化合物X最多可以与含2 mol NaOH的溶液发生反应
D.1 mol化合物X最多可以与5 mol H 发生加成反应
2
7.二氧化氯(ClO )是一种安全、高效的消毒剂。工业制备ClO 的一种方法为:ClO –+FeS +H+→
2 2 3 2
ClO ↑+Fe3++SO 2–+HO(未配平),下列说法正确的是
2 4 2
A.ClO 净水原理与明矾相同
2
B.ClO –的VSEPR模型为三角锥形
3
C.该反应中氧化剂与还原剂物质的量之比为15︰1
D.氧化产物只有Fe3+
8.大气中的臭氧层能有效阻挡紫外线、已知反应:O
3
+O·=2O
2
,在有Cl·存在时(Cl·对反应有催化作用)的反应机理为:基元反应①:O
3
+Cl·=ClO·+O
2
,基元反应②:ClO·+O·=Cl·+O
2
,反
应过程的能量变化如图所示。下列说法正确的是
A.a表示存在Cl·时反应过程的能量变化
B.Cl·是反应的催化剂,改变了反应历程,降低了ΔH
C.决定O
3
+O·=2O
2
反应速率的是基元反应①
D.增大压强和加入催化剂都能增大活化分子百分数
9.下列实验操作、现象和结论均正确的是
选项 操作 现象 结论
向某未知溶液中先加入BaCl 溶液,再加 先产生白色沉淀,加
A 2 溶液中一定含有SO 2–
稀盐酸 稀盐酸后沉淀不溶解 4
向盛有某未知溶液的试管中滴加NaOH
湿润的红色石蕊试纸
B 溶液,用湿润的红色石蕊试纸靠近试管 溶液中一定不含NH +
未变色 4
口
铜与稀硝酸反应生成
C 给试管中的铜与稀硝酸加热 产生少量红棕色气体
了NO
2
一段时间后,酸性高 乙醇被酸性高锰酸钾
D 向少量酸性高锰酸钾溶液中滴加乙醇
锰酸钾溶液褪色 溶液氧化
10.下列离子方程式正确的是
A.Ca(OH) 溶液中加入少量的Mg(HCO) 溶液:
2 3 2
Ca2++2OH–+Mg2++2HCO–=CaCO ↓+2HO+MgCO↓
3 3 2 3
B.饱和NaCO 溶液中通入过量CO:CO2–+CO +H O=2HCO –
2 3 2 3 2 2 3
C.盐酸滴入氨水中:H++OH–=H O
2
D.FeCl 溶液刻蚀铜电路板:2Fe3++Cu=2Fe2++Cu2+
3
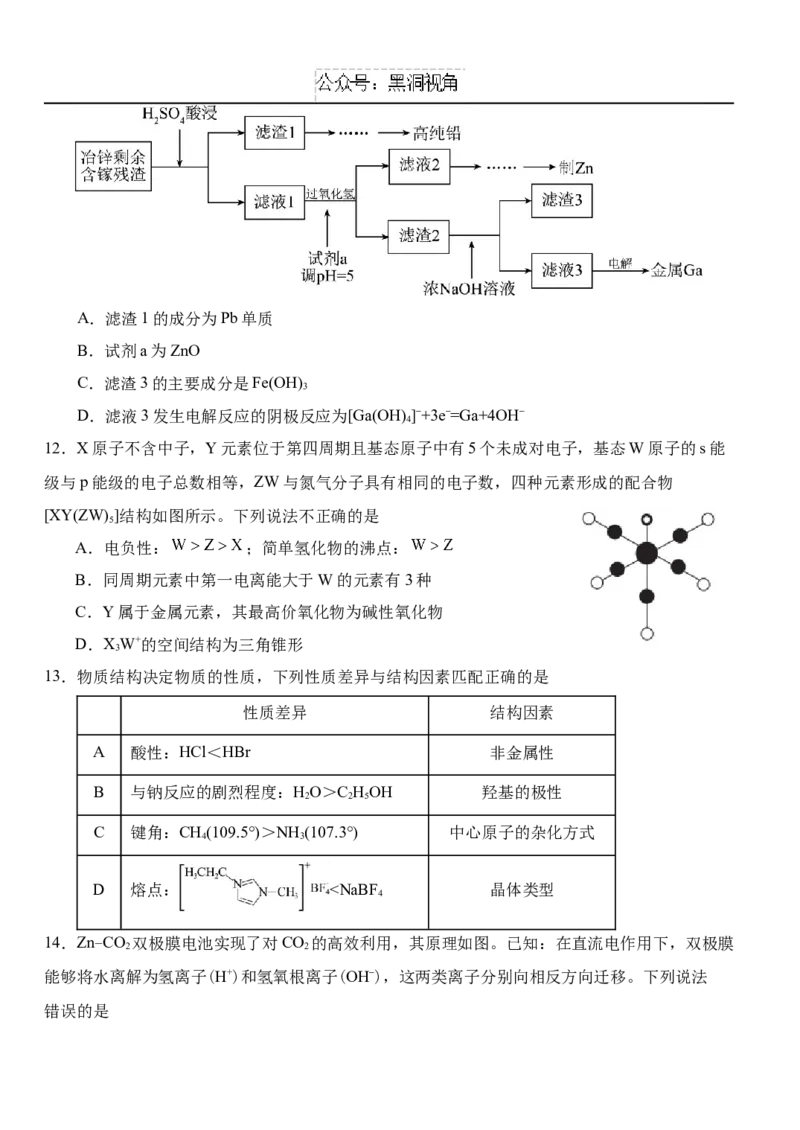
11.工业上处理闪锌矿冶锌后的残渣(主要含有 Zn、Pb、Fe、Ga 等元素)中,设计下述流程提取
铅、锌、镓。已知:Ga(OH) +OH–=[Ga(OH) ] –,对流程分析错误的是
3 4A.滤渣1的成分为Pb单质
B.试剂a为ZnO
C.滤渣3的主要成分是Fe(OH)
3
D.滤液3发生电解反应的阴极反应为[Ga(OH)]–+3e–=Ga+4OH–
4
12.X原子不含中子,Y元素位于第四周期且基态原子中有5个未成对电子,基态W原子的s能
级与p能级的电子总数相等,ZW与氮气分子具有相同的电子数,四种元素形成的配合物
[XY(ZW) ]结构如图所示。下列说法不正确的是
5
A.电负性: ;简单氢化物的沸点:
B.同周期元素中第一电离能大于W的元素有3种
C.Y属于金属元素,其最高价氧化物为碱性氧化物
D.XW+的空间结构为三角锥形
3
13.物质结构决定物质的性质,下列性质差异与结构因素匹配正确的是
性质差异 结构因素
A 酸性:HCl<HBr 非金属性
B 与钠反应的剧烈程度:HO>C HOH 羟基的极性
2 2 5
C 键角:CH(109.5°)>NH (107.3°) 中心原子的杂化方式
4 3
D 熔点: ”或“<”)时,CO 的平衡转化率小于H 的平衡转化率。
2 2
②当a=15时,该反应0~10 min内,υ(H )=_____MPa·min–1,压强平衡常数K =____MPa–4
2 p
(保留一位小数)。高三年级 9 月月考化学试卷 参考答案
1~15:CBBDB CCCDDACBBA
16.(14分,每空2分)(1) (2)SiO+2C高温 Si+2CO↑
2
(3)VO ++2OH–=VO–+HO;6.0≤pH<7.6 (4)10–37.4
2 3 2
(5)分液漏斗、烧杯 (6)2HO-4e–=4H++O↑
2 2
17.(14分,每空2分)(1)C→E→D
(2)Ca(ClO) +4HCl(浓)=CaCl +Cl↑+2HO;可以平衡气压,使浓盐酸顺利流下
2 2 2 2
(3)滤纸上只有紫红色无绿色 (4)84.6 (5)Cl+ Mn2++2H O=2MnO ↓+2Cl–+4H+
2 2 2
(6)Mn(OH) 的还原性比MnSO 强(或Mn2+的还原性随溶液碱性的增强而增强,在碱性条件下
2 4
可以被氧化到更高价态)
18.(13分,除标注外每空2分)(1)2-乙基苯酚
(2)取代反应(1分);保护酚羟基,防止被氧化 (3) (4)
(5)3 (6)4
19.(14分,每空2分)(1) ;低温 (2)a;c (3)<;0.3;9.5
【解析】
1.C.乒乓球台可变灯光系统的控制芯片主要成分为Si,C错误。
2.A.HO的空间结构为V形,A错误;B.NaCN中Na+与CN-间形成离子键,CN-中C和N之
2
间形成共价键,B正确;C.[Au(CN) ]-中CN-内含有1个σ键,Au与CN-间形成配位键也是σ键,
2
故1mol[Au(CN) ]-中含有4molσ键,C错误;D.NaOH的电子式为 ,D错误。
2
3.A.小试管中受热温度低,为对比二者的稳定性,小试管中应为碳酸氢钠,A不合题意;C.
生成的乙炔中混有硫化氢,均使溴水褪色,不能检验乙炔的性质,C不合题意;D.挥发的乙酸
与苯酚钠反应,不能比较碳酸、苯酚的酸性强弱,D不合题意。
4.A.标况下 不是气体,无法计算物质的量,A错误;B. 水解,粒子数目小于 ,
B错误;C. 氯气参加氧化还原反应,转移的电子数可能为 ,如氯气与水的反应,C错误
D.标准状况下, 和 的混合气体的物质的量为0.5mol,故分子数为 ,D正确。
5.A.饱和氯水具有强氧化性和酸性,饱和氯水中Fe2+、Br–、HCO –不能大量共存,A错误;
3
C.H+、 、 会反应生成氯气,不能大量共存,C错误;D.Fe3+、I–会发生氧化还原反应
不能大量共存,D错误。
6.A.化合物X分子中有酯基、羟基、羧基3种官能团,A错误;B.化合物X中与羟基相连碳上有氢,能被酸性 溶液氧化,使酸性 溶液褪色,B错误;C.化合物X分子中有酯
基、羧基可以与NaOH反应,1mol化合物X最多可以与含2molNaOH的溶液发生反应,C正确;
D.羧基、酯基中的碳氧双键不能与氢气加成,化合物X含有1个苯环,1mol化合物X最多可以
与 发生加成反应,D错误。
7.A.ClO 具有氧化性,可用于自来水的杀菌消毒,明矾是铝离子水解产生氢氧化铝胶体,胶体
2
吸附水中的悬浮物聚沉而除去,A 项错误;B.ClO –的中心原子 Cl 的价层电子对数为:
3
3+1/2(7+1-3×2)=4,VSEPR模型为四面体形,B项错误;C.ClO –为氧化剂,FeS 为还原剂,
3 2
中氯元素由+5价降到+4价,因此1个氯酸根离子发生反应时得到1个电子,FeS 中铁元素从
2
+2价升高到+3价,失去1个电子,硫元素从-1价升高到+6价,失去7个电子,因此1个FeS 发
2
生反应时失去15个电子,根据电子得失守恒可得,氧化剂与还原剂物质的量之比为15∶1,C项正
确;D.根据反应可知,该反应中ClO –为氧化剂,FeS 为还原剂,Fe3+、SO 2–为氧化产物,D项
3 2 4
错误。
8.A.催化剂能降低反应活化能,结合图示可知b过程活化能较低,应为存在催化剂 时反应
过程的能量变化,故A错误;B. 是反应的催化剂,改变了反应历程,但催化剂不影响 ,
故B错误;C.活化能越小反应越快,活化能越大反应越慢,决定总反应速率的是慢反应;反应
①的活化能更大,则决定总反应速率的是基元反应①,故C正确;D.加入催化剂增大活化分子
百分数,增大压强不改变活化分子百分数,故D错误。
9.A.溶液中可能含有银离子,故A错误;B.检验铵根离子必须先加氢氧化钠溶液后再加热,
主要原因是一水合氨受热分解,逸出氨气,故B错误;C.铜与稀硝酸加热反应生成一氧化氮,
一氧化氮在试管口与空气中氧气反应变为红棕色二氧化氮,故C错误。
10.A. 的溶解度小于 , 溶液中加入少量的 溶液,应该生成沉
淀 ,离子方程式为: ,A错误;
B.饱和NaCO 溶液中通入过量CO ,会析出碳酸氢钠沉淀: ,
2 3 2
B错误;C.一水合氨是弱电解质,盐酸滴入氨水中: ,C错误。
11.冶锌的残渣中主要含有Zn、Pb、Fe、Ga等元素,加入硫酸酸浸生成硫酸铅、硫酸锌、硫酸
亚铁、硫酸镓等,由各步最终获得的金属可知,过滤分离得到滤渣1为硫酸铅,滤液1中加入试
剂a调节pH,使Fe、Ga元素转化氢氧化铁和氢氧化镓沉淀(氢氧化亚铁易被氧化为氢氧化铁) ,
试剂a为ZnO等,滤液2为硫酸锌,滤渣2用浓NaOH溶解,Ga元素以[Ga(OH)]-形式存在滤液3
4
中,滤渣3为氢氧化铁,以此解答该题。
12.X原子不含中子,则X为H,Y位于第四周期且基态原子中有 5个未成对电子,则Y为
Mn,基态W原子的s能级与p能级的电子总数相等,ZW与氮气分子具有相同的电子数,则W为O,Z为C。A.同周期主族元素从左到右元素的电负性逐渐增大,同主族元素从上到下电负性
逐渐减小,故电负性: ,由于 分子间形成氢键,故沸点高于 ,A正确;B.第
二周期中第一电离能大于O的元素有N、F、Ne三种,B正确;C. 属于酸性氧化物,C错
误;D. 中O的价层电子对数目为3+1/2(5-3×1)=4,空间结构为三角锥形,D正确。
13.A.可以通过比较简单氢化物的稳定性,或最高价氧化物对应水化物的酸性来比较元素非金
属性,不能用非金属性解释酸性: ,A错误;B.甲基是推电子基团,水中羟基的极
性大于乙醇,则水中羟基H原子的活性比乙醇中羟基H原子活性大,故钠与水反应比与乙醇反应
剧烈,B正确;C. 的中心原子价层电子对数都是4,中心原子的杂化方式都是sp3杂化,
二者键角不同是因为后者中心原子有1个孤电子对,孤电子对对成键电子对的排斥使其键角减小,
C 错误;D. 与 NaBF 均为离子晶体,熔点与构成其晶体的离子半径有关,
4
的半径大于Na+, 中离子键键能较小,熔点较低,与晶体类型无关,D
错误。
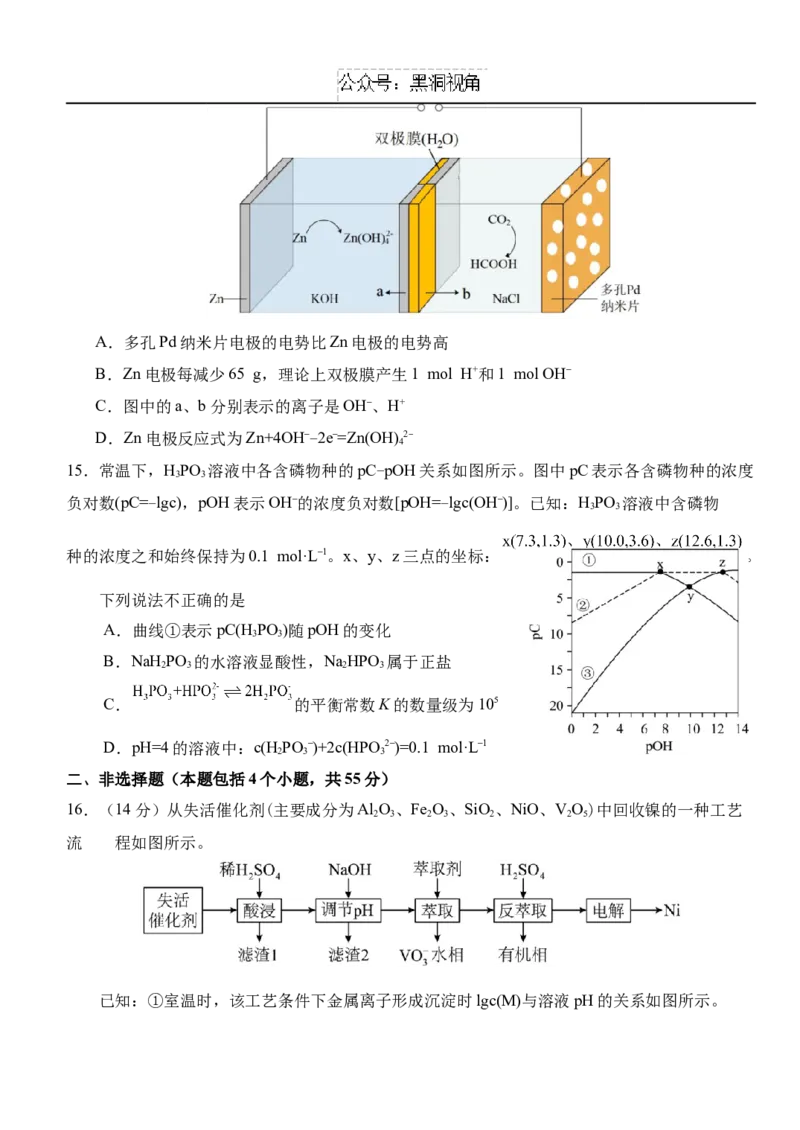
14.A.由分析可知,多孔Pd纳米片为正极,Zn为负极,则多孔Pd纳米片电极的电势比Zn电
极的电势高,故A正确;B.Zn电极每减少65g,转移电子数为2mol,由两极的反应式可知,双
极膜中需离解水的物质的量为2mol,产生2mol氢离子、2mol氢氧根离子,故B错误;C.原电
池中阳离子向正极移动、阴离子向负极移动,故b为 ,a为 ,故C正确;D.锌发生氧化
反应为负极,电极反应为 ,故D正确。
15.pOH值越大,碱性越弱,酸性越强,HPO 浓度越大,对应的负对数pC值越小,③曲线为
3 3
HPO 浓度负对数与pOH关系,②曲线为 浓度负对数与pOH关系,①曲线是 浓度负
3 3
对数与pOH的关系。x点为 浓度与 浓度相等,pOH值为7.3,c(OH-)=10-7.3mol/L,
c(H+)=10-6.7mol/L,K = =10-6.7,z点为 浓度与HPO 浓度相等,pOH值为12.6,
a2 3 3
c(OH-)=10-12.6mol/L,c(H+)=10-1.4mol/L,K = =10-1.4。B. 电离出的 既能
a1
发生水解又能发生电离,电离常数为K =10-6.7,水解常数为K = =10-12.6,电离大于水解,
a2 h
水溶液显酸性, 属于正盐,B正确;C. 的平衡常数K== = = =105.3,数量级为 ,C正确; 时pOH=10,此时c(HPO )=c(
3 3
, 由 于 溶 液 中 含 磷 物 种 的 浓 度 之 和 始 终 保 持 为 , 即
由于c(HPO )=c( 则 ,D正确。
3 3
16.由题给流程可知,失活催化剂中主要成分为 ,加入稀硫酸,二
氧化硅不与稀硫酸反应,得到含有二氧化硅的滤渣,同时产生含有可溶性硫酸盐的滤液,主要含
有: 、 、 、 ;向滤液中加入NaOH溶液,得到 、 、 、 ;加入
萃取剂萃取溶液中的镍元素,分液得到含有 的有机相和含有 水相;向水相中加入硫酸溶
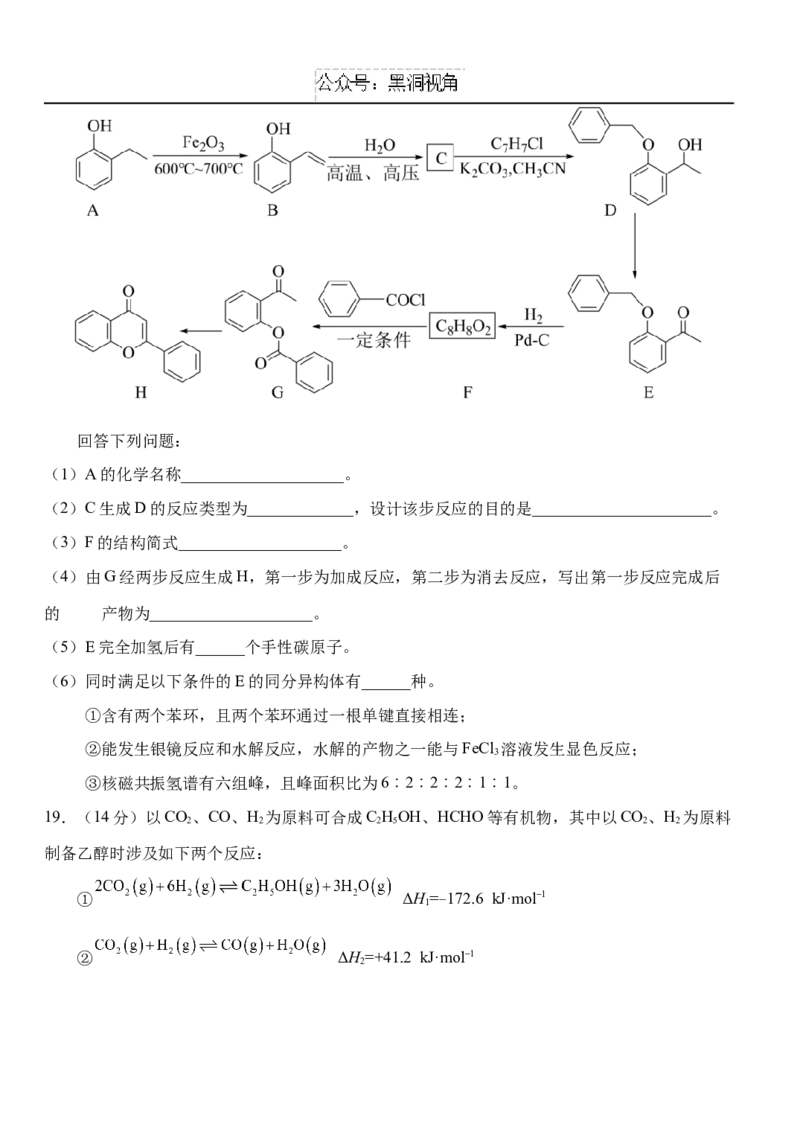
液,将镍离子反萃取入水相,电解硫酸镍溶液可得金属镍。(3)依题意,用 “调节 ”
将 转化为 的离子方程式为 。根据“五价钒在 时以 形式
存在”,并结合图中数据可知, 的调控范围是 。(4)室温下,当
时 , 溶 液 的 , 此 时 溶 液 中 , 则 的
。 ( 6 ) 用 惰 性 电 极 电 解 硫 酸 镍 溶 液 的 化 学 反 应 方 程 式 为
。
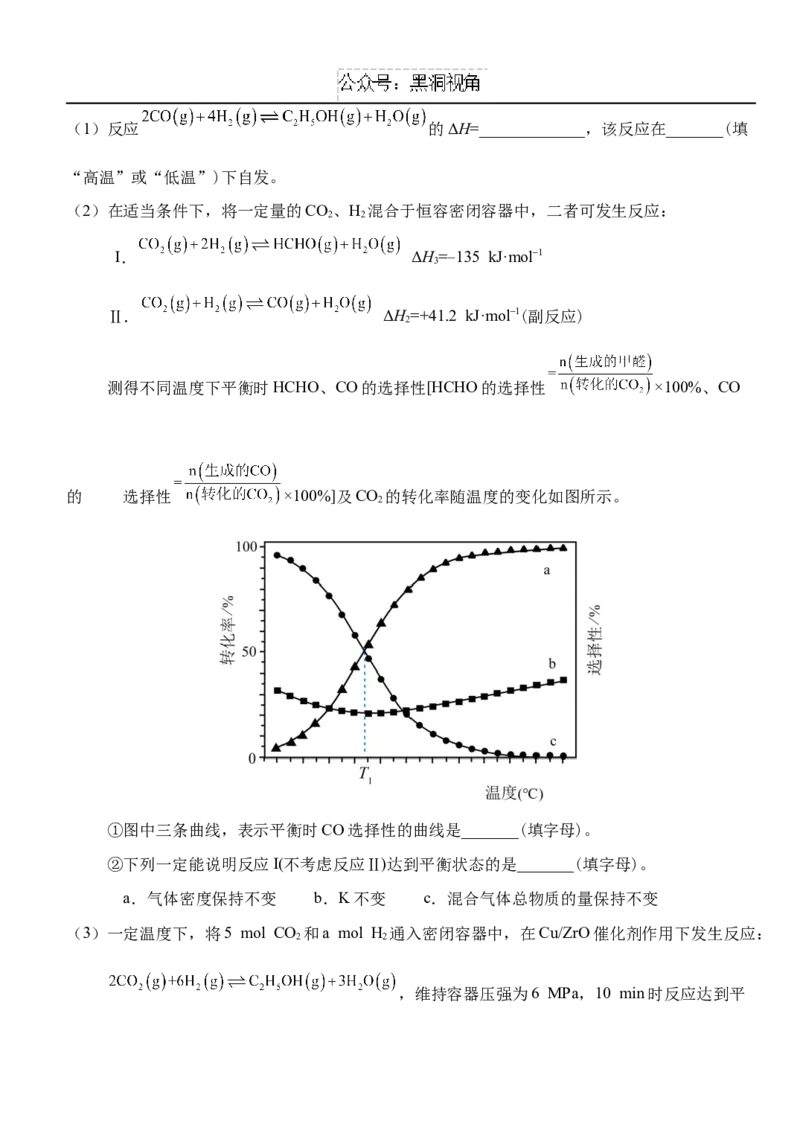
17.A制备氯气,C装置除氯气中的氯化氢,E装置用 氧化 制备 ,D装置用氢氧
化钠吸收氯气,防止污染。(1)根据已知③,为防止E中强碱溶液碱性减弱, 不稳定导
致 的产率降低,用饱和食盐水除去挥发出的 HCl;NaOH溶液用于尾气处理; 氧化
的反应在E中进行,气体无需浓硫酸干燥,所以顺序连接 A→C→E→D。(3)若反应完
全溶液中只有 ,没有 ,根据已知①,滤纸上只有紫红色无绿色,说明反应完全;(4)
滴定时消耗 23.90mL0.1400mol/L 的 HC O 标准溶液,则参加反应的 HC O 的物质的量为
2 2 4 2 2 4
0.0239L×0.1400mol/L=3.346×10-3mol,根据反应:2MnO -+5HC O +6H+=2Mn2++10CO +8HO
4 2 2 4 2 2
可知参加反应的 KMnO 的物质的量为 3.346×10-3mol×2/5=1.3348×10-3mol,则样品纯度=
4≈84.6%。;(5) 溶液通入 后,产生棕黑色沉淀,该沉淀为
MnO ,离子方程式为 ;(6)对比实验Ⅰ、Ⅱ,I中MnSO 被
2 4
Cl 氧化为MnO ,Ⅱ中Mn(OH) 被O 氧化为 MnO 且能被Cl 氧化为更高价的 ,Ⅱ中溶液
2 2 2 2 2 2
碱性更强,则二价锰化合物的还原性随溶液的碱性增强而增强,且 Mn(OH) 的还原性比 MnSO
2 4
的强。
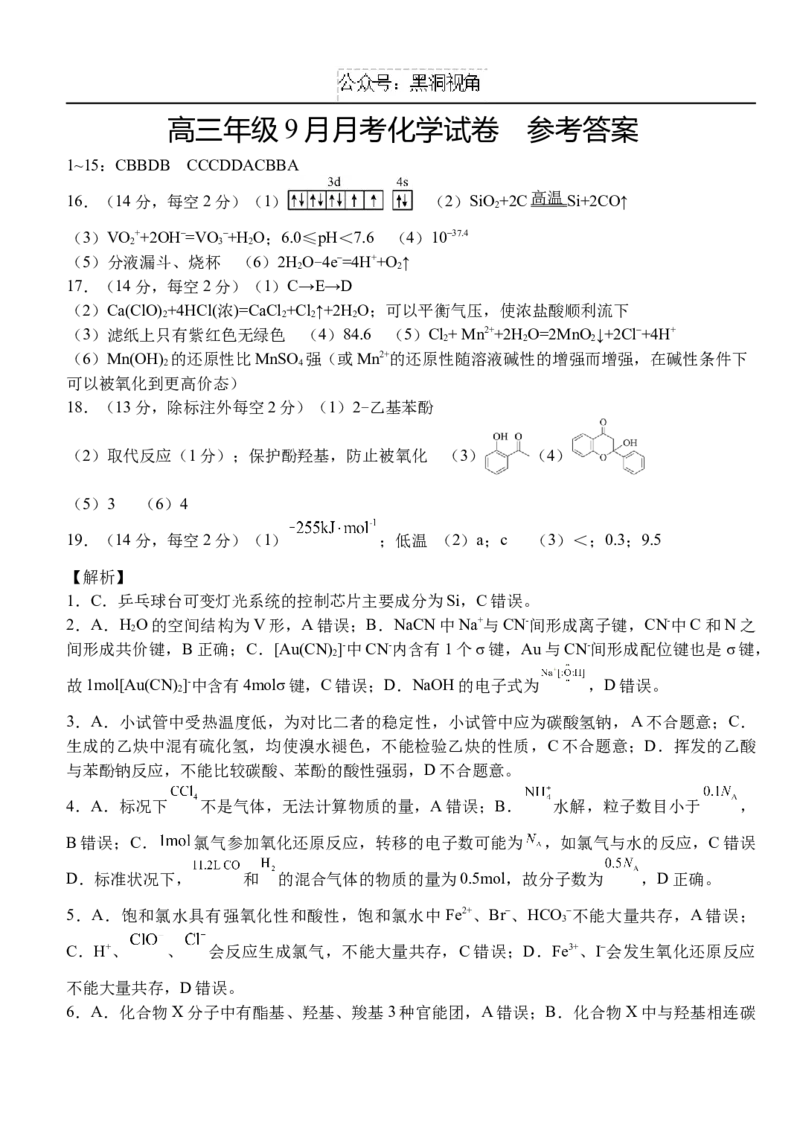
18.由有机物的转化关系可知,催化剂作用下 在600-700℃转化为 ,高温高压下
与水发生加成反应生成 ,则C为 ;催化剂作用下 与 发生取代反应生
成 ,催化剂作用下 与氧气共热发生催化氧化反应生成 ,催化剂作用
下 与氢气反应转化为 ,则F为 ;一定条件下 与 发生取代反应生成
, 先发生加成反应生成 、 发生消去反应生成 。
(2)由分析可知,C生成D的反应为催化剂作用下 与 发生取代反应生成 和
氯化氢,由 和 分子中都含有羟基、D→E时D中羟基被氧化可知,设计该步反应的目的
是保护酚羟基,防止被氧化;(5)由结构简式可知, 完全加氢的产物中含有如图*所示
的3个手性碳原子: ;(6)E的同分异构体含有两个苯环,且两个苯环通过一根单键直
接相连,能发生银镜反应和水解反应,水解的产物之一能与氯化铁溶液发生显色反应,说明同分
异构体分子中含有酚羟基酯基和醛基,核磁共振氢谱有六组峰,且峰面积比为 6︰2︰2︰2︰1︰1
说明同分异构分子中含有的取代基为甲酸酚酯基和2个处于对称位置的甲基,则同分异构体的结
构有如图数字标注的4种: 。19.(1)由盖斯定律可1,用①-2×②即可得: ;
依据 能自发进行,该反应 、 ,则在低温下自发进行;(2)①生成
甲醛的反应为放热反应,升温时平衡逆向移动,甲醛的选择性降低。生成 的反应是吸热反应,
升温有利于平衡向正反应方向移动,故a表示 的选择性、c表示甲醛的选择性,从而可确定b
表示 的转化率;②a.由于气体总质量保持不变,容器容积保持不变,故密度一直保持不变,
a项错误;b.K只随着温度变化,b项错误;c.由于向右进行的反应是气体分子数目减小的反应,
故当总物质的量保持不变时反应处于平衡状态,c项正确;(3)①当 、 物质的量之比等于
时,二者平衡转化率相等,当二者比值不等于化学计量数之比时,过量的物质转化率较小,
故填<;②恒温恒压条件下,容器体积之比等于气体物质的量之比,故达到平衡时气体总共为
,设甲醇的变化量为x,列三段式有
,则 5-2x+16-6x+x+3x=12mol,解得
x=2mol,各物质平衡分压: 、 、 、 ,
开 始 时 , ,
。