文档内容
4.盐类水解在生产和生活中有着广泛的应用,有关应用或说法与盐类水解无关的是 ( )
高二化学试卷(一) A.NHCl溶液可用于除铁锈
4
B.用FeCl饱和溶液制备Fe(OH)胶体
3 3
(本试卷满分100分,考试时间75分钟)
C.用稀硫酸除去铜器表面的铜绿Cu(OH)CO
注意事项:1.答题前,考生务必用黑色字迹的签字笔或钢笔将自己的姓名、准考证号分别填写 2 2 3
D.FeCl溶液的配制:FeCl晶体溶于浓盐酸中,然后再加水稀释到所需要的浓度
在试卷和答题卡规定的位置上。 3 3
5.N 为阿伏加德罗常数的值。下列说法正确的是 ( )
2.答选择题时,选出每小题答案后,用2B铅笔把答题卡对应题目的答案涂黑,如需 A
改动,用橡皮擦干净后,再涂其它答案。非选择题的答案必须用黑色字迹的签字 A.0.1L1mol/LFeCl 3 溶液中含Fe3+的数目为0.1N A
笔或钢笔写在答题卡上相应的区域内,写在本试卷上无效。 B.0.1molH 与0.1molI于密闭容器中充分反应后,容器内的分子数为0.2N
2 2 A
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5 C.100g46%的乙醇溶液中含有氧原子数为N
A
一 、选 择 题 : 本 题 共 15 小 题 ,每 小 题 3分 , 共 4 5分 。 在 每 小 题 给 出 的 四 个选项中,只有一项符 D.标准状况下,22.4LSO 中含有SO 的分子数为N
3 3 A
合题目要求。 6.下列叙述正确的是 ( )
1.下列说法不正确的是 ( ) A.明矾可以用于净水是因为:[Al(OH)]-幑幐Al(OH)+OH-
4 3
A.已知C(石墨,s)幑幐C(金刚石,s) ΔH>0,稳定性:石墨>金刚石 B.NaHSO 溶液的水解方程式:HSO-+HO幑幐HO++SO2-
3 3 2 3 3
B.2CO(g)2C(s)+O(g),已知ΔH>0,ΔS<0,则一定不能自发进行 C.MgCl溶液显酸性的原因:Mg2++2HO幑幐Mg(OH)+2H+
2 2 2 2
C.工业合成氨反应选择400~500℃作为反应温度是为了提高平衡转化率 D.小苏打能中和胃酸是因为:CO2-+HO幑幐HCO-+OH-
3 2 3
D.打开剧烈摇动后的碳酸饮料产生大量气泡的原因是压强对化学平衡的影响 7.下列事实一定能说明亚硝酸(HNO)是弱电解质的是 ( )
2
2.下列有关反应热说法错误的是 ( ) ①常温下HNO 溶液中存在的微粒有:H+、NO-、HNO、OH-、HO
2 2 2 2
A.中和热测定的装置中,填充碎泡沫、内外烧杯口齐平的目的都是减少热量损失 ②用HNO 溶液做导电性实验,灯泡很暗
2
B.已知:H+(aq)+OH-(aq)HO(l) ΔH=-57.3kJ·mol-1,则 NaOH稀溶液与稀醋 ③10mL1mol·L-1HNO 溶液恰好与10mL1mol·L-1NaOH溶液完全反应
2 2
酸生成1mol水时,反应热数值偏小 ④0.1mol·L-1HNO 溶液的c(H+)<0.1mol·L-1
2
C.已知:H(g)+I(g)幑幐2HI(g) ΔH=-akJ·mol-1,则1molI(g)和1molH(g)充分 A.①③ B.②③ C.②④ D.①④
2 2 2 2
反应,放出的热量小于akJ 8.利用CO 催化加氢可制得乙烯,反应方程式为2CO(g)+6H(g)幑幐CH(g)+4HO(g)
2 2 2 2 4 2
D.在101kPa下,C(s)的燃烧热ΔH=-393.5kJ·mol-1,则CO(g)分解的热化学方程式为 ΔH<0,在两个容积均为1L恒容密闭容器中,分别加入2molCO 和4molH,分别选用两种
2 2 2
2CO 2 (g)2C(s)+2O 2 (g) ΔH=+393.5kJ·mol-1 催化剂,反应进行相同时间,测得 CO 2 转化率随反应温度的变化如图所示。下列说法不正
确的是 ( )
3.常温下,下列各组离子一定能在指定溶液中大量共存的是 ( )
A.T温度下充入稀有气体,CO 转化率不变
K 5 2
A. w =10-12mol·L-1的溶液中:Na+、K+、SiO2-、Cl-
c(OH-) 3 B.温度高于T,CO 转化率降低的原因是温度导致的平衡
4 2
B.使甲基橙变黄的溶液中:NH+、Cu2+、NO-、SO2- 逆移
4 3 4
C.由水电离出的c(H+)=1.0×10-13mol·L-1的溶液中:Na+、CO2-、SO2-、Cl- C.从图中无法比较催化剂Ⅰ和催化剂Ⅱ谁更高效
3 3
D.使KSCN显红色的溶液中:NH+、K+、Cl-、HCO- D.b、d两状态下,化学反应速率d>b
4 3
高二化学试卷(一) 第1页 (共8页) 高二化学试卷(一) 第2页 (共8页)
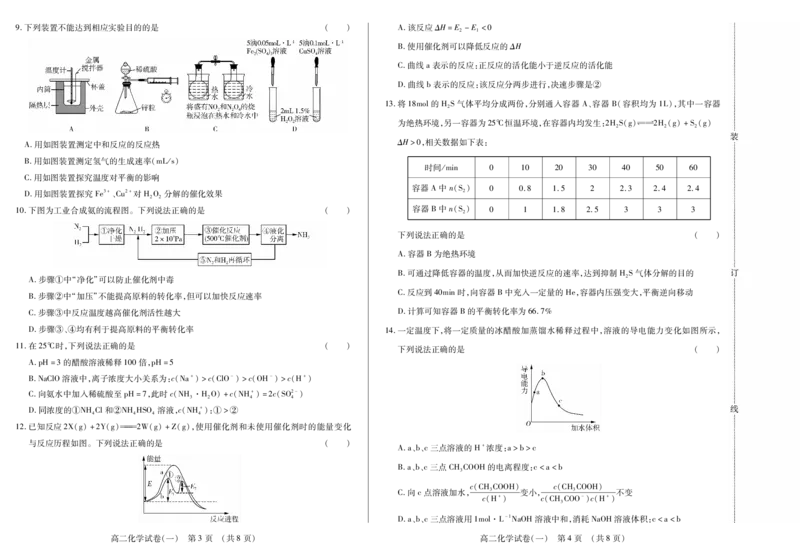
书书书9.下列装置不能达到相应实验目的的是 ( ) A.该反应ΔH=E-E<0
2 1
B.使用催化剂可以降低反应的ΔH
C.曲线a表示的反应:正反应的活化能小于逆反应的活化能
D.曲线b表示的反应:该反应分两步进行,决速步骤是②
13.将18mol的HS气体平均分成两份,分别通入容器 A、容器 B(容积均为1L),其中一容器
2
为绝热环境,另一容器为25℃恒温环境,在容器内均发生:2HS(g)幑幐2H(g)+S(g)
2 2 2
A.用如图装置测定中和反应的反应热 ΔH>0,相关数据如下表:
B.用如图装置测定氢气的生成速率(mL/s)
时间/min 0 10 20 30 40 50 60
C.用如图装置探究温度对平衡的影响
容器A中n(S) 0 0.8 1.5 2 2.3 2.4 2.4
D.用如图装置探究Fe3+、Cu2+对HO 分解的催化效果 2
2 2
10.下图为工业合成氨的流程图。下列说法正确的是 ( ) 容器B中n(S) 0 1 1.8 2.5 3 3 3
2
下列说法正确的是 ( )
A.容器B为绝热环境
B.可通过降低容器的温度,从而加快逆反应的速率,达到抑制HS气体分解的目的
A.步骤①中“净化”可以防止催化剂中毒 2
C.反应到40min时,向容器B中充入一定量的He,容器内压强变大,平衡逆向移动
B.步骤②中“加压”不能提高原料的转化率,但可以加快反应速率
C.步骤③中反应温度越高催化剂活性越大 D.计算可知容器B的平衡转化率为66.7%
D.步骤③、④均有利于提高原料的平衡转化率 14.一定温度下,将一定质量的冰醋酸加蒸馏水稀释过程中,溶液的导电能力变化如图所示,
11.在25℃时,下列说法正确的是 ( )
下列说法正确的是 ( )
A.pH=3的醋酸溶液稀释100倍,pH=5
B.NaClO溶液中,离子浓度大小关系为:c(Na+)>c(ClO-)>c(OH-)>c(H+)
C.向氨水中加入稀硫酸至pH=7,此时c(NH·HO)+c(NH+)=2c(SO2-)
3 2 4 4
D.同浓度的①NHCl和②NHHSO 溶液,c(NH+):①>②
4 4 4 4
12.已知反应2X(g)+2Y(g)2W(g)+Z(g),使用催化剂和未使用催化剂时的能量变化
与反应历程如图。下列说法正确的是 ( )
A.a、b、c三点溶液的H+浓度:a>b>c
B.a、b、c三点CHCOOH的电离程度:c<a<b
3
c(CHCOOH) c(CHCOOH)
C.向c点溶液加水, 3 变小, 3 不变
c(H+) c(CHCOO-)c(H+)
3
D.a、b、c三点溶液用1mol·L-1NaOH溶液中和,消耗NaOH溶液体积:c<a<b
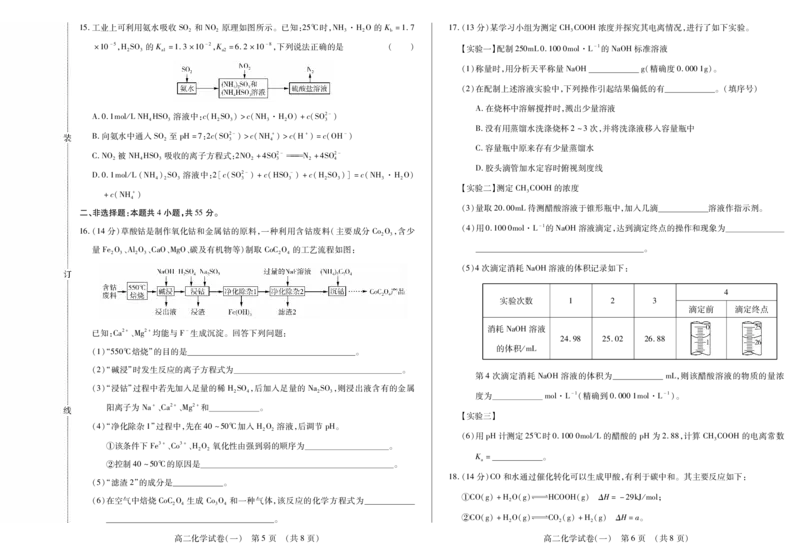
高二化学试卷(一) 第3页 (共8页) 高二化学试卷(一) 第4页 (共8页)15.工业上可利用氨水吸收 SO 和 NO 原理如图所示。已知:25℃时,NH·HO的 K =1.7 17.(13分)某学习小组为测定CHCOOH浓度并探究其电离情况,进行了如下实验。
2 2 3 2 b 3
×10-5,HSO 的K =1.3×10-2,K =6.2×10-8,下列说法正确的是 ( ) 【实验一】配制250mL0.1000mol·L-1的NaOH标准溶液
2 3 a1 a2
(1)称量时,用分析天平称量NaOH g(精确度0.0001g)。
(2)在配制上述溶液实验中,下列操作引起结果偏低的有 。(填序号)
A.在烧杯中溶解搅拌时,溅出少量溶液
A.0.1mol/LNHHSO 溶液中:c(HSO)>c(NH·HO)+c(SO2-)
4 3 2 3 3 2 3
B.没有用蒸馏水洗涤烧杯2~3次,并将洗涤液移入容量瓶中
B.向氨水中通入SO 至pH=7:2c(SO2-)>c(NH+)>c(H+)=c(OH-)
2 3 4
C.容量瓶中原来存有少量蒸馏水
C.NO 被NHHSO 吸收的离子方程式:2NO +4SO2-N +4SO2-
2 4 3 2 3 2 4
D.胶头滴管加水定容时俯视刻度线
D.0.1mol/L(NH)SO 溶液中:2[c(SO2-)+c(HSO-)+c(HSO)]=c(NH·HO)
4 2 3 3 3 2 3 3 2
【实验二】测定CHCOOH的浓度
+c(NH+) 3
4
(3)量取20.00mL待测醋酸溶液于锥形瓶中,加入几滴 溶液作指示剂。
二、非选择题:本题共4小题,共55分。
(4)用0.1000mol·L-1的NaOH溶液滴定,达到滴定终点的操作和现象为
16.(14分)草酸钴是制作氧化钴和金属钴的原料,一种利用含钴废料(主要成分 CoO,含少
2 3
量FeO、AlO、CaO、MgO、碳及有机物等)制取CoCO 的工艺流程如图: 。
2 3 2 3 2 4
(5)4次滴定消耗NaOH溶液的体积记录如下:
4
实验次数 1 2 3
滴定前 滴定终点
消耗NaOH溶液
已知:Ca2+、Mg2+均能与F-生成沉淀。回答下列问题:
24.98 25.02 26.88
的体积/mL
(1)“550℃焙烧”的目的是 。
(2)“碱浸”时发生反应的离子方程式为 。
第4次滴定消耗 NaOH溶液的体积为 mL,则该醋酸溶液的物质的量浓
(3)“浸钴”过程中若先加入足量的稀 HSO,后加入足量的 NaSO,则浸出液含有的金属
2 4 2 3 度为 mol·L-1(精确到0.0001mol·L-1)。
阳离子为Na+、Ca2+、Mg2+和 。
【实验三】
(4)“净化除杂1”过程中,先在40~50℃加入HO 溶液,后调节pH。
2 2
(6)用pH计测定25℃时0.1000mol/L的醋酸的 pH为2.88,计算 CHCOOH的电离常数
3
①该条件下Fe3+、Co3+、HO 氧化性由强到弱的顺序为 。
2 2
K= 。
a
②控制40~50℃的原因是 。
18.(14分)CO和水通过催化转化可以生成甲酸,有利于碳中和。其主要反应如下:
(5)“滤渣2”的成分是 。
①CO(g)+HO(g)幑幐HCOOH(g) ΔH=-29kJ/mol;
(6)在空气中焙烧CoCO 生成 CoO 和一种气体,该反应的化学方程式为 2
2 4 3 4
。 ②CO(g)+HO(g)幑幐CO(g)+H(g) ΔH=a。
2 2 2
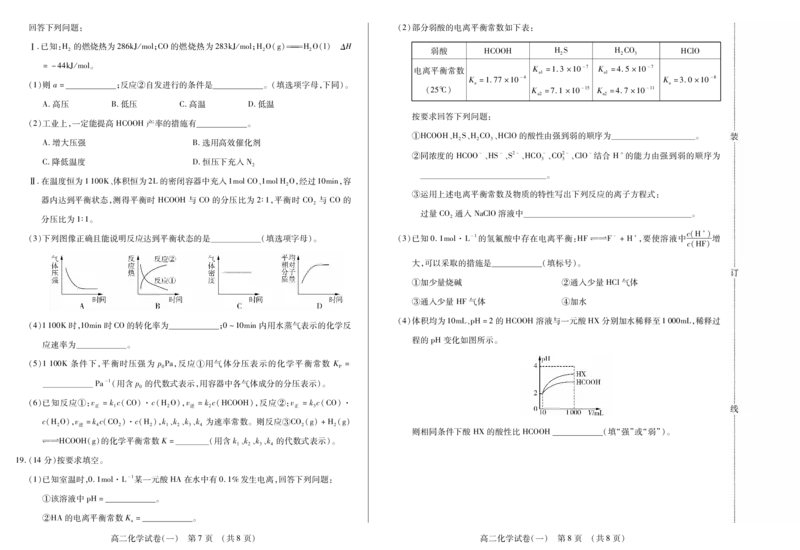
高二化学试卷(一) 第5页 (共8页) 高二化学试卷(一) 第6页 (共8页)回答下列问题: (2)部分弱酸的电离平衡常数如下表:
Ⅰ.已知:H 的燃烧热为286kJ/mol;CO的燃烧热为283kJ/mol;HO(g)HO(l) ΔH
2 2 2 弱酸 HCOOH HS HCO HClO
2 2 3
=-44kJ/mol。 电离平衡常数 K =1.3×10-7 K =4.5×10-7
a1 a1
K=1.77×10-4 K=3.0×10-8
(1)则a= ;反应②自发进行的条件是 。(填选项字母,下同)。 a a
(25℃) K =7.1×10-15 K =4.7×10-11
a2 a2
A.高压 B.低压 C.高温 D.低温
按要求回答下列问题:
(2)工业上,一定能提高HCOOH产率的措施有 。
①HCOOH、HS、HCO、HClO的酸性由强到弱的顺序为 。
2 2 3
A.增大压强 B.选用高效催化剂
②同浓度的HCOO-、HS-、S2-、HCO-、CO2-、ClO-结合 H+的能力由强到弱的顺序为
C.降低温度 D.恒压下充入N 3 3
2
。
Ⅱ.在温度恒为1100K、体积恒为2L的密闭容器中充入1molCO、1molHO,经过10min,容
2
③运用上述电离平衡常数及物质的特性写出下列反应的离子方程式:
器内达到平衡状态,测得平衡时 HCOOH与 CO的分压比为2∶1,平衡时 CO 与 CO的
2
过量CO 通入NaClO溶液中 。
分压比为1∶1。 2
c(H+)
(3)下列图像正确且能说明反应达到平衡状态的是 (填选项字母)。 (3)已知0.1mol·L-1的氢氟酸中存在电离平衡:HF幑幐F-+H+,要使溶液中 增
c(HF)
大,可以采取的措施是 (填标号)。
①加少量烧碱 ②通入少量HCl气体
③通入少量HF气体 ④加水
(4)体积均为10mL、pH=2的HCOOH溶液与一元酸HX分别加水稀释至1000mL,稀释过
(4)1100K时,10min时CO的转化率为 ;0~10min内用水蒸气表示的化学反
程的pH变化如图所示。
应速率为 。
(5)1100K条件下,平衡时压强为 pPa,反应①用气体分压表示的化学平衡常数 K =
0 P
Pa-1(用含p的代数式表示,用容器中各气体成分的分压表示)。
0
(6)已知反应①:v =kc(CO)·c(HO),v =kc(HCOOH),反应②:v =kc(CO)·
正 1 2 逆 2 正 3
c(HO),v =kc(CO)·c(H),k、k、k、k为速率常数。则反应③CO(g)+H(g)
2 逆 4 2 2 1 2 3 4 2 2
则相同条件下酸HX的酸性比HCOOH (填“强”或“弱”)。
幑幐HCOOH(g)的化学平衡常数K= (用含k、k、k、k的代数式表示)。
1 2 3 4
19.(14分)按要求填空。
(1)已知室温时,0.1mol·L-1某一元酸HA在水中有0.1%发生电离,回答下列问题:
①该溶液中pH= 。
②HA的电离平衡常数K= 。
a
高二化学试卷(一) 第7页 (共8页) 高二化学试卷(一) 第8页 (共8页)