文档内容
高 2024 级高二上期中期考试化学试题
出题人:高杰 审题人:何会梅
可能用到的相对原子质量:H-1 O-16 S-32 Fe-56
一、选择题:本题共14小题,每题3分,共42分。在每小题给出的四个选项中,只有一项
是符合题目要求的。
1.化学与生产、生活和社会发展密切相关,下列说法错误的是( )
A.含氟牙膏可以预防龋齿,利用了沉淀转化的原理,降低龋齿的发生率
B.水玻璃具有黏结力强、耐高温等特性,可作黏合剂和防火剂,它是一种强电解质
C.明矾水去除青铜器上的铜锈是利用盐类水解产生的酸与碱式盐反应
D.TiO 广泛用于涂料、橡胶和造纸等工业,可通过TiCl 与水反应制备
2 4
2.下列化学用语表示正确的是( )
A.如果25号Mn元素的基态电子排布式为1s22s22p63s23p63d7,则违反了构造原理
B.用电子式表示HCl的形成过程为
C.若硫原子核外电子排布图为 ,则违反了泡利原理
D.钠原子由1s22s22p63p11s22s22p63s1时原子释放能量,产生的原子光谱为吸收光谱
3.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.c (H+)=1×10-12mol·L-1 的溶液:[Al(OH) ]-、Na+、Cl-、SO2
水 4 4
K
B.
c
H
W =1×10-3mol·L-1 的溶液:NH
4
、Ca2+、Cl-、NO
3
C.澄清透明的溶液:K+、NH、MnO、HCO
4 4 3
D.使甲基橙变红的溶液:Na+、Fe2+、NO、SiO2
3 3
4.“宏观辨识与微观探析”是化学学科核心素养之一。下列解释事实的方程式正确的是
( )
A. 碳酸钠溶液呈碱性:CO22H OH CO 2OH
3 2 2 3
B.向漂白粉溶液中通入过量的SO :ClOSO HOHSOHClO
2 2 2 3
C.可溶性铁盐水解作净水剂的原理:Fe33H OFeOH 3H
2 3
D.硫代硫酸钠与稀硫酸的反应:S O22H SSO H O
2 3 2 2
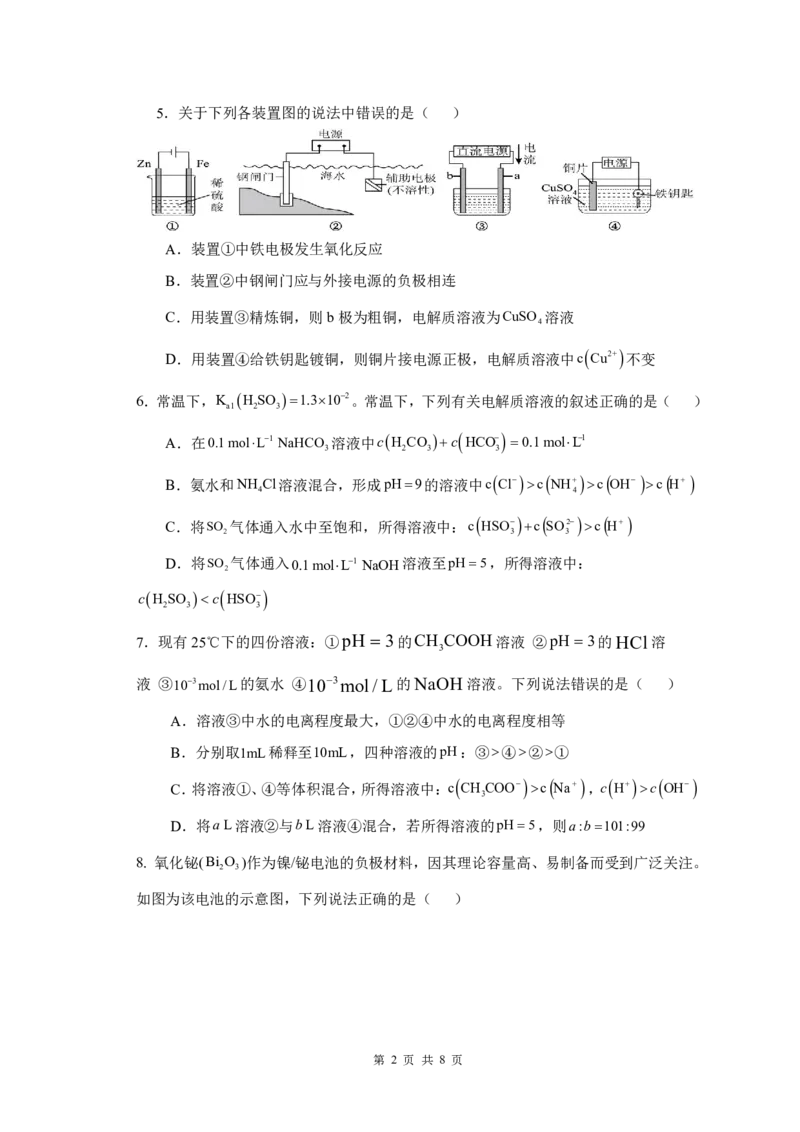
第 1 页 共 8 页5.关于下列各装置图的说法中错误的是( )
A.装置①中铁电极发生氧化反应
B.装置②中钢闸门应与外接电源的负极相连
C.用装置③精炼铜,则b极为粗铜,电解质溶液为CuSO 溶液
4
D.用装置④给铁钥匙镀铜,则铜片接电源正极,电解质溶液中c
Cu2+
不变
6.常温下,K H SO 1.3102。常温下,下列有关电解质溶液的叙述正确的是( )
a1 2 3
A.在0.1 molL1 NaHCO 溶液中cH CO c HCO 0.1 molL1
3 2 3 3
B.氨水和NH Cl溶液混合,形成pH9的溶液中c Cl c NH c OH c H
4 4
C.将SO 气体通入水中至饱和,所得溶液中:c HSO c SO2 c H
2 3 3
D.将SO 气体通入0.1 molL1 NaOH溶液至pH5,所得溶液中:
2
cH SO c HSO
2 3 3
7.现有25℃下的四份溶液:①pH 3的CH COOH溶液 ②pH 3的HCl溶
3
液 ③103mol/L的氨水 ④103mol/L的NaOH 溶液。下列说法错误的是( )
A.溶液③中水的电离程度最大,①②④中水的电离程度相等
B.分别取1mL稀释至10mL,四种溶液的pH:③④②①
C.将溶液①、④等体积混合,所得溶液中:c
CH
COO
c
Na
,c
H
c
OH
3
D.将aL溶液②与bL溶液④混合,若所得溶液的pH5,则a:b101:99
8. 氧化铋(Bi O )作为镍/铋电池的负极材料,因其理论容量高、易制备而受到广泛关注。
2 3
如图为该电池的示意图,下列说法正确的是( )
第 2 页 共 8 页A.放电时,OH从电极a移向电极b
B.放电时,总反应为6NiOOH2Bi6NiOBi O 3H O
2 3 2
C.充电时,电子从电源负极→电极a→电极b→电源正极
D.充电时,电路中转移1mol电子,阳极质量减少17g
9.X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X是宇宙中含量最多的
元素,基态Y原子的价电子中有3个未成对电子,Y与Z相邻,Z、M的核电荷数之比
为2:3,基态Q原子的价电子中s能级和p能级的电子数相等。下列说法不
.
正
.
确
.
的是( )
A.简单氢化物的稳定性:ZYQ
B.电负性:ZYXQM
C.Q的单质是良好的导体
D.1mol的M单质分别与足量Y、Z的单质反应转移的电子数目相同
10.以菱镁矿(主要成分为MgCO ,含少量SiO ,Fe O 和Al O )为原料制备高纯
3 2 2 3 2 3
镁砂(MgO)的工艺流程如下:
已知浸出时产生的废渣中有SiO ,FeOH 和AlOH 。下列说法正确的是( )
2 3 3
A.浸出镁的反应离子方程式为MgO2NH=Mg22NH ↑H O
4 3 2
B.浸出和沉镁的操作均应在较高温度下进行
C.“沉镁”后的操作需要用到的玻璃仪器有分液漏斗、烧杯、玻璃棒
D.分离Mg2与Al3、Fe3是利用了MgOH 的K 远小于FeOH 、AlOH 的K
2 sp 3 3 sp
11.根据下列实验操作和实验现象得到的结论正确的是( )
选 探究方案 探究目的
第 3 页 共 8 页项
向某FeCl 溶液样品中加入硫酸酸化的KMnO 溶液, 判断某FeCl 溶液样品中是
3 4 3
A
紫色褪去 否含有Fe2+
向3mL 1molL1 FeCl
3
溶液逐滴加入同体积同浓度 SO2与Fe3在水溶液中存
3
B Na SO 溶液,先出现红褐色沉淀,放置1h后沉淀消 在水解反应和氧化还原反
2 3
应的竞争
失,溶液变为绿色
用pH试纸测定浓度均为0.1molL1的NaClO溶液和 比较HClO、CH
3
COOH酸
C
CH COONa溶液的pH 性相对强弱
3
向Na CO 和Na S的混合溶液中滴入少量AgNO 溶 比较Ag CO 与Ag S溶解
2 3 2 3 2 3 2
D
液,先产生黑色沉淀(Ag S) 度相对大小
2
12.稀氨水中存在电离平衡:NH H O NH OH。室温下,向稀氨水中分别加入(或
3 2 4
通入)下列物质,下列正确的是( )
A.加水稀释,平衡正向移动,溶液pH增大
B.通入NH ,平衡正向移动,NH H O的电离程度增大,恢复至室温电离平衡常
3 3 2
数不变
C.通入HCl,平衡正向移动,溶液中c
NH
和c
OH
均增大
4
c
NH
D.加入NaOH固体,平衡逆向移动,恢复至室温, 4 减小
cNH H O
3 2
13.已知相同温度下,K (BaSO )G>F ②电负性:E>D>C
③简单离子半径:H3+>F+>E2- ④最高价含氧酸的酸性:J>I>C
(5)已知元素周期表中存在对角线规则,如B与H在元素周期表中处于对角线位置则化学
性质相似,B的氧化物、氢氧化物也有两性,写出B的氧化物与F的氢氧化物反应的离
第 5 页 共 8 页子方程式 。
16.(15分)铁是人体必需的微量元素,临床常见的贫血是缺铁性贫血。某实验小组为
了分析某补血剂FeSO ·7H O中铁元素的质量分数,设计如下实验。
4 2
步骤一:精确称量样品15.0g,加入适量硫酸溶解并配制成250mL溶液。
步骤二:取所配溶液25.00mL于锥形瓶中,用0.1000mol/LKMnO 溶液滴定至终点,重
4
复操作3次,记录消耗KMnO 溶液的体积。
4
(1)步骤二中KMnO 溶液应用 (选“a”或者“b”)滴定管盛装。滴定时发生
4
反应的离子方程式为 。
(2)滴定前,有关滴定管的正确操作为(选出正确操作并按序排列): 。
检漏→蒸馏水洗涤→___→___→___→___→___→开始滴定。
a.装入0.1000mol/LKMnO 溶液至零刻度以上 b.用0.1000mol/LKMnO 溶液润洗2
4 4
至3次 c.排除气泡 d.记录起始读数 e.调整液面至零刻度或零刻度以下
(3)滴定时,用左手控制滴定管的活塞,右手摇动锥形瓶,眼睛注视 ,直到滴定终点。
(4)到达滴定终点的现象是 。
(5)滴定数据如下表,则所测补血剂中铁元素的质量分数是 (结果精确到0.1%)。
0.1000mol/LKMnO 溶液体积/mL
4
实验序号 待测溶液体积/mL
滴定前刻度 滴定后刻度
1 25.00 0.00 19.02
2 25.00 0.56 20.00
3 25.00 0.22 19.20
(6)下列情况会造成测定结果偏高的是 。
a.盛装KMnO 溶液的滴定管,未用KMnO 溶液润洗
4 4
b.盛装补血剂样品溶液的锥形瓶,用蒸馏水洗过后未用样品溶液润洗
c.盛装KMnO 溶液的滴定管,滴定前尖嘴处有气泡,滴定后气泡消失
4
d.滴定过程中锥形瓶里不慎有液体溅出
e.滴定终点读数时,俯视滴定管的刻度
(7)若该小组配制溶液和滴定操作时引起的误差忽略,最终所测补血剂中铁元素含量仍偏
小,其可能的原因是 。
第 6 页 共 8 页17.(14分)甲酸(HCOOH)是一种有机化工原料,广泛用于农药、医药等工业。回答下
列问题:
(1)已知室温时,1molL1HCOOH在水中有1%发生电离,由其电离出的c
H
约为水电离
出的c
H
的 倍。
(2)部分弱酸、弱碱的电离平衡常数如下表:
弱酸、弱
HCOOH HClO H CO H SO NH H O
2 3 2 3 3 2
碱
K a 或 1.77104 4.7108 K
a1
4.2107 K
a1
1.54102
1.7105
K
b
(25℃) K
a2
5.61011 K
a2
1.02107
①等物质的量浓度的a.NH ClO溶液、b.NH HCO 溶液、c.NH HSO 溶液的pH由大
4 4 3 4 3
到小的顺序为 (填序号);
②将少量CO 通入NaClO溶液,反应的离子方程式是
2
③25℃时,向20mL 0.1molL1的氨水中滴加0.1molL1的HCOOH溶液,当滴加
VmLHCOOH溶液时,混合溶液的pH7,则V 20mL (填“>”“<”或“=”)。
④25℃时,将a molL1的HCOOH与b molL1的BaOH 溶液等体积混合(忽略溶液体积
2
变化),充分反应后,溶液中存在2c
Ba2+
c
HCOO
,则该混合溶液中HCOOH的电离
常数K HCOOH (用含a和b的代数式表示)。
a
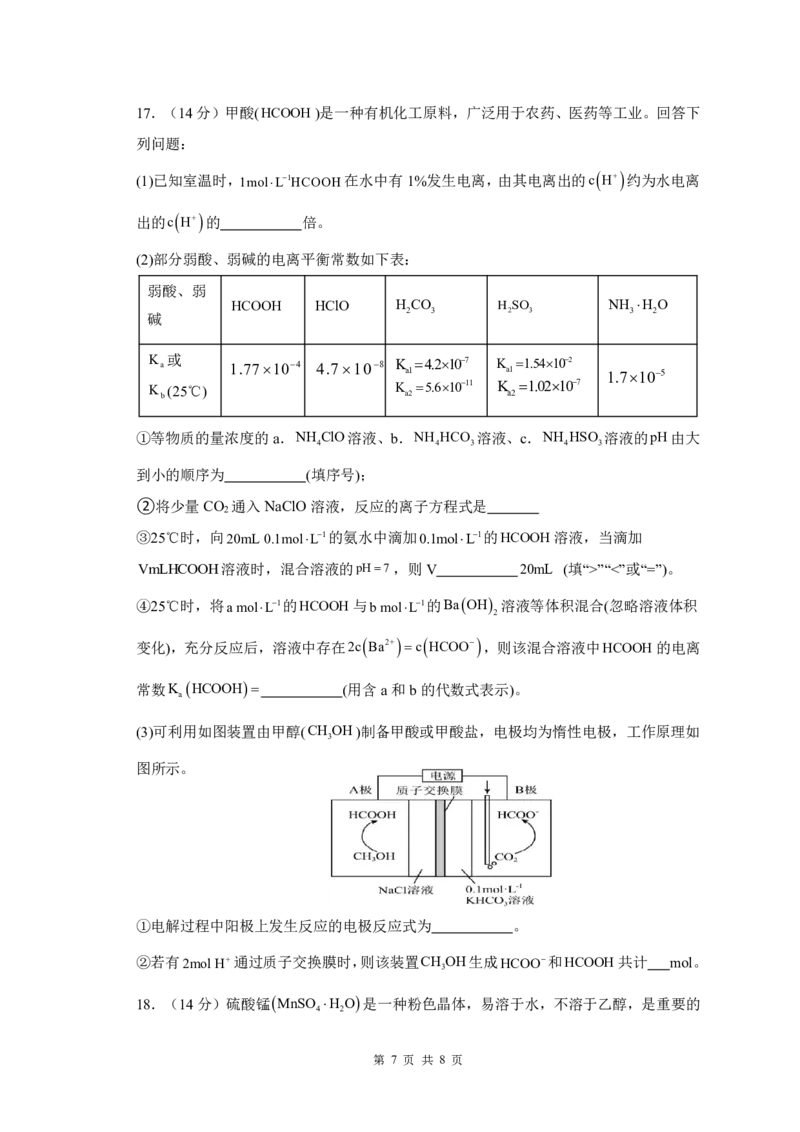
(3)可利用如图装置由甲醇(CH OH)制备甲酸或甲酸盐,电极均为惰性电极,工作原理如
3
图所示。
①电解过程中阳极上发生反应的电极反应式为 。
②若有2mol H通过质子交换膜时,则该装置CH OH生成HCOO和HCOOH共计 mol。
3
18.(14分)硫酸锰MnSO H O是一种粉色晶体,易溶于水,不溶于乙醇,是重要的
4 2
第 7 页 共 8 页微量元素肥料之一、工业上由天然二氧化锰与硫化锰矿(还含Fe、Al、Mg、Si等元素的
氧化物)制备硫酸锰的工艺如图所示。回答下列问题:
已知:①相关物质的溶度积常数
物质 MnOH FeOH MgOH FeOH AlOH MgF
2 2 2 3 3 2
K 2.01013 4.91017 5.61012 2.81039 1.31033 7.41011
sp
② 7.4 2.7
(1)为加快“溶浸”过程的浸出速率,可采取的措施有 (任写一种)。
(2)“滤渣1”中含有S和 ,请写出生成S主要的离子方程式 。
(3)加入H O 的作用是 。
2 2
(4)加入MnF 除镁时,需控制溶液中c(F-)> molL1才能将Mg2沉淀完全。
2
(5)“沉锰”时发生的离子方程式为 。
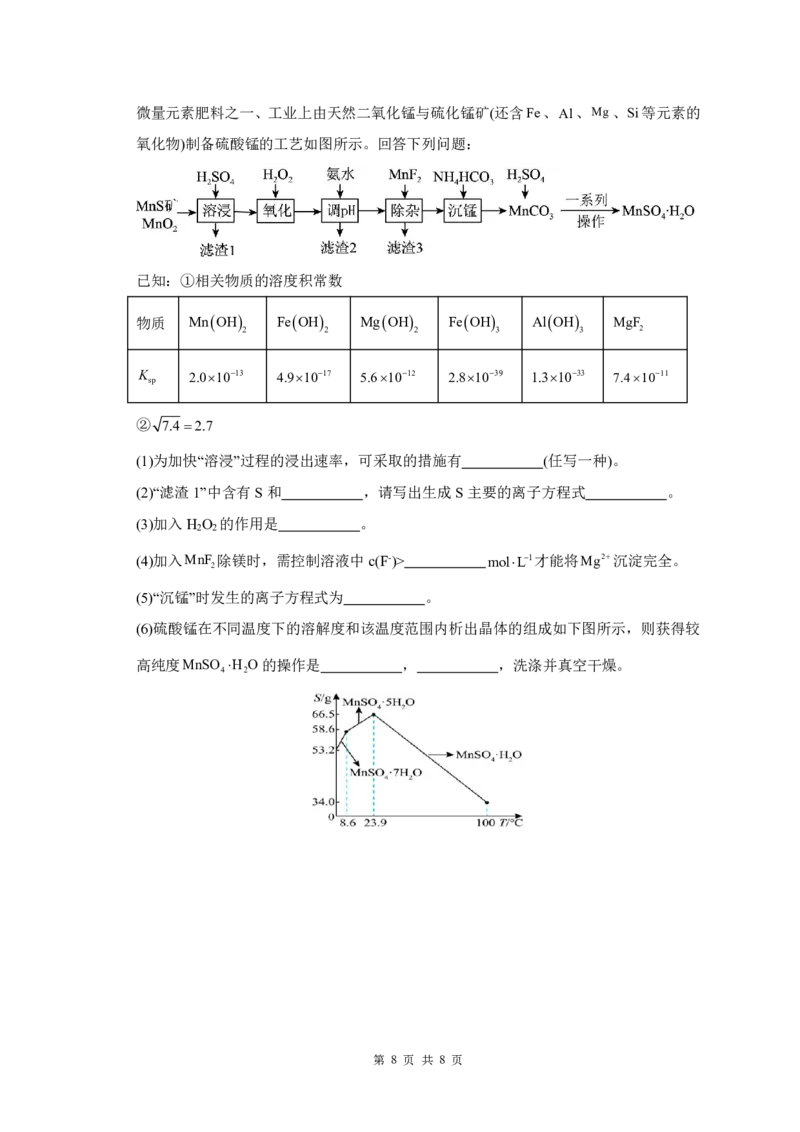
(6)硫酸锰在不同温度下的溶解度和该温度范围内析出晶体的组成如下图所示,则获得较
高纯度MnSO H O的操作是 , ,洗涤并真空干燥。
4 2
第 8 页 共 8 页