文档内容
名校联考联合体 2025 届新高三年级入学摸底考试
化学
时量:75分钟 满分:100分
得分:________
可能用到的相对原子质量:H~1 Li~7 C~12 N~14 O~16 Na~23 P~31 S~32
Ta~181
一、选择题(本题共 14 小题,每小题 3分,共 42分。在每小题给出的四个选项中,只有一
项是符合题目要求的)
1.在“厨房化学”中,下列相关化合物属于弱电解质的是( )
A.纯碱:Na CO B.大理石:CaCO C.白醋:CH COOH D.酒精:CH CH OH
2 3 3 3 3 2
2.镓溶于高氯酸可制备配合物,反应的化学方程式为
2Ga+6HClO +12H O=== 2
Ga ( H O )
( ClO ) +3H ↑。下列叙述错误的是( )
4 2 2 6 4 3 2
A.基态镓原子的电子排布式为[Ar]4s24p1
B.HClO 在水中的电离方程式为HClO === H+ +ClO−
4 4 4
C.H O的空间结构为
2
D.H 分子含s-sσ键
2
3.下列装置或操作能达到实验目的的是( )
A.选择装置Ⅰ利用电石和饱和食盐水制备乙炔
B.选择装置Ⅱ验证氨气易溶于水且水溶液呈碱性
C.选择装置Ⅲ分别干燥氯化氢、氧气、氨气和一氧化氮
D.选择装置Ⅳ利用NaOH溶液和FeSO
4
溶液制备Fe(OH)
2
4.如图表示硅、磷、硫、氯元素性质递变规律,纵坐标代表的性质是( )
学科网(北京)股份有限公司A.原子半径 B.电负性 C.第一电离能 D.单质的熔点
5.在下列指定溶液中,能大量共存的离子组是( )
A.在0.1mol⋅L−1K
Fe ( CN )
溶液中: Na+ 、Fe2+ 、SO2−、Cl−
3 6 4
B.在0.1mol⋅L−1HI溶液中: Al3+ 、Fe3+ 、HCO−、SO2−
3 4
C.在0.1mol⋅L−1氨水中: K+ 、Cu2+ 、NO−、Cl−
3
D.在0.1mol⋅L−1KAl(SO ) 溶液中: NH+、Na+ 、NO−、ClO−
4 2 4 3 4
6.五种短周期主族元素W、R、X、Y、Z的原子序数依次增大,部分元素的原子半径和最低化合价关系如
下图所示,基态X原子核外p能级上电子数比s能级上电子数多2。
R元素的部分逐级电离能数据如下表所示。
电离能/(kJ·mol-1)
元素
I I I I ……
1 2 3 4
R 738 1451 7733 10540 ……
下列叙述正确的是( )
A.熔点:RZ >RW
2
B.化学键中离子键成分的百分数:RW>RY
C.XW2−和YW2−的VSEPR模型相同
3 3
D.XZ 和Z W都是非极性分子
4 2
7.下列有关物质检验的叙述正确的是( )
A.用酸性KMnO 溶液可检验对甲基苯乙醇中的醇羟基
4
B.用AgNO 溶液可检验CH CH Br和CH CH I
3 3 2 3 2
C.用湿润的淀粉-KI试纸可检验NO
2
、N
2
O
4
的混合气体和Br (g)
2
D.用浓氨水可检验AgCl和Mg(OH)
2
8.丁基羟基茴香醚(BHA)常用作脂肪、油和乳化脂肪制品的抗氧化剂。其有如图所示两种结构。下列叙
学科网(北京)股份有限公司述正确的是( )
A.2-BHA和3-BHA互为同系物
B.BHA作抗氧化剂是因为它难与O 反应
2
C.等质量的2-BHA、3-BHA与足量的浓溴水反应时消耗Br 的量相等
2
D.1molBHA最多能消耗106gNa CO
2 3
9.粗乙酸异戊酯产品混有乙酸、异戊醇等杂质,提纯乙酸异戊酯流程如图所示。
已知:纯乙酸异戊酯的密度为0.876g/cm3,沸点为142.5℃。下列叙述错误的是( )
A.试剂1为烧碱溶液,操作1为分液
B.操作3为蒸馏,收集142.5℃左右馏分
C.操作2需要三种玻璃仪器:烧杯、漏斗和玻璃棒
D.操作1中有机相从分液漏斗上口倒出
10.第33届夏季奥运会于2024年7月在法国巴黎开幕。发令枪火药中的药粉含有氯酸钾(KClO )和红磷
3
(P)等物质,撞击引发的有关化学反应有:①5KClO +6P=== 3PO +5KCl;②
3 2 5
PO +3H O=2H PO (产生烟雾)。设N 为阿伏加德罗常数的值。下列叙述正确的是( )
2 5 2 3 4 A
A.反应①中,氧化产物、还原产物的物质的量之比为5∶3
B.反应①中,6.2gP完全反应转移电子数目为N
A
C.H PO 易溶于水的原因是磷酸与水存在分子内氢键
3 4
D.1molH PO 在水中电离产生的PO3−数目为N
3 4 4 A
11.经X射线衍射实验测定,某金属单质M有如图甲、乙所示两种晶胞。已知:甲晶胞参数为anm,乙晶
胞参数为bnm。下列叙述正确的是( )
图甲 图乙
学科网(北京)股份有限公司A.1个图甲晶胞含4个金属原子
B.M晶体由阴离子和阳离子构成
C.图乙中两个粒子之间最近距离为bnm
2a3
D.图甲和图乙晶体密度之比为
b3
12.常温下,向含(CH COO) Mg、CH
3
COOH的混合液中滴加氨水,混合液中[,pX=−lgX,
3 2
c
(
CH
COO−)
c
( NH+)
X=c ( Mg2+) 、 3 、 4 ]与pH关系如图所示。
c ( CH COOH ) c ( NH ⋅H O )
3 3 2
下列叙述错误的是( )
A.L 代表−lgc
( Mg2+)
与pH关系
3
B.Q点对应的溶液中c
(
CH
COO−)
=c
( NH+)
>c
( H+)
=c
( OH−)
3 4
K (CH COOH)
C.常温下,电离常数比 a 3 =1
K (NH ⋅H O)
b 3 2
D.Mg(OH) +2CH COOH Mg2+ +2CH COO− +2H O的平衡常数K =107.23
2 3 3 2
13.香港理工大学应用物理系的黄海涛教授基于对钙钛矿结构的重新解读,提出钙钛矿晶格可作为构筑孤立
活性位点的平台用于氧还原(ORR)选择性合成双氧水(H O )。电化学装置如图所示。
2 2
下列叙述错误的是( )
A.质子
( H+)
由a极区向b极区迁移
B.a极为阳极,发生氧化反应
学科网(北京)股份有限公司C.b极反应式为O +2e− +2H+ === H O
2 2 2
D.a极生成n(O )等于b极消耗n(O )
2 2
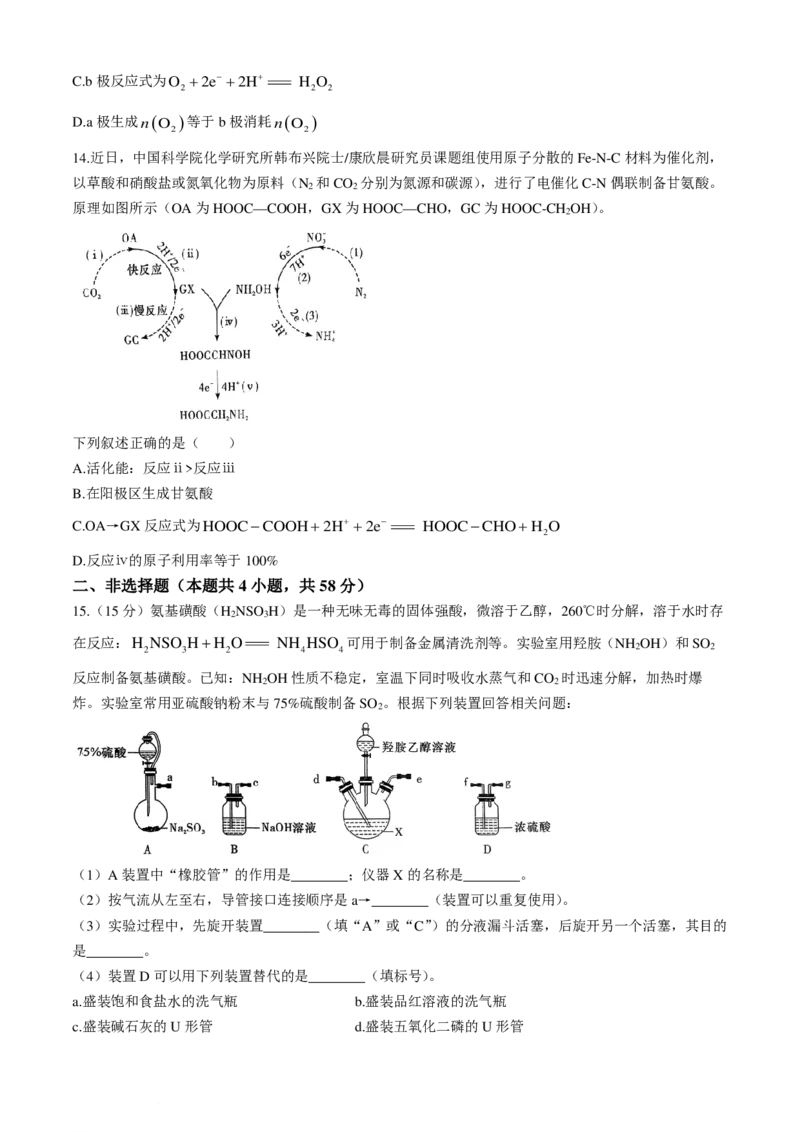
14.近日,中国科学院化学研究所韩布兴院士/康欣晨研究员课题组使用原子分散的Fe-N-C材料为催化剂,
以草酸和硝酸盐或氮氧化物为原料(N 和CO 分别为氮源和碳源),进行了电催化C-N偶联制备甘氨酸。
2 2
原理如图所示(OA为HOOC—COOH,GX为HOOC—CHO,GC为HOOC-CH OH)。
2
下列叙述正确的是( )
A.活化能:反应ⅱ>反应ⅲ
B.在阳极区生成甘氨酸
C.OA→GX反应式为HOOC−COOH+2H+ +2e− === HOOC−CHO+H O
2
D.反应ⅳ的原子利用率等于100%
二、非选择题(本题共 4小题,共 58分)
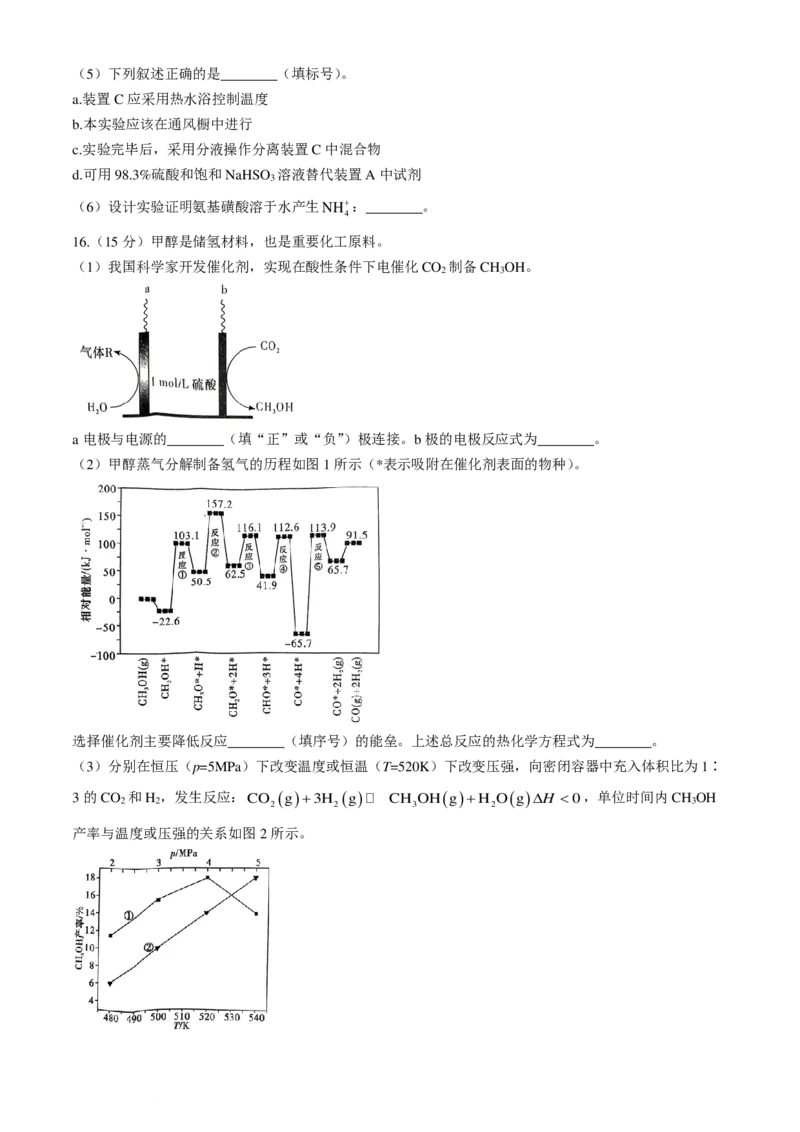
15.(15分)氨基磺酸(H NSO H)是一种无味无毒的固体强酸,微溶于乙醇,260℃时分解,溶于水时存
2 3
在反应:H NSO H+H O=== NH HSO 可用于制备金属清洗剂等。实验室用羟胺(NH OH)和SO
2 3 2 4 4 2 2
反应制备氨基磺酸。已知:NH OH性质不稳定,室温下同时吸收水蒸气和CO 时迅速分解,加热时爆
2 2
炸。实验室常用亚硫酸钠粉末与75%硫酸制备SO 。根据下列装置回答相关问题:
2
(1)A装置中“橡胶管”的作用是________;仪器X的名称是________。
(2)按气流从左至右,导管接口连接顺序是a→________(装置可以重复使用)。
(3)实验过程中,先旋开装置________(填“A”或“C”)的分液漏斗活塞,后旋开另一个活塞,其目的
是________。
(4)装置D可以用下列装置替代的是________(填标号)。
a.盛装饱和食盐水的洗气瓶 b.盛装品红溶液的洗气瓶
c.盛装碱石灰的U形管 d.盛装五氧化二磷的U形管
学科网(北京)股份有限公司(5)下列叙述正确的是________(填标号)。
a.装置C应采用热水浴控制温度
b.本实验应该在通风橱中进行
c.实验完毕后,采用分液操作分离装置C中混合物
d.可用98.3%硫酸和饱和NaHSO 溶液替代装置A中试剂
3
(6)设计实验证明氨基磺酸溶于水产生NH+:________。
4
16.(15分)甲醇是储氢材料,也是重要化工原料。
(1)我国科学家开发催化剂,实现在酸性条件下电催化CO 制备CH OH。
2 3
a电极与电源的________(填“正”或“负”)极连接。b极的电极反应式为________。
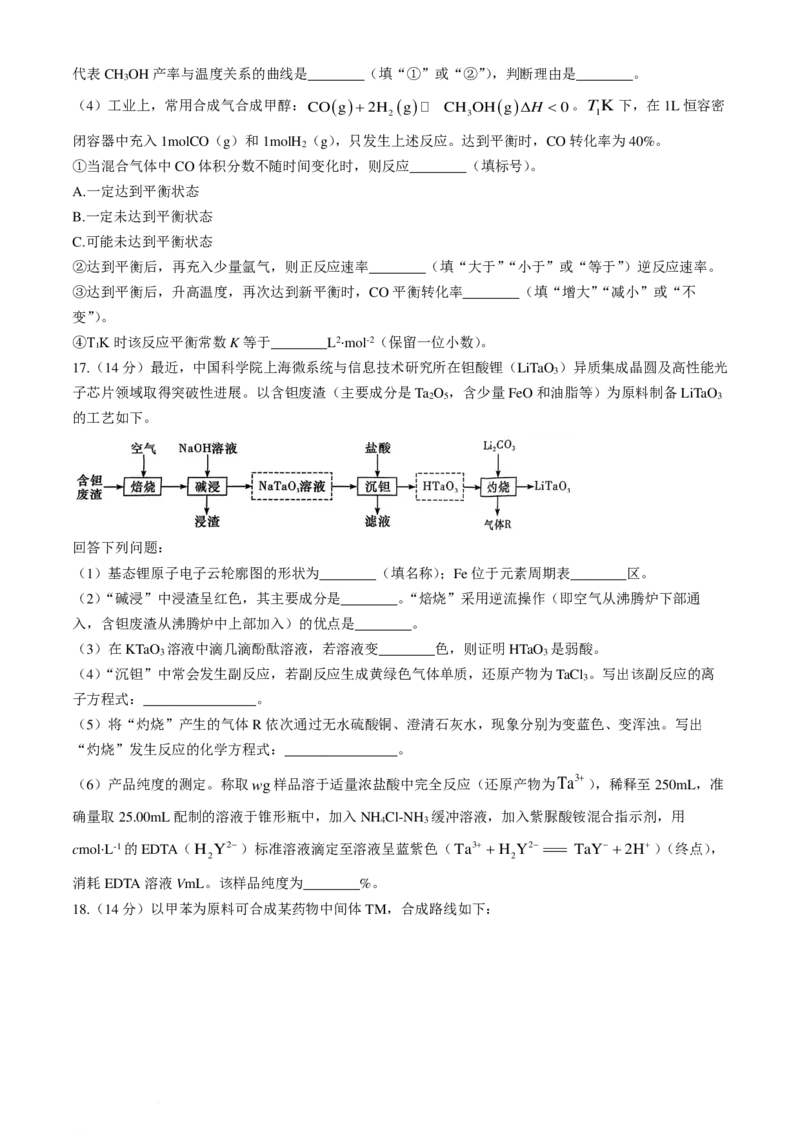
(2)甲醇蒸气分解制备氢气的历程如图1所示(*表示吸附在催化剂表面的物种)。
选择催化剂主要降低反应________(填序号)的能垒。上述总反应的热化学方程式为________。
(3)分别在恒压(p=5MPa)下改变温度或恒温(T=520K)下改变压强,向密闭容器中充入体积比为1∶
3的CO 2 和H 2 ,发生反应:CO (g)+3H (g) CH OH(g)+H O(g)∆H <0,单位时间内CH 3 OH
2 2 3 2
产率与温度或压强的关系如图2所示。
学科网(北京)股份有限公司代表CH OH产率与温度关系的曲线是________(填“①”或“②”),判断理由是________。
3
(4)工业上,常用合成气合成甲醇:CO(g)+2H (g) CH OH(g)∆H <0。TK下,在1L恒容密
2 3 1
闭容器中充入1molCO(g)和1molH (g),只发生上述反应。达到平衡时,CO转化率为40%。
2
①当混合气体中CO体积分数不随时间变化时,则反应________(填标号)。
A.一定达到平衡状态
B.一定未达到平衡状态
C.可能未达到平衡状态
②达到平衡后,再充入少量氩气,则正反应速率________(填“大于”“小于”或“等于”)逆反应速率。
③达到平衡后,升高温度,再次达到新平衡时,CO平衡转化率________(填“增大”“减小”或“不
变”)。
④T₁K时该反应平衡常数K等于________L2mol-2(保留一位小数)。
17.(14分)最近,中国科学院上海微系统与信息技术研究所在钽酸锂(LiTaO )异质集成晶圆及高性能光
⋅ 3
子芯片领域取得突破性进展。以含钽废渣(主要成分是Ta O ,含少量FeO和油脂等)为原料制备LiTaO
2 5 3
的工艺如下。
回答下列问题:
(1)基态锂原子电子云轮廓图的形状为________(填名称);Fe位于元素周期表________区。
(2)“碱浸”中浸渣呈红色,其主要成分是________。“焙烧”采用逆流操作(即空气从沸腾炉下部通
入,含钽废渣从沸腾炉中上部加入)的优点是________。
(3)在KTaO 溶液中滴几滴酚酞溶液,若溶液变________色,则证明HTaO 是弱酸。
3 3
(4)“沉钽”中常会发生副反应,若副反应生成黄绿色气体单质,还原产物为TaCl 。写出该副反应的离
3
子方程式:________________。
(5)将“灼烧”产生的气体R依次通过无水硫酸铜、澄清石灰水,现象分别为变蓝色、变浑浊。写出
“灼烧”发生反应的化学方程式:________________。
(6)产品纯度的测定。称取wg样品溶于适量浓盐酸中完全反应(还原产物为Ta3+
),稀释至250mL,准
确量取25.00mL配制的溶液于锥形瓶中,加入NH Cl-NH 缓冲溶液,加入紫脲酸铵混合指示剂,用
4 3
cmolL-1的EDTA(H Y2−)标准溶液滴定至溶液呈蓝紫色(Ta3+ +H Y2− === TaY− +2H+)(终点),
2 2
消耗⋅ EDTA溶液VmL。该样品纯度为________%。
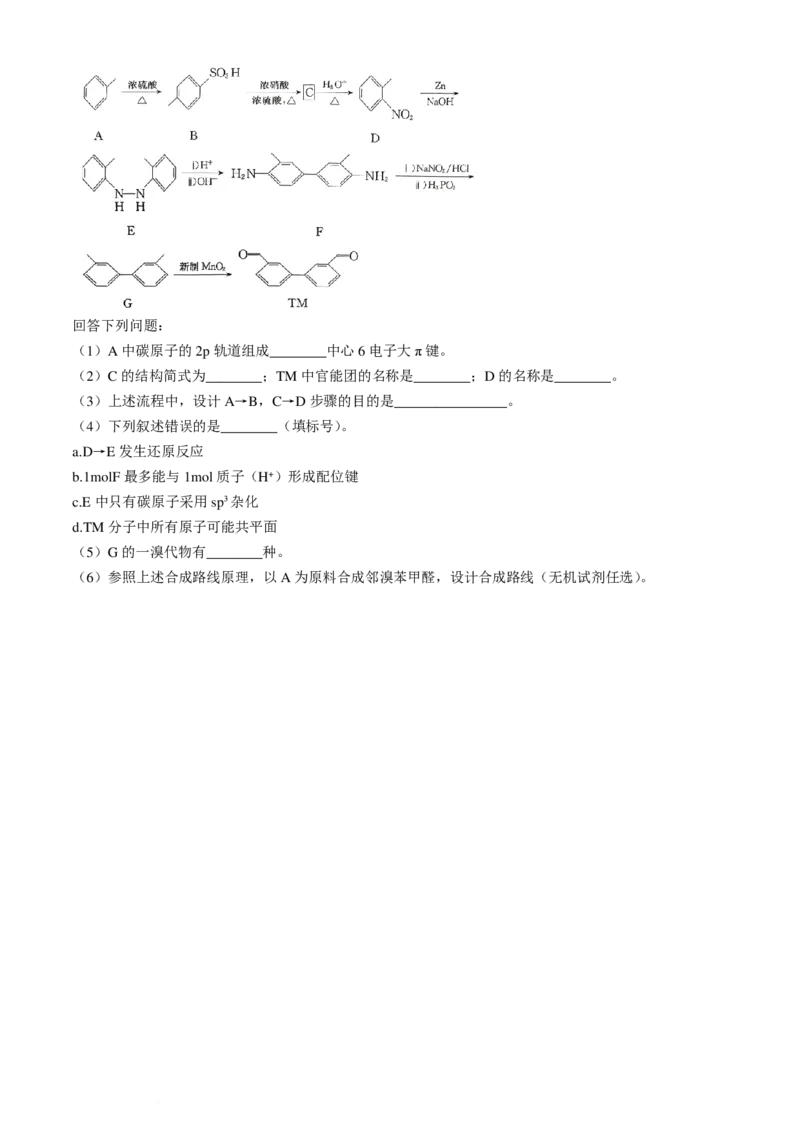
18.(14分)以甲苯为原料可合成某药物中间体TM,合成路线如下:
学科网(北京)股份有限公司回答下列问题:
(1)A中碳原子的2p轨道组成________中心6电子大π键。
(2)C的结构简式为________;TM中官能团的名称是________;D的名称是________。
(3)上述流程中,设计A→B,C→D步骤的目的是________________。
(4)下列叙述错误的是________(填标号)。
a.D→E发生还原反应
b.1molF最多能与1mol质子(H+)形成配位键
c.E中只有碳原子采用sp³杂化
d.TM分子中所有原子可能共平面
(5)G的一溴代物有________种。
(6)参照上述合成路线原理,以A为原料合成邻溴苯甲醛,设计合成路线(无机试剂任选)。
学科网(北京)股份有限公司名校联考联合体 2025 届新高三年级入学摸底考试
化学参考答案
一、选择题:本题共 14 小题,每小题 3分,共 42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 C A B C D B D D A B A B D C
1.C【解析】碳酸钠属于强电解质,A项不符合题意;碳酸钙溶于水的部分能完全电离,属于强电解质,B
项不符合题意;乙酸溶于水只部分电离,属于弱电解质,C项符合题意;乙醇属于非电解质,D项不符合
题意。
2.A【解析】基态镓原子的电子排布式为[ Ar ] 3d104s24p1,A项错误;高氯酸是强酸,HClO 在水中完全
4
电离,B项正确;H O的空间结构为V形,C项正确;H 分子中不存在杂化轨道,只存在s-sσ键,D项正
2 2
确。
3.B【解析】CaC
2
与水反应剧烈,放热多,产物Ca(OH) 微溶于水,不宜选择装置Ⅰ制备,A项错误;选
2
择装置Ⅱ能完成喷泉实验,可证明NH 易溶于水,水溶液呈碱性,B项正确;CaCl 能吸收NH ,C项错
3 2 3
误;选择装置Ⅳ制备Fe(OH) ,空气会氧化Fe(OH) ,D项错误。
2 2
4.C【解析】硅、磷、硫、氯的原子半径依次减小,A项不符合题意;硅、磷、硫、氯的电负性依次增大,
B项不符合题意;由于基态磷原子的3p轨道达到半充满结构,磷的第一电离能大于右邻元素硫,小于氯,
C项符合题意;硅晶体是共价晶体,熔点最高,磷、硫、氯的单质都是分子晶体,其熔点低于硅,氯气的
熔点最低,D项不符合题意。
5.D【解析】K+ +Fe2+ +Fe(CN) 3− === KFeFe(CN) ↓,A项不符合题意;
6 6
2Fe3+ +2I− === 2Fe2+ +I ,HCO− +H+ === CO ↑+H O,
2 3 2 2
Al3+ +3HCO− === Al(OH) ↓+3CO ↑,Fe3+ +3HCO− === Fe(OH) ↓+3CO ↑,B项不符合题
3 3 2 3 3 2
意;Cu2+ +2NH ⋅H O=== Cu(OH) ↓+2NH+,C项不符合题意;D项符合题意。
3 2 2 4
6.B【解析】五种短周期主族元素W、R、X、Y、Z的原子序数依次增大,根据图像可知,W为氧,Y为
硫,Z为氯;根据基态X原子的电子排布式为1s22s22p63s23p2可知,X为硅;根据R的逐级电离能数据
可知,I /I 约为2.0, I /I 约为5.3,故R最外层有2个电子,R为镁。MgO、MgCl 都是离子晶体,
2 1 3 2 2
MgO熔点高于MgCl ,,A项错误;O的电负性大于S,故MgO中离子键成分的百分数大于MgS,B项正
2
确;SiO2−中Si价层有3个电子对,SO2−中S价层有4个电子对,前者VSEPR模型为平面三角形,后
3 3
者VSEPR模型为四面体形,C项错误;SiCl 是非极性分子,而Cl O分子空间结构呈Ⅴ形,Cl O是极性
4 2 2
分子,D项错误。
学科网(北京)股份有限公司7.D【解析】苯环上的甲基也能被酸性高锰酸钾溶液氧化,A项错误;卤代烃在水中不能电离,正确的操
作是:加入氢氧化钠溶液,共热,冷却,滴加硝酸酸化,再滴加AgNO 溶液,根据沉淀颜色判断卤素元
3
素,B项错误;NO 和Br 都能氧化KI生成I ,C项错误;氯化银溶于氨水,氢氧化镁不溶于氨水,D项
2 2 2
正确。
8.D【解析】2-BHA和3-BHA互为同分异构体,A项错误;BHA含酚羟基,能吸收氧气,表现强还原
性,具有抗氧化性,能防止食品等被氧化,B项错误;2-BHA和3-BHA都能与浓溴水发生邻、对位取代
反应,1mol3-BHA最多能消耗1molBr ,1mol2-BHA最多能消耗2molBr ,C项错误;酚电离氢离子的能
2 2
力比碳酸的弱,与碳酸钠反应只生成碳酸氢钠,1molBHA只含1mol酚羟基,故1molBHA最多能消耗
106g(相当于1mol)Na CO ,D项正确。
2 3
9.A【解析】试剂1应选择饱和Na CO 溶液,因为在NaOH溶液中乙酸异戊酯接近完全水解,A项错误;
2 3
操作3采用蒸馏,根据产品沸点控制收集馏分温度,B项正确;操作2为过滤,需要烧杯、漏斗和玻璃棒
三种玻璃仪器,C项正确;根据已知信息可知,酯的密度小于水,酯在分液漏斗上层,上层液体从上口倒
出,D项正确。
10.B【解析】在反应①中,氧化产物为PO ,还原产物为KCl,其物质的量之比为3∶5,A项错误;
2 5
6.2gP物质的量为0.2mol,0.2molP完全反应时转移1mol电子,B项正确;H PO₁分子和水分子之间存在分
3
子间氢键,导致磷酸易溶于水,C项错误;磷酸是中强酸,在水中部分电离,D项错误。
11.A【解析】甲晶胞是面心立方晶胞,8个原子在顶点、6个原子在面心,1个甲晶胞含4个原子,A项正
确;金属晶体由金属阳离子、自由电子靠金属键构成,不含阴离子,B项错误;图乙晶胞中,体对角线上
3
3个粒子相切,两个最近粒子之间距离为d = bnm,C项错误;甲、乙晶胞含金属离子数分别为4、
2
ρ(甲) 4M N ×b3 2b3
2,二者密度之比为 = × A = ,D项错误。
ρ(乙) N ×a3 2M a3
A
12.B【解析】根据电离方程式、溶度积表达式可知, −lgc
( Mg2+)
=pK −2pK +2pH,
sp w
c
(
CH
COO−)
c
( NH+)
−lg 3 =pK −pH,−lg 3 =pK +pH−pK ,根据图像中直线斜率可知,
c ( CH COOH ) a c ( NH ⋅H O ) b w
3 3 2
c
(
CH
COO−)
c
( NH+)
L 代表−lg 3 和pH关系,L 代表−lg 4 和pH关系,L 代表−lgc ( Mg2+) 和
1 c ( CH COOH ) 2 c ( NH ⋅H O ) 3
3 3 2
pH关系,A项正确;Q点对应的溶液呈中性,溶液中还含有Mg2+,根据电荷守恒式有:
c
(
CH
COO−)
>c
( NH+)
>c
( H+)
=c
( OH−)
,B项错误;根据图像中数据计算,
3 4
K Mg ( OH ) =10−11.25,K = K =10−4.76,C项正确;
sp 2 a b
Mg(OH) +2CH COOH Mg2+ +2CH COO− +2H O的平衡常数
2 3 3 2
学科网(北京)股份有限公司K2×K ( 10−4.76 )2 ×10−11.25
K = a sp = =107.23,D项正确。
K2 ( 10−14 )2
w
13.D【解析】根据电源符号可知,a极为阳极,发生氧化反应;b极为阴极,发生还原反应,质子(H+)
由阳极区向阴极区迁移,A、B项正确;b极反应式为O +2e− +2H+ === H O ,C项正确;a极反应式
2 2 2
为2H O−4e− === 4H+ +O ↑,根据电子守恒,b极上消耗2molO 时,a极上生成1molO ,D项错
2 2 2 2
误。
14.C【解析】活化能越小,反应越快,活化能:反应ⅱ<反应ⅲ,A项错误;以草酸和硝酸盐为原料合成
H NCH COOH中,C、N的化合价都降低,发生了还原反应,故甘氨酸在阴极区生成,B项错误;根据题
2 2
图可知,OA生成GX,副产物为水,C项正确;反应ⅳ为
OHC−COOH+NH OH→HOOC−CHNOH+H O,原子利用率小于100%,D项错误。
2 2
二、非选择题:本题共 4小题,共 58分。
15.(15分)
(1)平衡气压,使硫酸顺利下滴(2分) 三颈(口)烧瓶(1分)
(2)f→g→d→e→f→g→b(2分)
(3)A(2分) 先通入SO ,排尽C中空气(2分)
2
(4)d(2分)
(5)bd(2分)
(6)取少量氨基磺酸样品于试管中,加入适量蒸馏水,再加入足量浓NaOH溶液,加热;用镊子夹一片
湿润的红色石蕊试纸放在试管口上方,若试纸变蓝色,则说明它溶于水产生NH+
4
【解析】(1)A装置中橡胶管将分液漏斗和烧瓶连通,在重力作用下,分液漏斗中硫酸顺利下滴。
(2)依题意,必须先制备干燥的SO ,否则产品混有杂质硫酸氢铵。用氢氧化钠溶液吸收尾气,要防止氢
2
氧化钠溶液中水挥发进入装置C。故装置排序为A、D、C、D、B。
(3)C中反应之前要排尽装置内CO 、水蒸气,即先旋开A中分液漏斗活塞,利用SO 将C中空气排
2 2
尽。
(4)D中浓硫酸用于干燥SO ,吸收水,可选择装有五氧化二磷的U形管替代装置D。
2
(5)依题意,NH OH性质不稳定,加热时爆炸,应用冷水浴控制温度,a错误;本实验有SO ,在通风
2 2
橱中进行,b正确;产品为固体,乙醇为液体,采用过滤操作分离,c错误;制备SO 中硫酸表现酸性,
2
又不能有过多水,因为SO 溶解度较大,可利用98.3%硫酸和饱和亚硫酸氢钠溶液反应制备SO ,d正
2 2
确。
(6)检验NH+时,先加入蒸馏水溶解,再加入足量浓氢氧化钠溶液,加热,将NH+转化成NH ,用湿润
4 4 3
的红色石蕊试纸检验NH 。
3
16.(15分)
(1)正(1分) CO +6H+ +6e− === CH OH+H O
2 3 2
学科网(北京)股份有限公司(2)⑤(1分) CH OH(g)=== CO(g)+2H (g)∆H =+91.5kJ⋅mol−1
3 2
(3)①(1分) 520K之前,未达到平衡,随着温度升高,反应速率增大,甲醇产率升高;520K后,达
到平衡,随着温度升高,平衡向左移动,甲醇产率降低(2分)
(4)①C(2分) ②等于(1分) ③减小(1分) ④16.7(2分)
【解析】(1)b极为阴极,CO 发生还原反应。a极为阳极,与电源正极连接。
2
(2)分析五步反应的能垒,第⑤步反应的能垒最大,速率最小,它是控速反应。选择催化剂主要降低速
控反应的能垒,提高总反应的速率。反应热等于产物、反应物的相对能量之差。
(3)分析反应特点,正反应是气体分子数减小的放热反应,增大压强,反应速率增大,平衡向右移动,
甲醇产率一直增大,曲线②代表甲醇产率与压强关系。曲线①代表甲醇产率与温度关系,平衡前,升高温
度,反应速率增大,甲醇产率增大;平衡后,升高温度,平衡向左移动,甲醇产率降低。
(4)①根据数据代入计算,CO体积分数始终为50%,不能据此判断反应是否达到平衡,选C;②恒容容
器中充入氩气,各反应气体浓度不变,正、逆反应速率不变;③升高温度,平衡向左移动,CO平衡转化
0.4
率减小,小于40%;④根据转化率计算:K = ≈16.7。
0.6×(0.2)2
17.(14分)
(1)球形(2分) d(2分)
(2)Fe O (1分) 增大空气与废渣接触面积,提高反应速率(2分)
2 3
(3)红(或粉红)(1分)
(4)TaO− +6H+ +2Cl− === Ta3+ +Cl ↑+3H O
3 2 2
高温
(5)2HTaO +Li CO 2LiTaO +CO ↑+H O↑
3 2 3 3 2 2
236cV
(6) (2分)
w
【解析】(1)基态锂原子的电子排布式为1s22s1,电子云轮廓图为球形。基态铁原子的电子排布式为
[ Ar ] 3d64s2,位于元素周期表d区。
(2)“焙烧”中FeO转化成Fe O ,Fe O 不溶于碱,故“浸渣”主要成分是Fe O (铁红)。逆流操作能
2 3 2 3 2 3
增大固体与气体接触面积,加快反应速率。
(3)溶液变红或粉红色,证明KTaO 是强碱弱酸盐,HTaO 是弱酸。
3 3
(4)钽酸钠氧化氯离子生成三氯化钽(完全电离)、氯气和水。
(5)依题意,气体R是H O和CO 。
2 2
(6)根据滴定反应式可知,n(LiTaO )=n(EDTA),
3
250
cV×10−3× ×236
236cV
ω( LiTaO )= 25.00 ×100%= %。
3 w w
学科网(北京)股份有限公司18.(14分)
(1)6(1分)
(2) 醛基(1分) 邻硝基甲苯(或2-硝基甲苯)(1分)
(3)起定位作用,在甲基邻位发生硝基取代(2分)
(4)bc(2分)
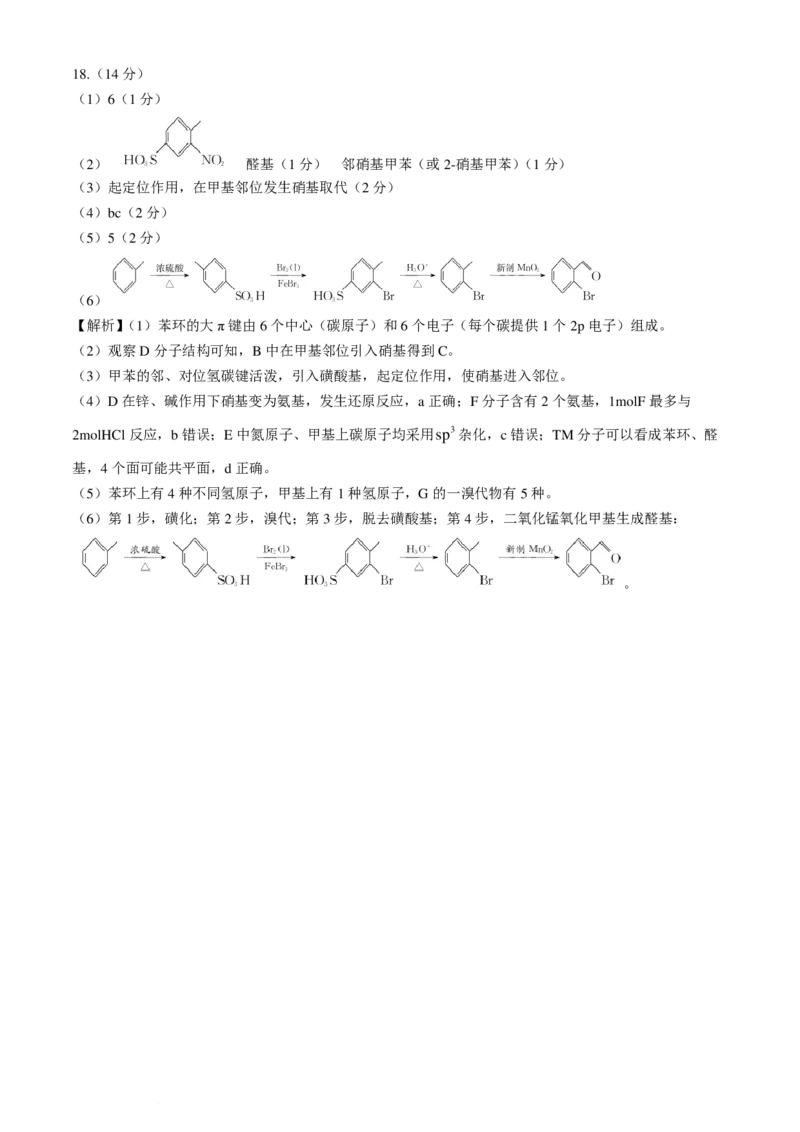
(5)5(2分)
(6)
【解析】(1)苯环的大π键由6个中心(碳原子)和6个电子(每个碳提供1个2p电子)组成。
(2)观察D分子结构可知,B中在甲基邻位引入硝基得到C。
(3)甲苯的邻、对位氢碳键活泼,引入磺酸基,起定位作用,使硝基进入邻位。
(4)D在锌、碱作用下硝基变为氨基,发生还原反应,a正确;F分子含有2个氨基,1molF最多与
2molHCl反应,b错误;E中氮原子、甲基上碳原子均采用sp3杂化,c错误;TM分子可以看成苯环、醛
基,4个面可能共平面,d正确。
(5)苯环上有4种不同氢原子,甲基上有1种氢原子,G的一溴代物有5种。
(6)第1步,磺化;第2步,溴代;第3步,脱去磺酸基;第4步,二氧化锰氧化甲基生成醛基:
。
学科网(北京)股份有限公司