文档内容
沅澧共同体 2025 届高三第二次联考(试题卷)
化 学
时量:75分钟 满分:100分
命题单位:常德市第七中学 审题单位:常德市教科院
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 P 31 Zn 65
一、选择题(每小题3分,共42分,每小题均只有一项符合题意)
1.化学与我国传统文化密切相关,下列说法正确的是
A.《抱朴子》中“丹砂(HgS)烧之成水银,积变又还成丹砂”,该过程发生了可逆反应
B.“美人首饰侯王印,尽是沙中浪底来”中提到古人从沙子中得到黄金的方法为物理方法
C.古陶瓷修复时所用的熟石膏,其成分为Ca(OH)
2
D.成语“刀耕火耨”蕴含的化学原理是放火烧去野草,用余灰肥田,还可降低土壤碱性
2.N 为阿伏加德罗常数的值,下列说法不正确的是
A
A.124 g白磷(P)含有的共价键数为6 N
4 A
B.100 g质量分数为 46%的乙醇水溶液中含有的氧原子数为4 N
A
C.50 mL12 mol/L 盐酸与足量MnO 共热,转移的电子数为0.3 N
2 A
D.2 mol NO 与1 mol O 在密闭容器中充分反应后,容器中的分子总数小于2 N
2 A
3.我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。在实际生产中,捕
捉废气中CO 的原理为CO+2NaOH = Na CO+H O,下列有关化学用语或说法正确的是
2 2 2 3 2
A.H、D、T互为同位素 B.HO的VSEPR模型为V形
2
C.CO 中碳原子的杂化方式为sp2 D.NaHCO 的电离方程式为:NaHCO = Na++H++CO2-
2 3 3 3
4.下列离子方程式书写正确的是
A.明矾溶于水产生Al(OH) 胶体:Al3++3HO=Al(OH) ↓+3H+
3 2 3
B.向Ca(HCO ) 溶液中加入过量NaOH溶液:Ca2++HCO +OH-=CaCO ↓+H O
3 2 3 2
C.向二元弱酸HPO 溶液中滴入足量烧碱溶液:HPO +3OH-= +3HO
3 3 3 3 2
D.NaHSO 溶液与Ba(OH) 溶液反应至 恰好沉淀完全:H++SO 2-+Ba2++ OH−=BaSO ↓+ H O
4 2 4 4 2
5.下列选项中的物质不能按图示路径一步转化的是
选项 A B C D
X Fe HS NaOH Al O
2 2 3
Y FeCl S NaCO NaAlO
3 2 3 2
Z FeCl SO NaHCO Al(OH)
2 3 3 3
6.关于下列仪器在相应的操作或实验中使用不合理的是A.②可用于量取一定体积的KMnO 溶液 B.①、④不可加热
4
C.⑤可用来萃取碘水中的碘并分液 D.③可用于分离苯(沸点80 ℃)和溴苯(沸点156 ℃)
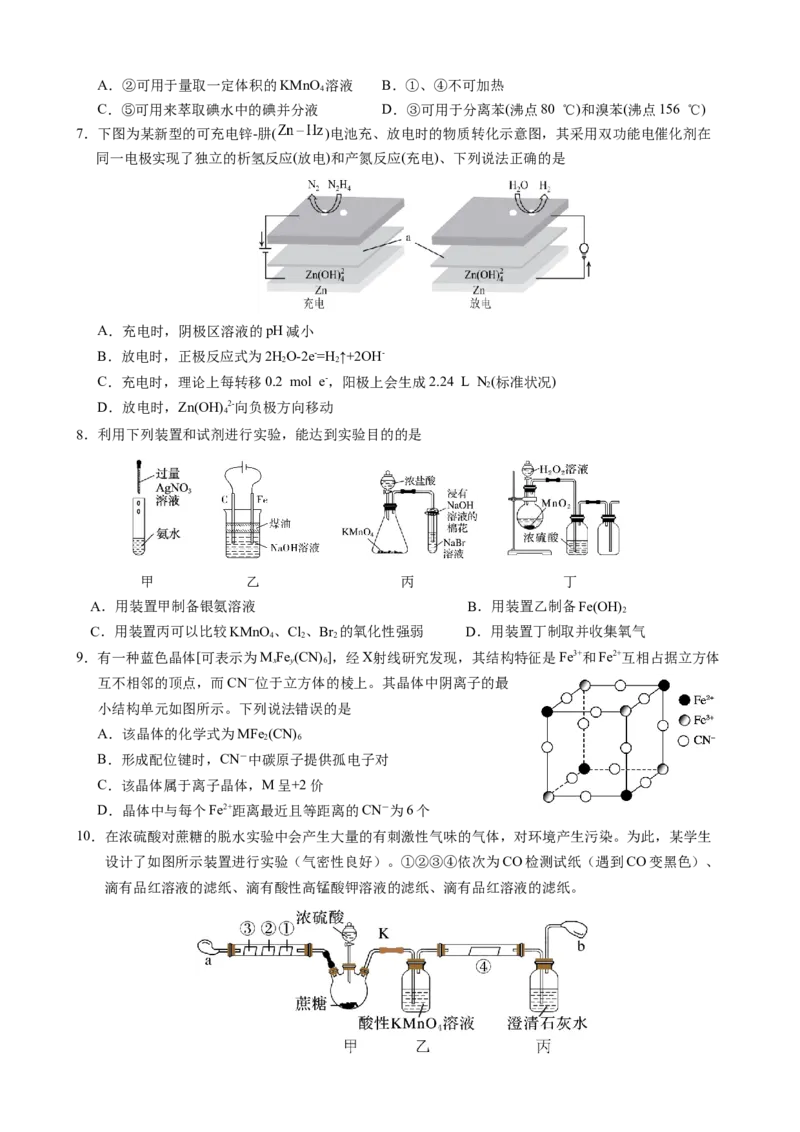
7.下图为某新型的可充电锌-肼( )电池充、放电时的物质转化示意图,其采用双功能电催化剂在
同一电极实现了独立的析氢反应(放电)和产氮反应(充电)、下列说法正确的是
A.充电时,阴极区溶液的pH减小
B.放电时,正极反应式为2HO-2e-=H ↑+2OH-
2 2
C.充电时,理论上每转移0.2 mol e-,阳极上会生成2.24 L N(标准状况)
2
D.放电时,Zn(OH) 2-向负极方向移动
4
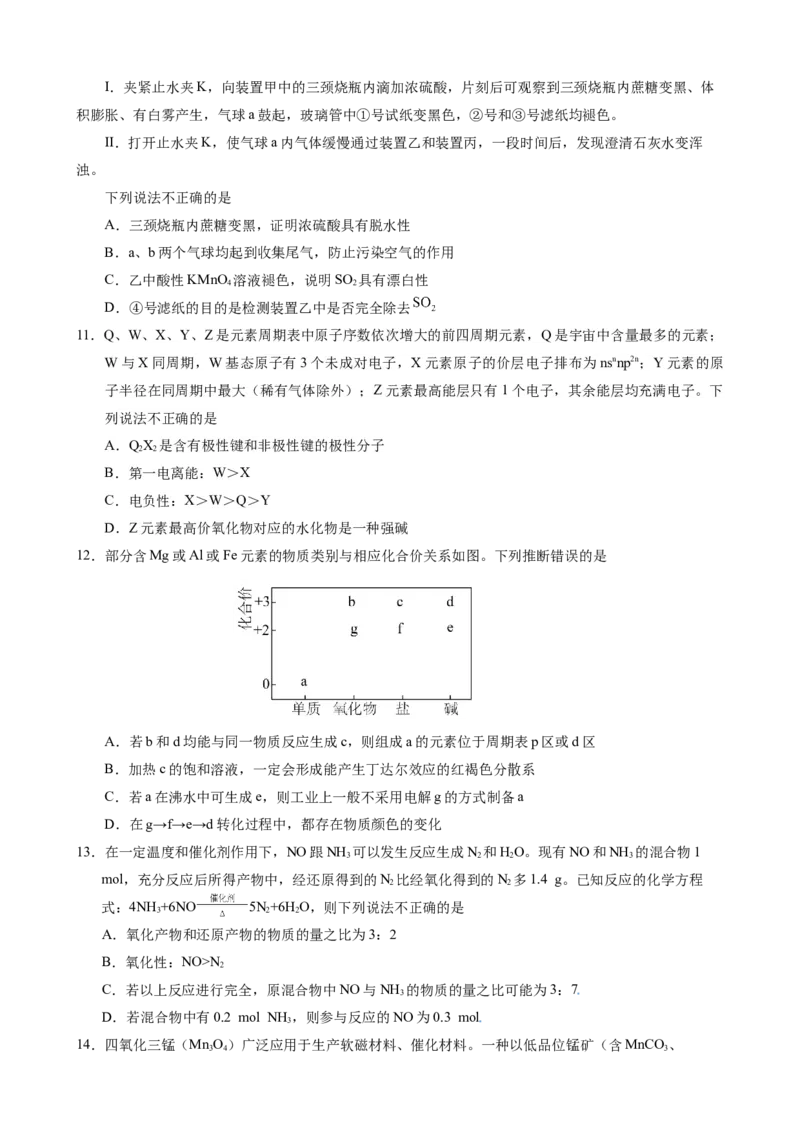
8.利用下列装置和试剂进行实验,能达到实验目的的是
甲 乙 丙 丁
A.用装置甲制备银氨溶液 B.用装置乙制备Fe(OH)
2
C.用装置丙可以比较KMnO 、Cl、Br 的氧化性强弱 D.用装置丁制取并收集氧气
4 2 2
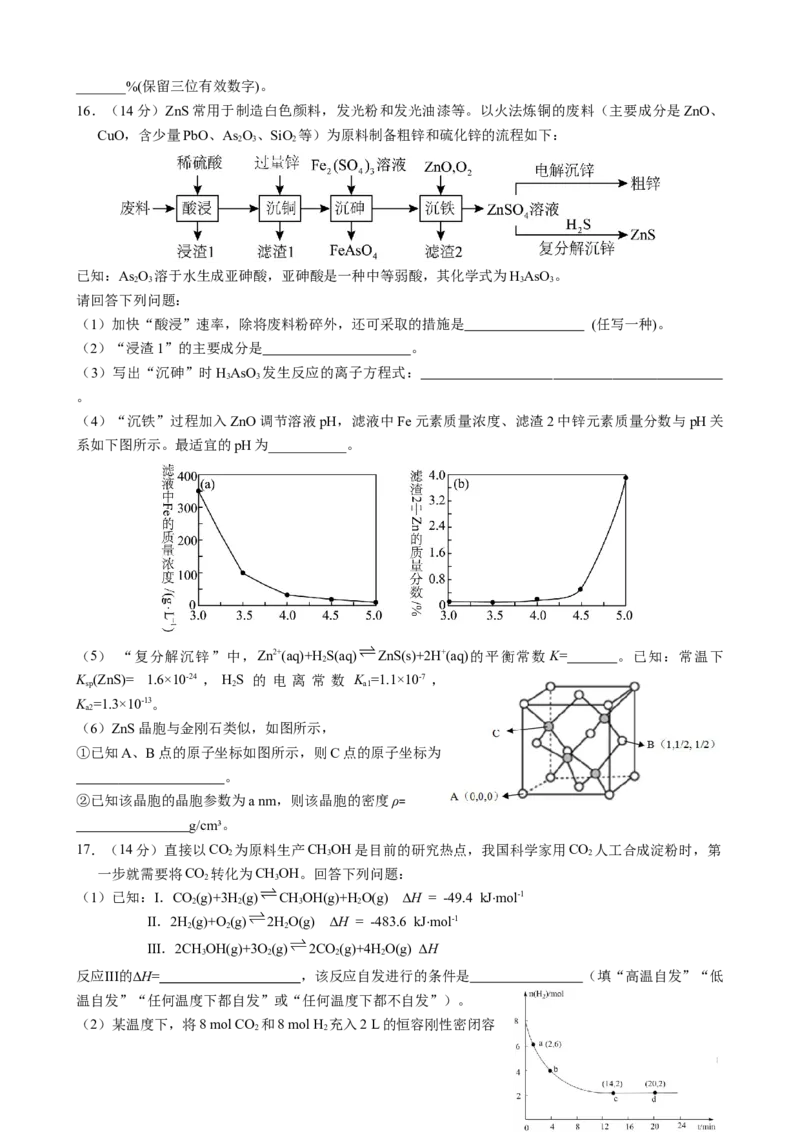
9.有一种蓝色晶体[可表示为MFe(CN) ],经X射线研究发现,其结构特征是Fe3+和Fe2+互相占据立方体
x y 6
互不相邻的顶点,而CN-位于立方体的棱上。其晶体中阴离子的最
小结构单元如图所示。下列说法错误的是
A.该晶体的化学式为MFe (CN)
2 6
B.形成配位键时,CN-中碳原子提供孤电子对
C.该晶体属于离子晶体,M呈+2价
D.晶体中与每个Fe2+距离最近且等距离的CN-为6个
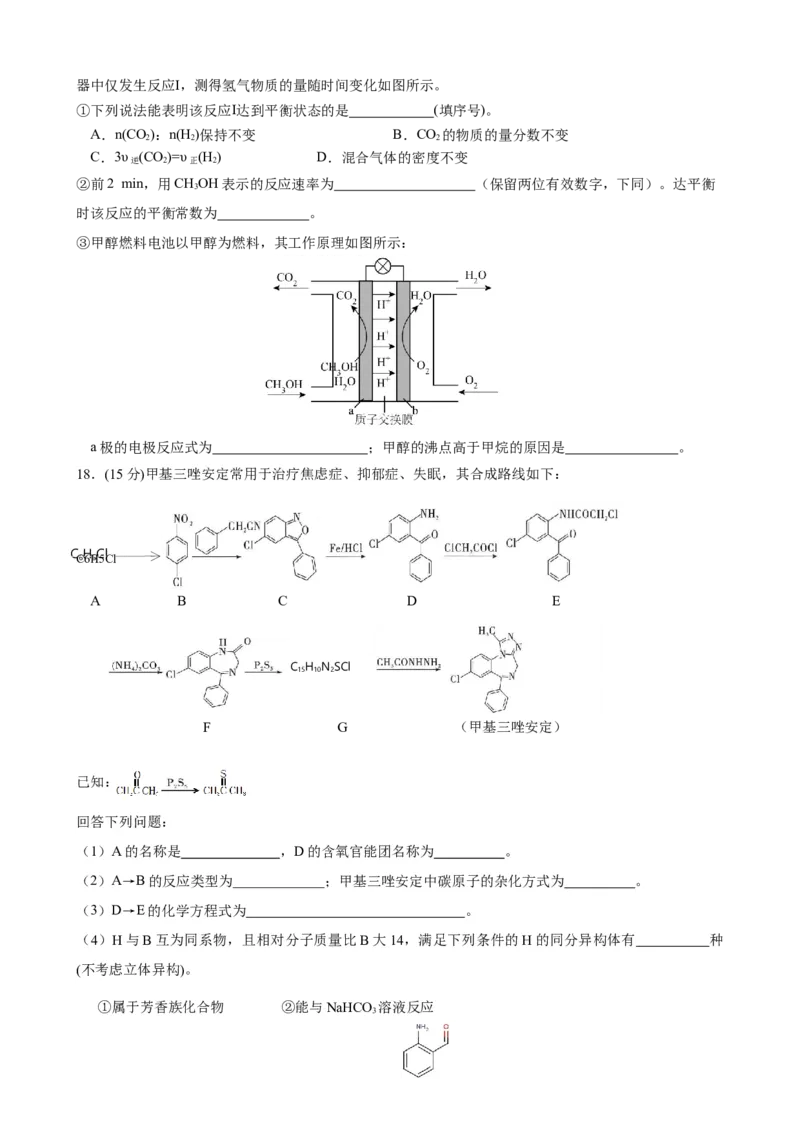
10.在浓硫酸对蔗糖的脱水实验中会产生大量的有刺激性气味的气体,对环境产生污染。为此,某学生
设计了如图所示装置进行实验(气密性良好)。①②③④依次为CO检测试纸(遇到CO变黑色)、
滴有品红溶液的滤纸、滴有酸性高锰酸钾溶液的滤纸、滴有品红溶液的滤纸。I.夹紧止水夹K,向装置甲中的三颈烧瓶内滴加浓硫酸,片刻后可观察到三颈烧瓶内蔗糖变黑、体
积膨胀、有白雾产生,气球a鼓起,玻璃管中①号试纸变黑色,②号和③号滤纸均褪色。
II.打开止水夹K,使气球a内气体缓慢通过装置乙和装置丙,一段时间后,发现澄清石灰水变浑
浊。
下列说法不正确的是
A.三颈烧瓶内蔗糖变黑,证明浓硫酸具有脱水性
B.a、b两个气球均起到收集尾气,防止污染空气的作用
C.乙中酸性KMnO 溶液褪色,说明SO 具有漂白性
4 2
D.④号滤纸的目的是检测装置乙中是否完全除去
11.Q、W、X、Y、Z是元素周期表中原子序数依次增大的前四周期元素,Q是宇宙中含量最多的元素;
W与X同周期,W基态原子有3个未成对电子,X元素原子的价层电子排布为nsnnp2n;Y元素的原
子半径在同周期中最大(稀有气体除外);Z元素最高能层只有1个电子,其余能层均充满电子。下
列说法不正确的是
A.QX 是含有极性键和非极性键的极性分子
2 2
B.第一电离能:W>X
C.电负性:X>W>Q>Y
D.Z元素最高价氧化物对应的水化物是一种强碱
12.部分含Mg或Al或Fe元素的物质类别与相应化合价关系如图。下列推断错误的是
A.若b和d均能与同一物质反应生成c,则组成a的元素位于周期表p区或d区
B.加热c的饱和溶液,一定会形成能产生丁达尔效应的红褐色分散系
C.若a在沸水中可生成e,则工业上一般不采用电解g的方式制备a
D.在g→f→e→d转化过程中,都存在物质颜色的变化
13.在一定温度和催化剂作用下,NO跟NH 可以发生反应生成N 和HO。现有NO和NH 的混合物1
3 2 2 3
mol,充分反应后所得产物中,经还原得到的N 比经氧化得到的N 多1.4 g。已知反应的化学方程
2 2
式:4NH +6NO 5N+6H O,则下列说法不正确的是
3 2 2
A.氧化产物和还原产物的物质的量之比为3:2
B.氧化性:NO>N
2
C.若以上反应进行完全,原混合物中NO与NH 的物质的量之比可能为3:7
3
D.若混合物中有0.2 mol NH ,则参与反应的NO为0.3 mol
3
14.四氧化三锰(MnO)广泛应用于生产软磁材料、催化材料。一种以低品位锰矿(含MnCO 、
3 4 3MnO、MnOOH及少量Fe O、Al O、SiO)为原料生产MnO 的工艺流程如图所示:
2 3 2 3 2 3 2 3 4
下列说法不正确的是
A.可用稀硫酸代替“溶浸”中的NH HSO
4 4
B.“溶浸”步骤中HO 作氧化剂
2 2
C.“沉锰”步骤中母液的主要成分为(NH )SO
4 2 4
△
D.“氧化”步骤中Mn(OH) 参加的反应:6Mn(OH) +O 2MnO+6HO
2 2 2 3 4 2
二、非选择题(本题共4小题,共58分)
15.(15分)在生活中亚硝酸钠(NaNO )应用十分广泛,少量可做食品的护色剂,可防止肉毒杆菌在
2
肉类食品中生长,还可用于治疗氰化物中毒等。某小组拟利用NO 制备亚硝酸钠,装置如图。
x
a
已知:①NO +NO+NaCO===2NaNO +CO;
2 2 3 2 2
②2NO +Na CO=== NaNO +NaNO +CO;
2 2 3 2 3 2
③酸性条件下,NO或NO都能与MnO反应生成NO和Mn2+。
请按要求回答下列问题:
(1)装置A中盛装稀硝酸的仪器的名称是 。
(2)气体a的化学式为 ;(1分)B装置的作用是________________。
(3)反应结束后,通入过量氮气,该操作的目的是____________________________________。
(4)NO不能单独被纯碱溶液吸收,为了使NO 完全被碱液吸收且产品纯度高,x= 。
x
(5)装置D中发生反应的离子方程式为 。
(6)实验完毕后,为检验装置C中制得NaNO ,取装置C中溶液少许分成三份,设计以下实验:
2
实验 实验操作 现象
甲 滴入无色酚酞溶液中 溶液变红
乙 滴入少量FeCl 溶液中,再加入盐酸酸化,振荡 溶液变黄色
2
丙 滴入少量酸性KMnO 溶液中,振荡 酸性KMnO 溶液褪色
4 4
上述实验中能够检验出装置C中一定制得NaNO 的是 (填标号)。
2
(7)芳香伯胺类药物在盐酸存在下,能定量地与亚硝酸钠发生重氮化反应。原理为ArNH+NaNO +2HCl
2 2
= [Ar-N≡N]Cl+NaCl+2H O,用已知0.5000 mol·L-1的盐酸滴定含0.36 g亚硝酸钠和足量芳香伯胺类药物
2
的混合物溶液25.00 mL,平行三次实验得消耗的盐酸的平均体积为20.00 mL,亚硝酸钠的含量为_______%(保留三位有效数字)。
16.(14分)ZnS常用于制造白色颜料,发光粉和发光油漆等。以火法炼铜的废料(主要成分是ZnO、
CuO,含少量PbO、As O、SiO 等)为原料制备粗锌和硫化锌的流程如下:
2 3 2
已知:As O 溶于水生成亚砷酸,亚砷酸是一种中等弱酸,其化学式为HAsO 。
2 3 3 3
请回答下列问题:
(1)加快“酸浸”速率,除将废料粉碎外,还可采取的措施是 (任写一种)。
(2)“浸渣1”的主要成分是 。
(3)写出“沉砷”时HAsO 发生反应的离子方程式:
3 3
。
(4)“沉铁”过程加入ZnO调节溶液pH,滤液中Fe元素质量浓度、滤渣2中锌元素质量分数与pH关
系如下图所示。最适宜的pH为___________。
(5) “复分解沉锌”中,Zn2+(aq)+H S(aq) ZnS(s)+2H+(aq)的平衡常数 K= 。已知:常温下
2
K (ZnS)= 1.6×10-24 , HS 的 电 离 常 数 K =1.1×10-7 ,
sp 2 a1
K =1.3×10-13。
a2
(6)ZnS晶胞与金刚石类似,如图所示,
①已知A、B点的原子坐标如图所示,则C点的原子坐标为
。
②已知该晶胞的晶胞参数为a nm,则该晶胞的密度ρ=
g/cm³。
17.(14分)直接以CO 为原料生产CHOH是目前的研究热点,我国科学家用CO 人工合成淀粉时,第
2 3 2
一步就需要将CO 转化为CHOH。回答下列问题:
2 3
(1)已知:I.CO(g)+3H(g) CHOH(g)+H O(g) H = -49.4 kJmol-1
2 2 3 2
II.2H(g)+O(g) 2HO(g) H = -483.6 kJmol-1
2 2 2
III.2CHOH(g)+3O (g) 2CO(g)+4HO(g) H
3 2 2 2
反应III的H= ,该反应自发进行的条件是 (填“高温自发”“低
温自发”“任何温度下都自发”或“任何温度下都不自发”)。
(2)某温度下,将8 mol CO 和8 mol H 充入2 L的恒容刚性密闭容
2 2器中仅发生反应I,测得氢气物质的量随时间变化如图所示。
①下列说法能表明该反应I达到平衡状态的是 (填序号)。
A.n(CO):n(H )保持不变 B.CO 的物质的量分数不变
2 2 2
C.3υ (CO)=υ (H ) D.混合气体的密度不变
逆 2 正 2
②前2 min,用CHOH表示的反应速率为 (保留两位有效数字,下同)。达平衡
3
时该反应的平衡常数为 。
③甲醇燃料电池以甲醇为燃料,其工作原理如图所示:
a极的电极反应式为 ;甲醇的沸点高于甲烷的原因是 。
18.(15分)甲基三唑安定常用于治疗焦虑症、抑郁症、失眠,其合成路线如下:
C H Cl
C66H55Cl
A B C D E
C H NSCl
15 10 2
F G (甲基三唑安定)
已知:
回答下列问题:
(1)A的名称是 ,D的含氧官能团名称为 。
(2)A→B的反应类型为_____________;甲基三唑安定中碳原子的杂化方式为 。
(3)D→E的化学方程式为 。
(4)H与B互为同系物,且相对分子质量比B大14,满足下列条件的H的同分异构体有 种
(不考虑立体异构)。
①属于芳香族化合物 ②能与NaHCO 溶液反应
3(5)参考上述信息,写出以苯与CHCN为原料制备 的合成路线。(其他试剂任选)(本小题3
3
分)