文档内容
沅澧共同体高三第二次联考化学参考答案
一、选择题
1. 【答案】B
A中反应条件不同,所以不为可逆反应;
C中熟石膏的成分为2CaSO .H O;
4 2
D中草木灰中含碳酸钾,不会降低土壤碱性。
2.【答案】C
A中1molP 中有6molP-P;
4
B中46g乙醇含1mol氧原子,54g水含3mol氧原子,共4mol;
C中随着盐酸变稀,无法与MnO 继续反应;
2
D项NO 中存在转化为N O 的可逆反应。
2 2 4
3.【答案】A
B中H O的价层电子互斥模型为四面体,
2
C中CO 中的碳原子杂化方式为sp,
2
D中应为NaHCO =Na++HCO - 。
3 3
4.【答案】D
A应为Al3++3H
2
OAl(OH)
3
(胶体)+3H+;
B应为Ca2++2HCO-+2OH-=CaCO ↓+2H O+CO 2-
3 3 2 3
C应为H PO +2OH-=HPO 2-+2H O
3 3 3 2
5. 【答案】B
B中S无法一步生成SO 。
3
6.【答案】B
①,④垫陶土网可加热
7.【答案】D
A充电时阴极区由Zn(OH) 2-得电子生成Zn和OH- ,所以PH会增大;
4
B正极反应应为得电子;
C项电子与N 的比例应为4:1,所以电子为0.2mol时,N 应该为标况下1.12L。
2 2
8.【答案】C
A银氨溶液应该将氨水滴入硝酸银溶液中,
B中Fe电极应为阳极;
D中应该为向上排空气法。
{#{QQABQYCAoggIABAAAAhCEQFSCECQkgCACSgOQFAEIAAByQNABAA=}#}9.【答案】C
从最小结构单元用均摊法算得CN- 为12×1/4=3 ,Fe3+和Fe2+为8×1/8=1,所以CN- 为6时
x应该为2,根据化合价之和为0,y=1,且M的化合价只能为+1。
10.【答案】C
酸性KMnO 溶液褪色,说明SO 具有还原性。
4 2
11.【答案】D
Q、W、X、Y、Z分别为H、N、O、Na或K、Cu,D项Cu(OH) 为弱碱。
2
12、【答案】B
A.假设b为Al O ,即d为Al(OH) ,c为铝盐,Al O 、Al(OH) 与稀盐酸反应均生成铝盐,
2 3 3 2 3 3
此时组成a的元素为Al,位于周期表p区,假设b为Fe O ,即d为Fe(OH) ,c为铁盐,
2 3 3
Fe O 、Fe(OH) 与稀盐酸反应均生成铁盐,此时组成a的元素为Fe,位于周期表d区,故A
2 3 3
正确;
B.由题意得,此时能产生丁达尔效应的红棕色分散系为Fe(OH) 胶体,c应为铁盐,加热
3
铁盐的饱和溶液,也有可能直接得到沉淀,故B错误;
C.若a在沸水中可生成e,此时a为Mg,e为Mg(OH) ,即g为MgO,工业上采用电解熔
2
融氯化镁的方法获得Mg,故C正确;
D.e能转化为d,此时e为Fe(OH) 白色沉淀,d为Fe(OH) 红褐色沉淀,说明在g→f→e→d
2 3
转化过程中,一定存在物质颜色的变化,故D正确;
13、【答案】A
6molNO被还原得到3molN ,4molNH 被氧化得到2molN ,二者相差1molN ,现相差
2 3 2 2
0.05molN ,相当于0.3mol NO和0.2molNH 反应,NO和NH 的混合物共1mol,证明其
2 3 3
中有一种过量,所以有两种情况:0.3mol NO和0.7molNH 或者0.2molNH 和0.8mol NO,
3 3
据此分析选择。
A.根据分析过程可知氧化产物和还原产物的物质的量比为:2:3; 故A错误;
B.根据分析过程可知NO是氧化剂,N 是氧化产物,氧化剂的氧化性强于氧化产物,故B
2
正确。
C.根据分析过程可知,原混合物中NO与NH 的物质的量之比为可能为3:7或者4:1,
3
C正确;
D.分析反应方程式可知,有0.2molNH 参加反应,需要NO0.3mol,故D正确;
3
14、【答案】B
A项,H SO 也能提供H+、SO2,故A正确;
2 4 4
{#{QQABQYCAoggIABAAAAhCEQFSCECQkgCACSgOQFAEIAAByQNABAA=}#}B项,H+与MnCO 、Fe O 、Al O 反应生成Mn2+、Al3+、Fe3+,根据流程图,沉锰后得到
3 2 3 2 3
+2价Mn,因此Mn O 、MnOOH在酸性条件下将H O 氧化成O ,本身被还原成Mn2+,
2 3 2 2 2
H O 作还原剂,故B错误;
2 2
C项,“沉锰”步骤母液中含有(NH ) SO ,故C正确;
4 2 4
D项,氧化过程中反应方程式为6Mn(OH) +O 2Mn O +6H O,故D正确。
2 2 3 4 2
二、填空题(除特殊说明外,其余均2分每空)
15.(15分)
(1)分液漏斗
(2)O (1分)将NO转化为NO
2 2
(3)反应后为排尽装置内NO,防止拆卸装置时污染环境
(4) 1.5
(5) 3MnO4H5NO3Mn25NO2H O
4 3 2
(6)丙
(7) 95.8%
根据反应ArNH 十NaNO 十2HCl=[Ar-N≡N]Cl+NaCl+2H O,可知NaNO ~2HCl,设NaNO
2 2 2 2 2
1 2
的浓度为c,可得 ,得c=0.2000mol/L,亚硝酸钠的含
25.00mLc 0.5000molL20.00mL
0.2000mol/L0.025L69g/mol
量= 100%≈95.8%,故答案为:95.8%。
0.36g
16.(14分)
(1)升温、适当增大硫酸的浓度、搅拌任答其一即可,答催化剂不给分。
(2)SiO PbSO
2 4
(3)3Fe3++H AsO +H O=FeAsO +2Fe2++5H+
3 3 2 4
(4)4.0-4.5范围内均可给分
(5)8.9×103
(6)①(1/4,1/4,3/4)②4×97/(a×10-7)3N
A
17.(14分)
(1)-1352kJ/mol (不带单位和没有“-”均不给分) 任何温度下都自发
(2)①ABC(大小写写错不给分) 0.17 0.33
②CH OH-6e-+H O=CO +6H+ CH OH中存在分子间氢键
3 2 2 3
17.(15分)
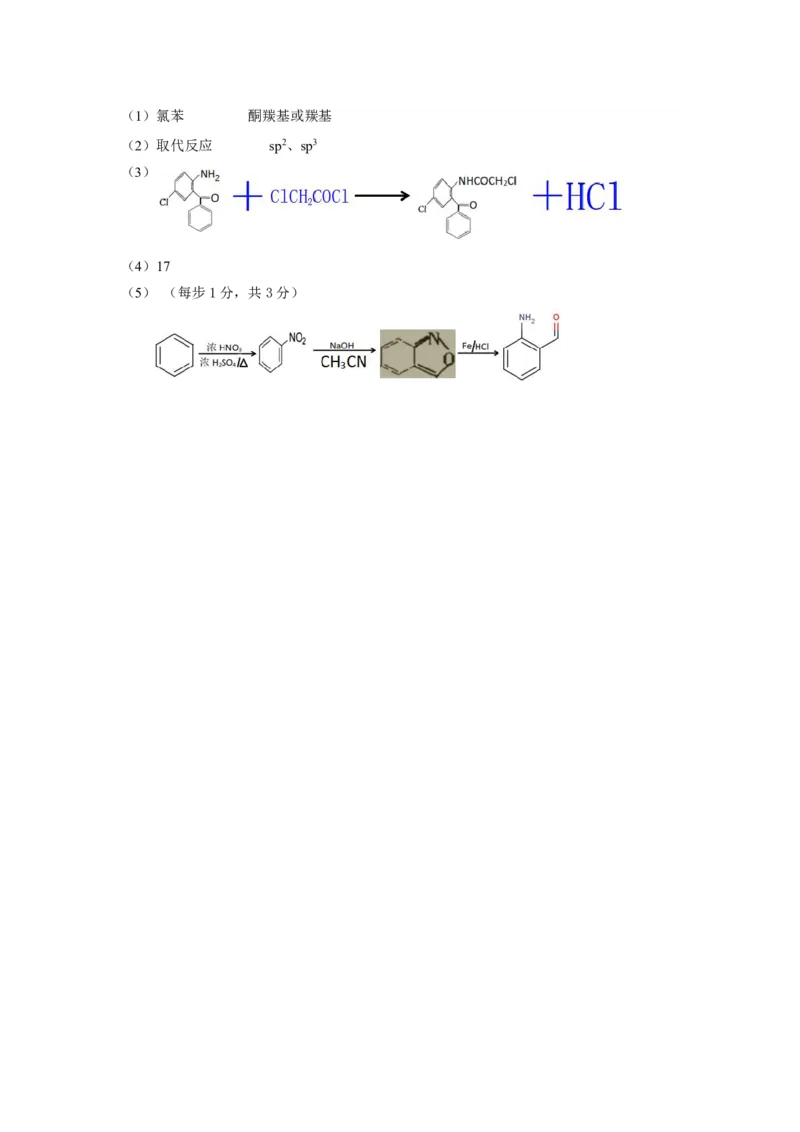
{#{QQABQYCAoggIABAAAAhCEQFSCECQkgCACSgOQFAEIAAByQNABAA=}#}(1)氯苯 酮羰基或羰基
(2)取代反应 sp2、sp3
(3)
(4)17
(5) (每步1分,共3分)
{#{QQABQYCAoggIABAAAAhCEQFSCECQkgCACSgOQFAEIAAByQNABAA=}#}