文档内容
2024-2025 学年度甘肃省兰州第一中学高三第三次诊断考试
化学试题
考试时间:75分钟 试卷总分:100分
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一
项是符合题目要求的。
1. 化学与生活密切相关, 下列说法错误的是( )
A. 利用丁达尔效应可检测气溶胶中的冠状病毒
B. 氮氧化合物与“光化学烟雾”、“臭氧层空洞”、“硝酸型酸雨”的形成有关
C. 单晶硅是一种半导体材料, 可用于制造硅电池
D. 硅燃烧放出的热量多, 且燃烧产物对环境污染程度低, 可做“未来石油”
2. 中华文化源远流长、博大精深,广东省馆藏文物是中华文化的重要代表。下列文物主要是由金属材料制
成的是( )
文物
鎏金高士图银杯 南宋德化窑青白釉撇口瓶 明代象牙雕寿星 战国青瓷罐
选项 A B C D
3.用下列实验装置进行相应的实验,能达到实验目的的是( )
A.用装置①制CaCO B.用装置②熔融NaCO
3 2 3
C.用装置③制取乙酸乙酯 D.用装置④滴定未知浓度的硫酸
4.“类比”是学习化学的重要思想,化学知识有规律可循,但也存在“反规律”现象,下列“类比”正
确的是( )
A.HCl气体用浓硫酸干燥,HBr气体也可以用浓硫酸干燥
B.碱金属元素单质熔点从Li到Cs逐渐降低,碱土金属元素单质熔点从Be到Ba也逐渐降低
C. 是两性氧化物, 也是两性氧化物
D.实验室用FeS与稀盐酸反应制 ,也可用CuS与稀盐酸反应制
5.高锰酸钾( )是一种重要的化工原料,也是实验室中常用的强氧化剂,在生物医药方面也有
重要用途。工业生产高锰酸钾涉及的一个反应为 。
学科网(北京)股份有限公司 第 1 页设 为阿伏加德罗常数的值,下列说法错误的是( )
A.11g金属锰其原子处于基态时,含有的未成对电子数为
B.该反应中有1mol 参与反应时,转移的电子数为
C.2L 0.5 的 溶液中 和 总数为
D. 中含有的π键数目为
标准状况下,11.2L
6. 第三周期元素 单的质及其化合物具有重要用途。例如,在熔融状态下,可用金属钠制备金属钾;MgCl
2
可制备多种镁产品:铝-空气电池具有较高的比能量,在碱性电解液中总反应式为4Al+3O +4OH-
2
+6H O=4[Al(OH) ]-,高纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氟硅烷(SiHCl ),再经
2 4 3
氢气还原得到高纯硅。下列有关物质的性质与用途具有对应关系的是( )
A. 钠的密度比钾大,可用于冶炼金属钾
B. 熔融的氯化镁能电解,可用作冶炼镁的原料
C. 铝的金属活泼性强,可用于制作铝金属制品
D. 晶体硅熔点高、硬度大,可用作通讯设备的芯片
7.下列实验操作对应的实验现象及结论均正确的是( )
选项 实验操作 实验现象 实验结论
A 有白色沉淀生成
将某气体通入 溶液 该气体可能是
B 向某溶液中加入足量氨水 最终有蓝色沉淀生成 该溶液中含有
C 溶液变浑浊
将某气体通入饱和 溶液 该气体可能是
先向某盐溶液中加入盐酸酸化,再滴加几滴
D 溶液变为红色 该盐一定属于三价铁盐
KSCN溶液
8. 自然界与人类活动均对硫的循环产生影响。下列说法不正确的是( )
A. 火山口附近的硫单质会被O 直接氧化为SO
2 3
B. 大气中的SO 遇雨水形成HSO 进入地面或海洋
2 2 4
C. 工业排放尾气中的SO 可与CaO和O 反应生成CaSO
2 2 4
D. 水垢中的CaSO 可与饱和NaCO 溶液反应生成CaCO
4 2 3 3
9.X、Y、Z、W为原子序数依次增大的前四周期元素,W的单质是目前应用最广泛的金属。化合物
XWZY4是一种常用的电极材料,该材料中的阴离子结构如图所示。下列说法错误的是( )
A.基态W原子的价电子排布式为
学科网(北京)股份有限公司 第 2 页B.简单氢化物的稳定性:Y>Z
C.工业上可采用电解法制备X单质
D.Z与氯形成的化合物中各原子最外层均满足8电子结构
10. 2-丁醇发生消去反应生成2-丁烯按如图机理进行:
下列说法不正确的是( )
A. 2-丁醇分子含1个手性碳原子 B. 2-丁烯存在顺反异构体
C. 该反应的副产物之一为1-丁烯 D. 2-丁烯中碳原子杂化轨道类型均为sp2
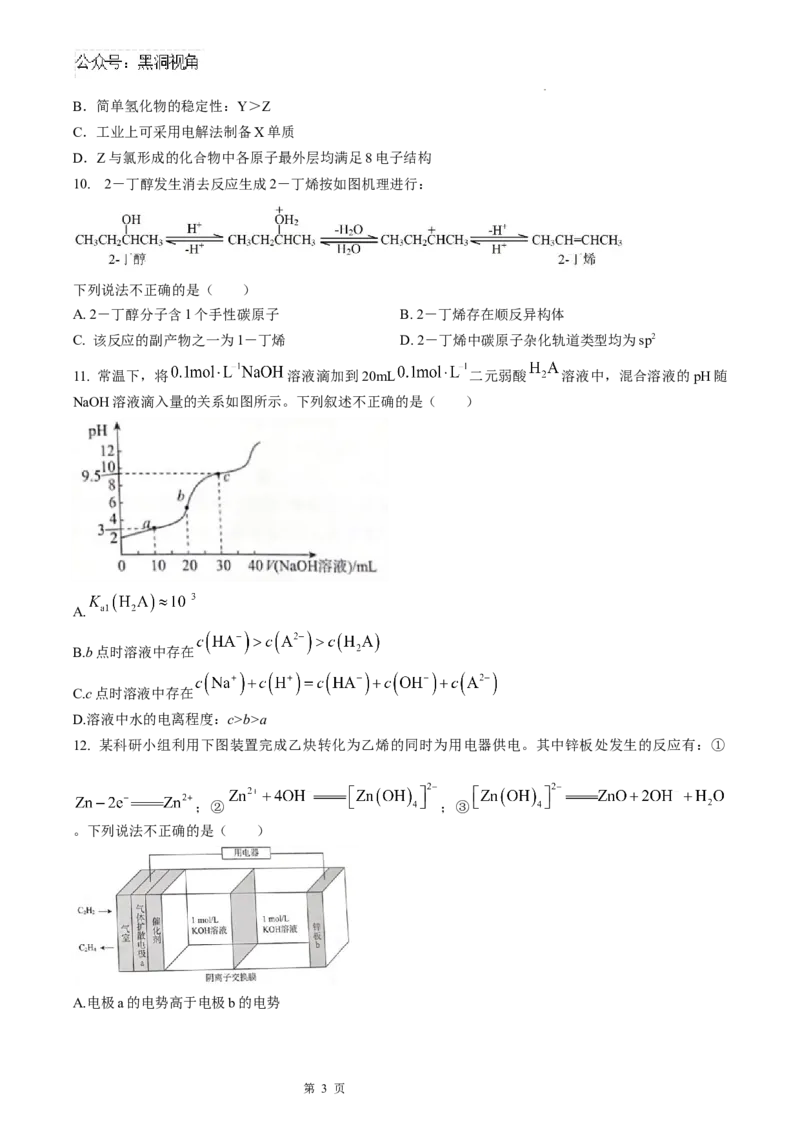
11. 常温下,将 溶液滴加到20mL 二元弱酸 溶液中,混合溶液的pH随
NaOH溶液滴入量的关系如图所示。下列叙述不正确的是( )
A.
B.b点时溶液中存在
C.c点时溶液中存在
D.溶液中水的电离程度:c>b>a
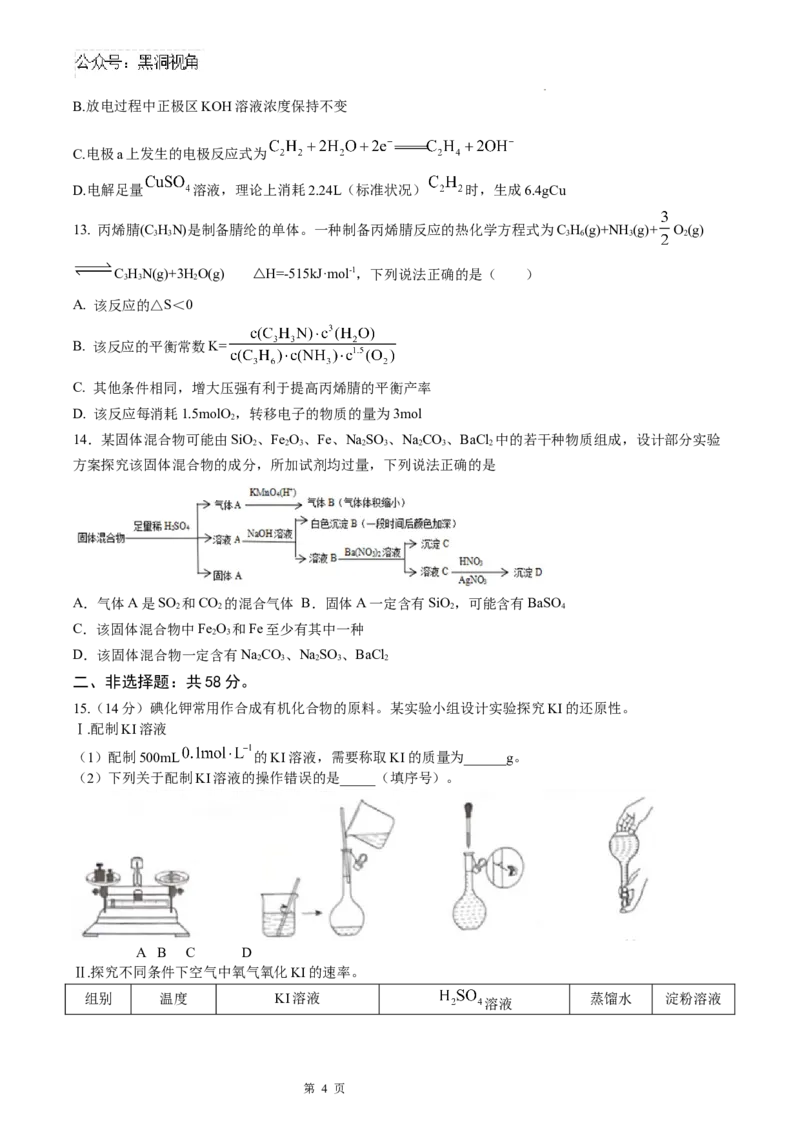
12. 某科研小组利用下图装置完成乙炔转化为乙烯的同时为用电器供电。其中锌板处发生的反应有:①
;② ;③
。下列说法不正确的是( )
A.电极a的电势高于电极b的电势
学科网(北京)股份有限公司 第 3 页B.放电过程中正极区KOH溶液浓度保持不变
C.电极a上发生的电极反应式为
D.电解足量 溶液,理论上消耗2.24L(标准状况) 时,生成6.4gCu
13. 丙烯腈(C HN)是制备腈纶的单体。一种制备丙烯腈反应的热化学方程式为C H(g)+NH (g)+ O(g)
3 3 3 6 3 2
C HN(g)+3H O(g) △H=-515kJ·mol-1,下列说法正确的是( )
3 3 2
A. 该反应的△S<0
B. 该反应的平衡常数K=
C. 其他条件相同,增大压强有利于提高丙烯腈的平衡产率
D. 该反应每消耗1.5molO,转移电子的物质的量为3mol
2
14.某固体混合物可能由SiO、Fe O、Fe、NaSO 、NaCO、BaCl 中的若干种物质组成,设计部分实验
2 2 3 2 3 2 3 2
方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的是
A.气体A是SO 和CO 的混合气体 B.固体A一定含有SiO,可能含有BaSO
2 2 2 4
C.该固体混合物中Fe O 和Fe至少有其中一种
2 3
D.该固体混合物一定含有NaCO、NaSO 、BaCl
2 3 2 3 2
二、非选择题:共58分。
15.(14分)碘化钾常用作合成有机化合物的原料。某实验小组设计实验探究KI的还原性。
Ⅰ.配制KI溶液
(1)配制500mL 的KI溶液,需要称取KI的质量为______g。
(2)下列关于配制KI溶液的操作错误的是_____(填序号)。
A B C D
Ⅱ.探究不同条件下空气中氧气氧化KI的速率。
组别 温度 KI溶液 蒸馏水 淀粉溶液
溶液
学科网(北京)股份有限公司 第 4 页c(KI) V V
1 298K 5mL 5mL 10mL 3滴
2 313K mL 5mL 10mL 3滴
3 298K 10mL 5mL 5mL 3滴
(3)酸性条件下KI能被空气中氧气氧化,发生反应的离子方程式为_____________________。
(4)通过实验组别1和组别2探究温度对氧化速率的影响。其中a=___________,b=______________。
(5)设计实验组别3的目的是_____________________。
Ⅲ.探究反应“ ”为可逆反应。
试剂: KI溶液, 溶液,淀粉溶液, 溶液,
KSCN溶液。
实验如下:
(6)甲同学通过试管 i 和试管 ii 中现象结合可证明该反应为可逆反应,则试管 i 中现象为
_____________________;乙同学认为该现象无法证明该反应为可逆反应,原因为_____________________。
(7)请选择上述试剂重新设计实验,证明该反应为可逆反应:_____________________。
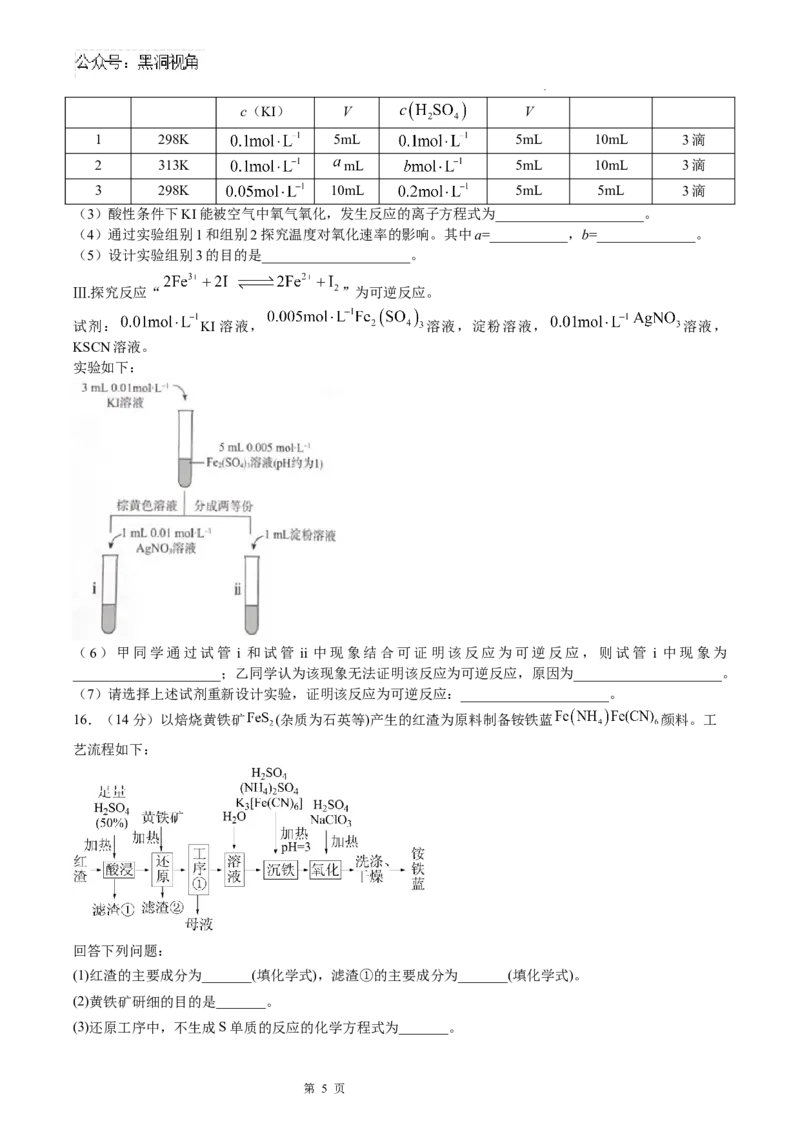
16.(14分)以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝 颜料。工
艺流程如下:
回答下列问题:
(1)红渣的主要成分为_______(填化学式),滤渣①的主要成分为_______(填化学式)。
(2)黄铁矿研细的目的是_______。
(3)还原工序中,不生成S单质的反应的化学方程式为_______。
学科网(北京)股份有限公司 第 5 页(4)工序①的名称为_______,所得母液循环使用。
(5)沉铁工序产生的白色沉淀 中 的化合价为_______,氧化工序发生反应的离子方程式
为_______。
(6)若用还原工序得到的滤液制备 和 ,所加试剂为_______和_______(填化学式,不
引入杂质)。
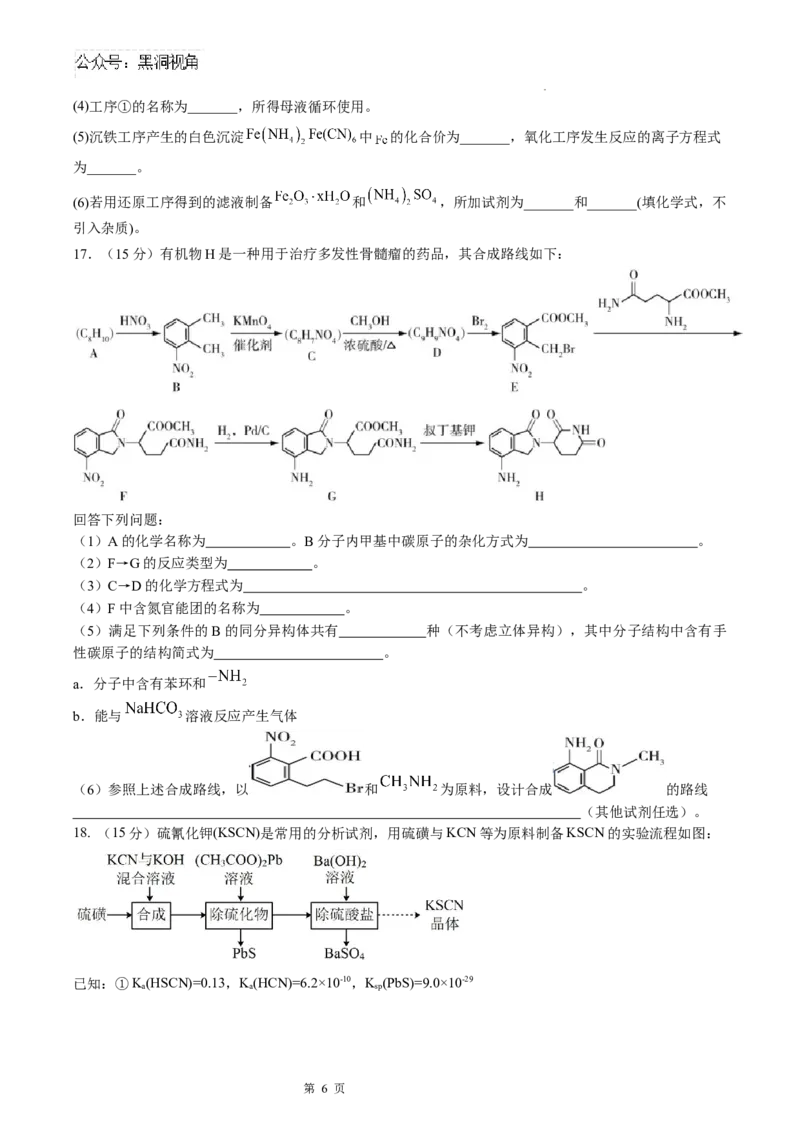
17.(15分)有机物H是一种用于治疗多发性骨髓瘤的药品,其合成路线如下:
回答下列问题:
(1)A的化学名称为 。B分子内甲基中碳原子的杂化方式为 。
(2)F→G的反应类型为 。
(3)C→D的化学方程式为 。
(4)F中含氮官能团的名称为 。
(5)满足下列条件的B的同分异构体共有 种(不考虑立体异构),其中分子结构中含有手
性碳原子的结构简式为 。
a.分子中含有苯环和
b.能与 溶液反应产生气体
(6)参照上述合成路线,以 和 为原料,设计合成 的路线
(其他试剂任选)。
18. (15分)硫氰化钾(KSCN)是常用的分析试剂,用硫磺与KCN等为原料制备KSCN的实验流程如图:
已知:①K(HSCN)=0.13,K(HCN)=6.2×10-10,K (PbS)=9.0×10-29
a a sp
学科网(北京)股份有限公司 第 6 页②S+KCN KSCN(放热反应)
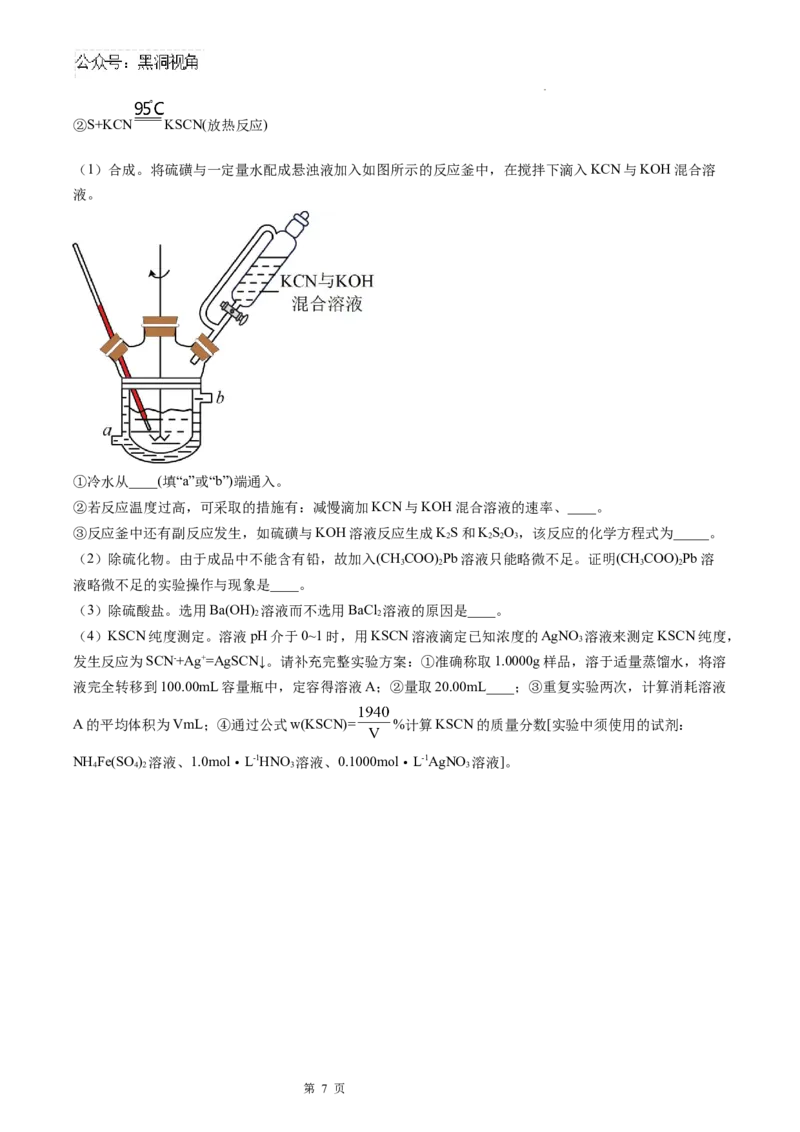
(1)合成。将硫磺与一定量水配成悬浊液加入如图所示的反应釜中,在搅拌下滴入KCN与KOH混合溶
液。
①冷水从____(填“a”或“b”)端通入。
②若反应温度过高,可采取的措施有:减慢滴加KCN与KOH混合溶液的速率、____。
③反应釜中还有副反应发生,如硫磺与KOH溶液反应生成KS和KSO,该反应的化学方程式为_____。
2 2 2 3
(2)除硫化物。由于成品中不能含有铅,故加入(CHCOO) Pb溶液只能略微不足。证明(CHCOO) Pb溶
3 2 3 2
液略微不足的实验操作与现象是____。
(3)除硫酸盐。选用Ba(OH) 溶液而不选用BaCl 溶液的原因是____。
2 2
(4)KSCN纯度测定。溶液pH介于0~1时,用KSCN溶液滴定已知浓度的AgNO 溶液来测定KSCN纯度,
3
发生反应为SCN-+Ag+=AgSCN↓。请补充完整实验方案:①准确称取1.0000g样品,溶于适量蒸馏水,将溶
液完全转移到100.00mL容量瓶中,定容得溶液A;②量取20.00mL____;③重复实验两次,计算消耗溶液
A的平均体积为VmL;④通过公式w(KSCN)= %计算KSCN的质量分数[实验中须使用的试剂:
NH Fe(SO ) 溶液、1.0mol·L-1HNO 溶液、0.1000mol·L-1AgNO 溶液]。
4 4 2 3 3
学科网(北京)股份有限公司 第 7 页2024-2025 学年度甘肃省兰州第一中学高三第三次诊断考试
化学参考答案
二、
选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
题号 1 2 3 4 5 6 7 8
答案 A A A B C B C A
题号 9 10 11 12 13 14
答案 D D C B B C
二、非选择题:共58分。
15.(1)8.3 (2)AC
(3)
(4)5 0.1
(5)探究硫酸的浓度对氧化速率的影响
(6)产生黄色沉淀 含 的溶液中加入 也能产生黄色沉淀(答案合理即可)
(7)向5mL(过量) 溶液中加入3mL(少量) 溶液,再向其中
加入KSCN溶液,溶液变红,说明含有过量 的溶液中存在 ,即可证明该反应为可逆反应(合理答
案即可)
16.(1) Fe O SiO
2 3 2
(2)增大固液接触面积,加快反应速率,提高黄铁矿的利用率
(3)7Fe (SO )+FeS +8H O=15FeSO +8H SO
2 4 3 2 2 4 2 4
(4)蒸发浓缩、冷却结晶、过滤洗涤
(5) +2; 6Fe(NH )Fe(CN) +ClO -+6H+=6Fe(NH )Fe(CN) +H O+Cl-+6 +3H O
4 2 6 3 4 6 2 2
(6) HO NH ·H O
2 2 3 2
17.(1)邻二甲苯(或1,2-二甲基苯)
(2)还原反应
(3)
(4)酰胺基、硝基
(5)17
学科网(北京)股份有限公司 第 1 页(6)
18.(1) ①. a ②. 加快冷却水的流速 ③. 4S+6KOH=3H O+2KS+KSO
2 2 2 2 3
(2)取沉淀后上层清液,向清液中滴加醋酸铅溶液,生成极少量的沉淀,说明(CHCOO) Pb溶液略微不
3 2
足
(3)Ba(OH) 溶液可以和硫酸根离子生成硫酸钡沉淀且使溶液显碱性利于生成KSCN,若选用BaCl 溶液
2 2
会引入氯离子杂质
(4)量取 20.00mL0.1000mol·L-1AgNO 溶液,加入 1.0mol·L-1HNO 溶液为调节 pH 为 0~1,加入几滴
3 3
NH Fe(SO ) 溶液,使用溶液A滴定硝酸银溶液至最后一滴溶液A加入后溶液显红色,且半分钟内不褪色
4 4 2
学科网(北京)股份有限公司 第 2 页