文档内容
2024 年中考第一次模拟考试(贵州卷)
化 学
一、单项选择题(本大题共7小题,每小题2分,共14分。每小题只有一个选项符合题意,请将符合题意
的选项用 2B 铅笔填涂在答题卡相应位置)
1.下列图示的实验操作正确的是( )
A. 点燃酒精灯 B. 滴加液体
C. 读液体体积 D. 闻药品气味
【答案】C
【解析】A、酒精灯的点燃方法:用火柴点燃,不能用酒精灯引燃,否则容易引起火灾,故A错;
B、胶头滴管要垂悬在试管口上方,不能伸入试管内,故B错;
C、量筒的读数方法:视线与凹液面最低处保持水平,故C正确;
D、闻气体气味的方法:用手扇着闻,不能将鼻孔凑到集气瓶口,故D错。
故选:C。
2.有一位同学暑假去西藏发生了严重的高原反应,医生让他吸入了一种气体后,症状得到缓解。此气体
可能是( )
A.氧气 B.氮气 C.稀有气体 D.二氧化碳
【答案】A
【解析】氧气的用途有:支持燃烧和供给呼吸等。严重的高原反应是由于高原地区空气稀薄,含氧气量
少,吸氧是为了供给人类呼吸。因此此气体是氧气。
故选:A。
3.小李同学用pH计测得生活中一些物质的pH如下表所示。下列说法正确的是( )
物质 肥皂水 牙膏 西瓜汁 洁厕灵
pH 10.2 8.5 5.8 1.4
A.牙膏显酸性
B.西瓜汁的酸性比洁厕灵的酸性强
C.肥皂水使紫色石蕊溶液显红色
D.蚊虫叮咬处可涂抹牙膏或肥皂水
【答案】D【解析】A.pH<7溶液呈酸性,pH>7溶液呈碱性,因为已知牙膏的pH为8.5,所以溶液呈碱性,故A
错误;
B.pH<7溶液呈酸性,pH越小,溶液的酸性越强,表中已知洁厕灵的 pH是1.4,西瓜汁的pH是5.8,
所以洁厕灵的酸性更强一些,故B错误;
C.据表所知肥皂水的pH为10.2,大于7,所以肥皂水呈碱性,碱性溶液能使紫色石蕊试液变蓝色,故C
错误;
D.据表所知牙膏的pH为8.5,肥皂水的pH为10.2,都大于7,所以都呈碱性,根据酸碱中和的原理,
可知蚊虫叮咬可涂抹弱碱性的溶液,故D正确;
故选:D。
4.金银花作为常见的中药材,具有清热解毒、消炎退肿等功效,其有效成分之一是绿原酸(C H O )。
16 18 9
下列有关绿原酸的说法正确的是( )
A.绿原酸分子由碳、氢、氧三个元素组成
B.绿原酸中碳元素的质量分数最大
C.绿原酸的相对分子质量是354g
D.绿原酸中碳、氢、氧元素的质量比为16:18:9
【答案】B
【解析】A.元素只讲种类,不讲个数,绿原酸由碳、氢、氧三种元素组成,故A不正确;
B.元素的质量分数= ,而绿原酸中碳、氢、氧三种元素质量比
为(16×12):(18×1):(9×16)=32:3:24,由此可知碳元素的质量分数最大,故B正确;
C.相对分子质量的单位为“1”,而不是“g”,故绿原酸的相对分子质量是354,故C不正确;
D.绿原酸中碳、氢、氧三种元素质量比为(16×12):(18×1):(9×16)=32:3:24,故D不正确。
故选:B。
5.在生活生产中碳单质的应用广泛。下列有关含碳物质的性质或用途正确的是( )
A.活性炭具有吸附性
B.木炭常温下化学性质很活泼
C.金刚石用作电极
D.石墨用作钻探机钻头
【答案】A
【解析】A、活性炭具有吸附性,故选项说法正确。
B、木炭常温下化学性质不活泼,故选项说法错误。
C、金刚石不具有导电性,不能用作电极,故选项说法错误。
D、石墨质软,不能用作钻探机钻头,故选项说法错误。
故选:A。
6.从生活走进化学,让化学服务于健康生活。下列说法错误的是( )
A.老年人骨质疏松可服用含CaCO 的钙片
3B.贫血病患者需服用葡萄糖酸锌
C.胃酸过多患者可服用含Al(OH) 的药物
3
D.坏血病患者可服用维生素C片
【答案】B
【解析】A、老年人缺钙易患骨质疏松,因此预防骨质疏松,可适当摄入钙元素,该选项说法正确;
B、人体缺铁时易患贫血,因此治疗贫血时,应补充铁元素,而不是锌元素,该选项说法错误;
C、胃酸的主要成分为盐酸,氢氧化铝是一种碱,能与胃液中的盐酸反应,因此氢氧化铝可用于治疗胃
酸过多,该选项说法正确;
D、人体缺乏维生素C易患坏血症,可服用维生素C片,该选项说法正确;
故选:B。
7.三种金属X、Y、Z相互之间的反应关系如下
①Y+H SO ——YSO +H ↑,Z和H SO 不反应
2 4 4 2 2 4
②Z+2XNO ——Z(NO ) +2X
3 3 2
则X、Y、Z的金属活动性顺序为( )
A.X>Y>Z B.X>Z>Y C.Y>X>Z D.Y>Z>X
【答案】D
【解析】①Y+H SO ——YSO +H ↑,Z和H SO 不反应,说明Y的位置排在氢的前面,Z的位置排
2 4 4 2 2 4
在氢的后面,即Y>H>Z;
②Z+2XNO ——Z(NO ) +2X,说明Z的金属活动性比X强,即Z>X;
3 3 2
则X、Y和Z的金属活动性顺序为:Y>Z>X。
故选:D。
二、非选择题(本大题共7小题,共46分)
8.(6分)铼被誉为“超级金属”,铼及其合金被广泛应用到航空航天领域。铼元素的部分信息如图所示,
请回答下列问题:
(1)铼原子的质子数为 7 5 ,x= 1 3 。
(2)铼元素属于 金属 元素(填“金属”或“非金属”),铼的相对原子质量是 186. 2 。
(3)请画出元素周期表中原子序数为12的元素的原子结构示意图 ,该元素与铼元素的化
学性质 相似 (填“相似”或“不相似”)。
【答案】(1)75;13;(2)金属;186.2;
(3) ;相似。
【解析】(1)元素名称的左上角数字表示原子序数,原子序数=质子数,因此铼原子的质子数为 75,
原子中核电荷数=核外电子数=原子序数,因此75=2+8+18+32+x+2,x=13;
(2)铼字带有钅字旁,属于金属元素,元素名称的正下方的数字表示相对原子质量,因此铼的相对原
子质量是186.2;
(3)原子序数为12的元素为镁,核外电子排布为2、8、2,原子结构示意图 ;元素的化学性质
主要由原子最外层电子数决定的,原子的最外层电子数相同,元素的化学性质相似,因此该元素与铼元
素的化学性质相似。
9.(4分)习近平总书记在党的二十大报告中强调,“完善能源消耗总量和强度调控,重点控制化石能源
消费,逐步转向碳排放总量和强度“双控’制度。”
(1)现阶段的能源结构仍以化石燃料为主,化石燃料包括煤、 石油 和天然气,天然气的主要成分
是甲烷,甲烷完全燃烧生成水和 二氧化碳 。
(2)目前,我国的一些地区正在使用乙醇汽油作为汽车燃料,乙醇汽油属于 混合物 (填“纯净
物”或“混合物”)。
(3)通过节约能源、提高能效以及调整能源结构,可减少二氧化碳的排放量。请写一条有利于节能减
排的建议 骑自行车出行(合理即可) 。
【答案】(1)石油;二氧化碳;
(2)混合物
(3)骑自行车出行(合理即可)。
【解析】(1)化石燃料包括煤、石油和天然气,天然气的主要成分是甲烷,甲烷完全燃烧生成水和二
氧化碳;
(2)乙醇汽油含有多种物质,属于混合物
(3)通过节约能源、提高能效以及调整能源结构,可减少二氧化碳的排放量,为了节能减排,建议骑
自行车出行等。
10.(5分)中国科学家首次从月壤样品中发现新矿物——嫦娥石。学习小组查得资料:嫦娥石是从月壤
样品的14万个颗粒中,利用针尖和颗粒之间静电吸附作用,分离出的一个粒径约 1.0×10﹣5m的单晶颗
粒,其化学式为Ca NaMg(PO ) 。请和小组同学一起研究。
9 4 7
(1)嫦娥石的吸附分离过程属于 物理变化 (填“物理变化”或“化学变化”)。
(2)嫦娥石由 5 种元素组成。
(3)围绕“人类在月球上生活”的话题,展开月球上嫦娥石应用的讨论:
①助力农业生产:嫦娥石可作为生产 磷肥 (填“氮肥”“磷肥”或“钾肥”)的原料。
②提炼金属单质:若用107.2g嫦娥石提炼金属镁,最多可得镁的质量为 2. 4 g(嫦娥石的相对分子
质量为1072)。③展望更多应用:根据嫦娥石的组成推测,其可能另有的用途是 制取氧气(或其他合理答案)
(填一种)。
【答案】(1)物理变化;
(2)5;
(3)①磷肥;
②2.4;
③制取氧气(或其他合理答案)。
【解析】(1)物理变化与化学变化的区别:是否有新物质生成,嫦娥石的吸附分离过程没有新物质生
成,属于物理变化;
(2)由嫦娥石的化学式:Ca NaMg(PO ) 可知嫦娥石由5种元素组成;
9 4 7
(3)①嫦娥石中含有磷元素,属于磷肥;
②107.2g× =2.4g;
③嫦娥石中含有氧元素,可以用来制取氧气。
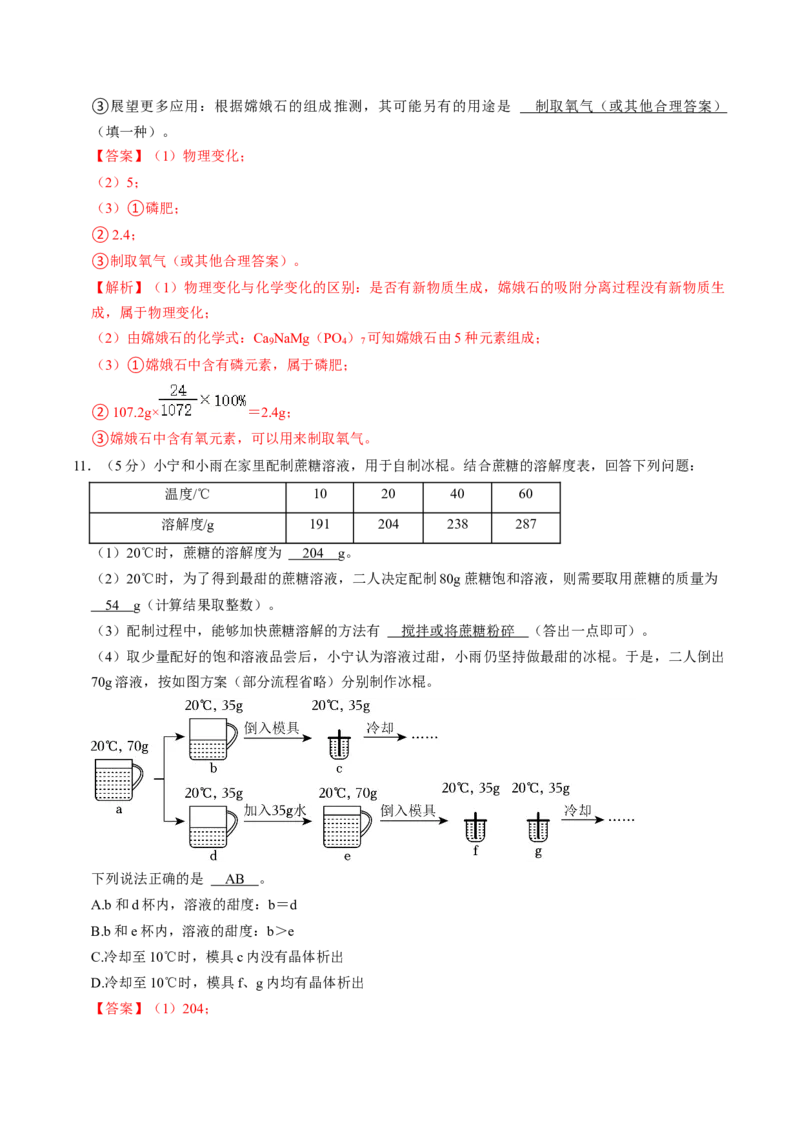
11.(5分)小宁和小雨在家里配制蔗糖溶液,用于自制冰棍。结合蔗糖的溶解度表,回答下列问题:
温度/℃ 10 20 40 60
溶解度/g 191 204 238 287
(1)20℃时,蔗糖的溶解度为 20 4 g。
(2)20℃时,为了得到最甜的蔗糖溶液,二人决定配制80g蔗糖饱和溶液,则需要取用蔗糖的质量为
5 4 g(计算结果取整数)。
(3)配制过程中,能够加快蔗糖溶解的方法有 搅拌或将蔗糖粉碎 (答出一点即可)。
(4)取少量配好的饱和溶液品尝后,小宁认为溶液过甜,小雨仍坚持做最甜的冰棍。于是,二人倒出
70g溶液,按如图方案(部分流程省略)分别制作冰棍。
下列说法正确的是 AB 。
A.b和d杯内,溶液的甜度:b=d
B.b和e杯内,溶液的甜度:b>e
C.冷却至10℃时,模具c内没有晶体析出
D.冷却至10℃时,模具f、g内均有晶体析出
【答案】(1)204;(2)54g;
(3)搅拌或将蔗糖粉碎;
(4)AB。
【解析】(1)由表中数据知20℃时,蔗糖的溶解度为204g;
(2)饱和溶液的浓度最大,得到的蔗糖溶液最甜,20℃时蔗糖的溶解度为204g,此时饱和溶液的溶质
质量分数为 =67.1%,配制
80g蔗糖饱和溶液,需要蔗糖的质量为80g×67.1%=54g;
(3)搅拌或将蔗糖粉碎可加快蔗糖溶解;
(4)A.b和d杯内溶液是将20℃时70g饱和溶液均分成两份,溶液具有均一性,故b和d杯内溶液的甜
度相等,A说法正确;
B.b和d杯内溶液浓度、溶液质量、溶质质量、溶剂质量等均相同,e杯溶液是在d杯溶液中加入35g水
进行稀释,溶液浓度变小,故b和e杯内,溶液的甜度b>e,B说法正确;
C.模具c内溶液是20℃时饱和溶液,蔗糖的溶解度随温度升高而增大,故冷却至10℃时有晶体析出,C
说法错误;
D.f杯内溶液是20℃时蔗糖的不饱和溶液,溶质质量是 d中溶质质量的一半,为35g× =
11.7g,溶剂质量为35g﹣11.7g=23.3g,10℃时,蔗糖的溶解度为191g,23.3g水中最多溶解蔗糖质量为
23.3g× =44.5g,故冷却至10℃时,模具f、g内溶液均是不饱和溶液,均没有晶体析出,D说法错
误;
故选AB。
12.(4分)根据如图所示的实验回答问题:
(1)A实验 不能 (填“能”或“不能”)用来测定空气中氧气的含量;
(2)B实验现象说明:空气中的氧气含量比呼出气体中的 高 (“高”或“低”);
(3)C实验中小灯泡发亮,说明石墨具有 导电 性;
(4)D实验用来验证质量守恒定律,其中气球的作用是 密封容器,缓冲气压 。
【答案】(1)不能 (2)高 (3)导电 (4)密封容器,缓冲气压
【解析】(1)木炭燃烧虽然会消耗氧气的,但会生成等体积的二氧化碳,装置内的压强不变,无法测
定空气中氧气的含量;故答案为:不能;
(2)将燃着的木条分别伸入盛有空气和呼出气体的集气瓶内,观察到伸入空气中的木条正常燃烧,伸入呼出气体中的木条熄灭,由此可知,空气中的氧气含量比呼出气体中的高;故答案为:高;
(3)C实验中小灯泡发亮,说明石墨具有导电性;故答案为:导电;
(4)在这个实验中气球的作用是密封容器,缓冲气压;故答案为:密封容器,缓冲气压。
13.(16分)氯化钠是重要的调味品。
探究一:古人智慧
(1)《水经注》中描述,“入汤口四十三里,有石,煮以为盐,石大者如升,小者如拳,煮之,水竭
盐成。”这样得到食盐的方法在化学上称为 蒸发结晶 。
(2)我国四川省自贡市劳动人民在公元1873年便开始尝试取井水煮卤,获得的氯化钠中仍然含有氯化
镁等杂质,古人采用“淋盐沥水”(用饱和氯化钠溶液洗涤粗盐)的方法来除去氯化镁,是因为 饱
和的氯化钠溶液里能继续溶解氯化镁 。
探究二:现代方法
智慧小组的同学想利用所学化学知识得到氯化钠晶体。他们查阅资料知道,通过晾晒海水或煮盐井水、
盐湖水等可得到粗盐。粗盐中含有多种可溶性杂质(如氯化镁、氯化钙、硫酸钠等)不溶性杂质(泥沙
等)。
除去不溶性杂质
(3)取少量粗盐,加足量水溶解,可通过 过滤 方法除去其中不溶性杂质。
除去可溶性杂质
(4)选择试剂:小民同学选择硝酸钡溶液除硫酸钠,反应的化学方程式是 Ba ( NO )
3
2+Na SO ═ BaSO ↓ +2NaNO 。
2 4 4 3
经小组讨论,认为他选的试剂不正确。
方法小结:除杂所选试剂需满足以下条件:只与杂质反应; 不产生新的杂质 。
最终,选择的试剂是氢氧化钠溶液、碳酸钠溶液、氯化钡溶液。
(5)实验探究:
滴加甲、乙、丙三种试剂的正确顺序最多有 3 种,请写出其中一种 NaOH 或 BaC l 或 N a CO
2 2 3
(写溶质的化学式,下同)。加入氢氧化钠溶液后,发生反应的化学方程式是 MgC l +2NaOH ═ Mg
2
( OH ) ↓ +2NaC l 。固体D的成分有 M g ( OH ) 、 BaSO 、 CaCO 、 BaCO 。
2 2 4 3 3
( 6 ) 反 思 评 价 : 液 体 E 中 加 入 稀 盐 酸 , 发 生 反 应 的 化 学 方 程 式 是
Na CO +2HCl ═ 2NaCl+CO ↑ +H O (写一个)。小郑同学认为上述实验可以将甲、乙、丙三种溶液
2 3 2 2
改成两种 B a ( OH ) 、 N a CO (按加入的先后顺序填写)。
2 2 3
【答案】(1)蒸发结晶;
(2)饱和的氯化钠溶液里能继续溶解氯化镁;(3)过滤;
(4)Ba(NO )2+Na SO ═BaSO ↓+2NaNO ;不产生新的杂质;
3 2 4 4 3
(5)3;NaOH或BaCl 或Na CO ;MgCl +2NaOH═Mg(OH) ↓+2NaCl;Mg(OH) 、BaSO 、
2 2 3 2 2 2 4
CaCO 、BaCO ;
3 3
(6)Na CO +2HCl═2NaCl+CO ↑+H O(或HCl+NaOH═NaCl+H O);Ba(OH) 、Na CO 。
2 3 2 2 2 2 2 3
【解析】(1)由于氯化钠的溶解度受温度影响不大,所以从氯化钠溶液中得到氯化钠晶体通常采用蒸
发结晶,
故答案为:蒸发结晶;
(2)饱和的氯化钠溶液里不能继续溶解氯化钠,还能继续溶解氯化镁,
故答案为:饱和的氯化钠溶液里能继续溶解氯化镁;
(3)过滤是将不溶性杂质与液体分离的一种操作方法,
故答案为:过滤;
(4)硝酸钡能和硫酸钠发生复分解反应生成硫酸钡沉淀和硝酸钠,
故答案为:Ba(NO )2+Na SO ═BaSO ↓+2NaNO ;
3 2 4 4 3
除杂质时应注意所加入的试剂只与杂质反应并且不能产生新的杂质,
故答案为:不产生新的杂质;
(5)粗盐提纯是加入试剂的顺序可以是氢氧化钠、氯化钡、碳酸钠或氯化钡、碳酸钠、氢氧化钠、或
氯化钡、氢氧化钠、碳酸钠3种设计方案,
故答案为:3;NaOH或BaCl 或Na CO ;
2 2 3
氢氧化钠能与氯化镁反应生成氢氧化镁沉淀和氯化钠,故
答案为: MgCl
2
+2NaOH═Mg(OH)
2
↓+2NaCl;
在粗盐提纯的过程中,氢氧化钠能与氯化镁反应生成氢氧化镁沉淀和氯化钠,硫酸钠和氯化钡反应生成
硫酸钡沉淀和氯化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钠和氯化钡反应生成碳酸钡
沉淀和氯化钠,
故答案为:Mg(OH) 、BaSO 、CaCO 、BaCO ;
2 4 3 3
(6)过滤后的滤液中含有碳酸钠和氢氧化钠以及氯化钠,其中氯化钠不与稀盐酸反应,碳酸钠能和稀
盐酸发生化学反应生成氯化钠和水和二氧化碳,氢氧化钠和稀盐酸反应生成氯化钠和水,
故答案为:Na CO +2HCl═2NaCl+CO ↑+H O(或HCl+NaOH═NaCl+H O);
2 3 2 2 2
氢氧化钡能和氯化镁反应生成氢氧化镁沉淀,氢氧化钡也能和硫酸钠反应生成硫酸钡沉淀,根据复分解
反应的条件,从离子的角度分析不难看出看,加入氢氧化钡溶液可以同时将镁离子和硫酸根离子这两种
杂质离子除去,而多余的钡离子,可以通过加入碳酸钠的方法除去,
故答案为:Ba(OH) 、Na CO 。
2 2 3
14.(6分)化学实验操作考试结束后,同学们想了解所用石灰石样品中碳酸钙的质量分数,进行了以下
实验。取25g石灰石样品于烧杯中,加入足量的稀盐酸至完全反应,测得烧杯内残留固体的质量为5g
(石灰石中的杂质不参加反应也不溶于水)。请计算。
(1)该石灰石样品中碳酸钙的质量分数。(2)实验过程中,理论上可生成二氧化碳的质量是多少?
【答案】解:(1)石灰石样品中碳酸钙的质量为:25g﹣5g=20g,碳酸钙的质量分数为: ×100%
=80%。
(2)设反应生成的二氧化碳质量为x。
CaCO +2HCl=CaCl +H O+CO ↑
3 2 2 2
100 44
20g x
x=8.8g
答:(1)该石灰石样品中碳酸钙的质量分数为80%
(2)理论上可生成二氧化碳的质量是8.8g。