文档内容
2024 年中考第二次模拟考试(苏州卷) 8.配制6%的氯化钠溶液,不需要用到的仪器是
化 学
A.玻璃棒 B.量筒 C.漏斗 D.烧杯
(满分:100分 考试时间:100分钟 )
9.下列 参与的反应中,属于中和反应的是
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。 A. B.
2.回答选择题时,选出每小题答案后,用 2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
C. D.
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
10.氧气的实验室制取与性质实验中,下列相关操作正确的是
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mn-55 Fe-56 Ni-59
A. B. C. D.
选择题(共 40 分)
单项选择题(包括20题,每题2分,共40分。每题只有一个选项最符合题意)
11.中学生应具备一定的生活安全常识,下列做法不符合安全要求的是
1.下列苏州美食中富含维生素的是
A.发现有同伴触电,要立即拉开同伴,然后赶紧切断电源
A.卤汁豆腐干 B.松鼠桂鱼 C.东山枇杷 D.阳澄湖大闸蟹
B.炒菜时油锅着火,立即盖上锅盖,使可燃物隔绝氧气而灭火
2.空气中含量较高且在食品包装中用作保护气的是
C.油库、加油站等场所严禁吸烟和拨打手机
A.氧气 B.氮气 C.二氧化碳 D.氦气
D.发现家中天然气或者液化气泄漏时,应先关闭阀门,并开窗通风
3.自然界中的物质大多数是化合物,下列化合物属于氧化物的是
12.我国在西汉初年就掌握炼铁技术,领先西方国家1000多年。下列说法错误的是
A.KOH B.C HO C.NaCO D.PO
2 6 2 3 2 5 A.生铁比纯铁的硬度高,抗腐蚀性更好
4.学校正推行垃圾分类。餐后的食物残渣应该投入印有下列哪种标识的垃圾箱中
B.铁是地壳中含量仅次于铝的金属元素
C.工业上炼铁是用一氧化碳做还原剂
A.可回收物 B.厨余垃圾 C.有害垃圾 D.其他垃圾
D.除去铁制品表面的油膜能更好防止其腐蚀
13.苏州盛产杨梅。杨梅中含有丰富的叶酸,对防癌抗癌有积极作用,其化学式为 下列有关叶
阅读下列材料,回答5~7题。
酸的说法中正确的是
镓元素在元素周期表中的信息如图所示,其形成的化合物氮化镓(GaN)是一种新型半导体材料,可通
A.叶酸的相对分子质量为
过以下反应获得: ,反应中氮元素的化合价不变。
B.叶酸由 个碳原子、 个氢原子、 个氮原子和 个氧原子构成
C.叶酸是由碳、氢、氮、氧四种元素组成的有机物
D.叶酸中氮元素与氧元素的质量比为7:6
14.钴(Co)的金属活动性与铁相似,钴的化合物相关性质如表。下列预测不合理的是
5.下列有关镓的说法不正确的是
物质 CoO Co(OH) CoCl CoCO
2 2 3
A.镓属于金属元素 B.镓原子的核外电子数为31
在水中的溶解
C.镓原子的核内中子数为31 D.元素的相对原子质量为69.72
难溶,灰绿色固体 难溶,粉红色固体 易溶,溶液呈粉红色 难溶,粉红色固体
性
6.获得氮化镓的反应所属的基本反应类型是
A.化合反应 B.分解反应 C.置换反应 D.以上均不正确 A.Co能从MgCl 2 溶液中置换出Mg
7.GaN中Ga的化合价为 B.CoO能与盐酸反应得到粉红色溶液
A.+1 B.+3 C.-3 D.-1 C.CoCO 3 能与盐酸反应生成CO 2………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
D.Co(OH) 也能与盐酸反应
2
15.下列物质性质和用途对应关系不正确的是
A.活性炭有吸附性,可用作除味剂
此
B.熟石灰有碱性,可用于治疗胃酸过多
C.油脂能溶于汽油,可用于除油污
卷
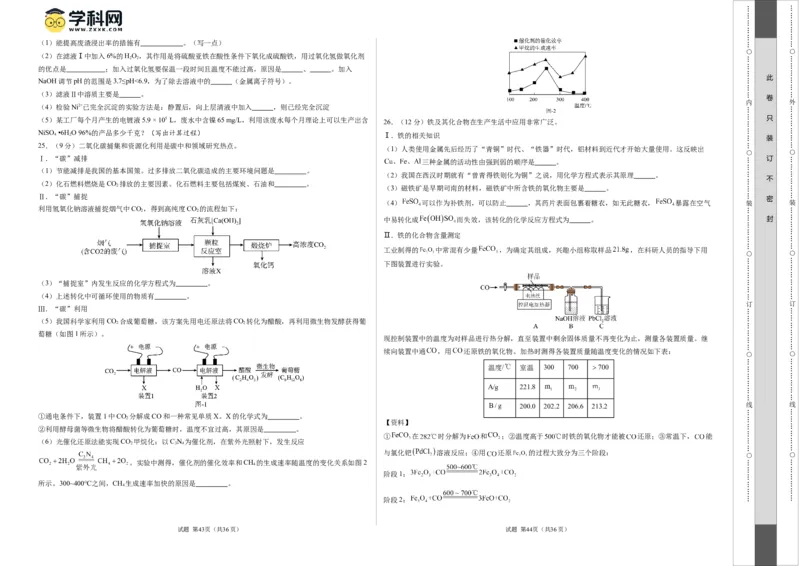
D.生石灰有吸水性,可用作食品干燥剂 A.空气中氧气的浓度大约为20%
16.如图为两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是 只
B.AB段氧气浓度增大,说明氧气在空气中能够较快地大量下沉
C.C点之后,氧气浓度减小,左侧区域中带火星的香复燃,燃着的蜡烛剧烈燃烧
装
D.实验结束时,氧气被完全消耗
订
20.科学家研究开发氢能源的脚步从未停止。如图乙为利用 热化学循环制氢的反应流程,反应前
后Mn的化合价均为+2价。下列说法中错误的是 不
密
A.甲的饱和溶液由t℃降温至t℃,变为不饱和溶液 2 1
B.t℃时,将25g甲放入50g水中,形成75g饱和溶液
1 封
C.t℃时,甲、乙两种物质的溶解度相同为50
1
D.乙溶液中含有少量甲,可用蒸发溶剂的方法提纯甲
17.如图a所示,向 稀溶液中缓缓通入 气体,测定该过程中溶液导电能力的变化,实验结果如图
A.若 中 ,则 中 与 的个数比为1∶2
b(溶液体积的变化忽略不计)。下列说法错误的是
B.与传统电解法制取氢气相比,该流程的优点是能够节约能源
C.利用该流程每生成48 kg氧气,理论上能得到氢气的质量是6 kg
D.氢气燃烧热值高,产物无污染,是最清洁的能源
非选择题(共 60 分)
21.(9分)苏州的许多传统与现代工艺都与化学息息相关。
A.该过程中溶液温度先升高再恢复至室温
Ⅰ.传统工艺
B.C点溶液中的微粒有 、 、
(1)文物贴金。金箔不易变色,说明黄金化学性质 (填“稳定”或“活泼”)。
C. 段变化,其他条件相同,导电能力: (2)传统粉墙。用石灰浆(氢氧化钙的悬浊液)抹墙后,墙壁表面变白且坚硬。在上述过程中,氢氧化钙
D. 段变化,溶液的导电能力除了与离子种类有关,还与离子浓度有关 发生反应的化学方程式为 。
18.物质之间可以相互转化,下列物质的转化方案中,正确的是 Ⅱ.矿物颜料
(3)朱砂可制成鲜红色颜料,主要成分为硫化汞( 、 的化合价分别为+2和-2)。硫化汞的化学式为
A.Cu CuSO B.Fe FeCl
4 3
。
C.BaCl NaCl D.NaNO KNO
2 3 3
(4)赤铁矿(主要成分 )可用于制作红棕色颜料,其中铁元素化合价为 。
19.某实验小组为探究氧气的性质,利用传感器绘制氧气浓度与时间的曲线图。曲线在AB段时,隔板未提
(5)孔雀石[主要成分为 ]可用于制作青色颜料,对酸敏感。补充完整下列化学方程式:
起:曲线在BC段时,隔板稍微向上提起。通过该实验不能获取的信息是
。
Ⅲ.创新科技
(6)新能源客车。电池充电时的能量转化方式:电能转化为 。
试题 第23页(共36页) 试题 第24页(共36页)(7)多晶硅制备。 气体被加热分解为硅和氢气,反应的化学方程式为 。
22.(11分)结合下图回答问题。
2023年我国同济大学用全氯化萘( )和全氯化蒽( )两种前驱体分子,在NaCl薄膜表面
上合成了两种环碳分子 和 。原子力显微镜显示, 和 均为累积烯炔型结构,如下图。
(1)仪器名称:① ,② 。
(2)用过氧化氢和二氧化锰制取氧气,可选用装置 (选填序号)和D组合,反应的化学方程式为
,二氧化锰的作用是 。
研究人员表示,该项研究提出的表面合成策略有望成为一种合成系列环碳的普适方法。
(3)实验室可用装置B或C制H,C装置相对于B的优点有 。用E装置收集H,气体应
2 2
(1)金刚石和石墨物理性质差异很大的原因是 。
从 (选填“a”或“b”)端通入。
(2)1个全氯化萘( )分子和1个全氯化蒽( )分子中所含原子个数之比是 ;已知苯
(4)用图1装置探究CO、SO 与水的反应。F装置中装入相应的药品反应可得到CO 或SO ,图2表示
2 2 2 2
CO、SO 与水反应过程中溶液pH的变化曲线。
2 2
的结构为 ,结合全氯化萘和全氯化蒽的分子结构可推断,1个全氯化苯分子中含有 个氯原子。
(3)制备 的转化过程中,碳元素的质量分数 (填“升高”、“降低”或“不变”);碳元
素的化合价 (填“升高”、“降低”或“不变”)。
(4)用 制备 的化学方程式为 。
(5)下列叙述正确的是 (填序号)。
a. 是碳的一种同素异形体
①装置F中用碳酸钠和稀硫酸反应得到CO,不选用稀盐酸的原因是 。
2
b. 的分子中每个碳原子与周围2个碳原子连接
②装置H中漏斗的作用是 。
③图2中最终曲线②比曲线①低的原因是 。 c. 与 中碳原子的连接方式都是单键与叁键交替连接。
23.(8分)新型碳材料——环碳有望成为新型半导体材料,在分子电子器件中有广阔的应用前景。 24.(11分)NiSO ▪6H O主要用于电镀行业镀镍,制镍催化剂等,它可由电镀废渣(除含镍外,还含有
4 2
碳是一种常见的元素,在自然界中有多种形式。其外在表现形式取决于每个碳原子周围与之连接的碳 Cu、Fe 杂质)为原料获得。工艺流程如图:
原子数目。当每个碳原子与周围4个碳原子连接时,就形成了金刚石;当每个碳原子与周围3个碳原子连接
时,就形成了石墨;当每个碳原子与周围2个碳原子连接时,则形成环形纯碳分子(环碳 )。
同种元素组成的不同单质称为同素异形体,环碳、金刚石、石墨都是碳的同素异形体。环碳中碳原子
与碳原子之间的连接方式(也叫成键方式)有两种:一种是累积烯炔型,碳原子通过连续双键连接,如 已知:25℃时,几种金属氢氧化物沉淀的pH范围如下表所示。
“ ”;另一种是聚炔型,碳原子通过单键与叁键交替连接,如“
名称 Fe(OH) Fe(OH) Ni(OH)
2 3 2
”。
开始沉
2019年,牛津大学的研究团队通过环氧碳分子 在5K(K是温度单位)温度下脱去CO制备环碳 6.5 1.5 6.9
淀
,验证了 为聚炔型结构,转化过程如图所示。
完全沉
9.7 3.7 8.9
淀
资料:①Ni能与稀硫酸反应;②NiSO 易溶于水,不溶于乙醇:NiCO 是一种不溶于水,易溶于强酸的沉
4 3
淀;③NaCO+NiSO=NaSO +NiCO 。
2 3 4 2 4 3………………
○
………………
外
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
………………
○
………………
内
………………
○
………………
装
………………
○
………………
订
………………
○
………………
线
………………
○
………………
(1)能提高废渣浸出率的措施有 。(写一点)
(2)在滤液Ⅰ中加入6%的HO,其作用是将硫酸亚铁在酸性条件下氧化成硫酸铁,用过氧化氢做氧化剂
2 2
的优点是 ;加入过氧化氢要保温一段时间且温度不能过高,原因是 、 。加入
此
NaOH调节pH的范围是3.7≤pH<6.9,为了除去溶液中的 (金属离子符号)。
(3)滤液Ⅱ中溶质主要是 。
卷
(4)检验Ni2+已完全沉淀的实验方法是:静置后,向上层清液中加入 ,则已经完全沉淀
(5)某工厂每个月产生的电镀液5.9 × 105 L,废水中含镍65 mg/L,利用该废水每个月理论上可以生产出含 26.(12分)铁及其化合物在生产生活中应用非常广泛。 只
NiSO ▪6H O 96%的产品多少千克?(写出计算过程)
4 2 Ⅰ.铁的相关知识
装
25.(9分)二氧化碳捕集和资源化利用是碳中和领域研究热点。
(1)人类使用金属先后经历了“青铜”时代、“铁器”时代,铝材料到近代才开始大量使用。这反映出
Ⅰ.“碳”减排 订 三种金属的活动性由强到弱的顺序是 。
(1)节能减排是我国的基本国策。过多排放二氧化碳造成的主要环境问题是 。
(2)我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理 。
不
(2)化石燃料燃烧是CO 排放的主要因素。化石燃料主要包括煤炭、石油和 。
2 (3)磁铁矿是早期司南的材料,磁铁矿中所含铁的氧化物主要是 。
Ⅱ.“碳”捕捉
密
(4) 可以作为补铁剂,可以防止 ,其药片表面包裹着糖衣,如无此糖衣, 暴露在空气
利用氢氧化钠溶液捕捉烟气中CO,得到高纯度CO 的流程如下: 2 2
中易转化成 而失效,该转化的化学反应方程式为 。 封
Ⅱ.铁的化合物含量测定
工业制得的 中常混有少量 ,为确定其组成,兴趣小组称取样品 ,在科研人员的指导下用
下图装置进行实验。
(3)“捕捉室”内发生反应的化学方程式为 。
(4)上述转化中可循环使用的物质有 。
Ⅲ.“碳”利用
(5)我国科学家利用CO 合成葡萄糖,该方案先用电还原法将CO 转化为醋酸,再利用微生物发酵获得葡
2 2
萄糖(如图1所示)。
现控制装置中的温度为对样品进行热分解,直至装置中剩余固体质量不再变化为止,测量各装置质量。继
续向装置中通 ,用 还原铁的氧化物。加热时测得各装置质量随温度变化的情况如下表:
温度/ 室温 300 700
A/g 221.8
200.0 202.2 206.6 213.2
①通电条件下,装置1中CO 分解成CO和一种常见单质X。X的化学式为 。
2
【资料】
②利用酵母菌等微生物将醋酸转化为葡萄糖时,温度不宜过高,其原因是 。
① 在 时分解为 和 ;②温度高于 时铁的氧化物才能被 还原;③常温下, 能
(6)光催化还原法能实现CO 甲烷化:以C N 为催化剂,在紫外光照射下,发生反应
2 3 4
与氯化钯 溶液反应;④用 还原 的过程大致分为三个阶段:
。实验中测得,催化剂的催化效率和CH 的生成速率随温度的变化关系如图2
4
阶段1:
所示。300~400℃之间,CH 生成速率加快的原因是 。
4
阶段2:
试题 第43页(共36页) 试题 第44页(共36页)阶段3:
(5)装置 的作用是 。
(6)样品中 的质量分数为 (精确到0.1%)。
(7) 时,装置 中固体为纯净物,表格中的 。
(8)当温度 时,测得此时装置 总质量为 ,则 中剩余固体的成分及对应的质量 。