文档内容
2025 年 9 月高二五校联考试题
化学
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Fe-56 Cu-64
一、单项选择题(每小题3分,共42分)
1. 化学与生产、生活密切相关。下列事实与化学反应速率无关的是
A. 食盐中添加碘酸钾 B. 铝合金门窗比钢门窗更耐腐蚀
C. 医护人员冷藏存放“流感”疫苗 D. 家用铁锅、铁铲等厨具保持干燥
2. 工业上常用NaClO处理氨氮废水,其原理为: ,下列有关说
法正确的是
A. 和 互为同素异形体 B. 属于弱电解质
C. 水分子的球棍模型: D. NaCl的电子式为:
3. 反应 的能量变化如图所示。下列说法正确的是
.
A 稳定性:
B. 该反应要发生一定需要加热
C.
D. 盐酸与碳酸氢钠反应的能量变化过程与该图相似
4. 设 为阿伏伽德罗常数的值,下列说法正确的是
A. 和 充分反应生成1 mol 时转移电子数为
B. 1 L 1 mol/L的HF溶液中含有H⁺数目为
第1页/共11页
学科网(北京)股份有限公司C. 64 g Cu与足量S完全反应转移的电子数为
D. 常温下,56 g铁片投入足量浓 中生成 个 分子
5. 下列能说明CHCOOH是弱电解质的是( )
3
A. CHCOOH溶液的导电能力比盐酸的弱
3
B. CHCOOH溶液与碳酸钙反应,缓慢放出二氧化碳
3
C. 0.1mol·L-1的CHCOOH溶液中,氢离子的浓度约为0.001mol·L-1
3
D. CHCOOH溶液用水稀释后,氢离子浓度降低
3
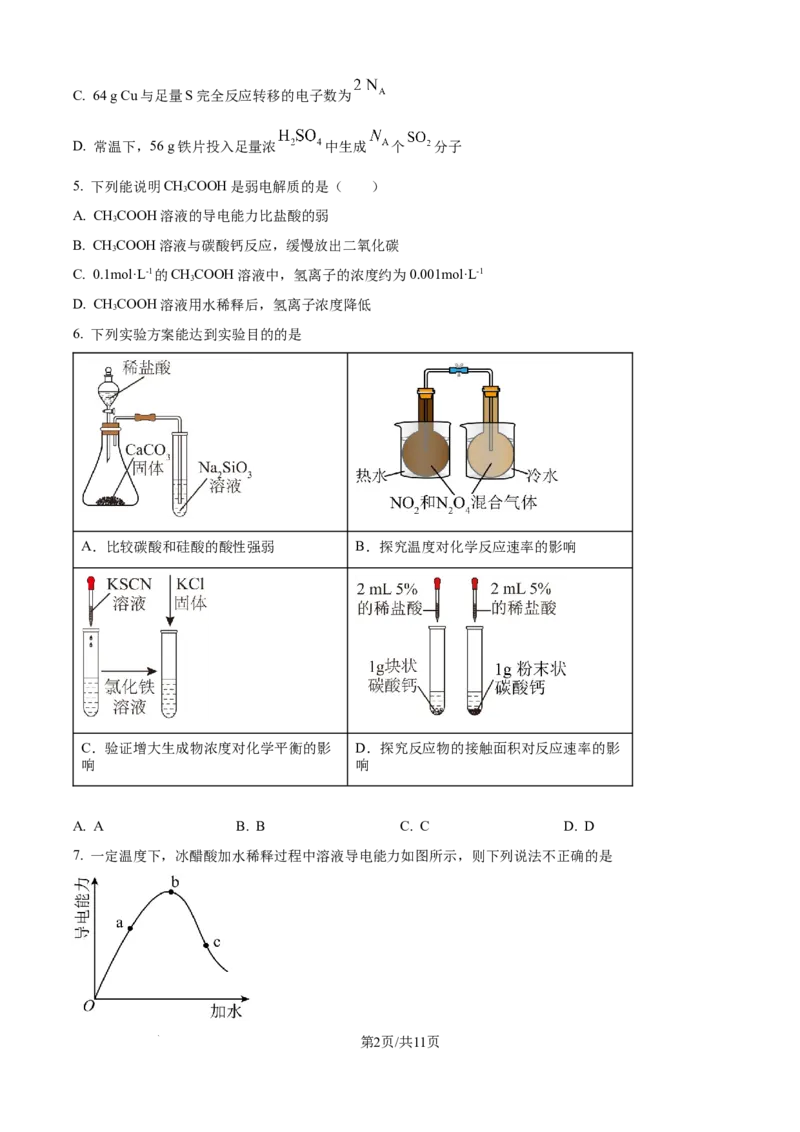
6. 下列实验方案能达到实验目的的是
A.比较碳酸和硅酸的酸性强弱 B.探究温度对化学反应速率的影响
C.验证增大生成物浓度对化学平衡的影 D.探究反应物的接触面积对反应速率的影
响 响
A. A B. B C. C D. D
7. 一定温度下,冰醋酸加水稀释过程中溶液导电能力如图所示,则下列说法不正确的是
第2页/共11页
学科网(北京)股份有限公司A. “0”点不导电的原因是冰醋酸中无自由移动的离子
B. b点时醋酸电离程度最大
C. c点溶液中加入 固体可使 增大、 减小
D. a、b、c三点溶液用1 mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积相等
8. 下列电离方程式或离子方程式正确的是
A. 气体溶于水后的电离方程式:
B. 醋酸铵在水中的电离方程式:
C. 酸性高锰酸钾溶液与草酸反应的离子方程式:
D. 硫代硫酸钠溶液中滴加稀硫酸产生浅黄色沉淀的离子方程式:
9. 下列实验操作、现象、结论均正确的是
选
实验操作 现象 结论
项
加热后溶
取
A 液变为黄
溶液于试管中,加热 绿色 的
加入
向 溶液
B 中分别滴加5滴等浓度的 比 催化效果好
溶液的反
和 溶液
应更剧烈
容器中气
温度不变,扩大盛有 体颜色先
平衡 先正向移
C 变浅后变
和 混合气体的密闭容
深,但比 动再逆向移动
器体积
原来的浅
取 溶
液于试管中,加入
溶液变血
D 溶 KI与 的反应存在限度
红色
液,充分反应后滴入5滴
的KSCN溶液
A. A B. B C. C D. D
10. 某有机物的结构如图所示,则下列说法正确的是
第3页/共11页
学科网(北京)股份有限公司A. 该有机物能与 反应
B. 该有机物中有4种官能团
C. 该有机物中能使酸性高锰酸钾溶液褪色的官能团有2种
D. 该有机物能发生加成反应和氧化反应,不能发生取代反应
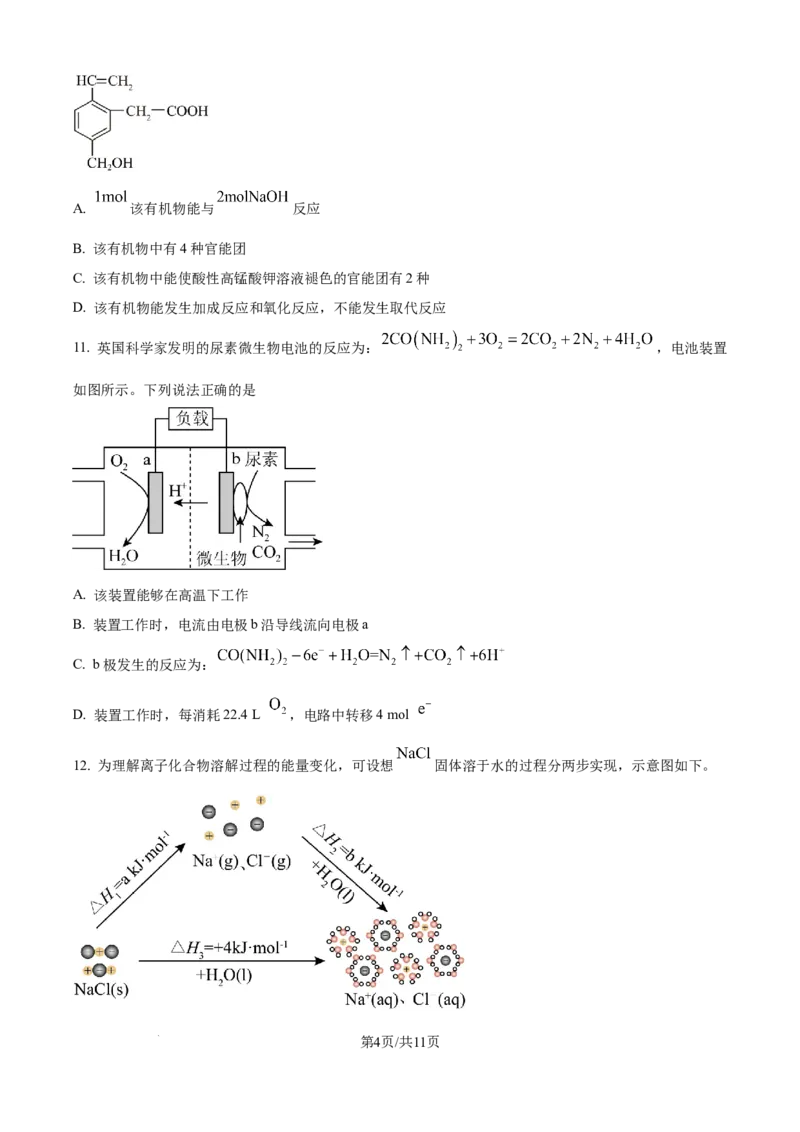
11. 英国科学家发明的尿素微生物电池的反应为: ,电池装置
如图所示。下列说法正确的是
A. 该装置能够在高温下工作
B. 装置工作时,电流由电极b沿导线流向电极a
C. b极发生的反应为:
D. 装置工作时,每消耗22.4 L ,电路中转移4 mol
12. 为理解离子化合物溶解过程的能量变化,可设想 固体溶于水的过程分两步实现,示意图如下。
第4页/共11页
学科网(北京)股份有限公司下列说法不正确的是
A. 固体溶解是吸热过程
.
B 根据盖斯定律可知:
C. 根据各微粒的状态,可判断 ,
D. 溶解过程的能量变化,与 固体和 溶液中微粒间作用力的强弱有关
13. 下表是在相同温度下三种酸的一些数据,下列判断不正确的是
酸 HX HY HZ
浓度/( ) 0.2 0.9 0.9 0.9
.
电离度 0.2 01 0.3 0.5
电离常数
A. 在相同温度下,电离常数:
的
B. 在相同温度下,从HX 数据可以说明:
C. 反应 能够发生
D. 表格中两种浓度的HX溶液中,从左至右 逐渐增大
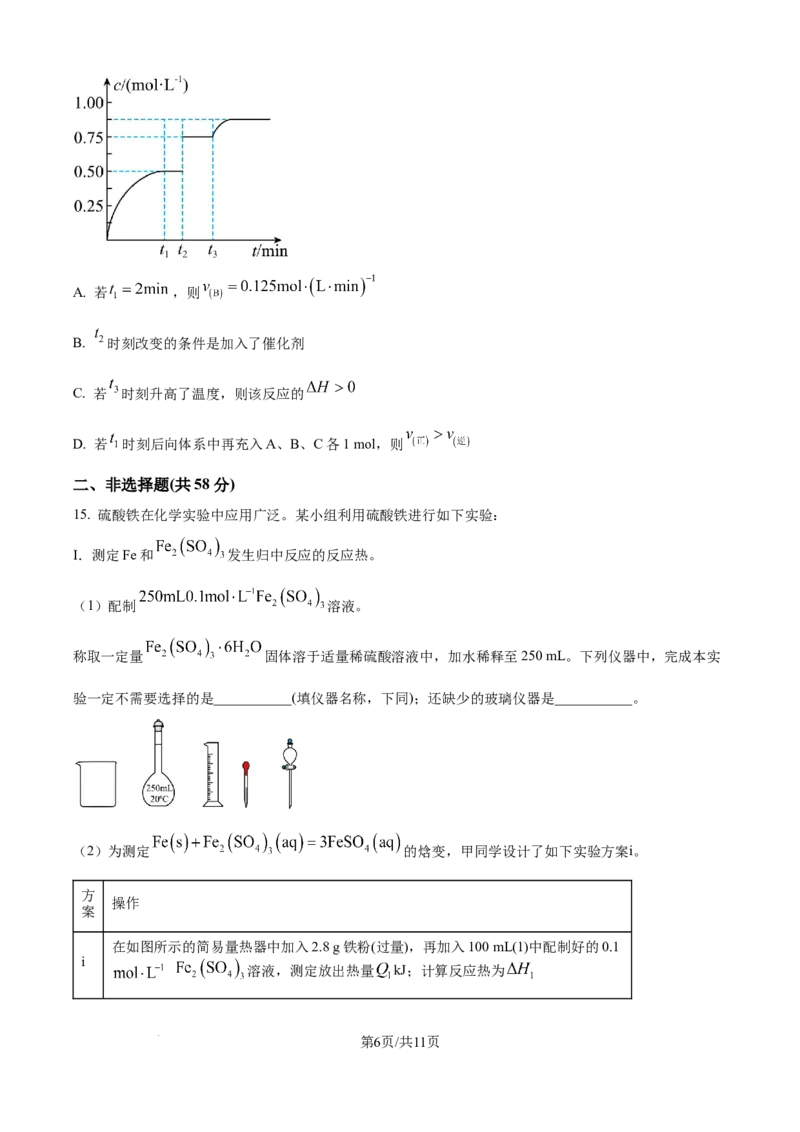
14. 一定温度下,将1 mol A和1 mol B气体充入2 L恒容密闭容器,发生反应
, 时达到平衡,在 、 时刻分别改变反应的一个条件,测得容器中气
体C的浓度随时间变化如图所示,下列说法错误的是
第5页/共11页
学科网(北京)股份有限公司A. 若 ,则
B. 时刻改变的条件是加入了催化剂
C. 若 时刻升高了温度,则该反应的
D. 若 时刻后向体系中再充入A、B、C各1 mol,则
二、非选择题(共58分)
15. 硫酸铁在化学实验中应用广泛。某小组利用硫酸铁进行如下实验:
Ⅰ.测定Fe和 发生归中反应的反应热。
(1)配制 溶液。
称取一定量 固体溶于适量稀硫酸溶液中,加水稀释至250 mL。下列仪器中,完成本实
验一定不需要选择的是___________(填仪器名称,下同);还缺少的玻璃仪器是___________。
(2)为测定 的焓变,甲同学设计了如下实验方案ⅰ。
方
操作
案
在如图所示的简易量热器中加入2.8 g铁粉(过量),再加入100 mL(1)中配制好的0.1
ⅰ
溶液,测定放出热量 kJ;计算反应热为
第6页/共11页
学科网(北京)股份有限公司①本实验中“搅拌”的操作方法是___________。若把玻璃搅拌器误用为铜质搅拌器,则计算结果 会
___________(填“偏高”、“偏低”或“不变”)。
②乙同学认为甲同学设计的实验方案测得的结果误差较大,判断依据是___________。基于相关原理,乙
同学重新设计了优化的实验方案ⅱ。
方
操作
案
第1步,在如图所示的简易量热器中加入2.8 g铁粉,再加入100 mL 0.1
溶液,测定放出热量 kJ,计算反应热为 ;
ⅱ
第2步,在如图所示的简易量热器中加入3.2 g铜粉,再加入100 mL(1)中配制好的
0.1 溶液,测定放出热量 kJ,计算反应热为 。
③根据方案ⅱ测定结果计算: ___________(用含 、
的代数式表示)。
Ⅱ.探究影响Cu和 反应速率的外界因素。
实 纯铜粉 0.1 水的体 水浴温 测定铜粉完全溶解
验 质量(g) 积(mL) 度(℃) 所用时间(min)
溶液体积(mL)
Ⅰ 0.3 60 0 35℃
Ⅱ 0.3 50 V 35℃
Ⅲ 0.3 60 0 45℃
(3)实验Ⅱ中, ___________。
的
(4)设计实验Ⅰ、Ⅱ 目的是探究其它条件相同时,___________对反应速率的影响。
第7页/共11页
学科网(北京)股份有限公司(5)实验结果: ,由此可推出的实验结论是___________。
16. 油气开采、石油化工、煤化工等行业产生的废气普遍含有硫化氢,需要回收处理并利用。已知下列反
应的热化学方程式:
① (平衡常数)
② (平衡常数)
③ (平衡常数)
(1)则 ___________; ___________(用含 和 的代数式表示)。
(2)下列叙述一定能说明反应②达到平衡状态的是___________(填标号)。
A. 断裂4 mol C-H的同时生成4 mol H-H
B. 在恒温恒容下, 和 浓度之比不再变化
C. 在恒温恒压下,混合气体的密度不再变化
D. 在恒容绝热下, 不再变化
(3)反应③在___________(填“高温”、“低温”或“任何温度”)下可自发进行。能同时提高反应③的
反应速率和 转化率的一种措施是___________。
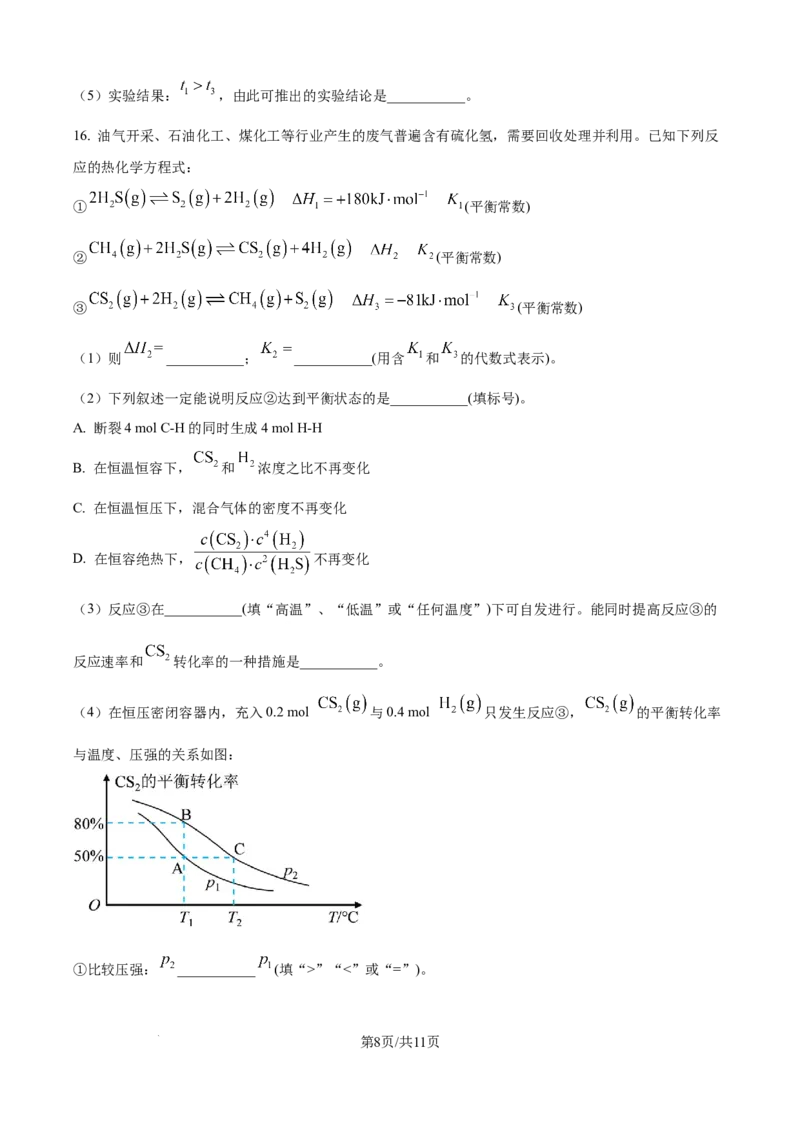
(4)在恒压密闭容器内,充入0.2 mol 与0.4 mol 只发生反应③, 的平衡转化率
与温度、压强的关系如图:
①比较压强: ___________ (填“>”“<”或“=”)。
第8页/共11页
学科网(北京)股份有限公司②维持温度不变,向A点状态的容器中充入氩气, 的转化率___________(填“升高”、“降低”或
“不变”)。
③B点处,容器体积为2L,则 ℃时该反应的平衡常数 ___________。
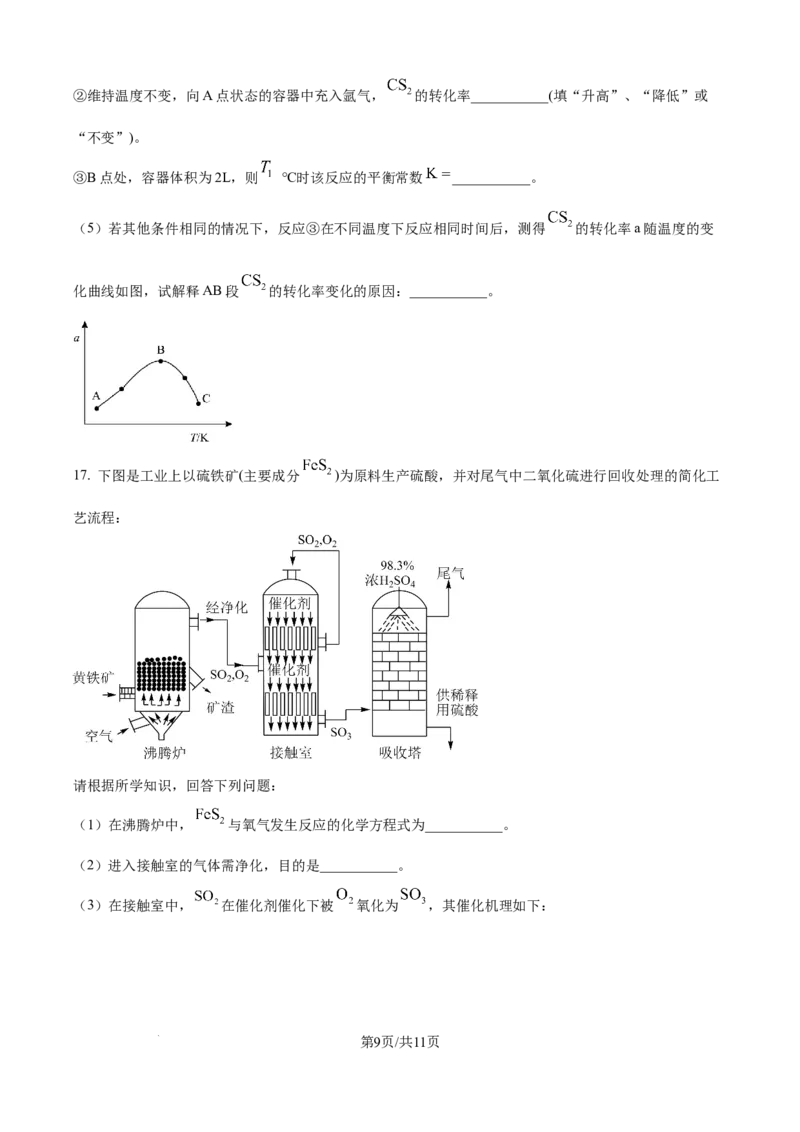
(5)若其他条件相同的情况下,反应③在不同温度下反应相同时间后,测得 的转化率a随温度的变
化曲线如图,试解释AB段 的转化率变化的原因:___________。
17. 下图是工业上以硫铁矿(主要成分 )为原料生产硫酸,并对尾气中二氧化硫进行回收处理的简化工
艺流程:
请根据所学知识,回答下列问题:
(1)在沸腾炉中, 与氧气发生反应的化学方程式为___________。
(2)进入接触室的气体需净化,目的是___________。
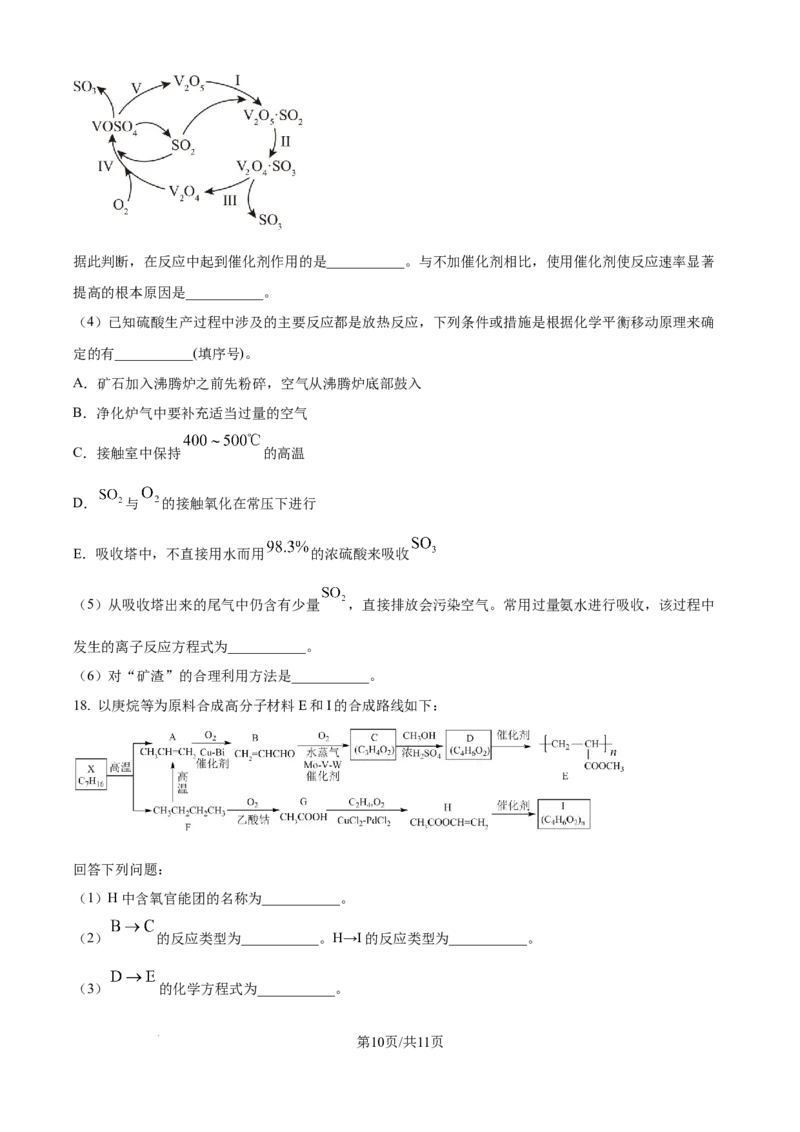
(3)在接触室中, 在催化剂催化下被 氧化为 ,其催化机理如下:
第9页/共11页
学科网(北京)股份有限公司据此判断,在反应中起到催化剂作用的是___________。与不加催化剂相比,使用催化剂使反应速率显著
提高的根本原因是___________。
(4)已知硫酸生产过程中涉及的主要反应都是放热反应,下列条件或措施是根据化学平衡移动原理来确
定的有___________(填序号)。
A.矿石加入沸腾炉之前先粉碎,空气从沸腾炉底部鼓入
B.净化炉气中要补充适当过量的空气
C.接触室中保持 的高温
D. 与 的接触氧化在常压下进行
E.吸收塔中,不直接用水而用 的浓硫酸来吸收
(5)从吸收塔出来的尾气中仍含有少量 ,直接排放会污染空气。常用过量氨水进行吸收,该过程中
发生的离子反应方程式为___________。
(6)对“矿渣”的合理利用方法是___________。
18. 以庚烷等为原料合成高分子材料E和I的合成路线如下:
回答下列问题:
(1)H中含氧官能团的名称为___________。
(2) 的反应类型为___________。H→I的反应类型为___________。
(3) 的化学方程式为___________。
第10页/共11页
学科网(北京)股份有限公司(4)写出C的结构简式___________。
(5)写出物质F的同分异构体的结构简式___________。
(6)下列有关说法不正确的是___________(填字母)。
A. 有机化合物X和G均难溶于水
B. 有机化合物C可以使 的 溶液褪色
C. 有机化合物B可以发生银镜反应
D. 有机化合物D和H互为同分异构体
第11页/共11页
学科网(北京)股份有限公司