文档内容
2023 级高二学年上学期期中考试
化 学 试 题
考试时间: 75 分钟 分值: 100分
命题人:辛爽 审题人:于艳丽
可能用到的相对原子质量 H1 O16 Na 23 K39 Cl35.5 Cr52 Cu 64 Ag 108
一、选择题(每道题只有一个正确选项,每题3分,共45分)
1. 化学与生产、生活、科技等密切相关。下列说法错误的是
A. 生活中常用明矾净水,可加速水中的悬浮物沉降
B. 加热蒸干 CuCl₂溶液得到 Cu(OH)₂固体
C. 处理锅炉水垢中的CaSO₄,可以先用饱和碳酸钠溶液浸泡,再用酸除去
D. 草木灰与 NH₄H₂PO₄混合施用,可更好为植物全面提供N、P、K三种营养元素
2. 下列事实能用勒夏特列原理解释的是
A. 加入催化剂有利于SO₂生成SO₃
B. 黄绿色的氯水光照后颜色变浅
C. 500℃比常温更有利于合成氨的反应
D. 由氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深
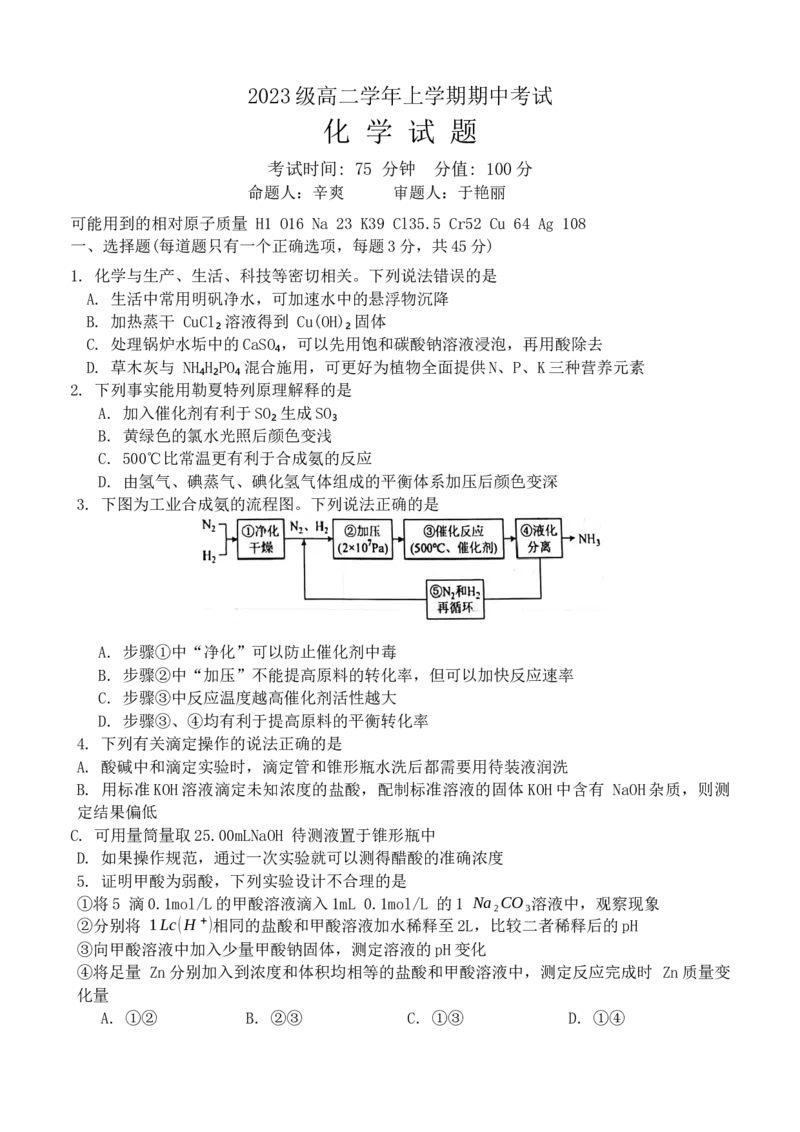
3. 下图为工业合成氨的流程图。下列说法正确的是
A. 步骤①中“净化”可以防止催化剂中毒
B. 步骤②中“加压”不能提高原料的转化率,但可以加快反应速率
C. 步骤③中反应温度越高催化剂活性越大
D. 步骤③、④均有利于提高原料的平衡转化率
4. 下列有关滴定操作的说法正确的是
A. 酸碱中和滴定实验时,滴定管和锥形瓶水洗后都需要用待装液润洗
B. 用标准KOH溶液滴定未知浓度的盐酸,配制标准溶液的固体 KOH中含有 NaOH杂质,则测
定结果偏低
C. 可用量筒量取25.00mLNaOH 待测液置于锥形瓶中
D. 如果操作规范,通过一次实验就可以测得醋酸的准确浓度
5. 证明甲酸为弱酸,下列实验设计不合理的是
①将5 滴0.1mol/L的甲酸溶液滴入1mL 0.1mol/L 的1 Na₂CO₃溶液中,观察现象
②分别将 1Lc(H⁺)相同的盐酸和甲酸溶液加水稀释至2L,比较二者稀释后的pH
③向甲酸溶液中加入少量甲酸钠固体,测定溶液的pH变化
④将足量 Zn分别加入到浓度和体积均相等的盐酸和甲酸溶液中,测定反应完成时 Zn质量变
化量
A. ①② B. ②③ C. ①③ D. ①④6. 科学家们发现水竟然有18种存在形态。下列有关水的说法正确的是
A. 温度升高,水的电离平衡正向移动, c(H⁺)增大,酸性增强
B. 当 c (H+)=c (OH−)时,溶液一定呈中性
H O H O
2 2
C. 室温下,pH=4的亚硫酸溶液中, c (H+)=2×10−10mol⋅L−1
H O
2
D. 向水中加入 NaHSO₄晶体,溶解后水的电离程度减小
7. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 澄清透明溶液中: Na+ 、Cu2+ 、Cl−、SO2−
4
B. 滴加KSCN 显红色的溶液中: N H+ 、Na+ 、Cl−、HCO−
4 3
C. 常温下,由水电离出的 c(H⁺)=10⁻¹²mol/L的溶液: Na+ 、NO−、SO2−、Fe2+
3 4
D. 中性溶液中: Fe3+ 、N H+ 、SO2−、NO−
4 4 3
8. 下列方程式正确的是
A.NH₄Cl溶于 D₂O中: NH4++D O⇌NH ⋅D O+H+
2 3 2
TiCl₄ TiO :
B. 利用 制备 2 TiCl +(x+2)H O TiO ⋅xH O↓+4HCl
4 2 2 2
C. 用惰性电极电解氯化镁溶液: 2Cl-+2H O 2OH-+H ↑+Cl ↑
2 2 2
D. 明矾净水的反应原理: Al³⁺+3H₂O⇌Al(OH)₃↓+3H⁺
9. 下列有关说法中错误的是
A. 某温度时的混合溶液中 K =c2(H+),说明该溶液呈中性
w
c(CH COO−)
3
B. 室温下向10mLpH=3的醋酸溶液中加入水稀释后,溶液中 不变
c(CH COOH)⋅c(OH−)
3
C. 已知电离常数: Ka(HCN)=5×10−10,H CO :K =10−6.4、K =10−10.4
2 3 a1 a2
向 KSCN 溶液中通入少量的 CO₂气体: CO +H O+2CN−=2HCN+CO2−
2 2 3
D.已知 Kₛ ₚ(AgCl)=1.56×10⁻⁰¹ ,Kₛ ₚ(Ag₂CrO₄)=9.0×10⁻¹²,向含有 Cl−、CrO2−且浓度均为
4
0.010mol/L溶液中逐滴加入0.010mol/L的 AgNO₃溶液时,Cl⁻先产生沉淀
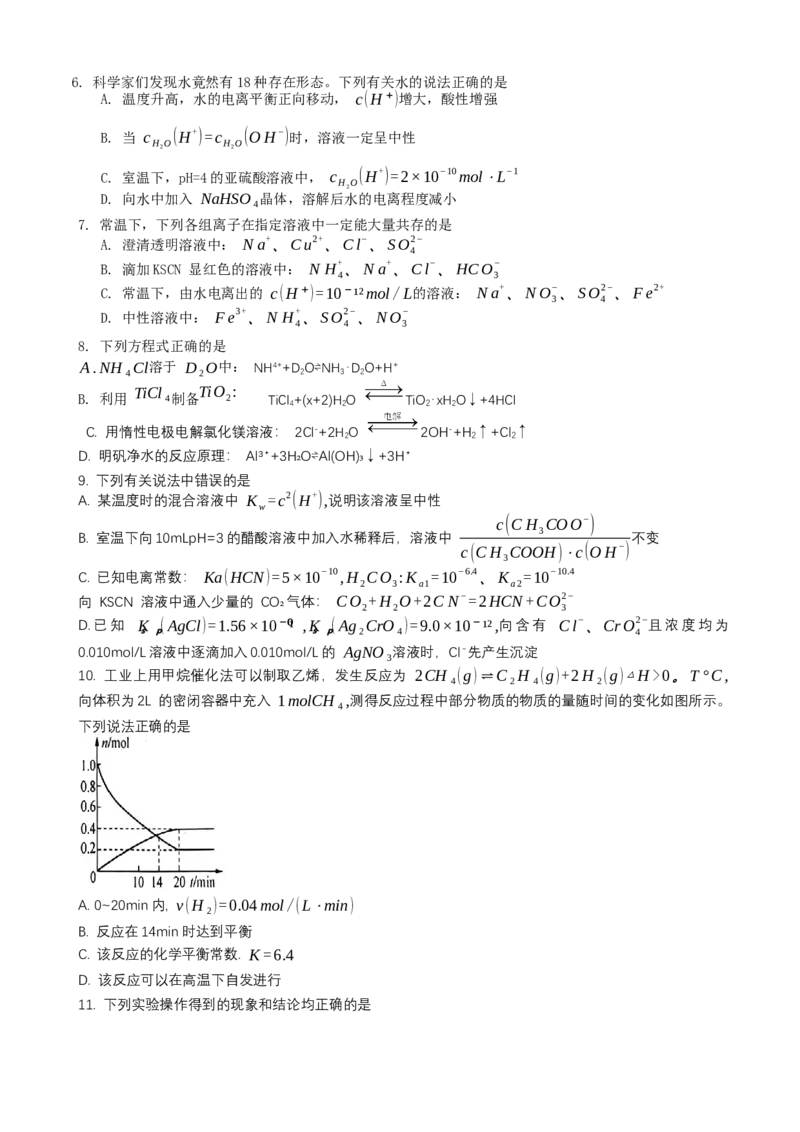
10. 工业上用甲烷催化法可以制取乙烯,发生反应为 2CH₄(g)⇌C₂H₄(g)+2H₂(g)△H>0。T°C,
向体积为2L 的密闭容器中充入 1molCH₄,测得反应过程中部分物质的物质的量随时间的变化如图所示。
下列说法正确的是
A. 0~20min内, v(H₂)=0.04mol/(L⋅min)
B. 反应在14min时达到平衡
C. 该反应的化学平衡常数. K=6.4
D. 该反应可以在高温下自发进行
11. 下列实验操作得到的现象和结论均正确的是选
实验操作 现象 结论
项
向5mL0.1mol·L⁻¹FeCl₃稀溶液中滴加5 滴等浓度的KI溶液, 2份溶液分别出现红 说明Fe³⁺+I⁻→Fe²⁺+I₂
A
振荡,将混合液分为2份,分别滴加KSCN溶液和淀粉溶液 色和蓝色 的反应是有限度的
用 pH 传感器分别测定等物质的量浓度的 NaClO 溶液和 NaClO 溶液的pH较 酸 性 :
B
CH₃COONa溶液的pH 大 HClO>CH₃COOH
溶 液 红 色 逐 渐 消
CO²⁻水解使溶液显碱
C 向滴有酚酞的Na₂CO₃溶液中多次少量加入BaCl₂固体 失,有白色沉淀产
性
生
先出现白
向5mL0.1mol·L⁻¹NaOH稀溶液中滴 Kₛₚ
色沉淀,后
D 加5滴0.1mol·L⁻¹的MgCl₂溶液,再 [Mg(OH)₂]>Kₛₚ[Cu(OH)
出现蓝色
滴加 5滴0.1mol·L⁻¹的CuSO₄溶液 ₂]
沉淀
12. 已知25℃时,物质的溶度积常数为 Kₛ ₚ(FeS)=6.3×10⁻¹⁸;Kₛ ₚ(CuS)=1.3×10⁻³⁶;
Kₛ ₚ(ZnS)=1.6×10⁻²⁴下列说法错误的是
A. 足量CuSO₄溶解在0.1mol/L 的 H₂S 溶液中, Cu²⁺能达到的最大浓度为 1.3×10⁻³⁵mol/L
B. 除去工业废水Fe²⁺中的 Cu²⁺,可选用 FeS 作沉淀剂
C. 在相同温度下,CuS 的溶解度小于 ZnS 的溶解度
D. 在 ZnS 的饱和溶液中, 加入 ZnCl₂溶液,平衡向生成沉淀方向移动,K (ZnS)不变
sp
13. 常温下,下列有关电解质溶液中微粒的物质的量浓度关系正确的是
A.0.1mol/LKHC₂O₄溶液中: c(K+)=c(HC O−)+c(C O2−)
2 4 2 4
B.pH=8的 CH₃COONa溶液: c(Na⁺)−c(CH₃COO⁻)=9.9×10⁻⁷mol⋅L⁻¹
C.0.1mol⋅L⁻¹的 NaHCO₃溶液: c(OH−)=c(H+)+c(HCO−)+2c(H CO )
3 2 3
D.同浓度的下列溶液中, ①N H HSO ②N H Cl③N H ⋅H Oc(N H+)由大到小的顺序是:
4 4 4 3 2 4
②>①>③
14. 海泥细菌通过消耗海底沉积层中的有机物获得营养,同时产生电子。科学家利用这一原理设计了海泥
细菌电池,该技术既可在海底加速石油污染物降解速率,又可产生电能,有很好的应用前景。其中海泥代
谢产物显酸性,电池工作原理如图所示。下列说法错误的是A. A电极的电势高于 B电极
B. 1mol质子通过海底沉积层和海水层交接面,A 电极消耗氧气5.6L(标准状况)
C. 负极的电极反应式为: CH₂O−4e⁻+H₂O=CO₂+4H⁺
D. 海水和海泥作为电解质的一部分,富含盐分,导电性高,有利于输出电能
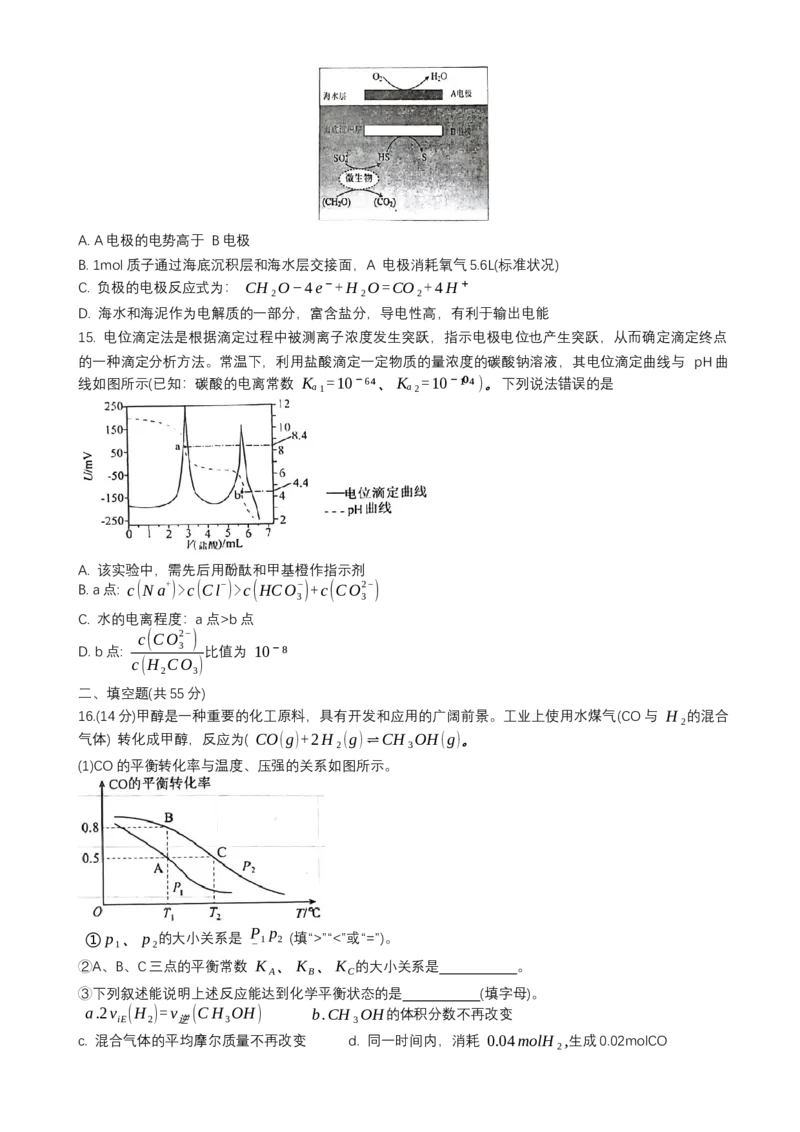
15. 电位滴定法是根据滴定过程中被测离子浓度发生突跃,指示电极电位也产生突跃,从而确定滴定终点
的一种滴定分析方法。常温下,利用盐酸滴定一定物质的量浓度的碳酸钠溶液,其电位滴定曲线与 pH曲
线如图所示(已知:碳酸的电离常数 Kₐ₁=10⁻⁶⁴、Kₐ₂=10⁻¹⁰⁴)。下列说法错误的是
A. 该实验中,需先后用酚酞和甲基橙作指示剂
B. a点:
c(Na+)>c(Cl−)>c(HCO−)+c(CO2−)
3 3
C. 水的电离程度:a点>b点
c(CO2−)
D. b点: 3 比值为 10⁻⁸
c(H CO )
2 3
二、填空题(共55分)
16.(14分)甲醇是一种重要的化工原料,具有开发和应用的广阔前景。工业上使用水煤气(CO与 H₂的混合
气体) 转化成甲醇,反应为( CO(g)+2H₂(g)⇌CH₃OH(g)。
(1)CO的平衡转化率与温度、压强的关系如图所示。
P p
①p₁、p₂的大小关系是 1 2 (填“>”“<”或“=”)。
¯
②A、B、C三点的平衡常数 K 、K 、K 的大小关系是 。
A B C
③下列叙述能说明上述反应能达到化学平衡状态的是 (填字母)。
a.2v (H )=v (CH OH) b.CH₃OH的体积分数不再改变
iE 2 逆 3
c. 混合气体的平均摩尔质量不再改变 d. 同一时间内,消耗 0.04molH₂,生成0.02molCO(2)在 T₂°C、p₂压强时,往一容积为2L的密闭容器内,充入0.3mol CO与( 0.4molH₂发生反应。
①平衡时 H₂的体积分数是 ;平衡后再加入1.0molCO后重新到达平衡,则CO的转化
率 (填“增大”“不变”或“减小”)。
② 若 以 不 同 比 例 投 料 , 测 得 某 时 刻 各 物 质 的 物 质 的 量 如 下 , (
CO:0.1mol、H₂:0.2mol、CH₃OH;0.2mol, 此时 v(正) v(逆)(填“>”“<”或
“=”)。
③若p₂压强恒定为p,则平衡常数 Kₚ = 用气体平衡分压代替气体平衡浓度计算,分压=总压×气
(Kₚ
体的物质的量分数,整理出含p的表达式)。
17.(14分)I.氨是重要的基础化工原料,工业上常用于制备氨水、亚硝酸( (HNO₂)、连二次硝酸
(H₂N₂O₂)、尿素 [CO(NH₂)₂]等多种含氮的化工产品。
c(H+)
(1)常温下, 0.01mol/L 的氨水中 =1×10−6,则该溶液的 pH=将 pH=2的盐酸 V₁L 与
c(OH−) ;
V V
0.01mol/L 氨水 V₂L 混合, 若混合溶液 pH=7,则 1 2(填“>”、 “<”或“=”)。
¯
(2)已知: 25°C时,亚硝酸和连二次硝酸的电离常数如下表所示:
化学式 HNO₂ H₂N₂O₂
电离常数 Kₐ=5.1×10⁻⁴ Ka₁=6.17×10⁻⁸、Ka₂=2.88×10⁻¹²
0.1mol/LNaHN₂O₂溶液中离子浓度由大到小的顺序为 。
(3)向浓度均为0.1mol/L的( CdCl₂和 ZnCl₂混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成
两 种 沉 淀 , 则 溶 液 中 [ 已 知 : Kₛ ₚ(CdCO₃)=1.0×10⁻¹²mol²⋅L⁻²,
Kₛ ₚ(ZnCO₃)=1.5×10⁻⁰¹ mol²⋅L⁻²]
(4)可乐中的食品添加剂有白砂糖、二氧化碳、焦糖色、磷酸、咖啡因等。可乐的辛辣味与磷酸(化
学式为 H₃PO₄,沸点高难挥发)有一定关系。羟基磷灰石 [Ca₅(PO₄)₃OH]是牙釉质的主要成分,在
唾液中存在平衡: Ca (PO ) OH(s)⇌5Ca2+ (aq)+3PO3+ (aq)+OH−(aq)。长期过量饮用可乐会破坏
5 4 3 4
牙釉质,造成龋齿。结合平衡移动原理解释原因: 。
Ⅱ. 回答下列问题:
(5)泡沫灭火器中 Al₂(SO₄)₃溶液与小苏打溶液发生相互促进的水解反应,离子方程式为
。
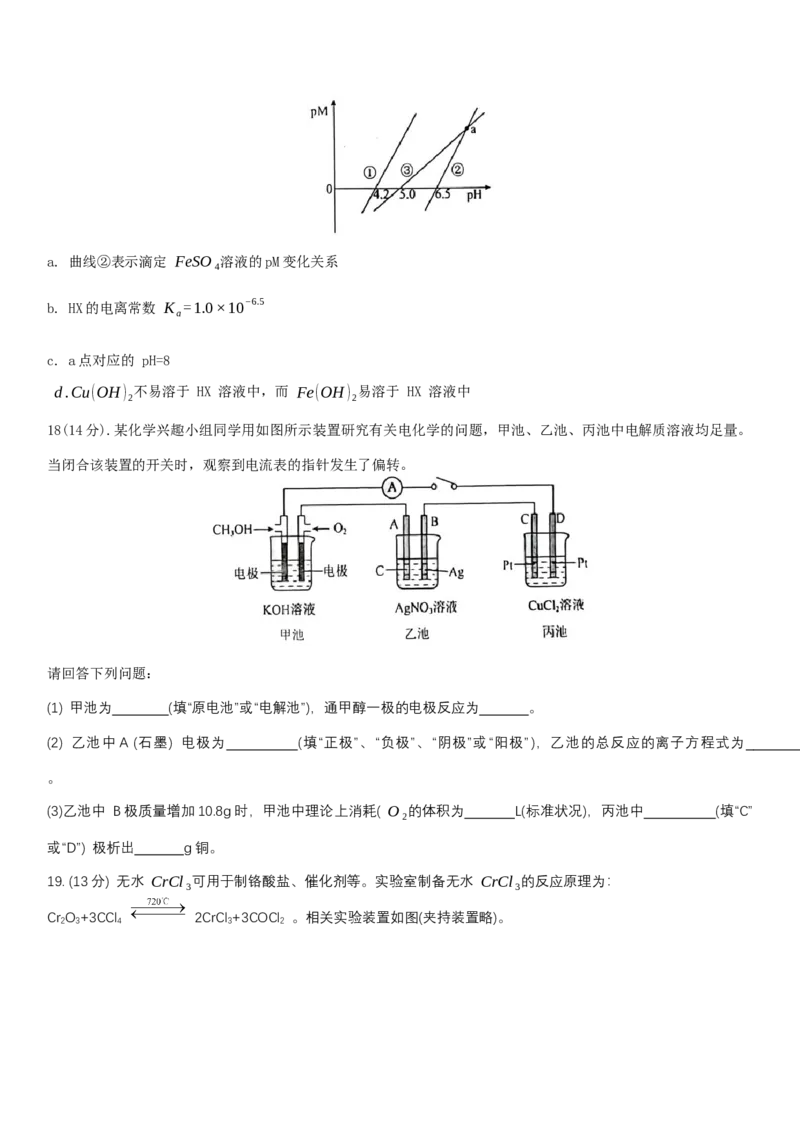
(6)25°C时,用NaOH溶液分别滴定 HX、 CuSO₄、FeSO₄三种溶液,pM[p表示负对数,M表示
c(HX)
, c(Cu²⁺),c(Fe²⁺)]随pH变化的关系如图所示,已知: Kₛ ₚ[Fe(OH)₂]>Kₛ ₚ[Cu(OH)₂](不考虑
c(X−)二价铁的氧化)。下列说法正确的是 。a. 曲线②表示滴定 FeSO₄溶液的pM变化关系
b. HX的电离常数 K =1.0×10−6.5
a
c. a点对应的 pH=8
d.Cu(OH)₂不易溶于 HX 溶液中,而 Fe(OH)₂易溶于 HX 溶液中
18(14分).某化学兴趣小组同学用如图所示装置研究有关电化学的问题,甲池、乙池、丙池中电解质溶液均足量。
当闭合该装置的开关时,观察到电流表的指针发生了偏转。
请回答下列问题:
(1) 甲池为 (填“原电池”或“电解池”),通甲醇一极的电极反应为 。
(2) 乙池中A (石墨) 电极为 (填“正极”、“负极”、“阴极”或“阳极”),乙池的总反应的离子方程式为
。
(3)乙池中 B极质量增加10.8g时,甲池中理论上消耗( O₂的体积为 L(标准状况),丙池中 (填“C”
或“D”) 极析出 g铜。
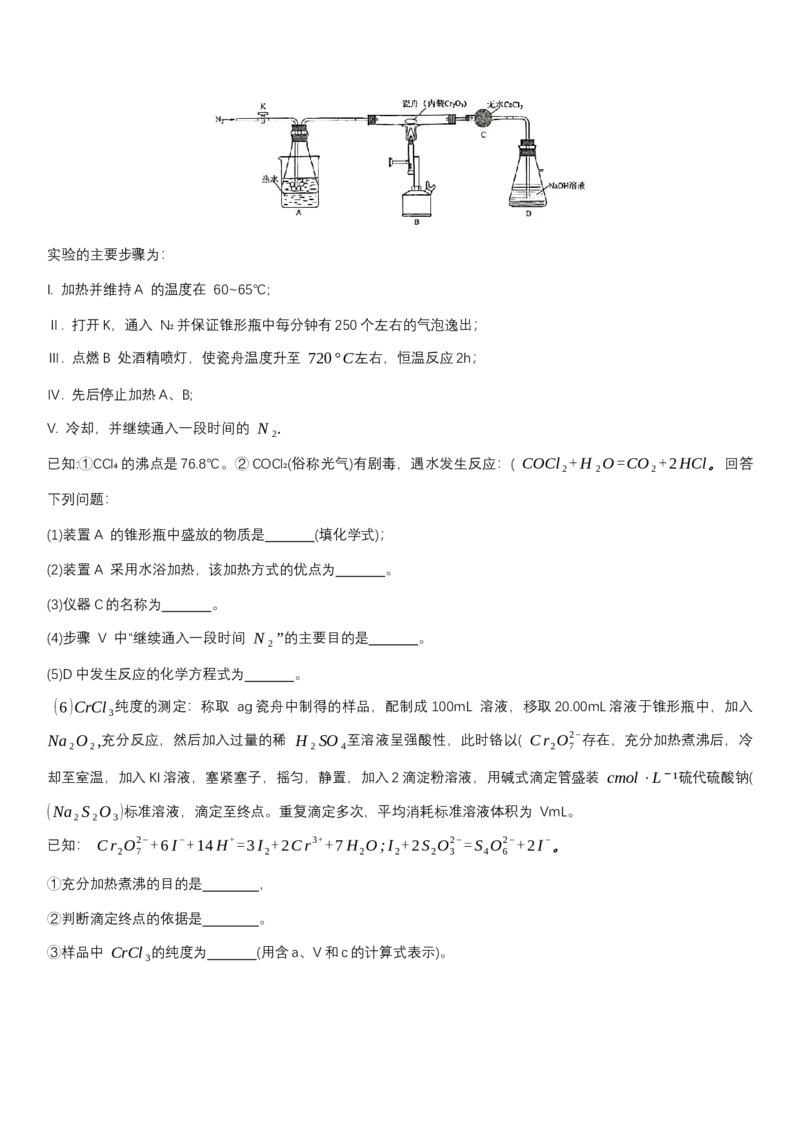
19. (13分) 无水 CrCl₃可用于制铬酸盐、催化剂等。实验室制备无水 CrCl₃的反应原理为:
Cr O +3CCl 2CrCl +3COCl 。相关实验装置如图(夹持装置略)。
2 3 4 3 2实验的主要步骤为:
I. 加热并维持A 的温度在 60~65℃;
Ⅱ. 打开K,通入 N₂并保证锥形瓶中每分钟有250个左右的气泡逸出;
Ⅲ. 点燃B 处酒精喷灯,使瓷舟温度升至 720°C左右,恒温反应2h;
Ⅳ. 先后停止加热A、B;
V. 冷却,并继续通入一段时间的 N₂.
已知:①CCl₄的沸点是76.8℃。②COCl₂(俗称光气)有剧毒,遇水发生反应:( COCl₂+H₂O=CO₂+2HCl。回答
下列问题:
(1)装置A 的锥形瓶中盛放的物质是 (填化学式);
(2)装置A 采用水浴加热,该加热方式的优点为 。
(3)仪器C的名称为 。
(4)步骤 V 中“继续通入一段时间 N₂”的主要目的是 。
(5)D中发生反应的化学方程式为 。
(6)CrCl₃纯度的测定:称取 ag瓷舟中制得的样品,配制成100mL 溶液,移取20.00mL溶液于锥形瓶中,加入
Na₂O₂,充分反应,然后加入过量的稀 H₂SO₄至溶液呈强酸性,此时铬以( Cr O2−存在,充分加热煮沸后,冷
2 7
却至室温,加入KI溶液,塞紧塞子,摇匀,静置,加入2滴淀粉溶液,用碱式滴定管盛装 cmol⋅L⁻¹硫代硫酸钠(
(Na₂S₂O₃)标准溶液,滴定至终点。重复滴定多次,平均消耗标准溶液体积为 VmL。
已知: Cr O2−+6I−+14H+=3I +2Cr3++7H O;I +2S O2−=S O2−+2I−。
2 7 2 2 2 2 3 4 6
①充分加热煮沸的目的是 ,
②判断滴定终点的依据是 。
③样品中 CrCl₃的纯度为 (用含a、V和c的计算式表示)。