文档内容
大庆外国语学校高三期中考试
化学试题
考试时间:75分钟;满分100分
出题人:梁月 校对人:刘振
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
O:16 Na:23 H:1 Cl:35.5 C:12
一、单选题(共45分,每题3分)
1.化学与生活、科技等密切相关,下列说法错误的是( )
A.通过红外光谱仪可检测核酸结构中是否存在氨基官能团
B.量子通信材料螺旋碳纳米管与石墨烯为同位素
C.无磁镍铬钛合金钢常用于舰体材料,其强度高于纯铁
D.“天和号”推进器上的氮化硼陶瓷属于新型无机非金属材料
2.下列化学用语或表述正确的是( )
A. 的空间结构: 形 B. 中的共价键类型:非极性键
C.基态 原子价电子排布式: D.顺-2-丁烯的结构简式:
3.科学家在利用回旋加速器进行的实验中,用含20个质子的钙元素的同位素反复轰击含95个质子的镅元
素,结果4次成功制成4个第115号元素的原子。这4个原子在生成数微秒后衰变成第113号元素。前者的
一种核素为 。下列有关叙述正确的是( )
A.核素 的质量数为288 B.核素 的质量数与中子数之差为173
C.113号元素属于非金属元素 D.115号元素的最高正化合价是+6
4.下列方程式与所给事实相符的是( )
A.漂白粉溶液吸收 后产生白色沉淀:
B.明矾净水:
C.红热的 粉和水蒸气反应生成黑色固体:
学科网(北京)股份有限公司D.苯酚钠溶液中通入 后变浑浊:
5.用下列实验装置能达到相关实验目的的是( )
A B C D
实验
装置
实验 除去 胶 配制 实验室灼烧
目的 收集 并吸收尾气
体中的 溶液 溶液
6.我国科学家合成了一种深紫外非线性光学晶体新材料 ,晶体中阴离子为 。元素M、
X、Y、Z均为短周期元素,M、Y与Z同周期,M的最外层电子数比次外层电子数多1,Z为电负性最强
的元素,Y是地壳中含量最高的元素,X的 轨道有3个电子。下列说法中不正确的是( )
A.电负性: B.简单离子半径:
C.简单气态氢化物的稳定性: D.M最高价氧化物对应水化物能与盐酸反应
7.将一小粒钠放在石棉网上,微热,待钠熔成球状时,将盛有氯气的集气瓶迅速倒扣在钠的上方,钠剧烈
燃烧,有白烟生成。下列分析不正确的是( )
A.钠熔化后体积增大,说明钠原子间的平均距离增大
B.反应过程中, 的 键断裂
C. 的形成过程可表示为
D.该实验说明 的氧化性比 的强
8.奥司他韦是目前治疗流感的最常用药物之一,其结构简式如图所示。下列有关该化合物的说法错误的是
( )
学科网(北京)股份有限公司A.分子中既含有 键,又含有 键
B.该物质可以使溴的四氯化碳溶液褪色
C. 该物质可以与 发生加成反应
D.分子中有2种官能团可以发生水解反应
9.南海是一个巨大的资源宝库,海水开发利用的部分过程如图所示,下列说法错误的是( )
A.物质 可以选用
B.操作1中玻璃棒的作用是引流
C.第①步中,蒸发结晶、高温烘干可以得到干燥的 固体
D.第②步反应的离子方程式为:
10.用如图所示装置进行实验,下列实验现象描述错误的是( )
选项 试剂甲 试剂乙 试剂丙 丙中的现象
A 浓氨水 有白色沉淀生成
溶液
B 浓硫酸 有白色沉淀生成
溶液
C 过氧化氢 酸性 淀粉溶液 溶液变为蓝色
D 浓盐酸 有淡黄色沉淀生成
溶液
11.下列有关不同价态含硫化合物的说法中错误的是( )
学科网(北京)股份有限公司A.工业接触法制备硫酸涉及到的转化为
B.实验室制备乙炔中的硫化氢杂质可用 溶液除去
C.黄铁矿的主要成分为 ,该化合物中阴阳离子个数比为
D.硫在过量氧气中燃烧能够生成
12.有氧条件下,在 基催化剂表面, 还原 的反应机理如图所示。该反应能够有效脱除烟气中的
,保护环境。下列说法不正确的是( )
A.在酸性配位点上, 与 通过配位键形成
B.增大压强有利于 与 吸附在 配位点上形成
C.在反应过程中, 基可以提高 的转化率
D.该反应的总方程式为:
13.工业烟气含有 ,可以用 溶液进行绿色化处理后再排放。设 为阿伏加德罗常数的值,下
列说法正确的是( )
A. 含有的电子数目为
B. 溶液中 的数目为
学科网(北京)股份有限公司C. (标准状况)与足量氧气反应,转移电子数目为
D. 溶液最多能吸收 的数目为
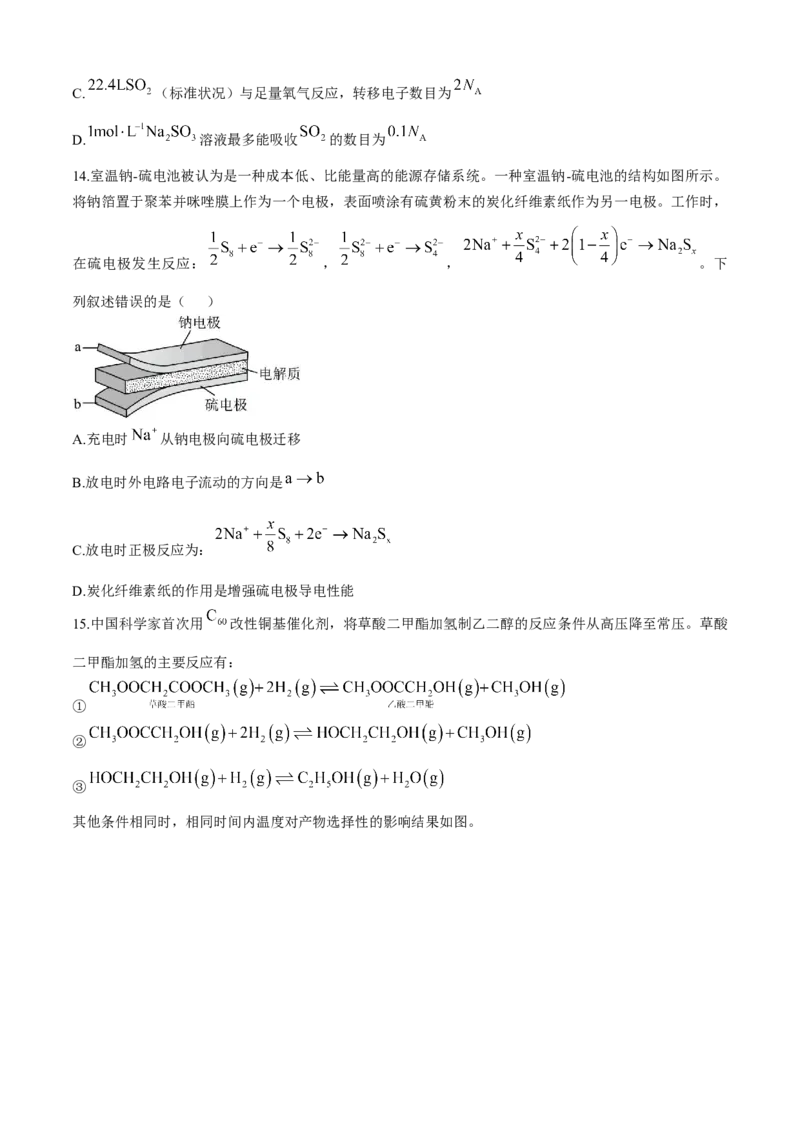
14.室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室温钠-硫电池的结构如图所示。
将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维素纸作为另一电极。工作时,
在硫电极发生反应: , , 。下
列叙述错误的是( )
A.充电时 从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是
C.放电时正极反应为:
D.炭化纤维素纸的作用是增强硫电极导电性能
15.中国科学家首次用 改性铜基催化剂,将草酸二甲酯加氢制乙二醇的反应条件从高压降至常压。草酸
二甲酯加氢的主要反应有:
①
②
③
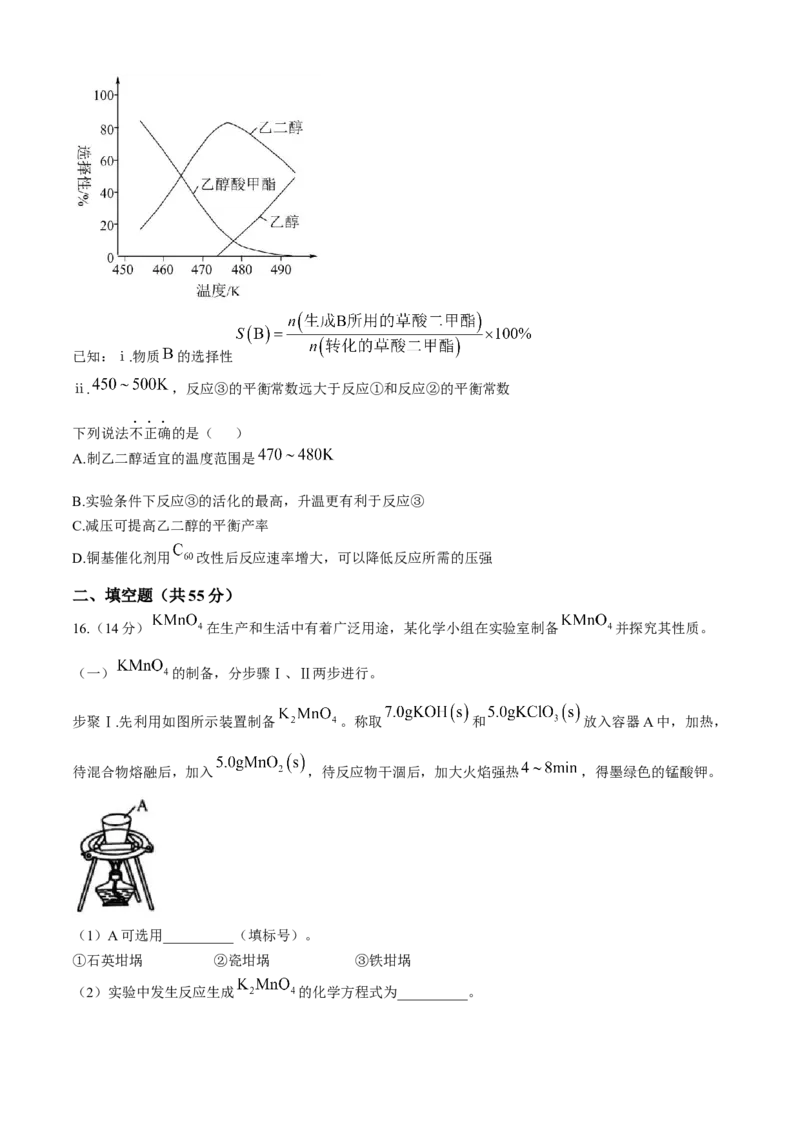
其他条件相同时,相同时间内温度对产物选择性的影响结果如图。
学科网(北京)股份有限公司已知:ⅰ.物质 的选择性
ⅱ. ,反应③的平衡常数远大于反应①和反应②的平衡常数
下列说法不正确的是( )
A.制乙二醇适宜的温度范围是
B.实验条件下反应③的活化的最高,升温更有利于反应③
C.减压可提高乙二醇的平衡产率
D.铜基催化剂用 改性后反应速率增大,可以降低反应所需的压强
二、填空题(共55分)
16.(14分) 在生产和生活中有着广泛用途,某化学小组在实验室制备 并探究其性质。
(一) 的制备,分步骤Ⅰ、Ⅱ两步进行。
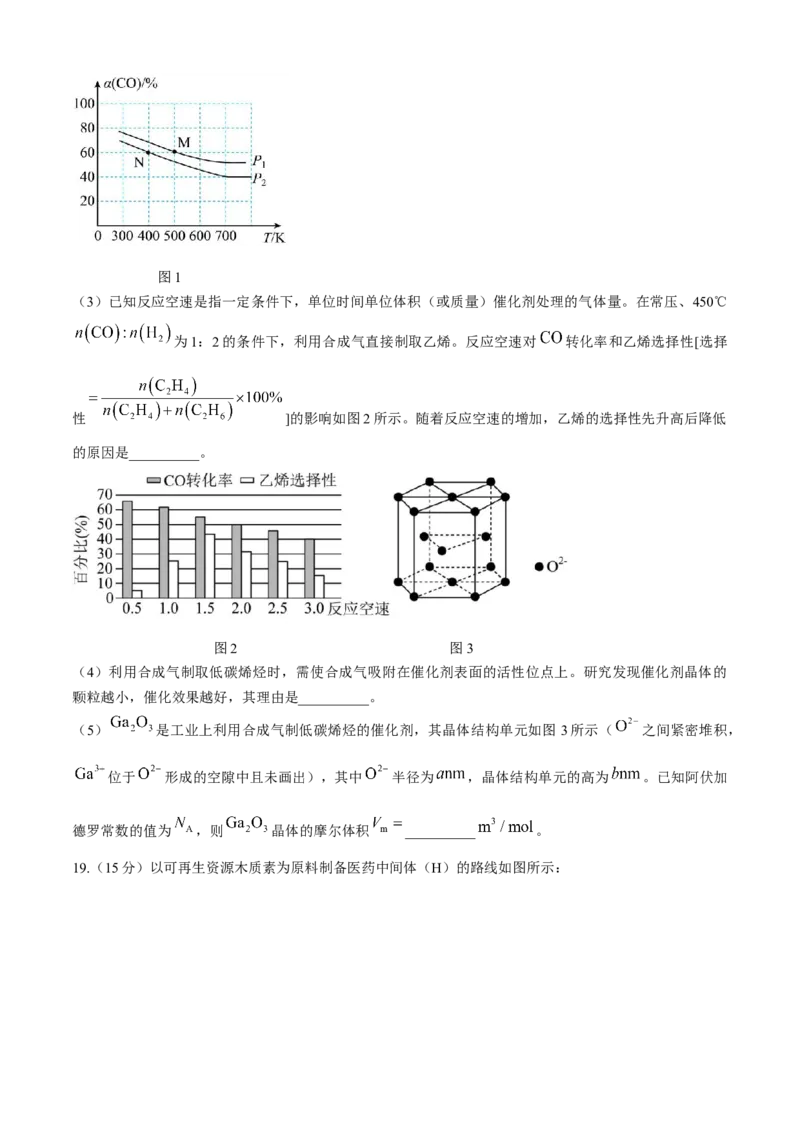
步聚Ⅰ.先利用如图所示装置制备 。称取 和 放入容器A中,加热,
待混合物熔融后,加入 ,待反应物干涸后,加大火焰强热 ,得墨绿色的锰酸钾。
(1)A可选用__________(填标号)。
①石英坩埚 ②瓷坩埚 ③铁坩埚
(2)实验中发生反应生成 的化学方程式为__________。
学科网(北京)股份有限公司Ⅱ.由 制备 。已知: 易溶于水,水溶液呈墨绿色。主要过程如下:
①待A处物料冷却后,用 溶液重复浸取,合并浸取液便得墨绿色的锰酸钾溶液。
②向滤液中通入足量 ,使 歧化为 和 ,过滤出生成的 。
③再将滤液进行一系列处理,得 晶体。
(3)过程②向滤液中通入足量 ,可观察到的现象为__________;检验 歧化完全的实验方法
是__________。
(二) 的性质。已知: 具有强氧化性,可与草酸( )反应:
。某化学小组选用硫酸酸化的
高锰酸钾溶液与草酸溶液反应,探究外界条件对化学反应速率的影响,进行了如下三组实验:
[实验内容及记录的数据]
室温下,试管中所加试剂及其用量 室温下溶液颜色
编号 褪至无色所需时
溶液 稀硫酸 间
溶液
1 3.0 1.0 4.0 2.0 4.0
2 2.0 2.0 4.0 2.0 5.2
3 1.0 3.0 4.0 2.0 6.4
(4)配制 的高锰酸钾溶液肯定不需要的仪器是__________(填标号)。
A.蒸发皿 b.容量瓶 c.玻璃棒 d.烧杯
e.坩埚 f.胶头滴管
(5)为达到实验目的, 溶液的物质的量浓度不低于__________。
(6)利用实验1中数据计算, 内,用 的浓度变化表示的反应速率:
__________。
17.(12分)工业上以铬铁矿[主要成分为 ,含少量 、 杂质]为主要原料制备红矾钾
( )的工艺流程如图所示:
学科网(北京)股份有限公司请回答下列问题:
(1)已知“高温连续焙烧”阶段 元素转化为 。
①焙烧时采取“多层逆流焙烧”,即将固体粉末从炉顶投料,氧气从炉底鼓入,这样做的优点为
__________。② 与纯碱反应的化学方程式为__________。
(2)滤液Ⅱ中发生反应的离子方程式为__________。
(3)一系列操作包括: 蒸发溶剂至有晶膜出现,停止加热、__________抽滤、重结晶。
(4)生产过程中产生的 酸性废液可通过钡盐沉淀法处理,其过程为:先将 酸性废液碱
化 处 理 , 再 加 入 。 废 液 需 进 行 碱 化 处 理 的 目 的 是 __________[ 已 知 :
]。
(5)除了“一系列操作”中所得母液可循环利用外,上述流程中可循环利用的物质还有 、
__________(填化学式)。
18.(15分)低碳烯烃是基础有机化工原料,工业上可利用合成气直接或间接制取。主要反应方程式如下。
间接制取低碳烯烃:
直接制取低碳烯烃:
回答下列问题:
(1)已知 ,则 __________ 。
(2)将 、 和 以体积比为 充入密闭容器中直接制取乙烯, 的平衡转化率与温度的关
系如图1所示,则 __________ (填“>”或“=”),M点的正反应速率__________N点的逆反应速率
(填“>”“<”或“=”)。在 ,压强为 的条件下,该反应的 __________(列出计算式)。
学科网(北京)股份有限公司图1
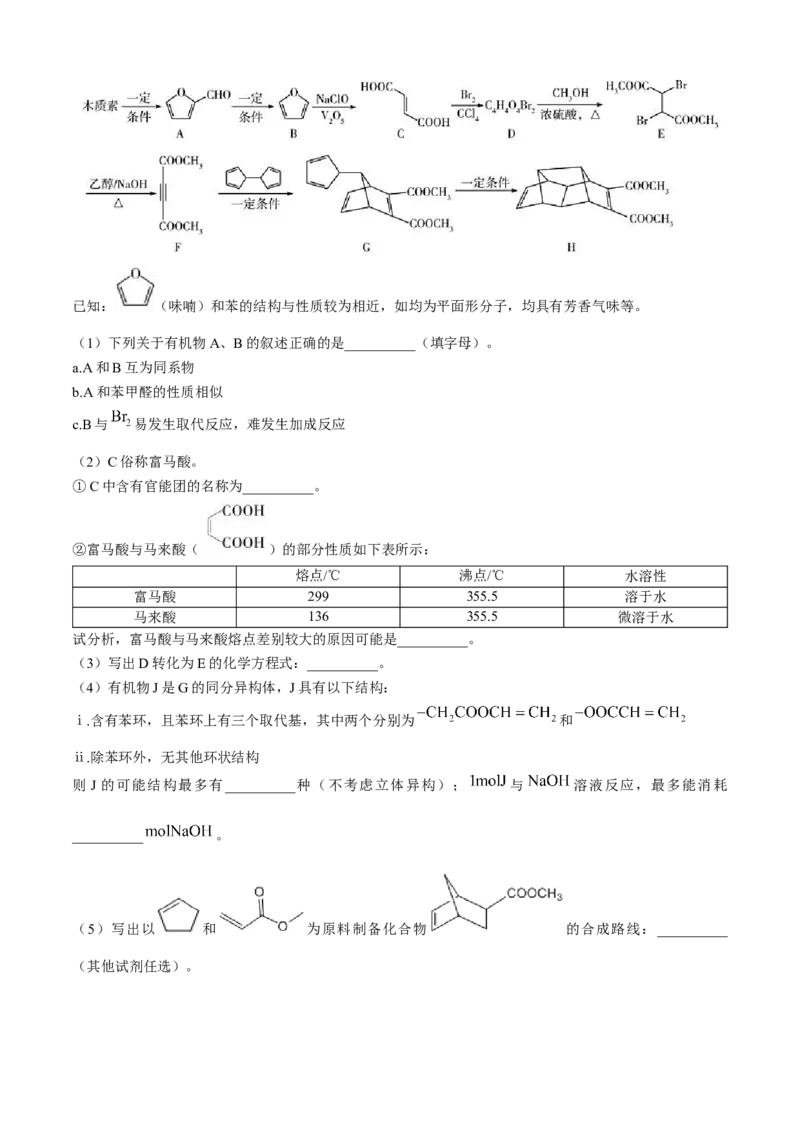
(3)已知反应空速是指一定条件下,单位时间单位体积(或质量)催化剂处理的气体量。在常压、450℃
为1:2的条件下,利用合成气直接制取乙烯。反应空速对 转化率和乙烯选择性[选择
性 ]的影响如图2所示。随着反应空速的增加,乙烯的选择性先升高后降低
的原因是__________。
图2 图3
(4)利用合成气制取低碳烯烃时,需使合成气吸附在催化剂表面的活性位点上。研究发现催化剂晶体的
颗粒越小,催化效果越好,其理由是__________。
(5) 是工业上利用合成气制低碳烯烃的催化剂,其晶体结构单元如图3所示( 之间紧密堆积,
位于 形成的空隙中且未画出),其中 半径为 ,晶体结构单元的高为 。已知阿伏加
德罗常数的值为 ,则 晶体的摩尔体积 __________ 。
19.(15分)以可再生资源木质素为原料制备医药中间体(H)的路线如图所示:
学科网(北京)股份有限公司已知: (味喃)和苯的结构与性质较为相近,如均为平面形分子,均具有芳香气味等。
(1)下列关于有机物A、B的叙述正确的是__________(填字母)。
a.A和B互为同系物
b.A和苯甲醛的性质相似
c.B与 易发生取代反应,难发生加成反应
(2)C俗称富马酸。
①C中含有官能团的名称为__________。
②富马酸与马来酸( )的部分性质如下表所示:
熔点/℃ 沸点/℃ 水溶性
富马酸 299 355.5 溶于水
马来酸 136 355.5 微溶于水
试分析,富马酸与马来酸熔点差别较大的原因可能是__________。
(3)写出D转化为E的化学方程式:__________。
(4)有机物J是G的同分异构体,J具有以下结构:
ⅰ.含有苯环,且苯环上有三个取代基,其中两个分别为 和
ⅱ.除苯环外,无其他环状结构
则 J 的可能结构最多有__________种(不考虑立体异构); 与 溶液反应,最多能消耗
__________ 。
(5)写出以 和 为原料制备化合物 的合成路线:__________
(其他试剂任选)。
学科网(北京)股份有限公司参考答案:
1.B 2.B 3.A 4.B 5.D
6.D 7.D 8.C 9.C 10.B
11.D 12.C 13.B 14.A 15.C
16.(13分)【答案】(1)③(1分)
(2) (2分)
(3)墨绿色溶液变为紫红色,同时有黑色固体生成(2分) 用玻璃棒蘸取溶液点到滤纸上,滤纸上只有
紫色而无绿色痕迹,则歧化完全(2分)
(4)ae(2分)
(5)
(6)
17.(12分)【答案】(1)增大反应物接触面积,提高反应速率,从而提高原料的利用率(2分)
(2分)
(2) (2分)
(3)冷却至室温(2分)
(4)促进 转化为 , 浓度升高,有利于与 生成 沉淀(2分)
(5) (2分)
18.(15分)【答案】(1) (2分)
(2)>(2分) >(2分) (2分)
(3)空速增加,生成乙烯增加,且乙烯与氢气反应较少,使得乙烯的选择性增大;空速过高时,气体流
速太快,反应时间缩短,使得乙烯的选择性降低(2分)
(4)催化剂晶体的颗粒越小,催化剂的表面积越大,活性位点越大(2分)
(5) (3分)
19.(15分)【答案】(1)bc(2分)
(2)羧基,碳碳双键(2分) 马来酸易形成分子内氢健,而富马酸易形成分子间氢健,故富马酸熔点较
学科网(北京)股份有限公司高(2分)
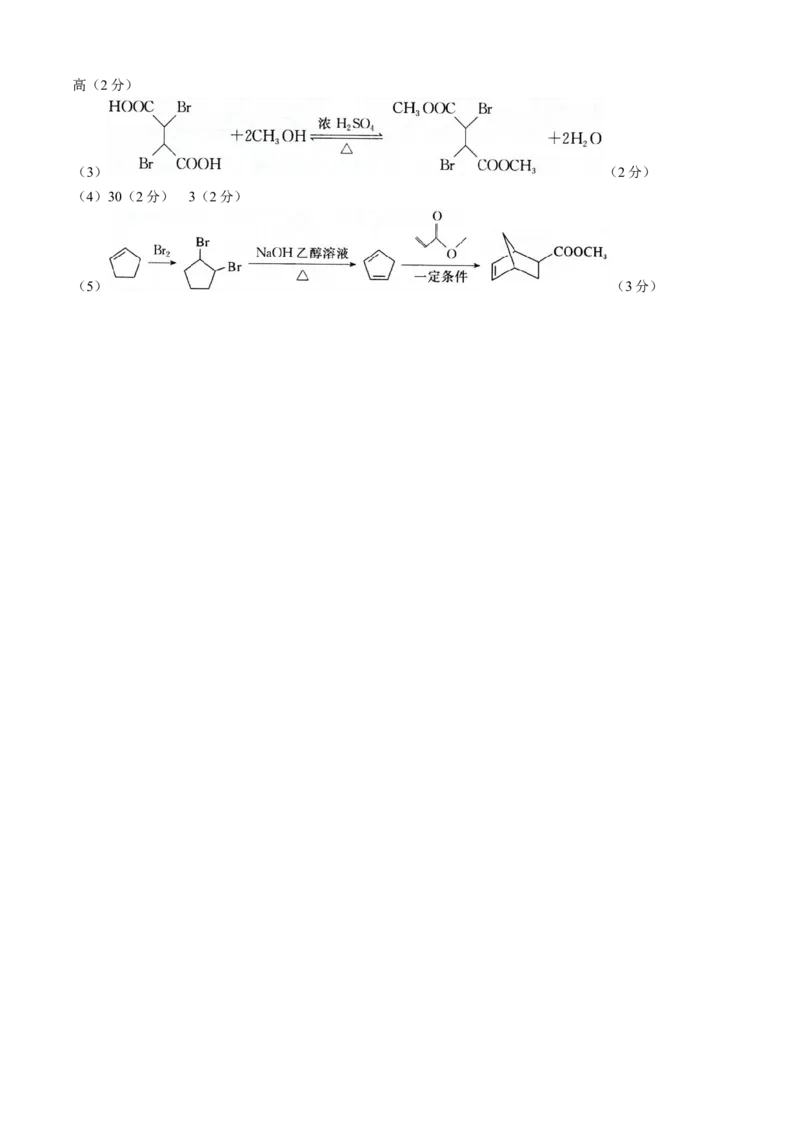
(3) (2分)
(4)30(2分) 3(2分)
(5) (3分)
学科网(北京)股份有限公司