文档内容
牡丹江市省级示范高中2024--2025学年度高三期中
化学试卷
考试时间:75分钟 分值:100分
I卷
可能用到的相对原子质量:O-16 Cu-64
一、单项选择题(本题包括15小题,每小题3分共45分)
1.文物见证历史,化学创造文明。东北三省出土的下列文物据其主要成分不能与
其他三项归为一类的是( )
A.金代六曲葵花婆金银盏 B.北燕鸭形玻璃注
C.汉代白玉耳杯 D.新石器时代彩绘几何纹双腹陶罐
2.下列有关化学用语表述正确的是( )
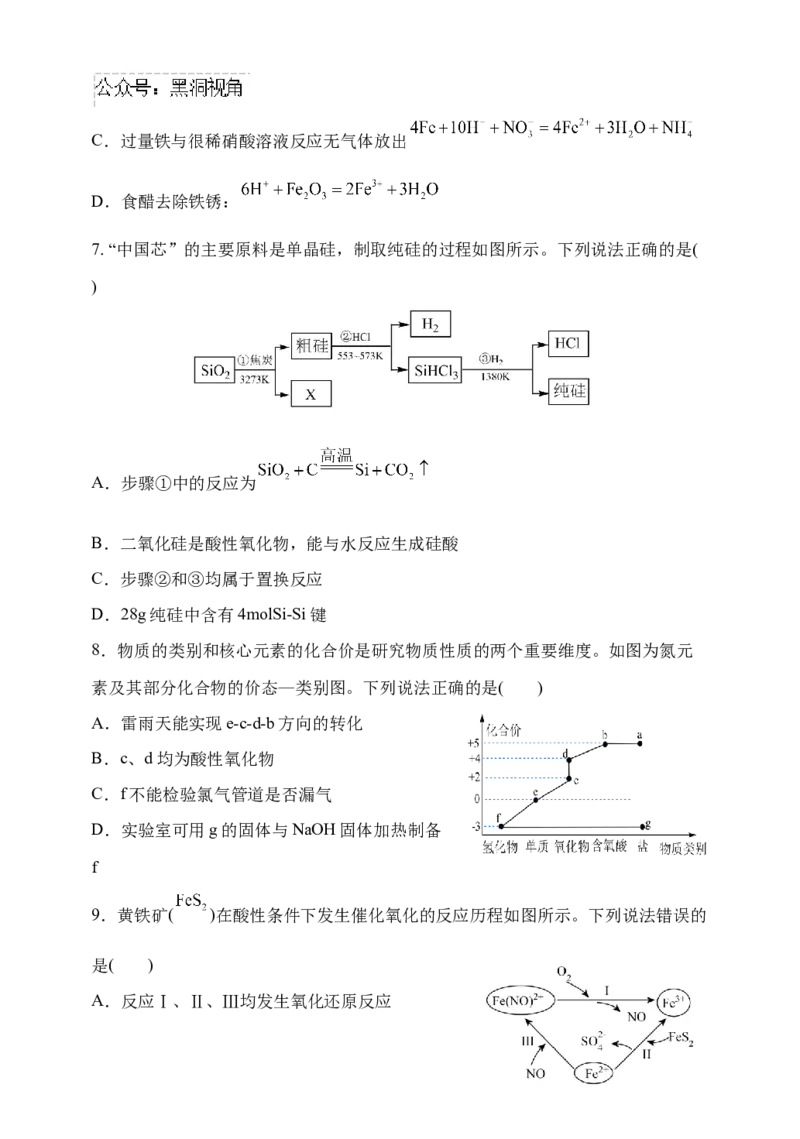
A.HF分子中σ键的电子云轮廓图:
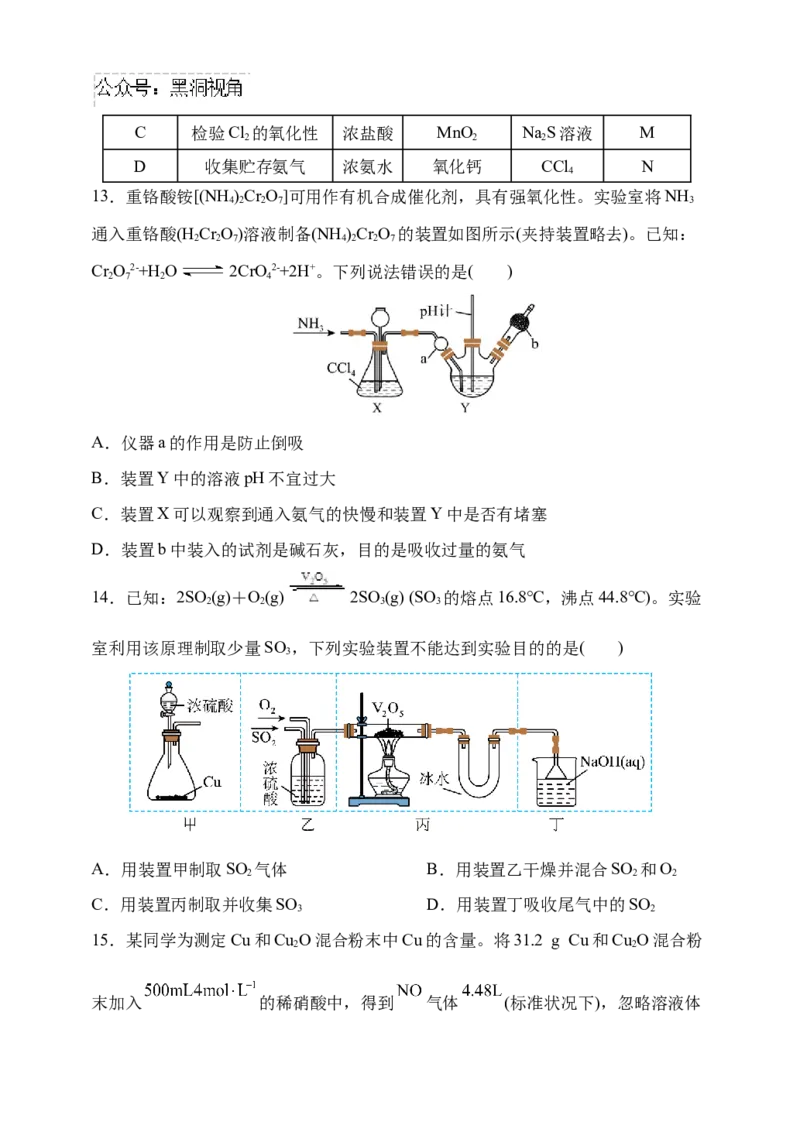
B.Fe2+的价层电子轨道表示式:
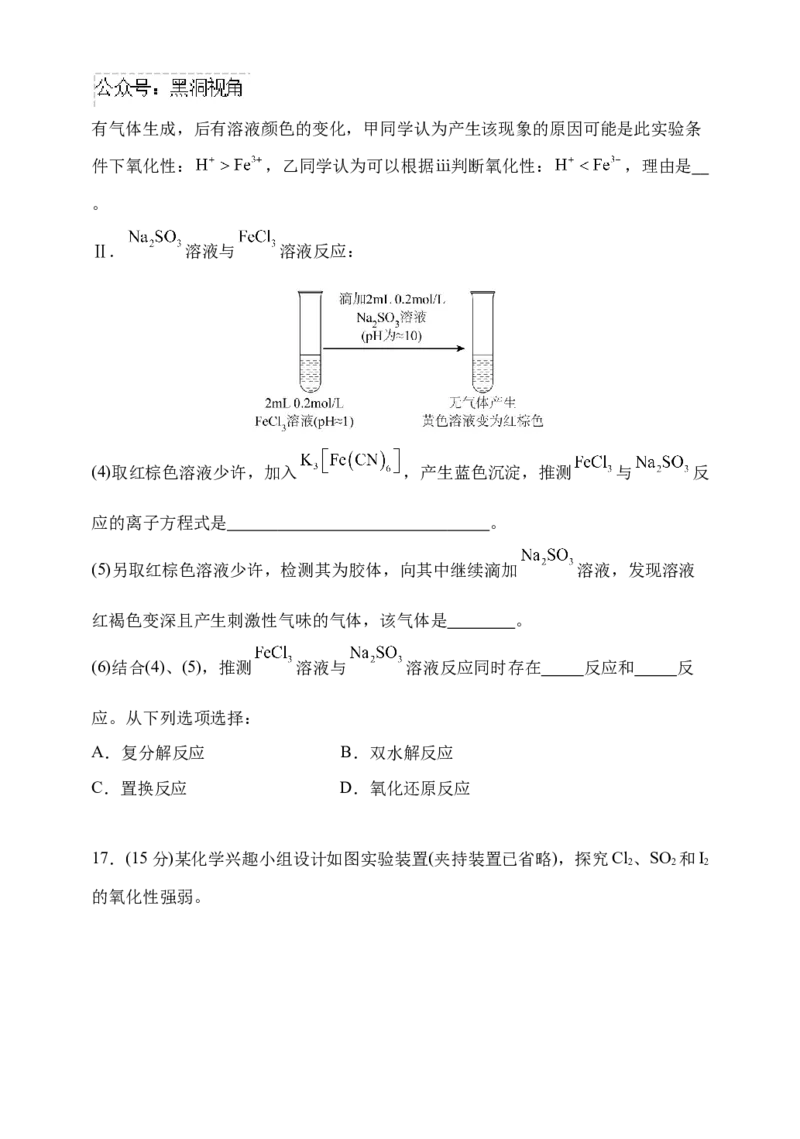
C.HCl的电子式:
D.中子数为9的氮原子: N
3.有关化学实验的说法错误的是( )
A.实验室储存的镁条着火时,不可以用泡沫灭火器灭火
B.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理
C.做蒸馏实验时,应在蒸馏烧瓶中加入沸石,以防暴沸。如果在沸腾前发现忘记
加沸石,应立即停止加热,冷却后补加
D.海带提碘中,为制取海带灰,可以将海带放在通风处加热灼烧,使其充分灰化4.设 为阿伏加德罗常数的值,下列说法正确的是( )
A.标准状况下, 溶于水,溶液中 和 的微粒数目之和为
B.3.36 L HF(标准状况)所含的分子数为
C.常温常压下, 与足量 反应,共生成 ,转移电子的数目为
D. 的 溶液显中性, 该溶液中含 的数目为
5.劳动创造幸福未来。下列劳动项目与所述的化学知识关联不合理的是( )
选项 劳动项目 化学知识
家务劳动:饭后用热的纯碱溶液洗涤餐
A 油脂在碱性条件下发生水解
具
B 社区服务:推广使用免洗手酒精消毒液 酒精能使蛋白质变性
C 工厂生产:冶炼钢铁 涉及氧化还原反应
有利于实现“碳达峰、碳中
D 科学研究:燃煤脱硫
和”
6.下列反应的离子方程式正确的是( )
A.同浓度同体积 溶液与 溶液混合:
B. 酸性溶液中滴入C.过量铁与很稀硝酸溶液反应无气体放出
D.食醋去除铁锈:
7. “中国芯”的主要原料是单晶硅,制取纯硅的过程如图所示。下列说法正确的是(
)
A.步骤①中的反应为
B.二氧化硅是酸性氧化物,能与水反应生成硅酸
C.步骤②和③均属于置换反应
D.28g纯硅中含有4molSi-Si键
8.物质的类别和核心元素的化合价是研究物质性质的两个重要维度。如图为氮元
素及其部分化合物的价态—类别图。下列说法正确的是( )
A.雷雨天能实现e-c-d-b方向的转化
B.c、d均为酸性氧化物
C.f不能检验氯气管道是否漏气
D.实验室可用g的固体与NaOH固体加热制备
f
9.黄铁矿( )在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的
是( )
A.反应Ⅰ、Ⅱ、Ⅲ均发生氧化还原反应B.反应Ⅰ中氧化剂与还原剂的物质的量之比为
C.反应Ⅱ的离子方程式为
D.总反应过程中氧气做氧化剂
10.下列说法正确的是( )
A.铁与碘反应易生成碘化铁
B.制备无水氯化镁需在HCl气流中加热
C.用石灰沉淀富镁海水中的Mg2+,生成碳酸镁
D.SO 通入BaCl 溶液中生成BaSO 沉淀
2 2 3
11.下列实验方案中元素价态转化正确的是( )
选 同元素不同价态之
实验方案
项 间转化
A 向NaSO 粉末中滴加70%硫酸,将气体通入氯水 S:+6→+4→+6
2 3
B 向稀硝酸中加入少量铁粉,再加入过量铜粉 Fe:0→+3→+2
C 加热NH Cl和Ca(OH) 混合物,将气体通入浓硫酸中 N:-3→0→+4
4 2
D 在KClO 中加入浓盐酸,将气体通入KI淀粉溶液中 Cl:-1→0→+5
3
12.甲、乙是实验室常用装置,选用适当实验药品,组装甲、乙能实现多种实验目
的。下列选项中试剂选取和操作能达到对应实验目的的是( )
选项 实验目的 a物质 b物质 乙中物质 乙进气口
A 检验SO 的漂白性 浓硫酸 NaSO 固体 品红溶液 N
2 2 3
B 收集贮存NO 浓硝酸 Cu 水 NC 检验Cl 的氧化性 浓盐酸 MnO NaS溶液 M
2 2 2
D 收集贮存氨气 浓氨水 氧化钙 CCl N
4
13.重铬酸铵[(NH )CrO]可用作有机合成催化剂,具有强氧化性。实验室将NH
4 2 2 7 3
通入重铬酸(H CrO)溶液制备(NH )CrO 的装置如图所示(夹持装置略去)。已知:
2 2 7 4 2 2 7
CrO2-+H O 2CrO2-+2H+。下列说法错误的是( )
2 7 2 4
A.仪器a的作用是防止倒吸
B.装置Y中的溶液pH不宜过大
C.装置X可以观察到通入氨气的快慢和装置Y中是否有堵塞
D.装置b中装入的试剂是碱石灰,目的是吸收过量的氨气
14.已知:2SO (g)+O(g) 2SO (g) (SO 的熔点16.8℃,沸点44.8℃)。实验
2 2 3 3
室利用该原理制取少量SO ,下列实验装置不能达到实验目的的是( )
3
A.用装置甲制取SO 气体 B.用装置乙干燥并混合SO 和O
2 2 2
C.用装置丙制取并收集SO D.用装置丁吸收尾气中的SO
3 2
15.某同学为测定Cu和Cu O混合粉末中Cu的含量。将31.2 g Cu和Cu O混合粉
2 2
末加入 的稀硝酸中,得到 气体 (标准状况下),忽略溶液体积的变化。下列有关说法正确的是( )
A.反应后有固体剩余
B.反应后的溶液中c(Cu2+)=0.8mol·L-1
C. 单质在混合粉末中的质量分数约为
D.在反应后的溶液中加入足量铁粉,可置换出
Ⅱ卷
(四道大题、共55分)
16.(13分)以 溶液为实验对象,研究物质之间反应的复杂多样性。实验如
下:
Ⅰ.金属与 溶液反应
装置 序 金 现象及产物检验
号 属
镁 立即产生大量气体,溶液颜色变红棕色;
ⅰ
条 片刻后气泡减少,金属表面产生红褐色沉淀。
开始时无明显气泡,半分钟后有气体产生,溶液颜
锌
ⅱ 色慢慢加深;一段时间后,金属表面产生红棕色沉
粒
淀
铜
ⅲ 无气体产生,溶液逐渐变为蓝绿色;
粉
(1)配制 溶液,需要 将固体先溶于浓盐酸,再稀释至指定浓度,原因是
。
(2)根据实验ⅰ中的现象,推测红褐色液体为胶体,通过 可以快速判
断其是否为胶体。
(3) 溶液与Cu反应的离子方程式为 ,实验ⅰ和ⅱ均先有气体生成,后有溶液颜色的变化,甲同学认为产生该现象的原因可能是此实验条
件下氧化性: ,乙同学认为可以根据ⅲ判断氧化性: ,理由是
。
Ⅱ. 溶液与 溶液反应:
(4)取红棕色溶液少许,加入 ,产生蓝色沉淀,推测 与 反
应的离子方程式是 。
(5)另取红棕色溶液少许,检测其为胶体,向其中继续滴加 溶液,发现溶液
红褐色变深且产生刺激性气味的气体,该气体是 。
(6)结合(4)、(5),推测 溶液与 溶液反应同时存在 反应和 反
应。从下列选项选择:
A.复分解反应 B.双水解反应
C.置换反应 D.氧化还原反应
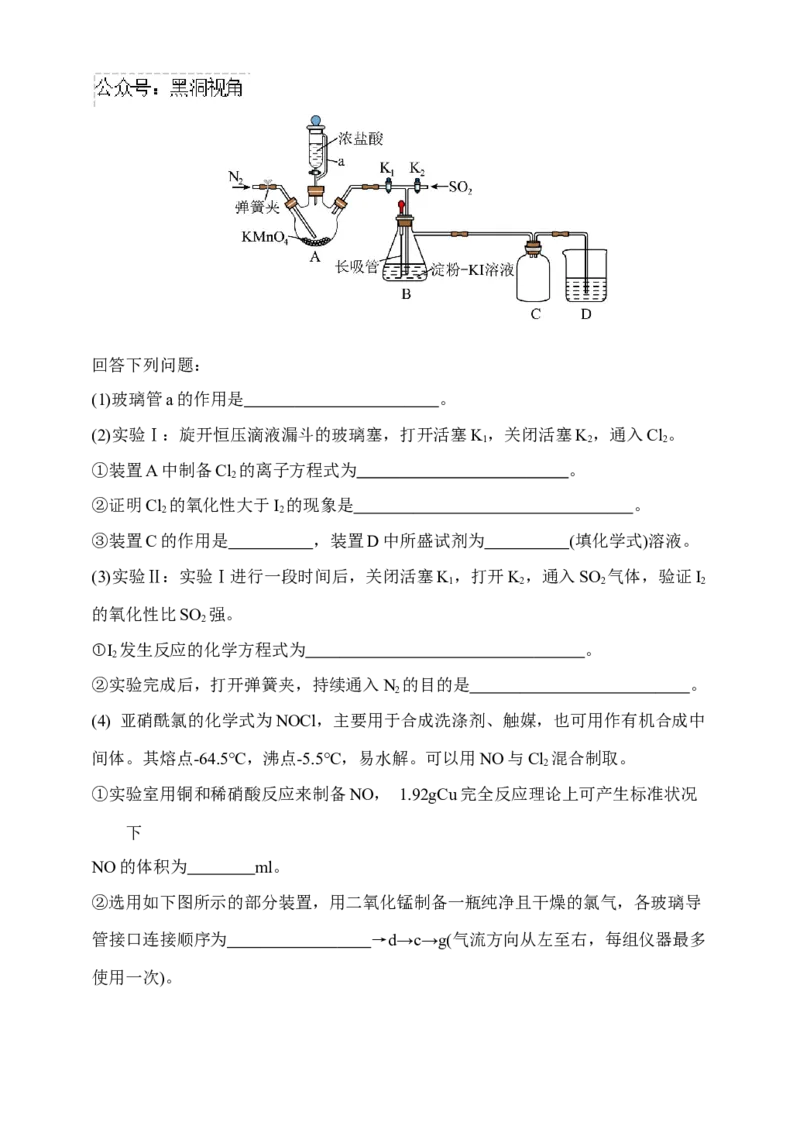
17.(15分)某化学兴趣小组设计如图实验装置(夹持装置已省略),探究Cl、SO 和I
2 2 2
的氧化性强弱。回答下列问题:
(1)玻璃管a的作用是 。
(2)实验Ⅰ:旋开恒压滴液漏斗的玻璃塞,打开活塞K,关闭活塞K,通入Cl。
1 2 2
①装置A中制备Cl 的离子方程式为 。
2
②证明Cl 的氧化性大于I 的现象是 。
2 2
③装置C的作用是 ,装置D中所盛试剂为 (填化学式)溶液。
(3)实验Ⅱ:实验Ⅰ进行一段时间后,关闭活塞K,打开K,通入SO 气体,验证I
1 2 2 2
的氧化性比SO 强。
2
①I 发生反应的化学方程式为 。
2
②实验完成后,打开弹簧夹,持续通入N 的目的是 。
2
(4) 亚硝酰氯的化学式为NOCl,主要用于合成洗涤剂、触媒,也可用作有机合成中
间体。其熔点-64.5℃,沸点-5.5℃,易水解。可以用NO与Cl 混合制取。
2
①实验室用铜和稀硝酸反应来制备NO, 1.92gCu完全反应理论上可产生标准状况
下
NO的体积为 ml。
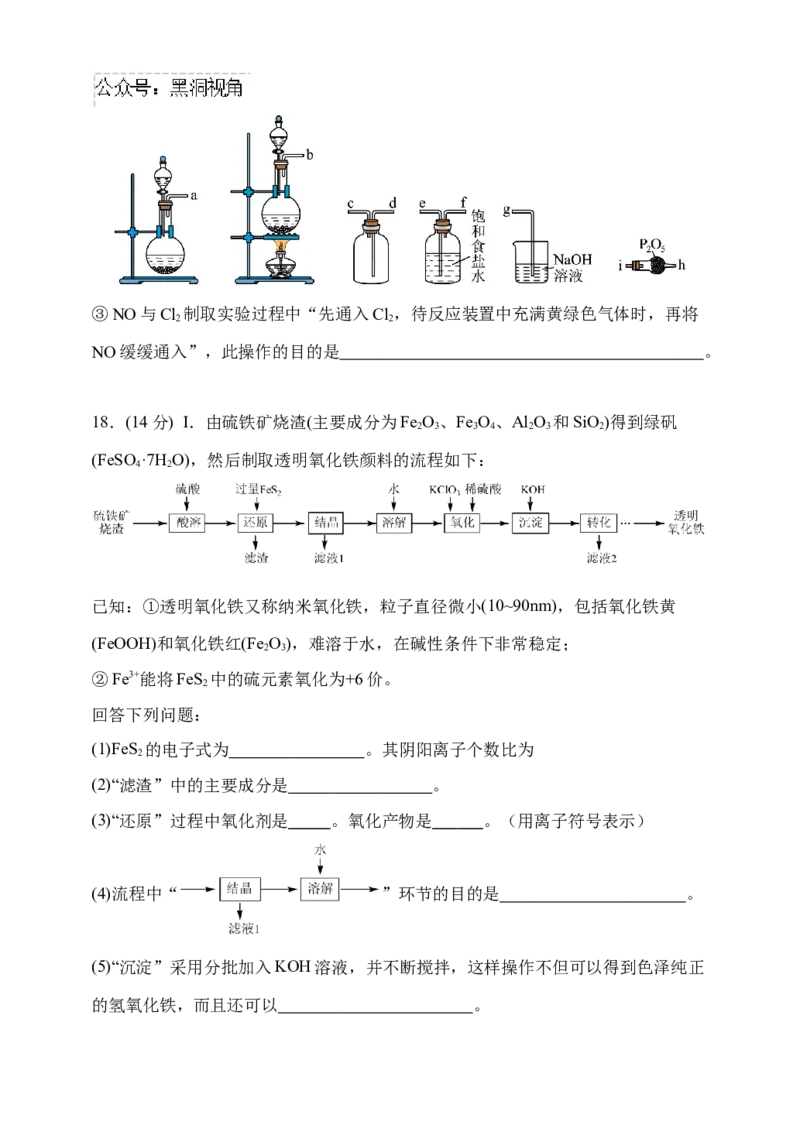
②选用如下图所示的部分装置,用二氧化锰制备一瓶纯净且干燥的氯气,各玻璃导
管接口连接顺序为 →d→c→g(气流方向从左至右,每组仪器最多
使用一次)。③NO与Cl 制取实验过程中“先通入Cl,待反应装置中充满黄绿色气体时,再将
2 2
NO缓缓通入”,此操作的目的是 。
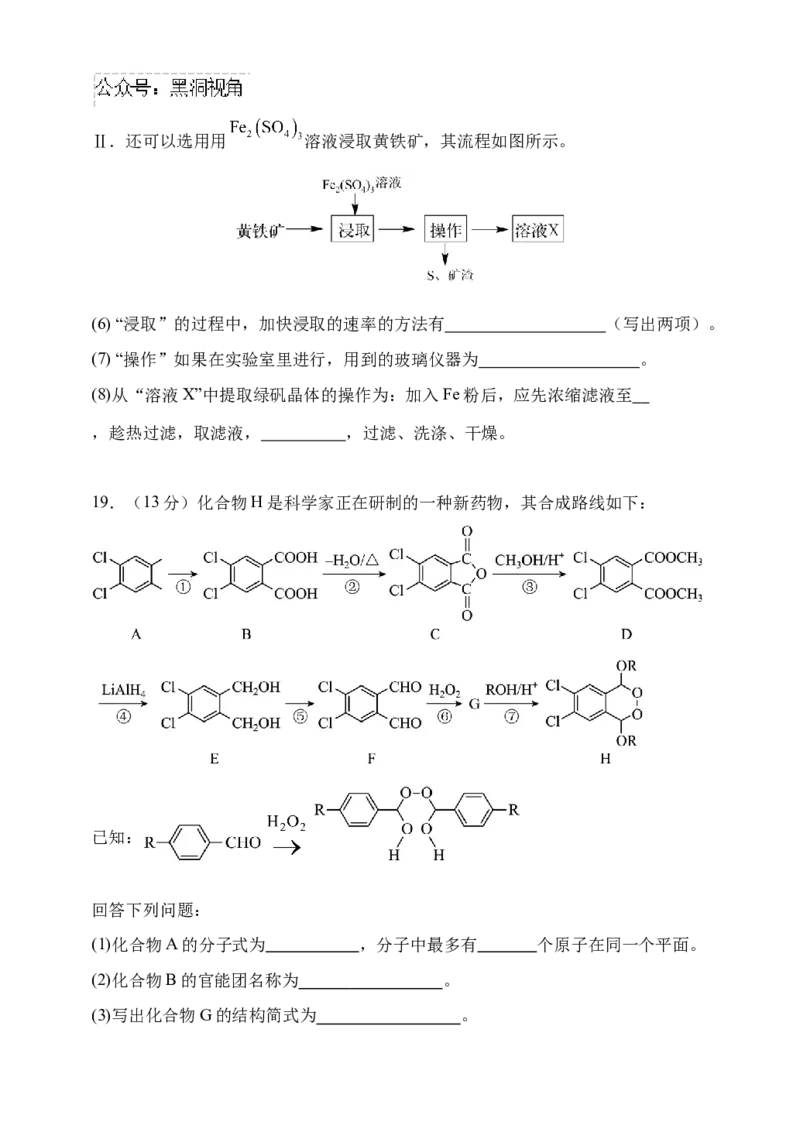
18.(14分) I.由硫铁矿烧渣(主要成分为Fe O、Fe O、Al O 和SiO)得到绿矾
2 3 3 4 2 3 2
(FeSO ·7H O),然后制取透明氧化铁颜料的流程如下:
4 2
已知:①透明氧化铁又称纳米氧化铁,粒子直径微小(10~90nm),包括氧化铁黄
(FeOOH)和氧化铁红(Fe O),难溶于水,在碱性条件下非常稳定;
2 3
②Fe3+能将FeS 中的硫元素氧化为+6价。
2
回答下列问题:
(1)FeS 的电子式为 。其阴阳离子个数比为
2
(2)“滤渣”中的主要成分是 。
(3)“还原”过程中氧化剂是 。氧化产物是 。(用离子符号表示)
(4)流程中“ ”环节的目的是 。
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正
的氢氧化铁,而且还可以 。Ⅱ.还可以选用用 溶液浸取黄铁矿,其流程如图所示。
(6) “浸取”的过程中,加快浸取的速率的方法有 (写出两项)。
(7) “操作”如果在实验室里进行,用到的玻璃仪器为 。
(8)从“溶液X”中提取绿矾晶体的操作为:加入Fe粉后,应先浓缩滤液至
,趁热过滤,取滤液, ,过滤、洗涤、干燥。
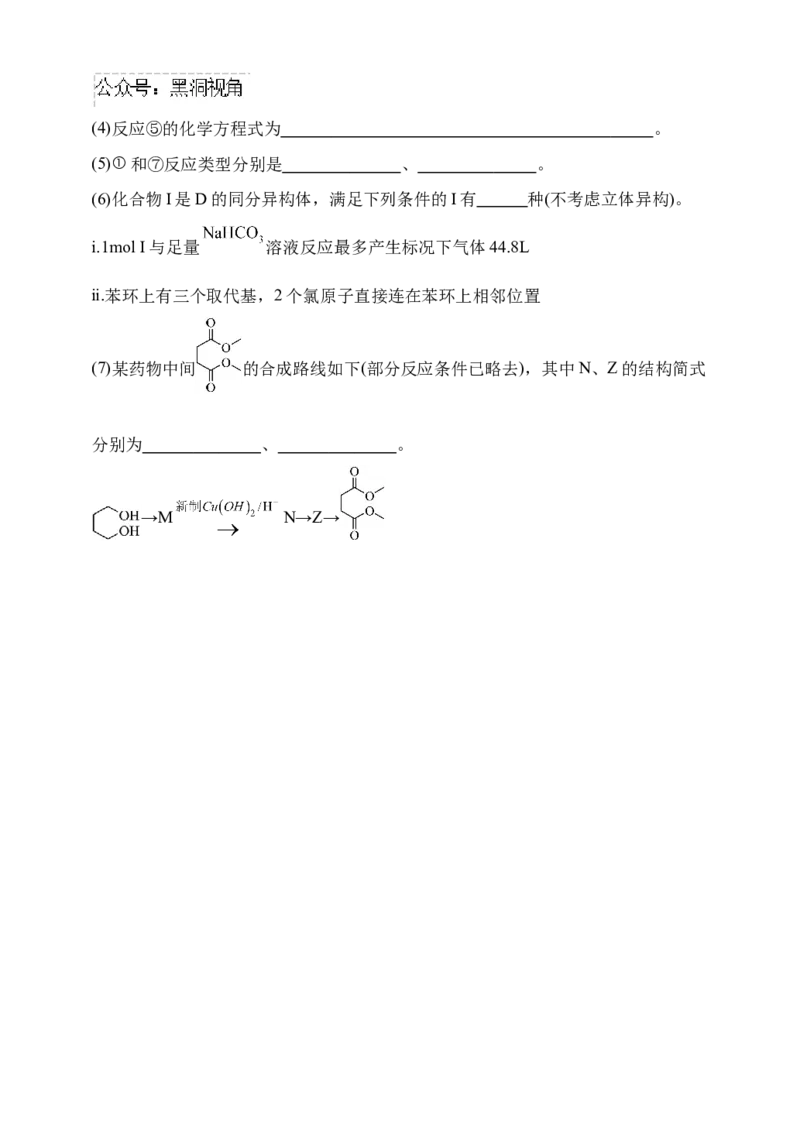
19.(13分)化合物H是科学家正在研制的一种新药物,其合成路线如下:
已知:
回答下列问题:
(1)化合物A的分子式为 ,分子中最多有 个原子在同一个平面。
(2)化合物B的官能团名称为 。
(3)写出化合物G的结构简式为 。(4)反应⑤的化学方程式为 。
(5)①和⑦反应类型分别是 、 。
(6)化合物I是D的同分异构体,满足下列条件的I有 种(不考虑立体异构)。
ⅰ.1mol I与足量 溶液反应最多产生标况下气体44.8L
ⅱ.苯环上有三个取代基,2个氯原子直接连在苯环上相邻位置
(7)某药物中间 的合成路线如下(部分反应条件已略去),其中N、Z的结构简式
分别为 、 。
→M N→Z→高三 化学
1-15题每题3分
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
A B B C D C C A A B B D D A D
16.(13分)
(1) 抑制 水解(2分)
(2) 丁达尔效应(1分)
(3) (2分) 可以氧化铜单质,但铜不与盐酸反应
(2分)
(4) (2分)
(5) (2分)
(6) B(1分) D(1分)
17.(15分)
(1) 平衡压强,使分液漏斗中的液体能顺利流下(1分)
(2) 2MnO -+16H++10Cl-=2Mn2+++5Cl↑+8H O(2分) B中溶液变蓝(1分)
4 2 2
防倒吸(1分) NaOH(1分)
(3) I+SO+2H O=2HI+HSO (2分)
2 2 2 2 4
将装置中残余的Cl,SO 等排出,使其被NaOH溶液吸收,防止其污染空气(2
2 2
分)
(4) ①448(2分) ② b→e→f→i→h(2分)
③排尽装置中的空气,防止NO被O 氧化(1分)
2
18.(14分)
(1) 1:1 (2)二氧化硅和二硫化铁(2分)
(3) Fe3+ SO 2-
4
(4) 除去溶液中的Al3+,得到FeSO 溶液
4(5) 形成细小的氢氧化铁颗粒
(6) 将黄铁矿粉碎,适当增加 溶液浓度,适当升温,搅拌(2分)
(7) 烧杯、漏斗、玻璃棒(2分)
(8)溶液表面出现晶膜 冷却结晶
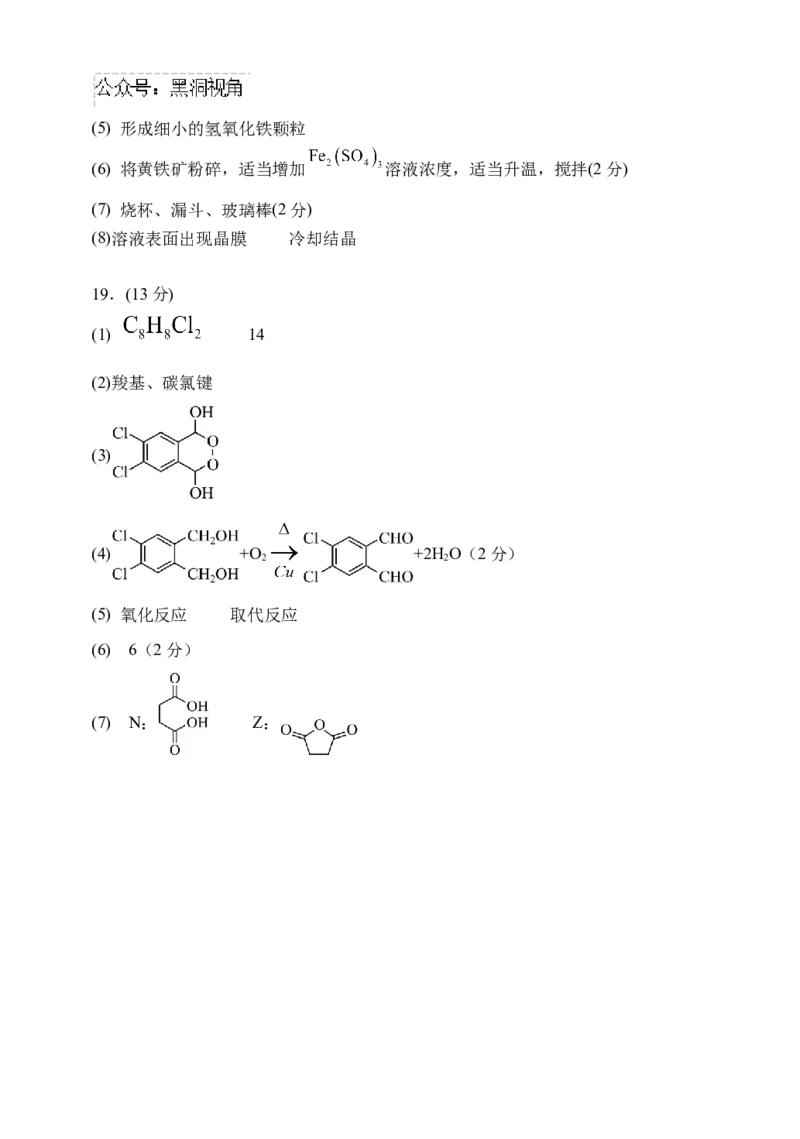
19.(13分)
(1) 14
(2)羧基、碳氯键
(3)
(4) +O +2H O(2分)
2 2
(5) 氧化反应 取代反应
(6) 6(2分)
(7) N: Z: